具有缺陷孔结构的炭膜分离CO2/CH4混合气的分子模拟
何流,赵昊瀚,李花,周子瑞,王同华,潘艳秋
具有缺陷孔结构的炭膜分离CO2/CH4混合气的分子模拟
何流1,赵昊瀚2,李花1,周子瑞1,王同华1,潘艳秋1
(1大连理工大学化工学院,辽宁大连 116024;2沈阳铝镁设计研究院有限公司,辽宁沈阳 110001)
基于炭膜无缺陷Z字形孔模型研究结果,建立随机缺陷、均匀缺陷与局部缺陷3种不同缺陷方式的炭膜微孔模型,研究等摩尔CO2/CH4混合气在缺陷膜孔中的吸附和扩散过程,探讨缺陷对炭膜气体分离的影响。结果表明,在273~348 K的温度范围内,CO2与CH4在缺陷炭膜孔模型内的平衡吸附量与扩散系数均低于无缺陷炭膜孔模型;与无缺陷、均匀缺陷和随机缺陷孔模型相比,局部缺陷孔模型的CO2/CH4总分离系数最低;温度低于298 K时,随机缺陷和均匀缺陷孔模型的总分离系数均大于无缺陷孔模型;随机缺陷孔模型的总分离系数大于均匀缺陷孔模型,说明随机删除碳原子的方式比均匀删除和局部删除更加合理。研究结果可为炭膜气体渗透机理的深入研究提供依据。
分子模拟;二氧化碳;甲烷;炭膜;缺陷孔模型
引 言
炭膜是由含碳物质在高温下热解得到的一种炭基膜材料,具有发达的纳米尺度微孔结构和优良的分离性能[1]。在气体分离领域,炭膜与聚合物膜相比有渗透选择性更高、热及化学稳定性好、耐腐蚀等优点,具备很好的发展潜力与应用前景。
对于炭膜内气体渗透分离过程,常规的实验方法难以详尽观测,且经典的传递理论与模型在纳米尺度的膜孔中并不完全适用。而目前发展起来的分子模拟技术,是研究气体在炭膜纳米尺度孔内渗透与分离机理的一种良好选择[2-4]。
研究人员以炭膜的单孔为基础,建立了不同的狭缝状孔模型,模拟炭膜气体渗透分离过程。这种模型结构较清晰,对于气体在炭膜微孔内短程渗透与分离,能够得到更加详尽直观的结果[5]。Xu等[6]利用双控体积-巨正则分子动力学(DCV-GCMD)法,模拟了CO2/CH4混合气在炭膜单孔的渗透。Wang等[7]利用DCV-GCMD模拟H2等气体在二维炭膜单孔结构内的渗透过程,对照实验数据,认为有必要改进单孔狭缝模型。Anderson等[8]采用巨正则蒙特卡罗(GCMC)法,模拟CO2/CH4/N23种气体在炭膜孔内的吸附,对比实验数据发现模拟结果总大于实验值,认为与模型的简化有关。吴志强[9]分别采用GCMC法与非平衡分子动力学(NEMD)法模拟了H2/CO在纳米孔炭膜中的平衡吸附分离以及非平衡态扩散分离,认为在混合气的吸附与扩散过程中,分子尺寸相比能量参数更关键。Yeganegi等[10-11]以单孔狭缝模型为基础,构建了不同收缩程度的二维孔模型,并分别采用GCMC法与MD法模拟甲烷与酸性气体在孔内的吸附与扩散,发现收缩孔模型吸附量与吸附热优于单孔狭缝模型。随后,他们将模型扩展到三维[12],模拟了甲烷在收缩碳纳米管内的吸附与扩散,发现与传统碳纳米管相比,收缩碳纳米管的模拟结果更接近甲烷在多孔炭内吸附与扩散的实验值。Su等[13]将实验与狭缝孔内气体渗透的分子模拟相结合,理论研究了孔径大小等因素对渗透性能的影响。Lithoxoos等[14]采用实验与GCMC模拟的方法,考虑了死孔的影响,研究了单壁碳纳米管对5种气体的吸附行为。雷广平等[15-16]以石墨烯结构为基础构建孔模型,模拟研究了H2S/CH4混合气在石墨烯膜内的气体吸附与扩散过程。温伯尧等[17]与Shan等[18]分别讨论了不同修饰方式对石墨烯孔结构气体分离的影响。
尽管目前研究人员在物理模型构建方面做了许多工作,但所建立的模型仍与实际结构存在差异,从而导致模拟与实验结果仍存在差距。因此,建立更加合理的孔模型,对炭膜气体分离过程机理的研究是必要的。以前期建立的Z字形单孔模型为基础[19],结合前期研究[1,20]得到的实际炭膜的微晶片层间存在极微孔且具有缺陷与错位这一结论,引入3种不同的孔缺陷形式,建立与实际炭膜情况更接近的物理模型,并模拟研究CO2/CH4二元体系在膜孔内的吸附与扩散性能,基于模拟结果讨论气体在炭膜孔内的渗透机制,以此作为炭膜制备及气体分离工艺研究与优化的基础。
1 模拟方法与模型
1.1 模拟方法
炭膜等多孔炭材料的气体渗透过程可分为吸附与扩散两个部分[9-12, 21]。据此采用巨正则蒙特卡罗方法和非平衡分子动力学方法,分别使用Materials Studio(MS)和Lammps软件进行吸附与扩散过程的模拟,考察温度以及孔缺陷对混合气体吸附及扩散分离过程的影响。
1.2 孔模型
以前期构建的无缺陷Z字形孔模型(参见图1)及模拟结果[19]为基础,构建长方体三维的模拟盒子(、方向的长度分别为30.20 nm和1.20 nm,方向的长度综合考虑孔径与截断半径两方面的因素,取为3.050 nm)。
真实炭膜的孔结构存在缺陷,且缺陷对气体分离过程会产生较大影响,但膜孔的缺陷率难以通过表征或实验手段确定。参考文献[22-23]中分离性能最优模型的数据,取碳原子缺陷数量为10 %。据此构建了3种不同形式的缺陷炭膜孔模型,其在方向的示意图见图2。
1.3 分子相互作用模型
模拟吸附过程和扩散过程时,均采用Lennard-Jones(L-J)势能函数来计算粒子间的作用力,并采用周期性边界条件以及最小映像原则;利用Metropolis抽样方法进行吸附过程的MC模拟,基于牛顿力学的基本方程进行非平衡分子动力学扩散过程模拟[3-4]。
L-J势能函数的计算公式[24]
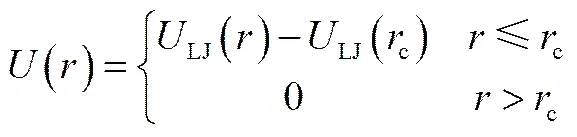
其中LJ()是标准L-J势能函数
(2)
不同原子和间的L-J参数和按Lorentz- Berthelot规则求取:,=(+)/2。由于截断半径c的取值范围一般为的2~4倍,故选取截断半径为1.0 nm。CO2、CH4和炭膜内碳原子的L-J势能参数见表1。
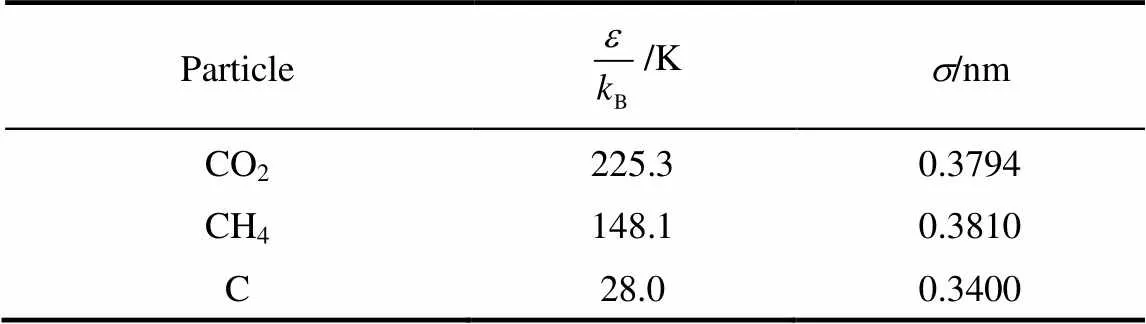
表1 模拟所采用的L-J势能参数值[6]
2 结果与讨论
2.1 模型验证
图3为Z字形无缺陷炭膜孔模型在298 K下对CO2的吸附等温线。可见,模拟结果与实验数据[25]具有相同的趋势且误差较小。可认为所建模型贴近实际炭膜的结构,预计使用该模型进行混合气的模拟能够得到更加合理的数据。
2.2 缺陷炭膜的模拟结果与讨论
以随机缺陷炭膜为例讨论膜缺陷对CO2/CH4混合气体(摩尔比1:1)分离效果的影响。
2.2.1 吸附模拟结果
(1)吸附平衡
图4(a)为随机缺陷炭膜孔模型的吸附等温线。可以发现,不同温度下CO2的吸附量均大于CH4。这是因为两种分子存在竞争吸附,且CO2与炭膜上活性中心的作用力强于CH4,占据更多的吸附位点。对比图4(b)的无缺陷孔模型中混合气体吸附等温线[19],发现两组分的吸附量均有所降低,这是由于缺陷孔模型的碳原子减少使得膜孔壁对气体的作用力减弱,导致等温等压下气体的吸附量下降。同时,引入缺陷后,平衡吸附量随压力变化增加趋势相对均匀,且低压时吸附量增速较无缺陷模型更加平缓,吸附等温线形状更接近文献[25-28]数据。因此认为向孔模型内引入缺陷来表示炭膜孔结构更加合理。
(2)吸附分离系数
利用组分对组分的吸附分离系数ad来分析吸附分离效果[26]。ad的计算见式(3)。式中,X/可认为是一定压力下组分与组分平衡吸附量的比值。因研究体系为等摩尔CO2/CH4混合气,故此处Y/Y的值取1。

图5为不同温度下混合气体的吸附分离系数ad随压力的变化规律。可见,ad随着系统压力的升高而增大且逐渐趋于定值。根据Langmuir理论[29],一定压力下气体吸附量大小与其饱和吸附量呈正比。与CH4相比,CO2在炭质材料微孔内的吸附能力更强,故其饱和吸附量更高。此外,混合气体在微孔内存在竞争吸附现象[30],导致CO2吸附量更多(参见图6)。随着压力的增大,混合气中CO2与CH4的浓度增量相同,但强吸附的CO2会占据更多空吸附位,使CH4吸附量的增加受到抑制。所以随着压力的增大,CO2的吸附增量大于CH4,因此ad增大。当压力增大到一定值后,吸附位基本被完全占据,吸附趋于饱和,进而ad逐渐稳定。温度对CO2吸附量的影响强于CH4[28],导致温度升高分离系数减小。
图4 CO/CH混合气在炭膜孔模型内的吸附等温线
Fig.4 Adsorption isotherms of CO/CH mixture in pore models of carbon membranes
unoccupied adsorption sites;adsorption sites occupied by CO2;adsorption sites occupied by CH4
(3)缺陷对混合气体吸附分离系数的影响
图7为压力100 kPa时随机缺陷与无缺陷炭膜孔模型ad的对比。可以发现,低温下缺陷孔模型的ad高于无缺陷孔模型,而常温及高温下则相反。这是因为低温下,缺陷使得膜的孔壁对气体的作用力减弱,而吸附量较小的CH4受到更多抑制,造成低温条件下缺陷孔模型的ad较高;而常温及高温时,温度的增高使得气体分子的热运动加剧,气体更难在作用力更弱的缺陷孔模型孔内吸附,从而使常温及高温下无缺陷孔模型具有较高的ad值。
2.2.2 扩散模拟结果 采用Einstein方程[31]计算组分中气体在膜孔中的扩散系数

(1)扩散系数
图8(a)为压力100 kPa时,随机缺陷炭膜孔模型内的扩散系数随温度变化情况。可见,与图8(b)所示的无缺陷孔模型的模拟结果[19]相比,缺陷孔模型对两种气体的扩散系数均下降。这是因为两种组分在同一空间扩散不仅受到彼此之间的作用力,还受到来自孔壁的作用力。如图9所示,缺陷孔模型孔壁的碳原子数减少使得原本存在的这些碳原子对气体分子的吸引力消失[如图9(b)中虚线所示],而相应的外层碳原子对气体分子的作用力因距离较远且受到内层其他碳原子的阻挡而较小,造成缺陷孔模型孔壁对气体的作用力减弱且变得不均匀,从而使扩散系数有所下降。
(2)缺陷对混合气体扩散分离系数的影响
根据两组分的扩散系数,可计算得到混合气的扩散分离系数diff[26]

图10对比了随机缺陷与无缺陷炭膜孔模型对混合气的扩散分离系数diff。不同温度下,二者的diff均接近1,可见扩散对混合气在炭膜内分离的影响有限。随机缺陷孔模型的diff随温度升高而下降,这与无缺陷孔模型的趋势相同;低温下缺陷孔模型的diff较低,常温与高温则相反。这是由于缺陷使膜孔壁对气体的作用力减弱,且低温下组分的扩散能力较低,从而得到的扩散分离系数接近于1,说明该条件下难以通过纯扩散过程实现混合气的分离;而常温及高温下,分子量较低的CH4热运动增加幅度更大,但缺陷的存在使膜孔壁对剧烈运动气体分子的作用力降低,且对CH4分子更为明显。因此在常温及高温下气体在缺陷孔模型中的扩散分离性能下降。
图10 不同温度下随机缺陷与无缺陷炭膜孔模型的扩散分离系数
Fig.10 Diffusion separation coefficients of carbon membranes’ pore models with random defect and without defect under different temperature conditions
2.2.3 吸附-扩散分离选择性 利用吸附分离系数与扩散分离系数来计算气体的总分离系数total[26]

汇总2.2.1、2.2.2节的吸附、扩散模拟结果,可得出混合气体的总分离系数total。图11对比了随机缺陷与无缺陷炭膜孔模型的计算结果。可以发现,在低温下,随机缺陷孔模型的total较高,说明低温下缺陷的形成有助于混合气体的分离;在常温及高温下,无缺陷孔模型的total高于缺陷孔模型,说明常温及高温下随机缺陷的形成不利于混合气体分离。
图11 不同温度下随机缺陷与无缺陷炭膜孔模型的总分离系数
Fig.11 Total separation coefficients of carbon membranes’ pore models with random defect and without defect under different temperature conditions
2.3 不同炭膜缺陷形式的比较
2.3.1 吸附模拟结果 图12比较了3种缺陷的炭膜与无缺陷炭膜孔模型对CO2/CH4混合气体的吸附分离系数。可以看到,与其他两种缺陷孔模型相比,不同温度下局部缺陷孔模型的ad均相对更低。这是因为局部缺陷孔模型的缺陷部分吸附量极小,使得CO2吸附量受到较大影响,从而导致ad减小;此外,随机缺陷和均匀缺陷孔模型删除原子的方式相同,因此二者的ad与温度的相关性不明显且相对差距较小。
2.3.2 扩散模拟结果 图13为CO2/CH4混合气体在缺陷与无缺陷炭膜孔模型中扩散分离系数diff的对比。可以看到,不同温度下,4种炭膜的diff均接近1,可见扩散部分对气体分离影响较小。同时,随机缺陷孔模型的diff均相对较高,而均匀缺陷孔模型均相对较低,说明随机缺陷不利于混合气体通过扩散的方式分离。这是因为随机缺陷会造成膜孔内阻力和推动力分布不均匀,阻力较大处限制混合气体的分离。而局部缺陷孔模型在缺陷位置的空洞会使得气体分离性能下降。因此均匀缺陷孔模型的扩散分离性能较好。
2.3.3 吸附-扩散分离选择性 将吸附、扩散模拟结果汇总,通过式(6)可得出混合气体的总分离系数total,结果见图14。可以发现,局部缺陷炭膜孔模型的total最低;较低温度下无缺陷孔模型的total相对较低,较高温度下则相反。此外,随机缺陷孔模型的total在各个温度下均大于均匀缺陷孔模型,且低温时二者差值较大。从ad与diff的计算结果可以看出,对于本文所构建的炭膜孔模型,吸附分离对总体分离的贡献更大。根据文献[26-28],压力一定时,炭膜上CO2的吸附热绝对值大于CH4。根据van’t Hoff表达式[28]

可知,随着环境温度的升高,CO2吸附量下降比率高于CH4。低温下,CO2吸附量大幅度增加,占据了炭膜内大量空间,从而使CH4的吸附受到限制。因热效应与空间限制的双重影响,认为低温时total更具优势的随机缺陷孔模型更适于表示炭膜的孔结构,即随机删除碳原子的缺陷方式比均匀删除与局部删除更加合理。
图14 不同温度下缺陷与无缺陷炭膜孔模型总分离系数
Fig.14 Total separation coefficients of carbon membranes’ pore models with three kinds of defect and without defect under different temperature conditions
3 结 论
在前期研究的基础上对Z字形孔模型进行缺陷处理,建立3种不同类型的缺陷炭膜孔模型,分别对CO2/CH4混合气的吸附与扩散分离过程进行分子模拟。
(1)吸附与扩散的模拟结果表明,与无缺陷炭膜孔模型相比,缺陷孔模型的吸附量与扩散系数均较低。低温下缺陷孔模型的吸附分离系数与扩散分离系数高于无缺陷孔模型,而常温及高温下则相反。
(2)不同缺陷孔模型的模拟结果表明,局部缺陷孔模型的吸附与扩散分离系数均相对更低;低温下随机缺陷及均匀缺陷孔模型的吸附分离系数高于无缺陷孔模型,常温及高温下则相反;随机缺陷和均匀缺陷孔模型的吸附分离系数与温度的相关性均不明显且在数值上相对差距较小。随机缺陷孔模型的扩散分离系数相对较高,而均匀缺陷孔模型的扩散分离系数相对较低。
(3)综合吸附与扩散的模拟结果,发现不同温度下局部缺陷孔模型的总分离系数均更低;在低温下,无缺陷孔模型的总分离系数与随机和均匀缺陷孔模型相比较低,温度较高时则相反;随机缺陷孔模型的总分离系数在各温度下均大于均匀缺陷孔模型,且低温时差值较大,认为随机删除碳原子的缺陷方式比均匀删除与局部删除更加合理。
致谢:感谢大连理工大学环境科学与技术学院工业生态与环境工程重点实验室对MS模拟软件的援助。
符 号 说 明

D——扩散系数,m2·s−1 Had——吸附热,J·mol−1 kB——Boltzmann常数,1.38×10−23 J·K−1 N——该种分子数量 p——压力,kPa q——吸附量,mg·g−1 ——指前因子 R——理想气体常数,8.314 J·mol−1·K−1 r——分子间的距离,nm rc——截断半径,nm rk(t), rk(0)——分别为第k个分子在时刻t和0的位置 S——分离系数 T——温度,K U——分子之间的势能,J ULJ——标准L-J势能函数,J X,Y——吸附相与游离相中组分的摩尔分率 ε——L-J势能能量参数,J s——L-J势能长度参数,nm 下角标 ad——吸附 diff——扩散 i, j——组分序号 k——原子序号 total——总体
References
[1] 李琳.聚酰亚胺基炭膜的制备、热解机理及结构调控[D].大连: 大连理工大学, 2013.Li L. Preparation, pyrolysis mechanism and structure modification of polyimide based carbon membrane[D]. Dalian: Dalian University of Technology, 2013.
[2] Gruber A, Salimath P S, Chen J H. Direct numerical simulation of laminar flame-wall interaction for a novel H2-selective membrane/injector configuration[J]. International Journal of Hydrogen Energy, 2014, 39(11): 5906-5918.
[3] Allen M P, Tildesley D J, Banavar J R. Computer Simulation of Liquids[M]. Oxford: Oxford University Press, 1987: 1-6.
[4] Frenkel D, Smit B, Ratner M A. Understanding Molecular Simulation: From Algorithms to Applications[M]. New York: Academic Press, 1996: 2-5.
[5] 潘艳秋. 炭膜分离过程的机理和建模研究[D]. 大连: 大连理工大学, 2008.Pan Y Q. Mechanisms and modeling of carbon membrane separation[D]. Dalian: Dalian University of Technology, 2008.
[6] Xu L F, Sahimi M, Tsotsis T T. Non-equilibrium molecular dynamics simulation of transport and separation of gases in carbon nanopores (Ⅰ): Basic results[J]. Journal of Chemical Physics, 1999, 111(7): 3252-3264.
[7] Wang S M, Yu Y X, Gao G H. Non-equilibrium molecular dynamics simulation on pure gas permeability through carbon membranes[J]. Chinese Journal of Chemical Engineering, 2006, 14(2): 164-170.
[8] Anderson C J, Tao W, Jiang J W,. An experimental evaluation and molecular simulation of high temperature gas adsorption on nanoporous carbon[J]. Carbon, 2011, 49(1): 117-125.
[9] 吴志强. 气体在纳米孔碳膜内吸附、扩散及分离的分子模拟研究[D]. 北京: 北京化工大学, 2008.Wu Z Q. Molecular simulation study on adsorption, diffusion and separation of gases in nanoporous carbon membranes[D]. Beijing: Beijing University of Chemical Technology, 2008.
[10] Gholampour F, Yeganegi S. Molecular simulation study on the adsorption and separation of acidic gases in a model nanoporous carbon[J]. Chemical Engineering Science, 2014, 117(1): 426-435.
[11] Yeganegi S, Gholampour F. Methane adsorption and diffusion in a model nanoporous carbon: an atomistic simulation study[J]. Adsorption, 2013, 19(5): 979-987.
[12] Gholampour F, Yeganegi S. Simulation of methane adsorption and diffusion in a CNT channel[J]. Chemical Engineering Science, 2016, 140(2): 62-70.
[13] Su J C, Lua A C. Experimental and theoretical studies on gas permeation through carbon molecular sieve membranes[J]. Separation & Purification Technology, 2009, 69(2): 161-167.
[14] Lithoxoos G P, Labropoulos A, Peristeras L D,. Adsorption of N2, CH4, CO and CO2gases in single walled carbon nanotubes: a combined experimental and Monte Carlo molecular simulation study[J]. The Journal of Supercritical Fluids, 2010, 55(2): 510-523.
[15] 雷广平, 刘朝, 解辉. H2S/CH4混合物在石墨烯表面吸附性能的分子动力学模拟[J]. 工程热物理学报, 2014, 35(3): 428-431.LEI G P, LIU Z, XIE H. Molecular dynamics simulations of adsorption performances for H2S/CH4mixture on graphene surface[J]. Journal of Engineering Thermodynamics, 2014, 35(3): 428-431.
[16] Lei G P, Liu Z, Xie H,. Separation of the hydrogen sulfide and methane mixture by the porous graphene membrane: effect of the charges[J]. Chemical Physics Letters, 2014, 599(4): 127-132.
[17] 温伯尧, 孙成珍, 白博峰. 多孔石墨烯分离CH4/CO2的分子动力学模拟[J]. 物理化学学报, 2015, 31(2): 261-267. WEN B Y, SUN C Z, BAI B F. Molecular dynamics simulation of the separation of CH4/CO2by nanoporous graphene[J]. Acta Physico-Chimica Sinica, 2015, 31(2): 261-267.
[18] Shan M X, Xue Q Z, Jing N N,. Influence of chemical functionalization on the CO2/N2separation performance of porous graphene membranes[J]. Nanoscale, 2012, 17(4): 5477- 5482.
[19] 赵昊瀚, 潘艳秋, 何流, 等. 炭膜分离CO2/CH4混合气的分子模拟[J]. 化工学报, 2016, 67(6): 2393-2400.Zhao H H, Pan Y Q, He L,. Molecular simulation on separation of CO2/CH4gas mixture with carbon membrane[J]. CIESC Journal, 2016, 67(6): 2393-2400.
[20] 张兵. 分子筛炭膜的制备、微结构及气体分离性能[D]. 大连: 大连理工大学, 2006.Zhang B. Preparation, microstructure and gas separation performance of molecular sieving carbon membranes[D]. Dalian: Dalian University of Technology, 2006.
[21] Fu S L, Sanders E S, Kulkarni S S,. Carbon molecular sieve membrane structure-property relationships for four novel 6FDA based polyimide precursors[J]. Journal of Membrane Science, 2015, 487(1): 60-73.
[22] Furukawa S, Sugahara T, Nitta T. Non-equilibrium MD studies on gas permeation through carbon membranes with belt-like heterogeneous surfaces[J]. Journal of Chemical Engineering of Japan, 1999, 32(2): 223-228.
[23] Furukawa S, Shigeta T, Nitta T. Non-equilibrium molecular dynamics for simulation permeation of gas mixtures through nanoporous carbon membranes[J]. J. Chem. En. Jpn., 1996, 29(4): 725-728.
[24] Jeon H J, Choi J H, Lee Y,. Highly selective CO2capturing polymeric organic network structures[J]. Advanced Energy Materials, 2012, 2(2): 225-228.
[25] 陈安亮. 炭膜的二氧化碳吸附扩散性能的研究[D]. 大连: 大连理工大学, 2012.Chen A L. The CO2adsorption and diffusion performances in carbon membrane[D]. Dalian: Dalian University of Technology, 2012.
[26] Ning X, Koros W J. Carbon molecular sieve membranes derived from Matrimid polyimide for nitrogen/methane separation[J]. Carbon, 2014, 66(1): 511-522.
[27] FU S L, WENZ G B, SANDERS E S,. Effects of pyrolysis conditions on gas separation properties of 6FDA/DETDA:DABA (3:2) derived carbon molecular sieve membranes[J]. Journal of Membrane Science, 2016, 520(24): 699-711.
[28] Fu S L, Sanders E S, Kulkarni S S,. Temperature dependence of gas transport and sorption in carbon molecular sieve membranes derived from four 6FDA based polyimides: Entropic selectivity evaluation[J]. Carbon, 2015, 95(1): 995- 1006.
[29] Langmuir I. The adsorption of gases on plane surfaces of glass, mica and platinum[J]. J. Am. Chem. Soc., 1918, 40(9): 1361-1403.
[30] 近藤精一, 石川达雄, 安部郁夫. 吸附科学[M]. 李国希, 译. 2版. 北京: 化学工业出版社, 2005: 96-101.Kondo S, Ishikawa T, Abe I. Kyuchaku no Kagaku[M]. LI G X, trans. 2nd ed. Beijing: Chemical Industry Press, 2005: 96-101.
[31] 曹伟, 吕玲红, 黄亮亮, 等. 不同管径碳纳米管中CO2/CH4分离的分子模拟[J]. 化工学报, 2014, 65(5): 1736-1742.Cao W, LÜ L H, Huang L L,. Molecular simulations on diameter effect of carbon nanotube for separation of CO2/CH4[J]. CIESC Journal, 2014, 65(5): 1736-1742.
Molecular simulation on separation of CO2/CH4gas mixture in carbon membranes with defect pore structure
HE Liu1, ZHAO Haohan2, LI Hua1, ZHOU Zirui1, WANG Tonghua1, PAN Yanqiu1
(1School of Chemical Engineering, Dalian University of Technology, Dalian 116024, Liaoning, China;2Shenyang Aluminum and Magnesium Engineering and Research Institute Company Limited, Shenyang 110001, Liaoning, China)
Three kinds of defect micropore models,, random defect, averaged defect and partial defect models, were established based on the defect-free zigzag pore model in carbon membrane. Adsorption and diffusion behaviors of equimolar CO2/CH4gas mixture within pores of carbon membrane were investigated in an effort to discuss the influences of pore defect in carbon membranes on gas separation. Results showed that under the operating temperatures ranging from 273 to 348 K, both equilibrium adsorption capacities and diffusion coefficients of CO2and CH4in the defect pore models were smaller than those of the defect-free pore model. Total CO2/CH4separation coefficient of the partial defect pore model was relatively low compared with the defect-free pore model and the other two defect pore models. When the temperature was less than 298 K, total separation coefficients of the random defect and averaged defect pore models were greater than the defect-free pore model, and the total separation coefficients of random defect pore model are beneficial to the averaged defect pore model. Random carbon atom deletion approach is more reasonable than average deletion and partial deletion. The results could provide a basis for the further study of gas permeation mechanism in carbon membranes.
molecular simulation; carbon dioxide; methane; carbon membranes; defect pore model
10.11949/j.issn.0438-1157.20161790
TQ 028.1
A
0438—1157(2017)08—3100—09
潘艳秋。第一作者:何流(1992—),男,博士研究生。
国家自然科学基金面上与重点项目(21176036,21376037);国家高技术研究发展计划项目(Z2012AA03A611)。
2016-12-22收到初稿,2017-03-28收到修改稿。
2016-12-22.
Prof. PAN Yanqiu, yqpan@dlut.edu.cn
supported by the National Natural Science Foundation of China (21176036, 21376037) and the National High Technology Research and Development Program of China (Z2012AA03A611).

