亚磷酸钠的生产工艺及结晶动力学研究
金 鑫,徐志高,2*,池汝安,黄晓慧,徐源来,周 芳
1.绿色化工过程教育部重点实验室(武汉工程大学),湖北 武汉 430205;2.中南民族大学催化材料科学国家民委-教育部暨湖北省重点实验室,湖北 武汉 430074;3.甘肃工业职业技术学院化工学院,甘肃 天水 741025
亚磷酸钠的生产工艺及结晶动力学研究
金 鑫1,徐志高1,2*,池汝安1,黄晓慧3,徐源来1,周 芳1
1.绿色化工过程教育部重点实验室(武汉工程大学),湖北 武汉 430205;2.中南民族大学催化材料科学国家民委-教育部暨湖北省重点实验室,湖北 武汉 430074;3.甘肃工业职业技术学院化工学院,甘肃 天水 741025
采用酸碱中和法制备亚磷酸钠并利用间歇动态法对亚磷酸钠的结晶动力学进行研究.借助电位滴定法分析亚磷酸中和过程的跃迁点,确定产物主要为亚磷酸氢二钠.探讨了中和反应温度、摩尔比和亚磷酸浓度等因素对反应产物的影响.利用激光粒度分析仪测试产品的粒度体积分数,根据粒数衡算和质量衡算关系经矩量变换法回归得到动力学方程,并探索影响产物晶体粒径的因素.结果表明:亚磷酸氢二钠生成的优化工艺为控制亚磷酸和氢氧化钠的摩尔比为1∶2,亚磷酸的浓度应控制在8.54 mol∕L以下,反应温度对其影响很小;亚磷酸和氢氧化钠很容易形成均匀细小的亚磷酸氢二钠,当粒度大于15 μm后,其晶体的生长与粒度无关,获得了亚磷酸氢二钠成核速率方程和成长速率方程;在亚磷酸氢二钠溶液结晶过程中,在介稳区的中部偏超溶解度曲线的位置加入少量粗晶径的晶种,控制蒸发温度在150℃左右,在200 r∕min搅拌速度下进行结晶,可以得到晶粒较大的亚磷酸氢二钠晶体.
亚磷酸钠;中和法;间歇动态法;结晶动力学
亚磷酸钠和次磷酸钠都是磷酸盐的新产品,在化工和材料领域应用较广,主要用做还原剂.次磷酸钠的还原性比亚磷酸钠强,将金、银、汞、镍、铬、钴等金属盐还原成相应的金属[1-2],可作为抗氧化剂用于纺织物整理及医药等行业[3],还因具有保鲜及抑菌作用,可作为食品添加剂使用[4].除此之外,次磷酸钠还可作为催化剂,加快化学反应速率[5].但由于次磷酸钠不稳定,加热易爆炸,受潮或加热后易分解产生一种易燃并且剧毒的气体PH3,导致应用过程中存在一些危险;另外,有一些反应需要弱还原性的还原剂,限制其应用.而亚磷酸钠的还原性较弱且较稳定,在一定程度上取代还原剂次磷酸钠,具有更好的稳定性和安全性.
亚磷酸钠盐主要是以亚磷酸氢二钠(Na2HPO3·5H2O)和 亚 磷 酸 二 氢 钠(NaH2PO3·2.5H2O)存在,两者均是结晶水合物.其主要用途是用作还原剂,可以将金属盐还原为相应的金属,还可以用作化学试剂,用来配制溶液或参加反应[6].除此之外,亚磷酸盐在微孔材料方面的应用也是当今研究的热点.亚磷酸盐以其HPO3“假四面体”取代PO4四面体,使得骨架中“阴离子”部分的对称性和电荷降低,从而使其结构发生较大变化,能够产生许多结构新颖的微孔亚磷酸盐[7].
国内外对于亚磷酸钠生产的相关研究较少,主要采用复分解反应从次磷酸钠的工业废渣中回收.王小妮[6]采用复分解法研究了从泥磷回收亚磷酸钠的工艺,所得产品纯度较低,且产品中的次磷酸钠和亚磷酸钠难以分离.王惠平等[8]用复分解法从次磷酸钠工业废渣中制得亚磷酸钠,然后用离子交换树脂法制得高纯亚磷酸,生产成本较高且操作步骤繁琐.
由于亚磷酸钠盐一般均需要从溶液中结晶析出,对其结晶动力学的研究显得尤为重要.结晶动力学测试的方法主要有连续稳态法、连续动态法和间歇动态法.其中连续稳态法[9]数据处理简单,但偏差大、测试周期长、工作量大和操作困难;连续动态法[10]偏差小,但测试周期很长;而间歇动态法[11]测试周期短、操作简单,在实际的工业结晶过程中应用较广.何兴学等[12]采用间歇动态法获得了醋酸钠的结晶动力学方程;党乐平等[13]采用间歇动态法得到了苊在乙醇溶液中的动力学方程;张迪[14]等用间歇动态法回归得到氯氧化铋在水中的结晶动力学方程.而对通过中和反应直接制备亚磷酸钠并研究其结晶动力学较少.
本文以氢氧化钠和亚磷酸为原料,采用中和法制备亚磷酸钠,对其结晶工艺及结晶动力学进行研究,以获得亚磷酸钠的优化工艺及结晶动力学方程,为工业化生产提供理论指导.
1 实验部分
1.1 实验原料
亚磷酸,国药集团化学试剂有限公司生产;氢氧化钠,天津博迪化工股份有限公司生产;亚磷酸氢二钠五水合物,阿拉丁试剂生产;碘化钾,阿拉丁试剂生产;碘,阿拉丁试剂生产;硫代硫酸钠,冰乙酸,国药集团化学试剂有限公司生产,以上药品均为分析纯.
1.2 仪器及装置

表1 主要实验仪器设备Tab.1 Main experimental instruments and equipment
1.3 实验方法
1.3.1 中和反应 将不同摩尔比的亚磷酸和氢氧化钠溶液,在烧杯中混合,并不断搅拌,反应一定时间后测定反应液的pH,然后蒸发结晶、过滤、洗涤、干燥和称重,计算亚磷酸钠的产率并根据国标方法 HG ∕T3253—2000[15]测定其纯度.
1.3.2 结晶动力学 向三口烧瓶中加入一定量的亚磷酸氢二钠和水,在一定的速度下搅拌,打开恒温系统,升温到100℃,然后自然降温一段时间后,加入定量晶种,每隔30 min用移液管取样,然后进行过滤、干燥和称重,并计算其悬浮密度,其粒度分布用粒度分析仪测定(见图1).
悬浮密度计算公式如下:

式中m1,m2分别指的是漏斗的质量和干燥后带有滤饼的漏斗的总质量;V指的是所取晶浆体积;MT为晶浆悬浮密度,kg∕m3.
产品粒数密度:

式中:Dωi为体积分数;kv为晶体体积形状因子;为测量相邻通道尺寸的平均值;D为测量相邻通道宽度;ρ为晶体密度.

图1 亚磷酸钠结晶动力学实验装置图Fig.1 Experimental setup for crystallization kinetics of sodium phosphite
2 结果与分析
2.1 电位滴定分析
以0.1 mol∕L的氢氧化钠标准滴定液为滴定剂,对20.0 mL 0.1 mol∕L的亚磷酸进行电位滴定,结果见图2所示.

图2 亚磷酸的电位滴定分析(插图:一阶微商图)Fig.2 Potentionmetric titration analysis of phosphoite acid(Inset:first order derivative diagram)
亚磷酸的电位滴定时存在两个拐点,对图2进行一阶微商,如图2中小图所示,可以看出亚磷酸的电位滴定存在两个非常明显的跃迁点.电位跃迁点将电位曲线分成三段,分别代表了亚磷酸电离出氢离子并被氢氧化钠中和的三个过程,即整个滴定过程亚磷酸有H3PO3→H2PO3-,H2PO3-→HPO32-,HPO32-→PO33-三个变化阶段,且在pH 6~8间主要是亚磷酸氢二钠.
2.2 温度对中和反应的影响
以 1.0 mol∕L H3PO3和 1.0 mol∕L NaOH 溶 液为原料进行中和反应,控制反应的摩尔比n(H3PO3)∶n(NaOH)分别为0.75、0.8、1.0、1.2、1.25、1.4、1.5、1.6、1.8、2.0和2.5,在不同的温度下混合反应1 h,然后测其pH(图3).

图3 温度对反应产物的影响Fig.3 Effects of temperature on reaction products
可以看出不同温度下的pH曲线基本稳定的重合于一条曲线上,说明温度对中和反应的影响微小,可以忽略不计.
2.3 摩尔比对亚磷酸钠纯度的影响
以 1.0 mol∕L H3PO3和 1.0 mol∕L NaOH 溶 液 为原料,控制反应的摩尔比n(H3PO3)∶n(NaOH)分别为 0.8、1.0、1.2、1.4、1.6、1.8、2.0和 2.2进行中和反应,反应后测结晶产品的产率和纯度(图4).
随着摩尔比的增加,产率和纯度逐渐增加.但当摩尔比超过1∶2后,其产率及纯度开始出现下降,可能是由于氢氧化钠含量过多使得过量的氢氧化钠从溶液中沉淀出来,从而影响到亚磷酸钠盐产物的质量.
2.4 亚磷酸浓度对于反应产物的影响
配制浓度为 7.32 mol∕L、8.54 mol∕L、9.75 mol∕L和 10.96 mol∕L 的 H3PO3溶 液以及 13.00 mol∕L 的NaOH 溶液,分别按摩尔比 1∶1.8、1∶1.85、1∶1.9、1∶1.95和1∶2.0的溶液混合,然后测其pH(见图5).
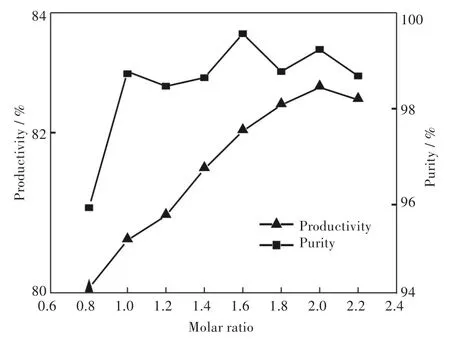
图4 摩尔比对反应产物的影响Fig.4 Effects of molar ratio on reaction products

图5 酸浓度对反应产物的影响Fig.5 Effects of acid concentration on reaction products
当摩尔比在1∶1.95以下时,所得产品的pH在7~8,根据图2结果可知主要为亚磷酸氢二钠;当摩尔比超过1∶1.95且亚磷酸浓度超过9.75 mol∕L后,产品中有过量的氢氧化钠会析出晶体,影响最终产品纯度.因此亚磷酸浓度最好控制在8.54 mol∕L以下.
2.5 亚磷酸氢二钠粒度分析
采用W2308c激光粒度分析仪测定所制得产品的粒度体积分数,根据式(2)计算粒数密度分布,结果如图6所示.
可以看出,当亚磷酸氢二钠粒度大于15 μm时,粒度密度分布的自然对数ln(n)与粒径d成良好的线性关系,说明在该粒数范围内亚磷酸氢二钠晶体的生长与粒度无关;当粒度小于15 μm时,ln(n)-d也成良好的线性关系;而在粒度为 15 μm时,粒数密度分布有一个拐点,说明亚磷酸氢二钠很容易形成非常均匀、细小的颗粒,然后再相互结合而长大,没有长不大的晶体,与常规的结晶过程略有不同[16].

图6 亚磷酸氢二钠粒数密度分布Fig.6 Population density distributions of disodium hydrogen phosphite
2.6 亚磷酸氢二钠结晶动力学
对实验得到的样品进行分析,获得不同温度下的溶液过饱和度S、溶液的悬浮密度MT以及样品的粒度分布,根据粒数衡算和质量衡算关系经矩量变换法计算,获得相应时间间隔下的成核速率B0,经回归得到反应结晶的成长速率方程G:

2.7 影响晶体粒径的因素讨论
2.7.1 晶种粒度对产品粒度的影响 在结晶的过程中,晶体产品的粒度分布是考察产品质量的一个重要因素,晶体产品的主粒度大且分布集中可以使得简化过滤操作.试验中,考察了未加入晶种以及加入不同粒径晶种对产品粒度分布的影响,如图7所示.

图7 晶种对产品粒径的影响Fig.7 Effects of added seed on product particle sizes
加入晶种后产品粒径得到了明显的增大,且加入粒度大的晶种所得产品粒度也较大,加入粒度小的晶种所得产品粒度也较小.其原因可能是晶种的粒度越小则表面积就越大,晶体的可生长点就越多,导致晶体的生长不够集中,产品的粒度偏小且不集中.因此,加入粒度大的晶种有利于获得粗颗粒的产品.
2.7.2 晶种加入时间对产品粒度的影响 确定了加入晶种的条件后,晶种的加入时机也是需要考虑的因素.试验中,考察了加入晶种的时机对产品粒度的影响(见图8).
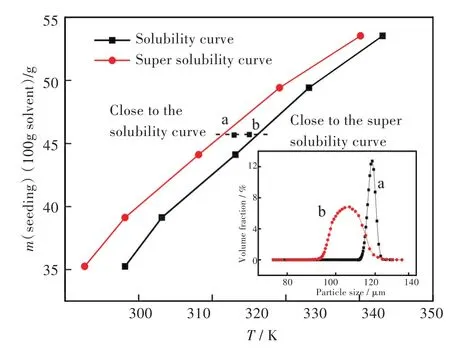
图8 晶种加入时机对产品粒径的影响Fig.8 Effects of seeding time on product particle sizes
选择在介稳区中a和b两个点时分别加入晶种,其对产品粒度的影响见小图,在靠近溶解度曲线的b点时加入晶种,晶种的加入对于产品的粒度影响很小,其原因可能是此时加入的晶种会部分溶解到溶液中;而在靠近超溶解度曲线的a点时加入晶种,可使产品的粒度变大.因此选择晶种加入的时机应在介稳区的中部偏超溶解度曲线的位置.2.7.3 搅拌速率对产品粒度的影响 在结晶的过程中,流体条件对于粒子的成核与生长有重要的影响,而搅拌速率又是影响流体力学的重要参数.试验中,考察了不同搅拌速率对产品粒度分布的影响(见图9).
当转速为425 r∕min以上时,产品粒度较小且分布不均匀,表明当转速较大时不利于晶体的生长,可能是过大的搅拌速率将晶核打散,使得出现很多细小的粒子.而就粒度大小比较可以看出,低速搅拌对粒度的增大更有利一些.200 r∕min时粒径大,且分布较150 r∕min时更窄,所以搅拌速率选择 200 r∕min.
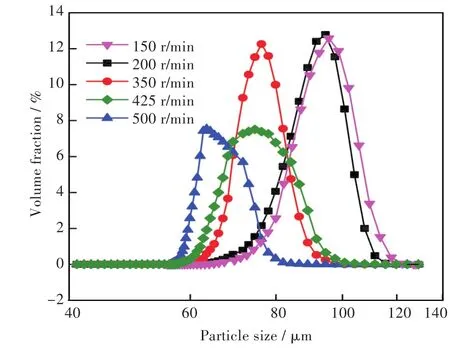
图9 搅拌速率对产品粒度的影响Fig.9 Effects of stirring rate on product particle sizes
2.7.4 蒸发温度对产品粒度的影响 过饱和度在结晶的过程中对于晶体的成核和生长具有决定性的作用,而蒸发温度又是过饱和度产生的一个重要因素.试验中,考察不同蒸发温度下的产品粒度分布的影响(见图10).

图10 蒸发温度对产品粒度的影响Fig.10 Effects of evaporation temperature on product particle sizes
由图10可知,蒸发温度为150℃时粒径较大,且分布较窄,当蒸发温度过高时,晶体的粒度偏小,其原因主要是过高的温度使得溶液中的晶体运动加剧,使得晶体与结晶器壁碰撞增多,形成细小的晶体;若蒸发温度过低,晶体在不断长大,但粒径分布较宽.因此,选择150℃蒸发结晶.
3 结 语
1)在亚磷酸钠中和反应中,亚磷酸和氢氧化钠的摩尔比应控制在1∶2左右,亚磷酸的浓度应控制在8.54 mol∕L以下,主要生成亚磷酸氢二钠,反应温度对其影响很小.
2)亚磷酸和氢氧化钠很容易形成均匀细小的亚磷酸氢二钠,当粒度大于15 μm后,其晶体的生长与粒度无关.采用间歇法测得亚磷酸氢二钠结晶动力学,其成核速率方程为B0=4.73×109G1.32M,成长速率方程为G=4.69×10-6S1.06.
3)在亚磷酸氢二钠溶液结晶过程中,选择处于介稳区中部偏向超溶解度曲线时加入少量粒度大晶种,并控制蒸发温度在150℃左右,200 r∕min搅拌速度下结晶,得晶粒较大亚磷酸氢二钠晶体.
[1]TOUIR R,LARHZIL H,EBNTOUHAMI M,et al.Electroless deposition of copper in acidic solutions using hypophosphite reducing agent[J].Journal of Applied Electrochemistry,2006,36(1):69-75.
[2]CHENG D H,XU W Y,ZHANG Z Y,et al.Electroless copper plating using hypophosphite as reducing agent[J].Metal Finishing,1997,95(1):34,36-37.
[3]熊家林,刘钊杰,贡长生.磷化工概论[M].北京:化学工业出版社,1994.
[4]马一平,王惠平.次磷酸钠的生产应用[J].江苏化工,1998,26(3):41-42.MA Y P,WANG H P.Production ofsodium hypophosphite[J].Jiangsu Chemical Industry,1998,26(3):41-42.
[5]陈克宁,贾炳颖,王超.次磷酸钠在CA整理体系中的催化作用[J]. 印染,2002(7):1-3,52.CHEN K N,JIA B Y,WANG C.Catalysis of sodium hypophosphite in CA finishing system[J].Printing and Dyeing,2002(7):1-3,52.
[6]王小妮.泥磷回收产品的净化提纯研究[D].昆明:昆明理工大学,2011.
[7]马红微,左萌萌,黄亮亮.亚磷酸盐微孔化合物研究进展[J]. 科技导报,2015,33(7):100-107.MA H W,ZUO M M,HUANG L L.Progress of metal phosphatemicroporouscompounds[J]. Science&Technology Review,2015,33(7):100-107.
[8]王惠平,马一平.从次磷酸钠生产废渣中提取亚磷酸[J]. 江苏化工,1998(4):21-23.WANG H P,MA Y P.Extraction of phosphorous acid from waste residue from sodium hypophosphite[J].Jiangsu Chemical Industry,1998(4):21-23.
[9]RANDOLPHAD,LARSONMA.Transient and steady-state distributions in continuous mixed suspension crystallizers[J].Aiche Journal,1962,8:639-645.
[10]SOWUL L E M.Crystallization kinetics of sucrose in a MSMPR evaporative crystallizer[J]. Industrial&Engineering Chemistry Process Design&Development,1981,20(2):197-203.
[11]TAVARE N S,GARSIDE J.Simultaneous estimation of crystalnucleation and growth kineticsfrom batch experiments[J].Chemical Engineering Research&Design,1986,4:109-118.
[12]何兴学.醋酸钠结晶动力学研究[D].杭州:浙江工业大学,2012.
[13]党乐平,王占忠,刘朋标,等.苊冷却结晶动力学的间歇动态法研究[J]. 化学工程,2010(4):17-20.DANG L P,WANG Z Z,LIU P B,et al.Cooling crystallization kinetics of acenaphthene by using a batch dynamic method[J].Chemical Engineering,2010(4):17-20.
[14]张笛,肖清贵,张炳烛,等.氯氧化铋反应结晶动力学研究[J]. 无机盐工业,2014(9):16-20.ZHANG D,XIAO Q G,ZHANG B Z,et al.Study on reaction crystallization kinetics of bismuth oxychloride[J].Inorganic Chemicals Industry,2014(9):16-20.
[15]全国化学标准化技术委员会.工业次磷酸钠:HG∕T 3253—2000[S]. 北京:中国标准出版社,2000.
[16]CHEMALY Z,MUHR H,FICK M.Crystallization kinetics of calcium lactate in a mixed-suspensionmixed-product removed crystallizer[J].Industrial&Engineering Chemistry Research,1999,38:2803-2808.
本文编辑:张 瑞
Manufacturing Technique and Crystallization Kinetics of Sodium Phosphite
JIN Xin1,XU Zhigao1,2*,CHI Ru’an1,HUANG Xiaohui3,XU Yuanlai1,ZHOU Fang1
1.Key Laboratory of Green Chemical Process(Wuhan Institute of Technology),Ministry of Education,Wuhan 430205,China;2.Key Laboratory of Catalysis and Materials Science of the State Ethnic Affairs Commission&Ministry of Education,Hubei Province,South-Central University for Nationalities,Wuhan 430074,China;3.School of Chemical Engineering,Gansu Industry Polytechnic College,Tianshui 740125,China
The sodium phosphite was prepared by acid-base neutralization method,and the crystallization kinetics in the crystallization process was investigated by the intermittent dynamic method.In acid-base neutralization experiment,the effects of reaction temperature,molar ratio and phosphorous acid concentration on reaction products were discussed.It was found that the optimized process for the production of disodium hydrogen phosphite was to control the molar ratio(phosphorous acid:sodium hydroxide) at 1∶2 and the concentration of phosphorous acid below 8.54 mol∕L.Meanwhile,the reaction temperature had little effect on the reaction.In the crystallization process,phosphoric acid and sodium hydroxide were easy to form the uniform crystal particle shape,then the growth of crystal could be expressed by the size-independent growth model when the particle size was larger than 15 μm.The nucleation rate equation and growth rate equation of disodiumhydrogen phosphite were obtained.In addition,the factors influencing the product partical size were discussed.A larger crystal of disodium hydrogen phosphite crystals can be obtained at a evaporation temperature of about 150 ℃ ,stirring speed of 200 r∕min and adding a small amount of coarse seeds at the position of the central partial in the metastable zone bias over super solubility curve.
sodium phosphite;neutral method;intermittent dynamic method;crystallization kinetics
TQ013.2
A
10.3969∕j.issn.1674⁃2869.2017.04.001
2017-03-29
湖北省磷资源开发利用协同中心创新开放基金(P201111);湖北省教育厅优秀中青年科技创新团队项目(T201506)
金 鑫,硕士研究生.E-mail:854433482@qq.com
*通讯作者:徐志高,博士,副教授,硕士研究生导师.E-mail:xuzhigaotc@126.com
金鑫,徐志高,池汝安,等.亚磷酸钠的生产工艺及结晶动力学研究[J].武汉工程大学学报,2017,39(4):307-312.
JIN X,XU Z G,CHI R A,et al.Manufacturing technique and crystallization kinetics of sodium phosphite[J].Journal of Wuhan Institute of Technology,2017,39(4):307-312.
1674-2869(2017)04-0307-06

