金@氧缺陷二氧化钛核壳纳米颗粒的制备及光催化产氢
寇书芳 封振宇 王春省 杨 剑
金@氧缺陷二氧化钛核壳纳米颗粒的制备及光催化产氢
寇书芳 封振宇 王春省 杨 剑*
(山东大学化学与化工学院,济南 250100)
通过水解TiCl3在金纳米颗粒外表生长TiO2,然后在Ar/H2气氛中高温煅烧成功地合成了核壳形貌的Au@H-TiO2缺陷结构。采用XRD、TEM、XPS、UV-Vis测试方法对产物的物相结构、形貌及光吸收能力做了系统的分析。与不存在缺陷态的TiO2和Au@A-TiO2相比,Au@H-TiO2表现出最高的产氢速率,这可以归因于其电荷分离效率的提高和电荷转移阻抗的降低,瞬态光电流测试以及电化学阻抗数据证实了这一结论。这些性能的改进可能与Au@H-TiO2中的Ti3+自掺杂和Au修饰有关。
二氧化钛;缺陷结构;纳米材料;光催化制氢
0 引 言
二氧化钛作为一种常见的光催化材料,在催化领域一直被广为研究。为了提高其光催化性能,人们对TiO2进行了各种各样的改性研究,较为常见的有金属[1]或非金属掺杂[2-3]、形状/尺寸控制[4-6]以及氢化处理[7-9]等等。其中,氢化处理即引入氧空位缺陷成为最近的一大研究热点。氢化处理可以引起材料的结构变化[10-13],同时改善光学性质、电子特性以及光催化性能[11-14]等。这是因为Ti3+在电子/空穴的转移过程中起到重要作用[15],引入氧空位缺陷的二氧化钛(H-TiO2)作为一个电子供体,可以提高光催化反应中染料分子的吸附稳定性,还能促进电荷的注入[16]。H-TiO2的上述性质使其在光催化、电化学等领域有着广泛的应用,并表现出优异的催化性能,例如光催化降解有机染料、光催化制氢、光电化学水裂解、染料敏化太阳能电池以及锂离子电池等[17-19]。
对Au修饰后的TiO2材料进行氢化处理或者氢化后的TiO2材料修饰Au可以有效地将贵金属修饰以及氢化还原处理两种手段相结合,利用两者的协同作用,更大程度地改进TiO2的催化性能,然而这种研究报道相对来说还很少。据我们了解,Montini和Santo的课题组通过对金属纳米颗粒担载的TiO2材料进行氢化处理成功地合成了单金属以及双金属(Pt-Au)修饰的氢化TiO2纳米颗粒,该复合材料在光催化产氢方面显示了卓越的性能优势[20-21]。此外,Xu的课题组室温条件下在氧缺陷富集的TiO2上沉积金纳米颗粒,实验表明金属颗粒的生成与沉积是通过TiO2表面上氧空位上的电子向溶液中的金离子转移实现的。文章还提到该催化剂在染料的光催化降解方面表现出良好的活性和稳定性[22]。这些工作都表明将氢化处理与金属修饰相结合,可以有效地改善材料的催化性能。两种手段都可以提高TiO2在可见光范围内的吸收能力,同时提高电荷的分离效率。但是,这些工作有一个共同之处,金属颗粒都是担载在TiO2的表面,这有利于电子和空穴的及时消耗扩散,提高催化的循环稳定性,但同时表面上的金属颗粒很容易团聚、被腐蚀甚至脱落到溶液中,可能因此使得催化剂失活[23-24]。而将金属颗粒包覆于TiO2内部可以有效地解决这一问题。
在本工作中,我们首先通过室温水解的方法,在金颗粒表面生长一层TiO2,然后在还原气氛Ar/ H2中高温煅烧得到氢化材料Au@H-TiO2。对产物进行催化产氢测试,发现氢化产物相较于同样条件下空气气氛煅烧得到的Au@A-TiO2以及A-TiO2,产氢速率有了明显的提升。对各种催化剂进行光学性质研究、瞬态光电流响应测试、电化学阻抗测试,证明在还原气氛中氢化处理以及金属颗粒的存在都可以改善催化剂的吸收能力、提高光生电荷的分离效率、降低电荷转移阻力。此外,我们合成了具有不同尺寸Au核的氢化核壳产物,并对其光催化性能进行了系统的研究。
1 实验部分
1.1 材料准备与合成
所有的试剂使用前未经过任何纯化处理。
聚苯乙烯磺酸钠包覆的Au纳米颗粒(PSS-Au)的制备。首先是PSS溶液的配制:取10 mL去离子水于干净的50 mL烧杯中,称取一定质量的PSS和氯化钠,使PSS和NaCl的浓度分别为2 g·L-1、6 mmol·L-1。在配制好的PSS溶液中,逐滴加入10 mL的金纳米颗粒溶液,搅拌至少4 h,离心,取净上层清液,沉淀物重新分散在200μL去离子水中,备用。高质量的金纳米颗粒是通过典型的晶种法合成得到的[25],共有3种不同尺寸:20、35、50 nm,使用之前离心一次,调吸光度约为2.0,具体制备过程见supporting information。
Au@TiO2核壳结构的制备[26]:核壳结构的合成过程是在干净的玻璃瓶中进行的。取6 mL去离子水,加入200μL提前配好的TiCl3水溶液(TiCl3含量为17.1%;HCl含量为20%),随后逐滴加入一定体积的0.93 mol·L-1NaHCO3溶液,并快速加入上述PSS-Au溶液。室温下反应30 min后,将反应产物分别用水和乙醇多次洗涤,并重新分散在少量乙醇中,60℃下过夜干燥,产物标记为Au@TiO2。利用不同尺寸的Au颗粒得到的Au@TiO2产物分别标记为Au@TiO2-20、Au@TiO2-35、Au@TiO2-50,三者的壳层厚度基本一致。
将上述产物置于磁舟中,在450℃条件下,还原气氛Ar/H2(5%H2,95%Ar,V/V)中煅烧2 h,自然冷却至室温后产物标记为Au@H-TiO2,待用。为了正确区分,我们将在空气气氛中同样条件下煅烧得到的样品标记为Au@A-TiO2。
1.2 样品测试与表征
产物的物相及晶体结构是通过X射线粉末衍射仪(XRD,德国,Bruker D8 Advance,Cu Kα,Cu靶,Kα波长为λ=0.154 18 nm,工作电压:40 kV,工作电流:40 mA,扫描范围:20°~80°)测试所得。样品的形貌、大小以及分散情况是由透射电子显微镜(TEM,JEM-1011,日本,加速电压100 kV)表征。紫外-可见分光光度计(UV-Vis,日本岛津,UV-2450型)用来检测样品的吸收光谱。X射线光电子能谱仪(XPS,ESCALAB 250,Thermal Fisher)对样品的表面元素化学组成及化学态进行测试分析研究,在XPS实验数据处理过程中,污染碳C1s电子结合能选择(284.6 eV)对样品光谱峰位进行校正。
1.3 光电化学测试
所制备样品的瞬态光电流测试以及交流阻抗测试分别通过电化学工作站CHI-760E(上海辰华)以及AUTOLAB PGSTAT204完成。两种电化学工作站均为标准的三电极体系,铂网作为对比电极,Ag/AgCl作为参比电极。工作电极的制备过程如下:称取15 mg固体粉末催化剂,将其分散在一定比例的乙醇/萘酚(0.5%)溶液中,超声使粉末尽量分散均匀。然后,将上述混合物均匀滴在面积为1.5 cm2的ITO导电玻璃上,室温下晾干。电解质溶液为0.5 mol·L-1Na2SO4溶液。开始进行电化学测试之前,整个实验体系都在高纯氮气气氛下吹扫30 min。用波长范围为320~780 nm的Xe弧光灯(XPS700,北京泊菲莱科技有限公司)作为光源,在0.5 V的电压条件下,测试样品光照以及未光照时的光电流。在不加偏压的情况下测试样品的交流阻抗。电化学工作站的工作频率范围为100~0.01 kHz。
1.4 光催化性能测试
光催化制氢测试是衡量催化剂催化性能的一个有力手段。具体实验过程如下:以25 mL的玻璃瓶为反应器,称取2.5 mg的催化剂,将其混合于体积比为1∶1的去离子水/甲醇溶液中,超声使其分散更为均匀。以翻口橡胶塞封闭体系,在开始制氢反应之前,对整个体系通最少0.5 min的高纯氩气,以尽量排除反应体系中的氧气以及溶液中的溶解氧。然后,在300 W氙灯(波长范围320~780 nm)的照射下进行光催化制氢反应。每隔1 h,利用体积为0.5 mL的微量注射器(HAMILTON)在瓶内采集气体,随之将气体注入带有热导检测器(TCD)的气相色谱分析仪(FULI GC-9790II,福立)中进行分析检测。催化剂的循环稳定性测试过程如下:将每次催化完成后的催化溶液离心,得到的固体催化剂重新进行光催化制氢反应,总共循环5次。之后,将催化剂离心、洗涤,对其进行TEM测试,观察形貌变化。
2 结果与讨论
2.1 产物形成过程及结构分析

图1 产物形成过程示意图Fig.1 Illustration on the formation process of core-shell nanoparticles
产物形成过程的简单示意图如图1所示。首先室温下通过TiCl3的水解在金纳米颗粒表面生长一层无定型的二氧化钛,初始的三价态钛离子在溶液中溶解氧分子的作用下很容易被氧化成四价态,生成TiO2的壳层。然后,将所得的Au@TiO2核壳结构在不同的气氛中450℃条件下煅烧2 h,分别得到Au@A-TiO2(空气气氛)、Au@H-TiO2(Ar/H2)。
我们以Au@H-TiO2-20为例,对不同处理条件下得到的核壳产物的性质进行研究对比。图2为不同催化剂的XRD图,煅烧前的样品Au@TiO2的衍射图中只有Au的衍射峰,并没有TiO2的峰,说明水解所得的壳层为无定型TiO2。这是由于壳层二氧化钛TiO2是在室温下进行水解反应所得,因而结晶性差。高温煅烧有利于壳层结晶性的提高,TiO2从无定型转为锐钛矿,因此经过热处理后样品的衍射峰中均出现锐钛矿二氧化钛的峰。
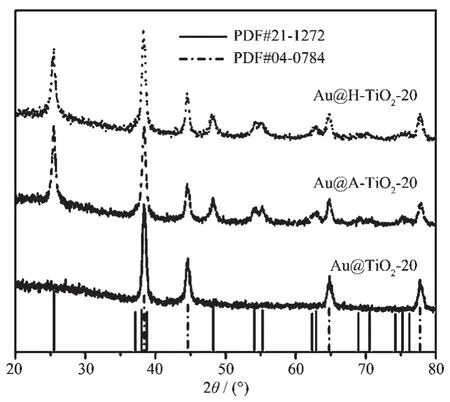
图2 不同催化剂的X射线粉末衍射图,图中底部给出的是金属Au(PDF#04-0784)以及TiO2(PDF#21-1272)的标准粉末衍射峰位置Fig.2 XRD patterns of different samples,Bottom bars present the standard diffractions of Au(PDF#04-0784)and TiO2(PDF#21-1272)
图3为基于20 nm大小的Au颗粒合成的不同核壳产物的电镜照片。从图中我们可以清楚地看到,初始的Au颗粒表面生长了一层TiO2,壳层的厚度平均为(26.5±1.6)nm,且表面粗糙。壳层的生长是通过TiCl3的水解反应实现的。金颗粒表面的活性剂PSS本身带负电,有利于带正电的Ti3+吸附于Au颗粒表面,而Ti3+在水溶液中不稳定,水解后会产生TiOH2+,然后被溶液中的溶解氧氧化成Ti4+,形成TiO2壳层,均匀的包覆在Au球表面。较低的水解温度、较慢的水解速率有效地避免了TiO2的自发成核,保证其在金纳米颗粒表面均匀的生长。经过煅烧后,样品保持了原有的核壳结构,且Au颗粒的尺寸及形貌均未发生明显变化。但是,样品的壳层厚度发生了变化,热处理后壳层的平均厚度为(20.2± 1.1)nm。壳层的收缩可能是因为在高温下,无定型二氧化钛中夹杂的溶剂得以释放,同时壳层的收缩使得TiO2自身结构以及Au颗粒与TiO2之间的接触更为紧凑,这会促进电荷的分离,从而提高光催化能力[22,27-28]。

图3 不同处理条件所得产物的TEM照片Fig.3 TEM images of the samples treated under differentconditions
2.2 产物的X射线光电子能谱分析
同样以20 nm尺寸的金颗粒为例,我们测试了不同气氛煅烧所得的金@二氧化钛核壳结构的XPS数据,如图4所示。从图(a)上部分的图中可以看出,Au@H-TiO2的Ti2p峰相较于Au@A-TiO2向低结合能方向移动,这说明氢化处理会导致壳层TiO2中的部分Ti元素价态降低。将两者的Ti2p数据相减得到图4(a)下部分的图,458.9和465.1 eV处的峰分别对应于四价钛离子的 Ti2p3/2、Ti2p1/2[29];458.1和463.5 eV处的峰则分别对应于三价钛离子的 Ti2p3/2、Ti2p1/2[30-31]。这表明还原气氛煅烧在壳层TiO2中成功引入了三价钛。Au@A-TiO2以及Au@HTiO2的O1s峰的分析数据如图4(b)所示。两者的O1s峰均在530.0 eV处有一个拟合峰,这对应TiO2中的Ti-O的结合能[29]。此外,相较于空气气氛中煅烧得到的产物,氢化后的产物在较高结合能位置532.2 eV处的拟合峰比例增大,这说明氢化处理会给核壳结构的表面引入更多的Ti-OH基团[31-32]。

图4 不同样品的X射线光电子能谱分析Fig.4 XPS spectra ofdifferentsamples
2.3 产物的光学、电化学、催化性能分析
缺陷态TiO2对产物的紫外-可见吸收光谱有着显著的影响。由图5(a)可知,与空气中煅烧所得产物A-TiO2相比,Au@TiO2-20在不同的气氛中煅烧后得到的产物的吸收能力均有所增强。其中,Au@HTiO2-20的吸收能力相较于Au@A-TiO2-20增强幅度更大,这归因于外层氢化的TiO2上的Ti3+以及氧空位缺陷的存在。因为氢化材料所存在的Ti3+以及氧空位缺陷会导致价带拖尾、增强材料的可见光吸收能力[33]。
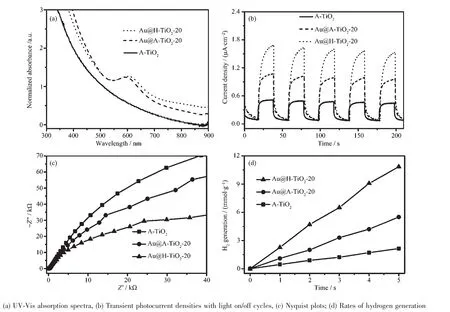
图5 不同产物的各性质分析图Fig.5 Analysis on different properties of various samples
在光催化反应中,电子-空穴的分离效率起着重要的作用,而瞬态光电流的大小可以反映光催化剂中电荷的分离效率,光电流值越大说明电荷的分离效率越高。由图5(b)可以看出,在波长范围为320~780 nm的光照射下,Au@A-TiO2-20的电流值大于同样条件下处理所得的A-TiO2,这是因为Au与TiO2接触之后,两者界面处会形成一个肖特基结,由于Au的费米能级位置相对较低,因此光生电子会从TiO2转移到Au上,这就有效地提高了电子-空穴的分离效率[34-35]。此外,Au@H-TiO2-20与Au@A-TiO2-20相比,光电流值有着明显的增强,这说明在还原气氛中进行热处理,可以有效地提高电子-空穴的分离效率,提高样品的光催化性能。
光生电子产生后在电极表面与电解质溶液间的迁移速率同样对催化剂的光催化活性有着至关重要的影响。一般来讲,交流阻抗曲线的半径越小,电子迁移速率越高。图5(c)为3种不同催化剂的交流阻抗图谱。从图中可以看出,Au@H-TiO2相较于Au@A-TiO2和A-TiO2有着更小的半径,这说明在还原气氛中得到的氢化材料的电荷迁移阻力较小,因此,界面处的电子迁移速率最高,同时极大地减少了光生载流子的复合几率。
将3种不同的催化剂进行光催化制氢性能评估,结果如图5(d)所示。从图中我们可以看出,无定型二氧化钛经过空气热处理过后的产物A-TiO2的产氢速率约为0.452 mmol·h-1·g-1,而同样条件处理得到的核壳结构Au@A-TiO2-20的产氢速率则为1.102 mmol·h-1·g-1,这是因为贵金属Au的存在提高了电子-空穴的分离效率,从而改善TiO2的光催化能力。此外,经过还原气氛Ar/H2处理的产物Au@H-TiO2-20的产氢速率提高至2.269 mmol·h-1· g-1。由于其与Au@A-TiO2-20唯一的区别在于热处理气氛的不同,因此产氢性能的提升应该是来源于氢化的壳层中存在的三价钛离子以及氧空位缺陷。据文献报道,还原气氛所带来的这些缺陷可以窄化材料的带隙,有效地增强光吸收能力[13,35],进而提高催化效率。
我们对Au@H-TiO2-20进行了光催化产氢的循环稳定性测试。从图S1中可以看出,经过5次循环后,催化剂仍保持了较高的产氢效率,下降的幅度并不明显,效率下降可能是因为在循环过程中离心时催化剂会有不同程度的损失。另一方面,我们对循环后的催化剂离心、洗涤,利用透射电子显微镜对其形貌进行表征,如图S2所示,进行多次催化反应后,催化剂的结构基本保持不变,这说明其具有良好的稳定性。
2.4 基于不同尺寸的金核所得氢化产物的性能评价
我们还对具有不同尺寸金核的氢化产物进行了系统研究。与上述Au@H-TiO2-20类似,Au@HTiO2-35及Au@H-TiO2-50与煅烧之前相比较,仍保持了核壳结构,且壳层出现收缩现象,即壳层厚度变薄,煅烧前后的电镜照片如图S3所示。图6(a)为各产物的粉末X射线衍射图。随着金纳米颗粒尺寸的增大,氢化产物中金所占的比例增加,因此Au所对应的衍射峰相对强度越来越高,这说明缺陷态TiO2在整个体系中所占的比重随着Au尺寸的增大而 减小。

图6 基于不同尺寸的Au颗粒所得氢化核壳产物的(a)XRD图,图中底部给出的是金属Au(dash-dot)以及TiO2(solid)的标准粉末衍射峰位置;(b)产氢速率图Fig.6 XRD patterns ofdifferent hydrogenated products based on different-sized Au core,Bottom bars present the standard diffractions of Au(dash-dot)and TiO2(solid);(b)Rates of hydrogen generation
此外,金颗粒尺寸增大使Au的特征吸收峰向长波长方向移动,从而样品的吸收峰会发生明显的红移,如图S4(a)所示。同时,吸收峰短波长方向的吸收相对强度降低,这是壳层在颗粒整体中所占的比重逐渐降低所致。不同的吸收能力以及吸收峰位置使得3种不同样品的水溶液颜色存在差异,如图S4(b)所示,随着Au核尺寸的增大,氢化核壳产物的水溶液颜色由灰蓝色逐渐变为绿色。如图6(b)所示,随着Au核尺寸的增大,氢化产物的产氢速率呈下降趋势。Au@H-TiO2-20、Au@H-TiO2-35、Au@HTiO2-50所对应的产氢速率分别为2.269、1.888和1.552 mmol·h-1·g-1。这说明Ti3+以及氧空位缺陷对催化剂的光催化制氢能力有着显著的影响。Au核的尺寸越小,催化剂的比表面积就相应的越大,越有利于制氢反应的进行,不同样品的比表面数值见表S1。
在该体系的催化过程中,金主要起到提高电子转移速率以及实现电子-空穴有效分离的作用,这一点在我们之前报道的工作进行过详细的阐述[36]。如图7所示,因为TiO2与Au的直接接触会在界面处形成一个肖特基势垒,由于Au的费米能级位置相对较低,因此光生电子会从TiO2转移到Au上,直至两者的费米能级达到平衡处于同一位置上,这就有效地提高了电子-空穴的分离效率,抑制了载流子的复合,改善催化剂的催化能力。此外,壳层良好的结晶性保证了电子在核壳之间的快速迁移。

图7 Au@H-TiO2体系中光催化产氢的潜在机理及电子转移路径示意图Fig.7 Schematic illustration of proposed mechanism for H2evolution and electron transfer pathways in Au@H-TiO2
3 结 论
在该工作中,我们先通过室温下的水解反应得到不同尺寸的Au@TiO2核壳纳米颗粒,然后利用还原气氛中高温煅烧的方法成功合成氢化核壳产物Au@H-TiO2。高温氢化改善了壳层结晶性的同时,保持了原有样品的核壳结构,并且在壳层二氧化钛上成功引入Ti3+以及氧空位缺陷,将金属修饰以及氢化自掺杂两种改性手段有效地结合。以光催化制氢反应为模型评价催化剂的光催化性能,实验结果表明氢化产物Au@H-TiO2的催化性能明显高于其它催化剂,Au@H-TiO2>Au@A-TiO2>A-TiO2。此外,工作还对不同尺寸的Au纳米颗粒所得的氢化核壳产物进行了系统的性能对比。
Supporting information is available athttp://www.wjhxxb.cn
[1]Zheng Z K,Huang B B,Meng X D,et al.Chem.Commun., 2013,49:868-870
[2]Zhang H J,Chen G,He X D,et al.Mater.Res.Bull.,2012, 47:4483-4486
[3]Jung S M,Choi I T,Lim K,et al.Chem.Mater.,2014,26: 3586-3591
[4]Yang H G,Sun C H,Qiao S Z,et al.Nature,2008,453:638-641
[5]Wang Z Y,Lv K L,Wang G H,et al.Appl.Catal.B,2010, 100:378-385
[6]Sun W,Zhou S X,You B,etal.Chem.Mater.,2012,24:3800-3810
[7]Zuo F,Wang L,Wu T,et al.J.Am.Chem.Soc.,2010,132: 11856-11857
[8]Liu L,Chen X B.Chem.Rev.,2014,114:9890-9918
[9]Xia T,Zhang Y L,Murowchick J,et al.Catal.Today,2014, 225:2-9
[10]Lu Z G,Yip C T,Wang L P,et al.ChemPlusChem,2012, 77:991-1000
[11]Naldoni A,Allieta M,Santangelo S,et al.J.Am.Chem. Soc.,2012,134:7600-7603
[12]Li G C,Zhang Z H,Peng H R,et al.RSC Adv.,2013,3: 11507-11510
[13]Wang Z,Yang C Y,Lin T Q,et al.Adv.Funct.Mater., 2013,23:5444-5450
[14]Chen X B,Li C,Grtzel M,et al.Chem.Soc.Rev.,2012,41: 7909-7937
[15]Justicia I,Ordejón P,Canto G,et al.Adv.Mater.,2002,14: 1399-1042
[16]Ling Y C,Cooper J K,Yang Y,et al.Nano Energy,2013,2: 1373-1382
[17]Tan H Q,Zhao Z,Niu M,et al.Nanoscale,2014,6:10216-10223
[18]Dong J Y,Han J,Liu Y S,etal.ACS Appl.Mater.Interfaces, 2014,6:1385-1388
[19]Su T,Yang Y L,Na Y,et al.ACS Appl.Mater.Interfaces, 2015,7:3754-3763
[20]Gallo A,Marelli M,Psaro R,et al.Green Chem.,2012,14: 330-333
[21]Gallo A,Montini T,Marelli M,et al.ChemSusChem,2012, 5:1800-1811
[22]Pan X Y,Xu Y J.Appl.Catal.,A,2013,459:34-40
[23]Dong K,Liu Z,Ren J.CrystEngComm,2013,15:6329-6334
[24]Corma A,Garcia H.Chem.Soc.Rev.,2008,37:2096-2126
[25]Chen H J,Shao L,Man Y C,etal.Small,2012,8:1503-1509
[26]Liu R,Sen A.J.Am.Chem.Soc.,2012,134:17505-17512
[27]Hidalgo M C,Maicu M,Navío J A,et al.J.Phys.Chem.C, 2009,113:12840-12847
[28]Tian B Z,Zhang J L,Tong T Z,et al.Appl.Catal.,B,2008, 79:394-401
[29]Lazarus M S,Sham T K.Chem.Phys.Lett.,1982,92:670-674
[30]Werfel F,Brümmer O.Phys.Scr.,1983,28:92-96
[31]McCafferty E,Wightman J P.Surf.Interface Anal.,1998,26: 549-564
[32]Lu X H,Zheng D Z,Zhai T,et al.Energy Environ.Sci., 2011,4:2915-2921
[33]Chen X B,Liu L,Liu Z,et al.Sci.Rep.,2013,3:1510
[34]Subramanian V,Wolf E E,Kamat P V.J.Am.Chem.Soc., 2004,126:4943-4950
[35]Tian J,Leng Y H,Zhao Z H,et al.Nano Energy,2015,11: 419-427
[36]Kou S F,Ye W,Guo X,et al.RSC Adv.,2016,6:39144-39149
Facile Synthesis of Core-Shell Au@H-TiO2Nanoparticles for Photocatalytic Hydrogen-Generation
KOU Shu-Fang FENG Zhen-Yu WANG Chun-Sheng YANG Jian*
(Ministry of Education School of Chemistry and Chemical Engineering,Shandong University,Jinan 200050)
Gold nanoparticles coated by oxygen-deficient TiO2(Au@H-TiO2)were successfully synthesized by a slow hydrolysis of TiCl3in the presence of gold nanoparticles,followed with a high-temperature annealing in Ar/ H2.XRD patterns,TEM images,XPS spectra and UV-Vis absorption spectra were measured to reveal the crystal structure,morphology and light absorption properties of Au@H-TiO2.Compared to TiO2and Au@A-TiO2that is absent of oxygen deficiency,Au@H-TiO2shows the highest photocatalytic rate for hydrogen evolution.This result could be attributed to enhanced charge-separation efficiency and reduced charge-transfer resistances,as supported by transient photocurrent response and electrochemical impedance spectra.These improvements could be correlated to Ti3+self-doping and Au modification in Au@H-TiO2.
TiO2;defective structure;nanomaterials;photocatalytic hydrogen generation
O614.41+1
A
1001-4861(2017)08-1390-07
10.11862/CJIC.2017.161
2017-02-18。收修改稿日期:2017-04-24。
国家自然科学基金(No.21172076)山东省泰山学者基金(No.ts201511004)资助项目。
*通信联系人。E-mail:yangjian@sdu.edu.cn

