腹腔镜下精准肝切除临床应用价值分析
王军保
腹腔镜下精准肝切除临床应用价值分析
王军保
肝癌;腹腔镜;精准肝切除
随着外科医学的不断发展,手术的模式也在不断发生变化,过去主要以追求手术速度,彻底清除病灶为主要目的,如今外科手术在此基础上还力求做到微创,在切除病灶的同时,尽可能地保留残余脏器的最大功能,提高患者预后[1]。肝脏外科也在此基础上进入了腹腔镜下精准肝切除时代。精准肝切除是结合术前患者的基本指标、相关影像学检查,术前肝脏储备功能评估,通过图像软件处理等不同手段,实行精细化、合理化的治疗[2]。原发性肝癌主要是肝细胞或肝内胆管上皮细胞发生癌变,发病率和死亡率逐年递增,手术切除是目前原发性肝癌主要的治疗方式[3-4]。传统肝切除术具有创伤大,术后恢复慢,预后生活质量一般,而腹腔镜下精准肝切除术具有创伤小,在切除病灶的同时,最大程度保留残余肝脏组织的功能,患者预后较好[5]。笔者通过腹腔镜精准肝切除术与开腹常规肝切除术进行比较,发现腹腔镜精准肝切除术具有更好的临床效果,现报道如下。
1 临床资料
1.1 一般资料2012年1月—2015年1月我院原发性肝癌患者78例,随机分为两组,对照组39例,男22例,女17例,年龄(20~73)岁,平均(51.8±10.9)岁,平均病程(7.1±2.3)个月,平均肿瘤直径(2.5±1.4)cm;Child A级23例,Child B级16例[6];合并肝硬化14例。观察组39例,男23例,女16例,年龄(22~72)岁,平均(52.3±11.2)岁,平均病程(6.5±2.6)个月,平均肿瘤直径(2.8±1.5)cm;Child A级24例,Child B级15例;合并肝硬化12例。两组患者在性别、年龄、肝功能分级、病情严重程度等方面差异均无统计学意义(P>0.05),具有可比性。
1.2 纳入及排除标准纳入标准[7]:经影像学及相关穿刺活检诊断为原发性肝癌;所有被发现的病灶均位于左半肝内;所有病灶直径均不超过5cm;肿瘤较为局限,未侵犯至其他部位;术前评估患者肝功能Child-Pugh分级为A级或B级;患者均签署知情同意书。排除标准:患者有自身免疫性疾病,合并有严重心、肝、肾功能障碍及有门静脉癌栓转移、肝门淋巴结转移、远处部位转移者,住院期间死亡者。
2 方法
2.1 手术方法观察组采用腹腔镜下精准肝切除术。观察组患者采用气管全麻,建立CO2气腹,头高脚低30°侧卧位,术前通过患者症状、体征,结合术中腹腔镜超声等手段共同帮助准确定位病灶所在部位,以达到精准肝切除的要求,术中尽可能避免对肿瘤的挤压、切割,切除肿瘤时应保证足够切缘,切除标本经标本袋取出,避免肿瘤扩散、种植转移等情况发生。腹腔镜下精准肝切除术主要通过游离肝脏后将第一、二肝门的血管预先处理,完全或者部分控制入肝或者出肝血流,再将病灶部位切除,具体的操作方式包括:左肝外叶切除术、左半肝切除术等[8]。
对照组采用常规开腹肝切除术,取仰卧位,切口为正中反“L”切口,余手术流程及原则与腹腔镜精准肝切除相同[9]。
所有患者术后均于肝断面放置腹腔引流管,术后常规心电监护,抗生素使用,营养支持,定期复查肝肾功能,密切观察术后病情变化。
2.2 观察指标及方法术中情况:手术时间、术中出血量、是否输血、是否行肝门血流阻断。术后情况:术后携带胃管时间、携带腹腔引流管时间、术后住院时间、住院总费用、术后肝脏功能变化情况、术后并发症情况。手术前1天及术后第7天各抽血1次,测定丙氨酸转氨酶(ALT)、天冬氨酸转氨酶(AST)、白蛋白(ALB)、总胆红素(TBIL)。测定方法为生化速率法,仪器为日立707自动生化分析仪。
2.3 统计学方法应用SPSS13.0软件包处理,正态分布的计量资料用均数±标准差() 表示,组间比较采用独立样本t检验,计数资料采用χ2检验,生存率的比较采用log-rank检验,P<0.05为差异有统计学意义。
3 结果
3.1 两组患者术中情况比较两组患者手术时间无明显差异,而术中出血、输血及肝门阻断比较,观察组显著优于对照组(P<0.05),见表1。
表1 两组肝切除患者术中情况比较()

表1 两组肝切除患者术中情况比较()
组别对照组观察组P值例数39 39手术时间(min)139.6±60.4 161.7±58.2>0.05术中出血(mL)310.5±40.7 190.4±50.5<0.05输血[例(%)] 12(30.8)4(10.3)<0.05肝门阻断[例(%)] 20(51.3)4(10.3)<0.05
3.2 两组患者术前、术后肝功能比较两组患者术前肝功能相关指标(AST、ALT、ALB、TBIL)无明显差异(P>0.05),术后肝功能指标较术前均有所改善,差异有统计学意义(P<0.05),观察组患者术后肝功能指标改善较对照组更为明显(P<0.05),见表2。
3.3 两组患者术后并发症比较观察组较对照组术后并发症发生率更低,分别为12.8%比23.1%,差异有统计学意义(P<0.05),其中常见的术后并发症有腹水、出血、胆漏、肝周积液、胸腔积液、肺部感染,术后无1例患者死亡,见表3。
3.4 两组患者术后相关情况比较观察组患者术后携带胃管时间、携带引流管时间、术后住院时间显著少于对照组患者(P<0.05),观察组患者花费更高(P<0.05),见表4。
4 讨论
原发性肝癌发病因素较为复杂,多由肝炎、肝硬化等疾病发展而来,目前临床上首选治疗方式是外科手术切除病灶。传统的开腹肝切除操作空间超大,手感好,可以及时的处理并控制术中突发性大出血等情况,安全性高。随着近年来外科技术的不断发展和完善,手术也从以往盲目肝切除、规则性肝切除、局部肝切除、解剖性肝段切除进入到精准肝切除阶段[10]。尤其是伴随着腹腔镜技术的成熟,采用腹腔镜下精准肝切除的治疗方式将会进入更高的层次。腹腔镜下精准肝切除的治疗理念是以微创为前提,在彻底切除病灶的基础上,尽可能减少对残余组织的创伤,确保剩余肝脏组织的功能,有效改善患者预后和生活质量[11]。
尽管腹腔镜下精准肝切除存在诸多优点,但其操作仍然较为复杂,手术难度较大,手术难点主要包括:(1)腹腔镜下对于突发性的大出血往往束手无策,这也是中转开腹的重要原因[12]。(2)腹腔镜下施行血管缝合、阻断、止血等操作难度较大,操作不慎易损伤周围毗邻的组织[13]。因此,腹腔镜下精准肝切除治疗应遵从以下原则:(1)术前应结合相关检查指标及影像学定位,充分评估患者肝脏功能,明确病灶大小、数目、具体部位,并掌握病灶与肝内胆管、血管的关系,精准预判拟切除的范围,确保手术的安全性与根治性。(2)手术操作务必精细,避免术中发生医源性损伤,对切除的病灶应注意保护,避免发生肿瘤扩散甚至是种植转移等情况的发生。(3)术中可采用区域性肝门阻断术,即根据需要选择性的阻断入肝血流,如只阻断拟切除肝叶、段的血管分支,尽可能的保护残余肝脏的功能。(4)术中对于肝实质离断可采用电刀、超声刀、氩气刀等,对于不同的血管,可分别予以处理,包括烧灼、钛夹夹闭、丝线结扎、缝扎等处理。(5)对于肝脏断面的处理,尤其是经过止血处理后,局部还有少量渗血的部位,可考虑直接用氩气刀直接喷灼,若条件允许,可以大网膜填塞、覆盖,促进局部组织愈合,预防出血、感染[14-16]。本研究结果提示,两组患者手术时间无明显差异,其中观察组患者术中出血、输血及肝门阻断患者的人数少于对照组(P<0.05)。两组患者术前肝功能相关指标(AST、ALT、ALB、TBIL)无明显差异,术后肝功能指标较术前均有所改善(P<0.05),其中观察组患者术后肝功能指标改善更为明显(P<0.05)。观察组较对照组术后并发症发生率更低,分别为12.8%对23.1%(P<0.05)。观察组患者术后携带胃管时间、携带引流管时间、术后住院时间显著少于对照组患者(P<0.05),而观察组患者住院花费更高(P<0.05)。因此,本研究认为,腹腔镜下精准肝切除较常规开腹肝切除在治疗原发性肝癌中更加安全、有效。腹腔镜下精准肝切除手术也存在其适应症:(1)肿瘤增长速度较快,或伴有临床症状,保守治疗难以控制。(2)肿瘤直径不超过10cm,且肿瘤没有明显压迫第一和第二肝门。(3)病灶较为局限,且肝硬化程度不重,无明显门静脉高压症。(4)肿瘤尚未侵犯毗邻脏器,未发生肿瘤破裂情况。(5)影像学检查难以定性,避免诊断性穿刺引起的穿刺针道转移情况的发生。(6)多发性肿瘤,但肿瘤病灶相对局限,且能保证切缘阴性。(7)肝功能分级应处于Child-Pugh分级A级或B级,术前评估残留肝脏功能能够满足代偿[17-19]。以上适应证也并非绝对不变,手术方式应结合患者具体情况,选择最有效的治疗方式。腹腔镜下精准肝切除主要包括完全腹腔镜肝切除(TLH)、手助腹腔镜肝切除(HALH)及辅助的腹腔镜肝切除(ALH)。TLH切口小,手术难度大,手术时间长;HALH可提高手术速度,降低手术难度,控制出血,但价格昂贵;ALH需结合开腹状态下切肝;三种手术方式各有优势。
表2 两组肝切除患者术前、术后肝功能比较()

表2 两组肝切除患者术前、术后肝功能比较()
注:与术前比较,*P<0.05;AST:天冬氨酸转氨酶;ALT:丙氨酸转氨酶;ALB:白蛋白;TBIL:总胆红素
组别对照组观察组P值例数39 39 AST(U/L)ALT(U/L)ALB(g/L)TBIL(μmmol/L)术前39.1±3.1 38.9±3.2>0.05术后15.4±3.7* 10.3±2.6*<0.05术前43.6±2.8 43.7±3.0>0.05术后30.2±2.9* 21.1±3.3*<0.05术前39.7±3.4 39.1±3.5>0.05术后42.2±2.3* 56.4±2.5*<0.05术前20.1±2.1 20.5±1.8>0.05术后15.7±1.2* 17.6±1.3*<0.05

表3 两组肝切除患者术后并发症比较(例)
表4 两组肝切除患者术后相关情况比较(d,)
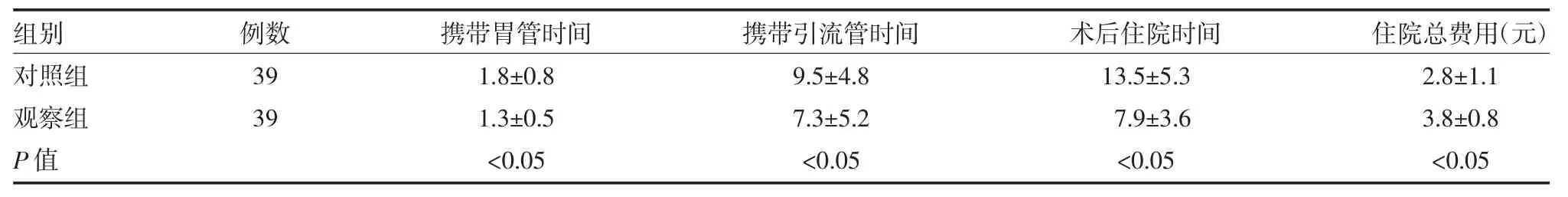
表4 两组肝切除患者术后相关情况比较(d,)
组别对照组观察组P值例数39 39携带胃管时间1.8±0.8 1.3±0.5<0.05携带引流管时间9.5±4.8 7.3±5.2<0.05术后住院时间13.5±5.3 7.9±3.6<0.05住院总费用(元)2.8±1.1 3.8±0.8<0.05
综上所述,腹腔镜精准肝切除应结合相关指标、影像学检查、三维成像等结果,术前精确评估患者肝功能及拟切除范围,并掌握肿瘤病灶与其周围重要组织、血管的解剖关系,以达到精准切除的目的。术后患者创伤小,肝功能损伤小,并发症少,预后较好,生活质量更高,值得临床上进一步深入研究。
[1]陈晓鹏,张卫东.腹腔镜精准肝切除治疗肝内胆管结石病[J].肝胆外科杂志,2016,24(2):87-89.
[2]林健群,洪建文,杨熙,等.精准肝切除在肝胆管结石病中的临床应用分析[J].腹腔镜外科杂志,2016,21(2):112-115.
[3]彭球,马娜,龚连生.完全腹腔镜下精准肝切除围手术期观察及治疗体会[J].中国现代医学杂志,2014,24(31):68-71.
[4]张志华,郭晓东,赵新,等.精准肝切除术治疗原发性肝癌的临床效果分析[J].现代生物医学进展,2014,14(19):3714-3717.
[5]黄高,文明波,姚红兵,等.精准理念下指导腹腔镜右半肝切除治疗肝肿瘤效果观察[J].临床合理用药杂志,2016,9(19):157-158.
[6]吴孟超.肝脏外科学[M].上海:上海科学技术文献出版社,2000:572-576.
[7]徐继威,温苑章,李嘉,等.腹腔镜精准肝切除临床应用价值分析[J].中国微创外科杂志,2016,16(7):590-593.
[8]张生军,刘敏丽,常琦,等.精准肝切除术与传统肝切除术治疗肝内胆管结石的效果比较[J].临床肝胆病杂志,2015,31(10):1648-1651.
[9]荚卫东.精准肝切除治疗肝细胞癌关键技术[J].中国普通外科杂志,2014,23(1):1-5.
[10]荚卫东,乔晓斐.加速康复外科理念在精准肝切除治疗肝细胞癌中的应用策略[J].中国实用外科杂志,2016,36(6):692-694,698.
[11]汪磊,李宏.腹腔镜超声在腹腔镜解剖性肝切除术中的应用[J].中国微创外科杂志,2014,14(5):385-388.
[12]胡红强.腹腔镜下精准肝蒂解剖行肝切除术52例分析[J].人民军医,2015,58(3):309-310.
[13]蒋星星,曾志峰.精准肝切除和非规则性肝切除在肝胆管结石病中的比较[J].江西医药,2015,50(8):777-779.
[14]黄海,秦锡虎,柳咏.精准肝切除治疗原发性肝癌的临床疗效[J].江苏医药,2014,40(1):42-44.
[15]汪一彪,纪小兰.精准肝切除术在肝胆管结石治疗中的临床应用效果[J].实用心脑肺血管病杂志,2013,21(11):130-131.
[16]武金才,李灼日,周开伦,等.完全腹腔镜肝切除术在肝肿瘤治疗中的应用和评价[J].肝胆胰外科杂志,2014,26(3):192-194.
[17]徐献忠,丁建忠,孙胜利,等.精准肝切除在原发性肝癌中的临床应用研究[J].中国医学创新,2016,13(17):117-120.
[18]周锦都,林泽伟.腹腔镜下精准肝蒂解剖在肝切除术中的应用评价[J].黑龙江医学,2016,40(7):588-589.
[19]王海涛,王锦波.精准肝切除的理念和临床技术特点及发展[J].实用医药杂志,2015,32(5):406-408.
(收稿:2016-10-20修回:2017-02-08)
浙江省金华广福医院腹部肿瘤外科(金华321000)

