芹菜甲素分子印迹聚合物的制备及其吸附性能研究
张稳,梁浩,谭倪,郁建生
(1.铜仁职业技术学院,贵州铜仁554300;2.南华大学,湖南衡阳421001)
芹菜甲素分子印迹聚合物的制备及其吸附性能研究
张稳1,2,梁浩1,谭倪2,郁建生1
(1.铜仁职业技术学院,贵州铜仁554300;2.南华大学,湖南衡阳421001)
以芹菜甲素为模板分子,通过沉淀聚合法制备了芹菜甲素分子印迹聚合物(MIPs)和非分子印迹聚合物(NIPs),并通过动态吸附、静态吸附和选择性吸附实验对所制备的分子印迹聚合物的吸附性能进行了表征.结果表明,当芹菜甲素的浓度为0.1 mmol L-1,吸附时间为12 h时,MIPs达到吸附平衡且最大吸附量为3.561 mgg-1.Scatchard分析表明,在MIPs中存在高亲和性和低亲和性两种结合位点,而在NIPs中只存在一种非特异性结合位点.选择吸附实验表明,MIPs对芹菜甲素具有高选择性和良好的专一识别性能.该研究可为芹菜甲素分子印迹聚合物作为固相萃取材料分离提取中药中有效成分芹菜甲素提供了理论基础.
分子印迹聚合物;芹菜甲素;沉淀聚合;吸附
分子印迹技术是将功能单体和模板分子在交联剂和引发剂存在的条件下引发聚合,得到高度交联的聚合物的技术,其中聚合物中的模板分子经化学法或溶剂萃取法移除后得到具有一定空穴结构和识别位点的分子印迹聚合物(MIPs).MIPs对模板分子具有预先识别和专一选择的特性且具有制备简单,性质稳定,可回收再利用及对环境有着较好耐受性的优点[1-3].近年来,MIPs在中草药有效成分的提取,酶催化模拟,固相萃取,传感器等方面得到了广泛的应用.芹菜甲素是一种重要的具有生物活性的苯酞类衍生物,存在于能够为药物研发提供重要研发资源的中草药中,尤其是人们日常生活中使用的当归、川芎和芹菜等伞形科植物.芹菜甲素具有保护心肌细胞[4],改善慢性脑缺血[5]和阿尔茨海默症[6]等生物活性,在生物化学、临床及制药研究等方面受到越来越多的关注.
本文采用分子印迹技术,以芹菜甲素为模板分子通过沉淀聚合法制备了芹菜甲素分子印迹聚合物,并对聚合物吸附及识别性能进行了探究,为从复杂的中草药基质中提取分离芹菜甲素提供了一种有效方法.
1 实验部分
1.1 仪器和试剂
DHT型恒温搅拌型电热套(山东鄄城华鲁仪器有限公司);FA2204B电子天平(上海精科天美科学仪器有限公司);DZ系列真空干燥箱(天津市泰斯特仪器有限公司);KaidaTD4低速台式自动平衡离心机(湖南凯达科学仪器有限公司);KS康氏调速备用振荡器(长沙索拓科学仪器设备有限公司);80 WBG-01超声波清洗器(广州邦洁电子产品有限公司);UV-8500紫外可见分光光度计(上海天美科学仪器有限公司).
芹菜甲素(Butylphthalide,99.6%,中国药品生物制品检定所);3-正丙基茚苯酞(3-n-Propylidenephthalide,96%,中国药品生物制品检定所);丙烯酰胺(Acrylamide,分析纯,广东省汕头市西陇化工厂有限公司);乙二醇二甲基丙烯酸酯(Etylene glycol dimethacrylate,99%,低温保存,萨恩化学技术(上海)有限公司);偶氮二异丁腈(2,2,-Azobisisobutyronitrile,化学纯,上海山浦化工有限公司),使用前用乙醇进行热过滤,除去不溶物,取滤液进行重结晶;其余试剂均为市售分析纯.
1.2 MIPs的制备
称取35.54 mg(0.5 mmol)的丙烯酰胺于25 mL的圆底烧瓶中,加入12.5 mL的丙酮及23.78 mg的芹菜甲素,室温条件下超声溶解5 min后静置4 h,以形成稳定的芹菜甲素-丙烯酰胺复合物,加入0.4956 g交联剂乙二醇二甲基丙烯酸酯(EDTA,2.5 mmol)和20 mg的引发剂偶氮二异丁腈(AIBN),超声振荡脱气5 min,通氮脱氧15 min,密封反应体系,在N2保护下于60℃恒温水浴中热聚合24 h.反应合成的聚合物用乙醇-乙酸(8:2,v/v)进行多次振荡洗脱,洗去模板分子及未聚合的功能单体和交联剂,直至紫外检测无以上物质的吸收,再用乙醇洗去残留的乙酸至中性,即得到芹菜甲素分子印迹聚合物(MIPs),60℃真空干燥24 h,置于干燥器中备用.非分子印迹聚合物(NIPs)的制备除不加模板分子外其余方法同上.图1是芹菜甲素和其结构相似物的分子结构示意图,图2是上述MIPs的制备过程.
1.3 MIPs的吸附及识别性能
1.3.1 聚合物的静态吸附实验
准确称取7份10 mg的MIPs和NIPs,分别向其加入8 mL的浓度为0.01-0.14 mmol L-1的芹菜甲素标准溶液,置于室温下分别振荡12 h[7,8],取其上清液,测其吸光度,计算聚合物在不同浓度下的饱和吸附量Q(mg g-1),并做Scathard分析.相关公式如下[9]:

其中,C0为芹菜甲素的初始浓度(mmol L-1);C是芹菜甲素经聚合物吸附后的浓度(mmol L-1);V是吸附时混合液的总体积(L);m是加入的聚合物的质量(g);M是芹菜甲素的摩尔质量(190.24 gmol-1).
Scathard方程:

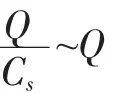

图1 芹菜甲素和其结构相似物的分子结构式
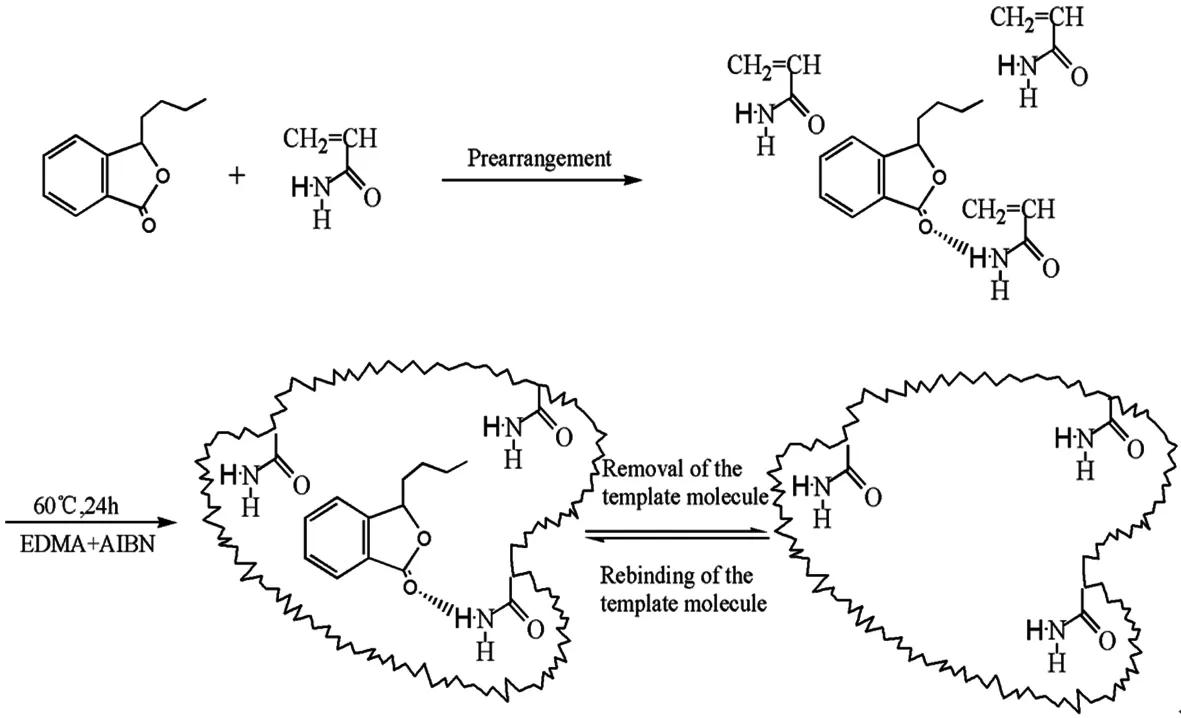
图2 MIPs合成过程图
1.3.2 聚合物的动态吸附实验
准确称取9份10 mg的MIPs和NIPs,分别加入8 mL浓度为0.1 mmol L-1的芹菜甲素标准溶液,置于室温下分别振荡不同的时间,计算聚合物对芹菜甲素在不同吸附时间下的吸附量.
1.3.3 聚合物的选择性吸附实验
选用与芹菜甲素结构相似的3-正丙基茚苯酞分别作为底物,称取10 mg的MIPs和NIPs,分别加入0.1 mmol L-1的各底物的乙醇溶液,按照上述方法,测定MIPs和NIPs对底物的吸附量.
静态吸附分配系数(Kd),印迹因子(α)和选择性系数(β)用来表征MIPs和NIPs对芹菜甲素及其相似结构化合物的专一识别性能,公式如(3)-(5)所示[10]:

其中,Cp为吸附平衡时底物在聚合物中的浓度,即聚合物吸附底物的量(mgg-1);Cs为吸附平衡时底物在溶液中的浓度(mmol L-1).

其中,QMIPs和QNIPs分别是聚合物对模板分子的吸附量或相似结构底物结合在聚合物上的量.

其中,α1和α2分别是模板分子以及相似结构底物的印迹因子.

图3 MIPs和NIPs的静态吸附曲线
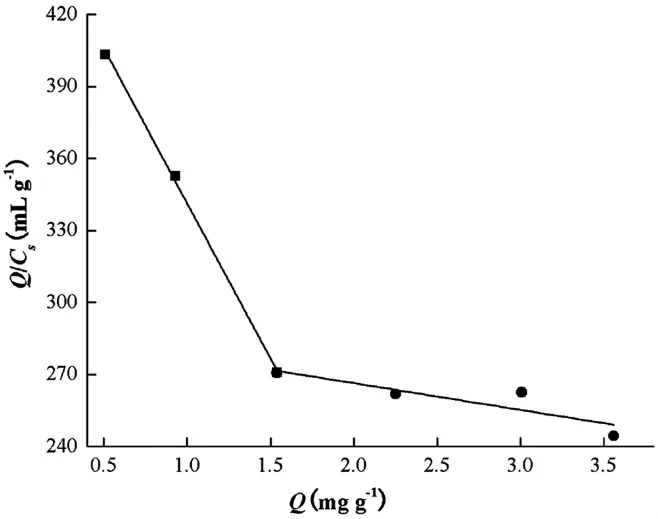
图4 MIPs的Scatchard分析

图5 NIPs的Scatchard分析
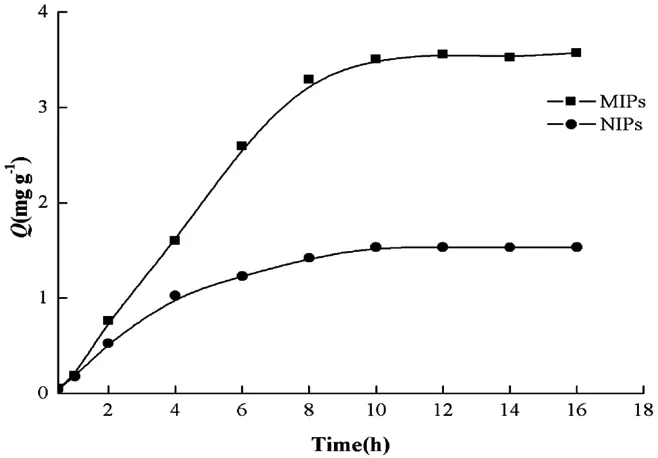
图6 MIPs和NIPs的动态吸附曲线
2 结果与讨论
2.1 静态吸附
从图3可以看出,在吸附初始阶段,MIPs对芹菜甲素的吸附量随着芹菜甲素浓度的增加而增长;当芹菜甲素的浓度增至0.1 mmol L-1时,MIPs对芹菜甲素的吸附达到饱和,且吸附量达到最大3.561 mg g-1,表明在印迹过程中生成了大量的芹菜甲素的特异结合位点.相同吸附条件下,MIPs对芹菜甲素的结合量比NIPs高.
2.2 Scathard分析
图4是MIPs的Scatchard分析图,两条直线的线性回归方程分别是Q/Cs=470.471-129.195Q和Q/Cs= 288.618-11.118Q,这表示在MIPs中生成了两类不同的结合位点.对高亲和性结合位点,其分布常数和最大表观结合量分别是0.008 mgmL-1和3.642 mgg-1;对低亲和性结合位点,其分布常数和最大表观结合量分别是0.090 mgmL-1和25.960 mgg-1.
图5中只有一条直线,表明在NIPs中只存在一种非特异性结合位点,其线性回归方程是Q/Cs=431.985-227.415Q,得到相应结合位点的分布常数和最大表观结合量分别是0.004 mgmL-1和1.900 mgg-1.
2.3 动态吸附
由图6可以看出,吸附的初始阶段(0-8 h),MIPs和NIPs对芹菜甲素都有着较高的吸附速率且Q也随时间单调增长,8 h后二者对芹菜甲素的吸附速率变得平缓且在12 h达到了吸附平衡.相同吸附条件下,MIPs对芹菜甲素的吸附量高于NIPs对芹菜甲素的吸附量.实验表明MIPs对芹菜甲素的结合具有高选择性和亲和性的结合位点.
2.4 选择性吸附
从表1可以看出,芹菜甲素MIPs对3-正丙基茚苯酞的吸附量为1.238 mgg-1,而对模板分子芹菜甲素有更高的吸附量3.561 mgg-1.芹菜甲素MIPs对3-正丙基茚苯酞的吸附量非常接近NIPs的吸附量.此外,芹菜甲素MIPs对芹菜甲素的分布常数为0.243 Lg-1,高于其对3-正丙基茚苯酞的分布常数0.078 Lg-1,进一步说明其对模板分子芹菜甲素的吸附有高选择性.MIPs和NIPs对模板分子芹菜甲素的印迹因子大于另种吸附底物的印迹因子,同时,两种聚合物对3-正丙基茚苯酞的选择因子为2.034.结果表明MIPs对于目标分子芹菜甲素有着良好的识别性能和分离吸附量.

表1 MIPs和NIPs的选择性吸附
3 结论
研究结果表明,相同吸附条件下,芹菜甲素MIPs对芹菜甲素的结合量比NIPs高,且芹菜甲素分子印迹聚合物对芹菜甲素的识别具有良好的专一选择性与亲和性能,将其作为固相萃取吸附剂用于提取分离实际样品如中草药中的芹菜甲素具有很大应用潜力.
[1]Sanagi MM,Salleh S,Ibrahim WAW,et al.Molecularly imprinted polymersolid-phaseextractionfortheanalysisof organophosphorus pesticides in fruit samples[J].Journal of Food Composition and Analysis,2013,32(2):155-161.
[2]Yongfeng K,Wuping D,Yan L,et al.Molecularly imprinted polymers of allyl-β-cyclodextrin and methacrylic acid for the solid-phase extraction of phthalate[J].Carbohydrate Polymers,2012,88(2):459-464.
[3]Martín-EstebanA.Molecularly-imprintedpolymersasa versatile,highly selective tool in sample preparation[J].TrAC Trends in Analytical Chemistry,2013,45:169-181.
[4]WangYG,Li Y,WangCY,et al.L-3-n-butylphthalide protects rats'cardiomyocytesfrom ischaemia/reperfusion-induced apoptosis by affecting the mitochondrial apoptosis pathway[J]. Acta Physiologica,2014,210(3):524-533.
[5]Xu J,Wang Y,Li N,et al.l-3-n-butylphthalide improves cognitive deficits in rats with chronic cerebral ischemia[J]. Neuropharmacology,2012,62(7):2424-2429.
[6]Peng Y,Hu Y,Xu S,et al.l-3-n-Butylphthalide regulates amyloid precursor protein processing by PKC and MAPK pathways in SK-N-SH cells over-expressing wild type human APP695[J].Neuroscience Letters,2011,487(2):211-216.
[7]S.Zschocke.I.klaiber,R.Bauer,et al.HPLC-coupled spectroscopic techniques(UV,MS,NMR)for the structure elucidation of phthalides in Ligusticum chuanxiong[J].Molecular Diversity,2005,9:33-39.
[8]鄢学芬,詹瑾,黄叶宁,等.丁苯酞的药理作用与临床评价[J].中国医院药学杂志,2008,28(17):1498-1500.
[9]Sun X,Wang J,Li Y,et al.Highly selective dummy molecularly imprinted polymer as a solid-phase extraction sorbent for five bisphenols in tap and river water[J].Journal of Chromatography A,2014,1343(1):33-41.
[10]She Y-x,Cao W-q,Shi X-m,et al.Class-specific molecularly imprintedpolymersfortheselectiveextractionand determination of sulfonylurea herbicides in maize samples by high-performanceliquidchromatography-tandemmass spectrometry[J].Journal of Chromatography B,2010,878(23):2047-2053.
Synthesis and Adsorption Properties of l-3-n-butylphthalide Molecularly Imprinted Polymers
ZHANG Wen1,2,LIANG Hao1,TAN Ni2,YU Jian-sheng1
(1.Tongren Polytechnic College,Tongren,Guizhou 554300;2.University of South China,Hengyang,Hunan 421001)
In this thesis,l-3-n-butylphthalide molecularly imprinted polymers(MIPs)and non-molecularly imprinted polymers(NIPs)were synthesized through precipitation polymerization for the first time.Meanwhile the adsorption properties of the MIPs were studied by the static,dynamic and the selective adsorption experiments respectively.The results revealed that when the concentration of l-3-n-butylphthalide was 0.1mmol L-1and the adsorption was 12 h,the MIPs attained adsorption equilibrium and the mostadsorptioncapacity was 3.561 mg g-1.Scatchard analyses revealed that there were high and low affinity sites formed in the MIPs,however,there were only nonspecific sits in the NIPs.The selective adsorption experiments showed that MIPs have high selectivity and good specific recognition properties to l-3-n-butylphthalide.The present paper research provide theoretical basis for using l-3-nbutylphthalide MIPs as the solid phase extraction materials to separate and extract active ingredient l-3-n-butylphthalide in the traditional Chinese medicine.
molecularly imprinted polymers;l-3-n-butylphthalide;precipitation polymerization;adsorption
O63
A
1671-9743(2017)05-0058-04
2016-11-21
张稳,1988年生,女,山东济宁人,助教,硕士,研究方向:天然产物的提取和分离.

