荧光碳量子点催化鲁米诺发光体系测定2-甲氧基雌二醇*
李文武,赵维维,张素歌,肖向勤,曾文渊,贾 欣#,姚寒春#
1)河南省食品药品评价中心 郑州 450018 2)郑州大学药学院药物分析教研室 郑州 450001
荧光碳量子点催化鲁米诺发光体系测定2-甲氧基雌二醇*
李文武1),赵维维2),张素歌2),肖向勤2),曾文渊2),贾 欣2)#,姚寒春2)#
1)河南省食品药品评价中心 郑州 450018 2)郑州大学药学院药物分析教研室 郑州 450001
#通信作者,贾欣,女,1975年8月生,硕士,讲师,研究方向:药物分析与药物治疗学,E-mail:jiaxin@zzu.edu.cn;姚寒春,女,1979年1月生,博士,副教授,研究方向:纳米荧光探针在药物分析中的应用,E-mail:yhch@zzu.edu.cn
碳量子点;鲁米诺;化学发光;2-甲氧基雌二醇
目的:基于荧光碳量子点(CQDs)的催化特性,建立CQDs -鲁米诺化学发光新体系用于2-甲氧基雌二醇(2-ME)的含量测定。方法:利用微波热解法合成荧光CQDs,采用透射电镜及光谱技术对其进行表征。将CQDs应用于鲁米诺发光体系中,考察不同浓度试剂对发光强度的影响,在最优条件下,对冻干粉剂及血浆样品中的2-ME含量进行测定。结果:CQDs溶液可以增强鲁米诺-铁氰化钾体系的发光信号,因2-ME对这一体系的发光有抑制作用,且该作用与2-ME的浓度呈正比关系,因此建立了检出限为5.4×10-10g/mL,RSD为1.8%(n=11)的2-ME含量测定的新方法。结论:该方法灵敏度高、简单快速,适用于药物制剂及生物样品中2-ME的含量测定。
碳量子点(carbon quantum dots,CQDs)是粒径在10 nm左右的外形类似球形的碳纳米材料,具有优良的光学性能、良好的生物相容性、低毒性及制备成本低[1]等特殊优势,在化学发光领域被用作金属量子点的理想替代品。铁氰化钾能直接氧化CQDs,产生较强的化学发光,一些金属离子和生物分子对发光有抑制作用,据此建立了测定Cr(Ⅵ)和肾上腺素的化学发光分析法[2]。将CQDs作为催化剂应用于鲁米诺-过氧化氢发光体系,钝化后的CQDs对该发光体系的催化过程是一个典型的1O2诱导发光机制[3]。有学者[4]发现CQDs在无外加氧化剂下也可以催化鲁米诺化学发光,认为CQDs具有的电子供体、受体的性质是其催化特性的来源,且通过改变CQDs的表面基团可以调控其催化性能。
2-甲氧基雌二醇(2-methoxyestradio,2-ME)是内源性雌激素17β-雌二醇非极性的代谢产物[5]。研究[6-10]表明:2-ME对多种肿瘤细胞的增殖有抑制作用,可以通过下调转录因子(如缺氧诱导因子)来调节血管生成、抑制微管蛋白聚合而导致细胞死亡,并证实它对恶性肉瘤、乳腺癌、胃癌、肺癌、多发性骨髓瘤和前列腺癌等多种肿瘤有治疗作用。HPLC[11-13]、GC[14]、放射免疫法[15]及化学发光法[16-17]均可用于测定2-ME。Zhang等[17]基于纳米银对鲁米诺-铁氰化钾化学发光体系的催化特性,利用2-ME对体系的抑制作用进行含量测定。作者利用CQDs对鲁米诺-铁氰化钾体系的催化特性,基于2-ME对该体系强烈的抑制作用,建立了一种2-ME含量测定的新方法,并分析了其发光机制。
1 材料与方法
1.1 主要仪器与试剂 850W Glanz 微波炉(珠海格力电器股份有限公司),Nano-ZS90 激光纳米粒度分析仪(英国马尔文公司),IFFM-E型流动注射化学发光分析仪(西安瑞迈分析仪器有限公司),DZF-6021型真空干燥箱(上海精宏实验设备有限公司),UV-2550型紫外分光光度计(日本岛津科学仪器公司),RF-5301型荧光分光光度计(日本岛津科学仪器公司)。柠檬酸(宜兴协联生物化学有限公司),二甘醇(天津市风船化学试剂科技有限公司),PEI2500(上海攻碧克新材料科技有限公司),2-ME冻干粉剂(郑州大学药学院自制,纯度≥99%),鲁米诺(北京索莱宝科技有限公司),铁氰化钾(天津盛奥化学试剂有限公司),浓硫酸(H2SO4,体积分数95.0%~98.0%)购于北京康普汇维科技有限公司。实验用水为超纯水,实验试剂均为分析纯。
1.2 实验方法 按照图1所示连接各流路,启动仪器,首先用超纯水将整个流路冲洗10 min至信号稳定。再通过各自的流路将铁氰化钾溶液、鲁米诺溶液、CQDs溶液及空白样品(超纯水)经蠕动泵带入分析系统,得到发光信号。待信号稳定后,记录发光强度I0。用2-ME样品溶液替换超纯水注入流路,得到发光强度Is。采用光电倍增管(工作电压为900 V)对系统的发光信号进行收集与检测。以相对化学发光强度ΔI(ΔI=I0-Is)与浓度的关系对2-ME进行定量分析。

a:鲁米诺溶液;b:样品溶液;c:铁氰化钾溶液;d:CQDs溶液;P:蠕动泵 (P1为主泵;P2为副泵);V:进样阀;F:流通池;W:废液;D:检测器;PC:计算机处理系统。图1 流动注射化学发光分析流路图
1.3 CQDs的制备及表征
1.3.1 CQDs的制备 CQDs采用微波热解法制备[17]:将0.2 g PEI2500、1.0 g 柠檬酸和3 mL二甘醇置于100 mL烧杯中,混匀,然后将此混合物放入功率为850 W的微波炉中,在200 ℃下加热3 min,反应产物呈棕黑色固-液混合物。将混合物加水并进行超声溶解,离心15 min(4 000 r/min),将上清液置于超纯水中透析48 h(MWCO=3 500的透析膜),以除去多余的PEI2500和二甘醇,即得浅棕色CQDs水溶液。
1.3.2 CQDs的表征 在紫外灯下(λ=365 mm)观察CQDs水溶液的发光情况,在200~600 nm波长范围内对CQDs水溶液进行紫外全波长扫描。用RF-5310型荧光分光光度计对其进行荧光光谱的表征。在300~480 nm范围内分别用不同的激发波长激发CQDs水溶液,考察CQDs发射波长的变化。采用高分辨透射电镜对其进行形态表征,采用激光纳米粒度分析仪考察CQDs的粒径分布。
1.4 实验条件优化 鲁米诺的发光需要在碱性条件下进行。该实验用NaOH调节鲁米诺溶液的pH,考察了NaOH在0.03~0.40 mol/L范围内对相对化学发光强度的影响。此外,该实验考察了鲁米诺浓度在8.0×10-8~3.0×10-6mol/L范围内、铁氰化钾浓度在5.0×10-6~3.0×10-4mol/L范围内对相对化学发光强度的影响。在该体系中,CQDs对鲁米诺-铁氰化钾体系具有很强的发光增敏作用。该实验考察了CQDs用量对相对化学发光强度的影响。
1.5 方法学考察
1.5.1 分析特性 作者配制了一系列不同浓度的2-ME标准溶液,在选定的实验条件下,采用发光分析仪对其浓度进行测定。以2-ME浓度C为横坐标,相对发光强度ΔI为纵坐标绘制标准曲线,得到线性回归方程。按照IUPAC的计算规定(3σ),根据数据计算检出限。对1.0×10-7g/mL的2-ME进行11次平行测定,考察其精密度。该实验还考察了金属离子、药用辅料及可能存在的干扰成分对2-ME标准溶液(1.0×10-7g/mL)测定的影响。
1.5.2 样品制备 称取适量不同批次的2-ME冻干粉末,先使用甲醇通过超声溶解,再用0.22 μm的微孔滤膜过滤,取适量滤液定容于100 mL容量瓶中作为储备液,于4 ℃保存。人血浆来自河南省红十字血液中心。各取3份100 μL血浆,分别加入高、中、低3个不同浓度的2-ME标准溶液,然后加入600 μL甲醇以去除蛋白,涡旋3 min使其混合均匀,12 000 r/min离心15 min,收集上清液备用。另取一份不加2-ME的血浆按同样方法处理作为空白对照溶液。
1.6 反应机制探讨 用紫外分光光度计和荧光分光光度计(关闭光源)对CQDs、2-ME、鲁米诺-铁氰化钾、鲁米诺-铁氰化钾-CQDs及鲁米诺-铁氰化钾-CQDs-2-ME的紫外吸收光谱和发射光谱进行扫描。通过峰位置和强度的变化,结合文献报道,判断发光体,推测可能的反应机制。
2 结果
2.1 CQDs的表征 CQDs水溶液在紫外灯照射下(λ=365 nm)呈现明亮的蓝色荧光,紫外全波长扫描显示CQDs在230及290 nm处各有一个特征吸收峰(图2)。激发波长在300~480 nm范围内,随着激发波长的增加,发射波长也逐渐增大,CQDs的发射峰强度在激发波长为340 nm时最大(λem=400 nm)(图3)。高分辨透射电镜表征见图4,CQDs的外观呈粒径在4~7 nm的球形且大小分布均匀;单个CQDs表面具有间距在0.7 nm左右晶格条纹,CQDs的粒径主要分布在6 nm左右。

右上图为CQDs水溶液和紫外灯照射下的荧光图2 CQDs的紫外扫描图谱
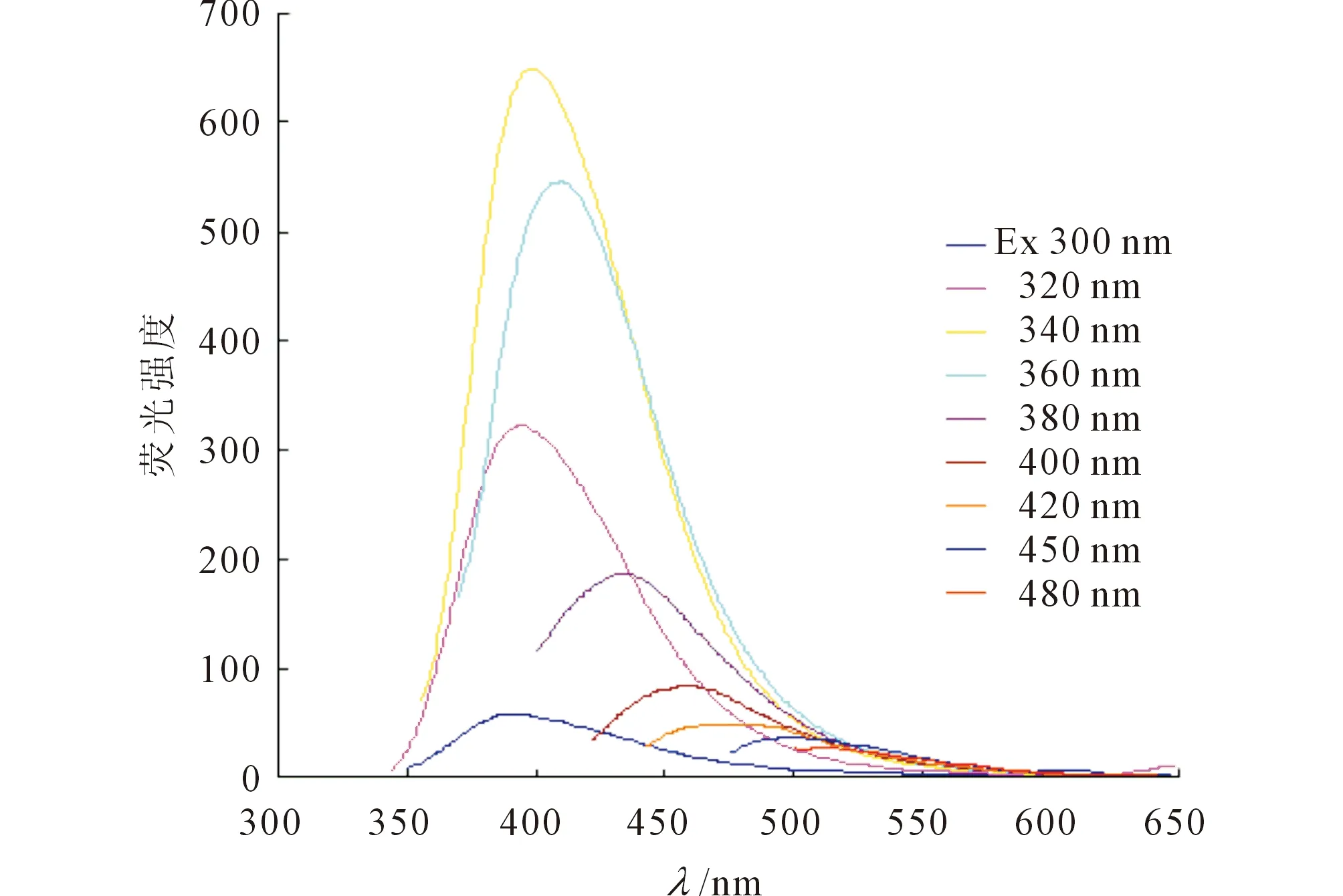
图3 不同激发波长下CQDs的发射光谱图
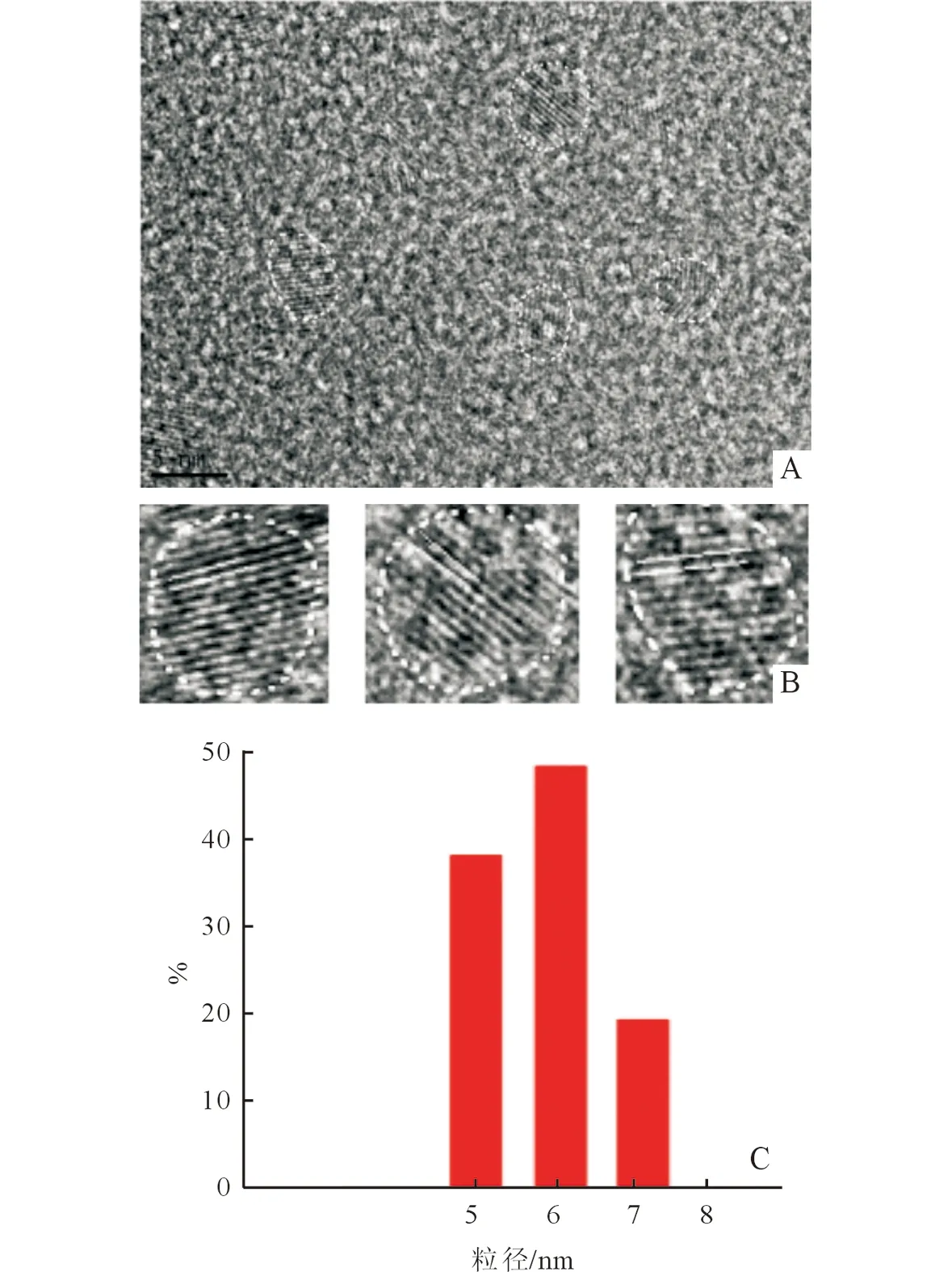
图4 CQDs高分辨透射电镜图(A,B)及粒径分布(C)
2.2 实验条件 如图5A所示,当NaOH浓度增加至0.2 mol/L时ΔI达最大,因此实验选择的NaOH浓度为0.2 mol/L。根据图5B所示,ΔI的变化与鲁米诺浓度呈正相关,综合考虑信噪比、峰稳定性和试剂消耗,选用2.0×10-6mol/L的鲁米诺溶液。随着铁氰化钾浓度的增加ΔI逐渐增大,当铁氰化钾浓度为5.0×10-5mol/L时,ΔI达到最大(图5C),之后ΔI逐渐降低,所以铁氰化钾最佳浓度为5.0×10-5mol/L。如图5D所示,当所用CQDs溶液稀释6.0×104倍时,ΔI达到最大,而后ΔI逐渐降低,因此CQDs的最佳稀释倍数为6.0×104倍。

图5 NaOH、鲁米诺、铁氰化钾和CQDs稀释度对发光强度的影响
2.3 方法学考查结果 ΔI与C在(2.0×10-9~5.0×10-7) g/mL范围内线性关系良好,线性回归方程为ΔI=39.183C+51.397,r=0.999 1,检出限为5.4×10-10g/mL。以2-ME标准溶液为例,11次平行测定的RSD为1.8%。相对误差不大于5%的情况下,干扰实验结果见表1,可以看出一些常见离子和药物添加剂对2-ME的测定基本没有影响。

表1 干扰实验结果
2.4 样品含量测定 依据上述实验步骤对冻干粉剂储备液中和人血浆中2-ME的含量进行测定,加标回收率测定结果见表2