基于三种检测方法的17α羟孕酮临床检测比对
渠海 吕萌萌 朱宇皇 付光宇
基于三种检测方法的17α羟孕酮临床检测比对
渠海1吕萌萌2朱宇皇1付光宇1
目的 评价具有不同检测原理的3个17α羟孕酮试剂盒,分析其临床检测结果的相关性和一致性。方法收集2015年2月至10月临床确诊为先天性肾上腺皮质增生症患者的血清120例,设为试验组;收集同期体检健康者血清120例,设为对照组。分别采用3个产品的17α羟孕酮试剂盒进行定量检测,对检测结果进行统计分析。结果3个产品的相关性R2分别为0.82、0.76和0.77,临床的阳性符合率为100%、100%和99.2%,阴性符合率为97.5%、98.3%和98.3%,总符合率为98.8%、99.2%和98.8%。3个产品的临床符合率差异无统计学意义(P〉0.05)。结论不同检测原理的3个产品的17α羟孕酮试剂盒的临床检测结果具有等效性,符合临床应用要求。
17α羟孕酮;放射免疫法;酶联免疫法;磁微粒化学发光法
先天性肾上腺皮质增生症(congenital adrenal hyperplasia,CAH)是一种由于肾上腺皮质激素合成途径中酶的缺陷引起的疾病,属常染色体隐性遗传病[1]。常见的缺陷酶包括21-羟化酶、17-羟化酶、3-羟脱氢酶和11-羟化酶等,其中21-羟化酶缺陷症(21-hydroxylase deficiency,21-OHD)约占CAH的90%~95%[2]。临床上通常把CAH分为经典型和非经典型,其中非经典型又称做迟发型(nonclassic 21-hydroxylase deficiency,NCCAH)。经典型多发于新生儿,发病率约为10/10万;迟发型多发于非新生儿,发病率约为前者的l0倍,女性多于男性[3]。
由于21-羟化酶在类固醇激素的代谢过程中起着至关重要的作用,所以其在体内的缺失会导致 17α 羟孕酮(17α-OH-progesterone,17α-OHP)含量逐渐的升高。17α-OHP被认为是CAH特别是NCCAH诊断中的最显著的指标[4]。目前市场上针对非新生儿检测的试剂盒多种多样,检测方法也各异。主要有放射免疫、酶联免疫以及化学发光等检测方法。经查询国家食品药品监督管理总局网站,郑州安图生物工程股份有限公司的17α-OHP检测试剂盒是针对非新生儿CAH的首个全自动磁微粒化学发光产品。而且在国际上,该厂家的17α-OHP检测试剂也是首次成功应用到全自动磁微粒化学发光的检测系统中的产品。
本文选择3种方法学的商业试剂盒进行研究,以临床诊断结果作为金标准,进行临床样本比对工作。研究目前医院应用较为广泛的17α-OHP商业试剂盒之间的差异及与临床结果的符合率,为临床使用单位选择适宜试剂产品提供参考依据。
1 材料和方法
1.1 样本
2015年2月至10月从郑州市第六人民医院收集临床确诊为先天性肾上腺皮质增生症的患者血清120例,设为试验组。收集同期体检健康者血清120例设为对照组。健康样本来源人群,无现病史及近期手术史,排除孕妇和产妇。每例样本均记录性别、年龄、临床诊断,女性样本应当确认其生理周期。样本使用无添加剂采血管(红盖)收集,37℃静置30 min,离心15 min,-20℃保存备用。严重溶血、脂血或浑浊的样本不能用于检测,需重新采集。
1.2 试剂和主要仪器
主要仪器:PHO mo酶标仪和Auto Lumo A2000全自动化学发光测定仪(郑州安图生物工程股份有限公司),GC-911γ放射免疫计数器(中佳光电仪器)。试剂:美国DSL公司(产品A)放射免疫17α-OHP检测试剂盒,货号ACTIVE 17α-OHP PROGESTERONE DSL-5000;郑州安图生物工程股份有限公司(产品B)生产的磁微粒化学发光17α-OHP检测试剂盒,批号20150728;德国DRG公司(产品C)生产的酶联免疫17α-OHP检测试剂盒,货号EIA-1292。商业第三方控制品(Lyphochek®Immunassay Plus Control 40271-40273,5 mL/瓶,Bio-Rad Laboratories,Inc)。
1.3 方法学比对
分析3个试剂盒的线性范围以及正常值参考范围,使用商业第三方控制品确认3个试剂盒在重复性和准确度之间的差异,保证检测结果的合理有效性。
重复性与准确度的考察参照美国临床和实验室标准化协会颁布的EP系列文件,主要步骤如下:
重复性:试剂盒检测高、中、低值3支质控品,要求重复测定5天,每天重复4次。根据拟合标准曲线计算测量结果,再计算每个浓度水平至少20次测量结果的平均值M和标准差SD,根据公式CV=SD/M×100%得出变异系数CV。
准确度:试剂盒检测高、中、低值3支质控品,按照1∶9的比例分别加入到相同的基质样本中,制成回收样本,加入高值样本的体积不得超过总体积的10%。每个回收样本重复检测3次求均值,计算回收率。
通过对相同人群样本的临床检测,对3家同类产品进行比较,结合240份临床诊断结果,分析商业试剂盒与诊断结果之间的符合率。排除线性范围外的40份样本后,通过对线性范围内的200份样本进行两两比对,对检测结果的相关性作图,得出相应的R2,分析测定结果差异的原因。
1.4 判断标准
临床符合率根据各个厂家提供的产品说明书中的正常人参考值范围进行判定,参考值范围内为阴性,参考值范围外为阳性。
1.5 操作人员要求
经专业上岗培训并且取得相应上岗证的医学检验专业人员。
1.6 统计学处理
采用SPSS 17.0统计学软件进行相关回归分析,分别计算3个厂家产品检测结果的阳性符合率和阴性符合率,以P<0.05为差异有统计学意义,相关系数R2>0.9表示测定结果相关性好。
2 结果
2.1 3个厂家试剂盒的操作过程分析
根据厂家说明书,比较3个厂家试剂盒的操作过程,产品B整个过程优于产品A和产品C,见表1。
2.2 3个厂家试剂盒的线性范围分析
根据厂家说明书,比较3个厂家试剂盒的线性范围,厂家B具有最宽的线性范围,厂家A具有最低的检测能力,见表2。
2.3 3个厂家试剂盒的正常值参考范围
根据厂家说明书,比较3个厂家试剂盒的正常值参考范围,3个厂家试剂盒的正常值参考相差较小,可以进行临床平行比对,见表3。
2.4 3个厂家试剂盒的重复性和准确度比较
采用商业第三方质控比较3个厂家试剂盒的重复性和准确度,3个厂家试剂盒在重复性和准确度方面均无显著的差异,见表4、5。

表1 3个厂家试剂盒的操作过程Table 1 The test procedure of 3 kits
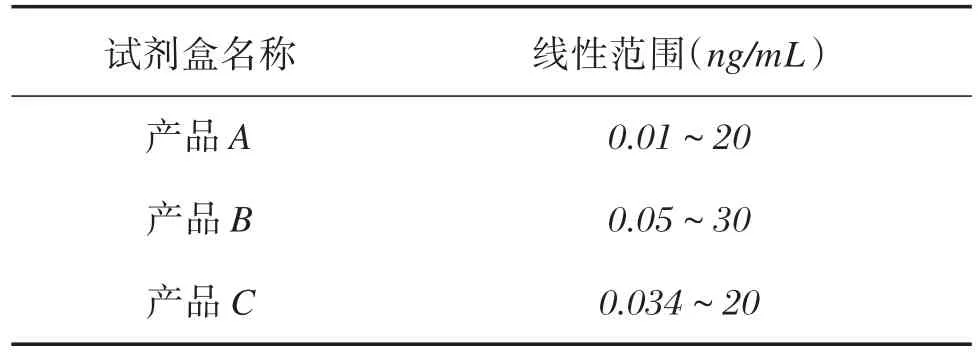
表2 3个厂家试剂盒的线性范围Table 2 The assay dynamic range of 3 kits
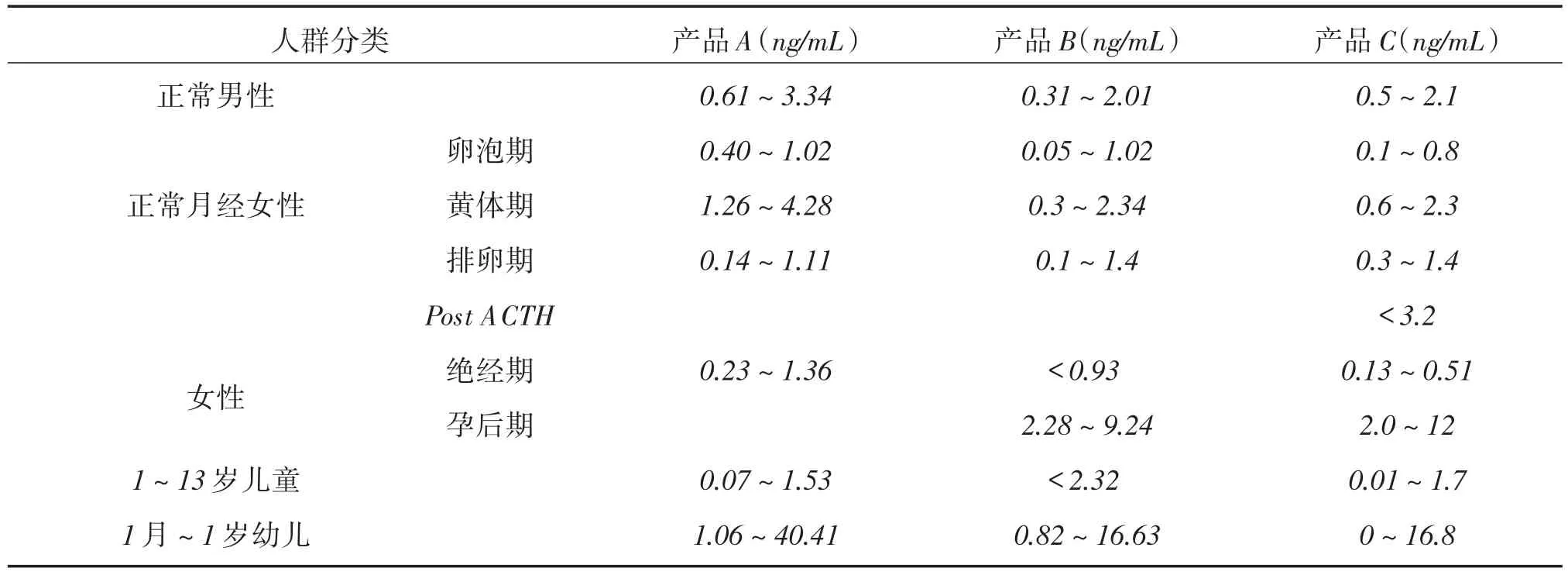
表3 3个厂家试剂盒的正常值参考范围Table 3 The expected normal values of 3 kits

表4 3个厂家试剂盒的重复性Table 4 The reproducibility of 3 kits

表5 3个厂家试剂盒的准确度Table 5 The accuracy of 3 kits
2.5 3个厂家试剂盒的阳性率、阴性率及总符合率比较
以临床诊断作为实验检测的金标准,试验组120例血清经3个厂家试剂盒检测后的结果与金标准的阳性符合率见表6。对照组120例血清经3个厂家试剂盒检测后的结果与金标准的阴性符合率见表7。3个厂家试剂盒检测后的结果与金标准的总符合率见表8。3个厂家产品的检测结果差异在试验组及对照组中均无统计学意义(P〉0.05)。
2.6 3个厂家试剂盒间的相关性分析
从2.2的结果可以看出,产品B的线性范围与产品A和C相比,增加了20~30 ng/mL的检测区间,为了验证该区段之间的相关性,以产品B的线性范围0~30 ng/mL为参考,分别对范围内的3个厂家试剂盒的200份临床样本的定量检测结果进行两两比对,产品A与B、A与C以及B与C的斜率为 1.09、0.94和0.79,其R2值分别为0.82、0.76和0.77,见图1~3。

表6 3个厂家试剂盒的试验组与金标准阳性符合率统计Table 6 The positive coincidence rate of 3 kits and gold standard in experimental group
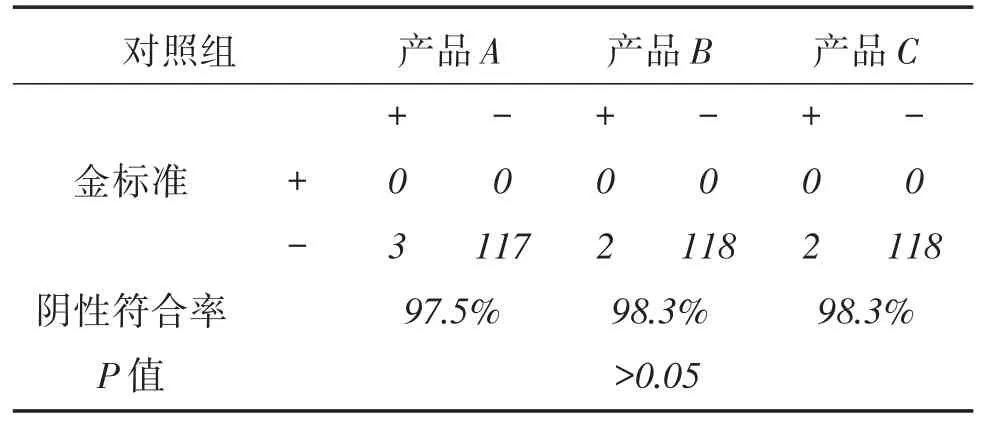
表7 3个厂家试剂盒的对照组与临床诊断阴性符合率统计Table 7 The negative coincidence rate of 3 kits and gold standard in control group
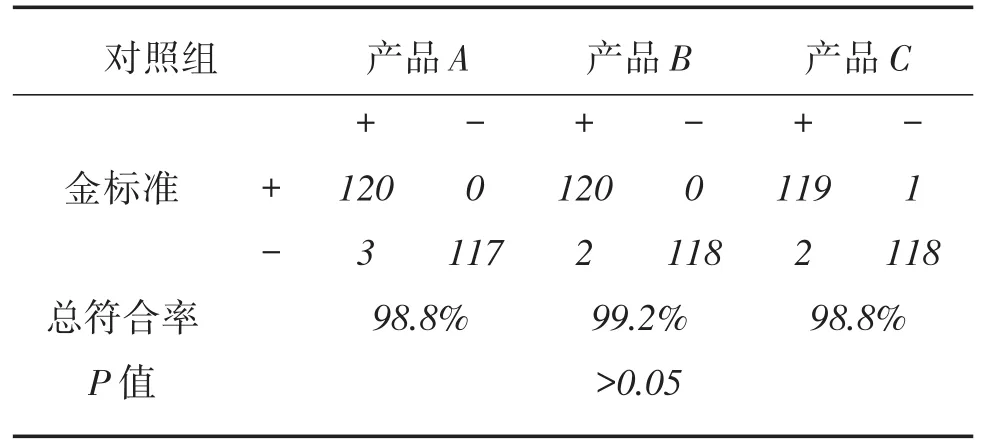
表8 3个厂家试剂盒的对照组与临床诊断符合率统计Table 8 The total coincidence rate of 3 kits and gold standard in control group
2.7 3个厂家试剂盒的异常样本分析
由2.4和2.6结果可以观察到,3个厂家试剂盒变异在10%以内,产品两两比对的斜率在25%以内,所以选出厂家间数值差异在1.5倍以上的样本进行分析,根据各个厂家试剂盒的正常值参考范围,确定与金标准之间的差异,结果表明数值异常样本对临床诊断结果影响较小,见表9。
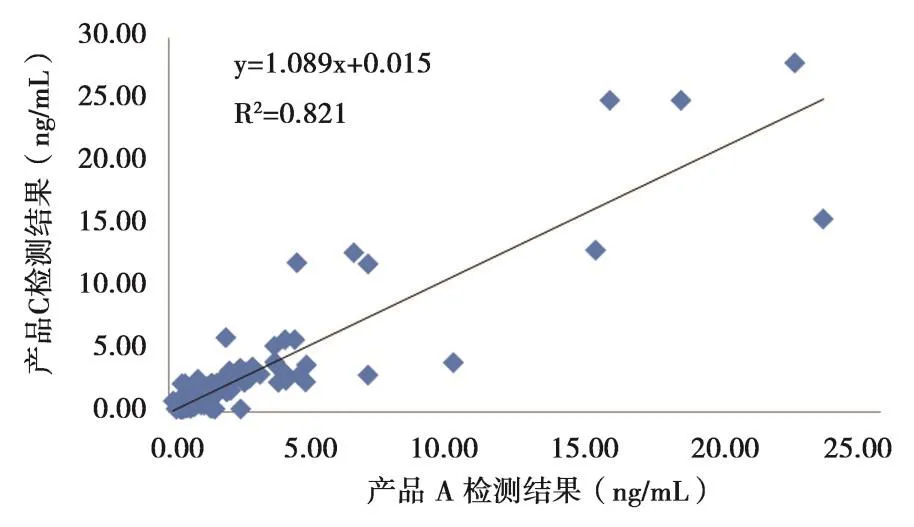
图1 产品A和B相关性分析Figure 1 The clinical correlation of A and B
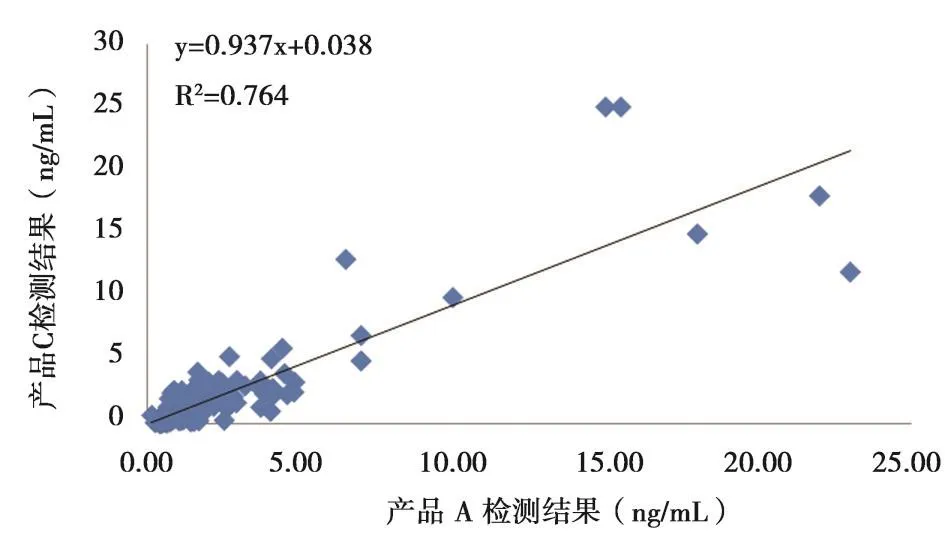
图2 产品A和C相关性分析Figure 2 The clinical correlation of A and C
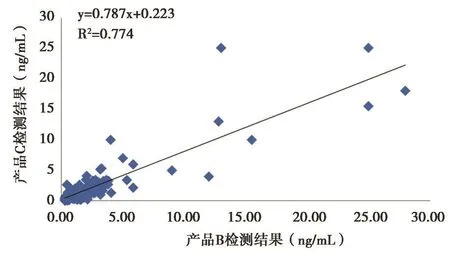
图3 产品B和C相关性分析Figure 3 The clinical correlation of B and C
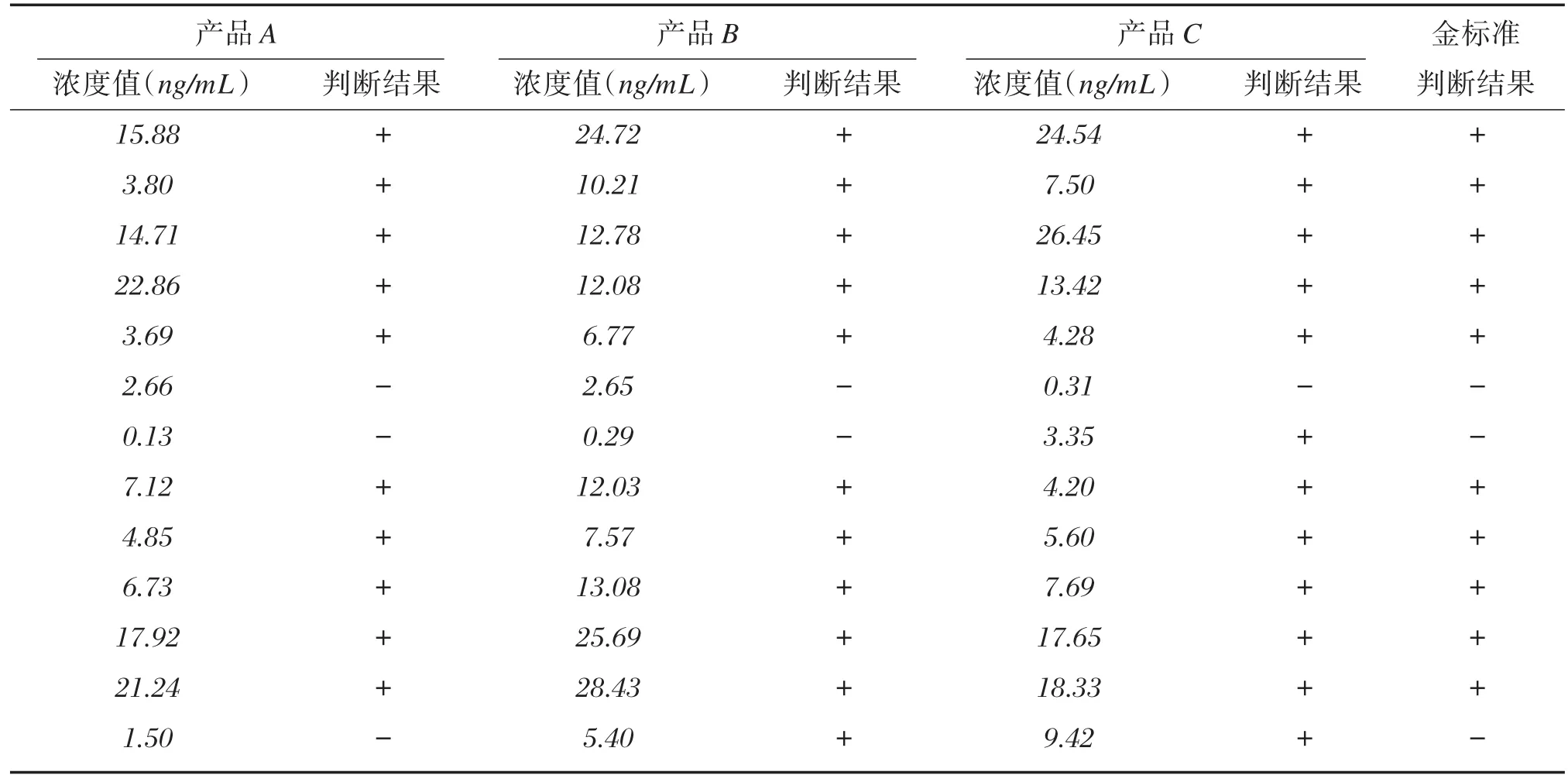
表9 3个厂家试剂盒实质异常样本的结果分析Table 9 The result of variation sample in 3 kits
3 讨论
由于CAH属于染色体隐形遗传病的一种,所以对于CAH的关注,早期主要集中在对新生儿的筛查。1977年17α-OHP的测定方法出世,使非新生儿21-羟化酶缺陷症筛查成为可能[5]。随着发达国家对该疾病研究的深入,以及近年来因NCCAH所造成的临床误诊引起了国内一些学者及医学工作者关注,除了对新生儿筛查的研究[6-7]外,对17α-OHP在NCCAH检测中的意义也得到了广大共识,逐渐兴起了研究的热潮[8-9]。
17α-OHP是由肾上腺皮质及性腺产生,其活性很低,经21-羟化酶作用下生成皮质醇的前体化合物[10-11]。17α-OHP在体内具有与肾上腺皮质醇一致的昼夜节律变化。目前市场上存在有放射免疫、酶联免疫以及化学发光等不同原理的17α-OHP检测试剂盒。放射免疫分析法灵敏度高,几乎可测定生物体内任何物质,但检测操作相对繁琐,同时存在放射性污染的问题。酶联免疫试剂具备试剂稳定、无危害污染、操作简便等优点,得以迅速推广应用。至今酶联免疫仍是免疫分析方法中较常用的方法。化学发光免疫分析是将具有高灵敏度的化学发光测定技术与高特异性的免疫反应相结合的检测分析技术。免疫磁珠是免疫学和磁微粒技术结合而发展起来的一类新型材料,此固相材料有较多的优点,既可提高混匀速度和分离效率,又达到扩大抗原抗体反应接触面积的目的,并且可以同时在磁场的作用下,快速使抗原抗体复合物和游离蛋白得到分离,以达到缩短反应时间和简化操作步骤的目的。磁微粒化学发光免疫分析系统是免疫磁珠、化学发光与免疫反应3个体系相结合而建立的检测体系,是用于检测微量抗原或抗体的一种标记免疫测定技术。该体系既具有放射免疫分析的高灵敏度,又避免放射性污染;即具有酶联免疫的操作简便性,又具有使用自动化设备实现单个反应标准化管理的特点,减低手工操作或板式产品批量管理造成的检验结果误差;试剂稳定,保质期长,成为最有前途的免疫分析方法之一。
通过线性范围、正常值参考范围及分析性能的比对,3个厂家的试剂盒具备临床比对的特征。结果显示3种方法与金标准的符合率较优(阴阳性符合率〉98%)。但是3个厂家试剂盒之间临床浓度值有较大差异,低值区个别样本可能由于各厂家方法学间的差异会出现假阳性,两两比对相关性R2均未达到0.9以上。这也与国际上之前的研究结果相一致[12],针对该类样本需继续跟踪,进行数据积累统一分析。此情况可能是由于各个厂家使用的抗体不同,不同抗体与体内小分子类似物的交叉反应程度不同,从而不能达到量值上的一致性。3个厂家试剂盒没有明显的差异性,都存在假阳性的问题,这也是与色谱质谱联用的金标准比较存在不足的地方[13]。高效液相色谱串联检测17α-OHP,在国外已经得到了广泛的应用,相应的基础研究也有很多,均表现出了与临床诊断结果有良好的一致性[14-15]。许多国外的临床诊断机构都已经应用到实际工作中,如美国的QUEST和Labcorp。色谱方法虽然检测结果准确可靠,被视为小分子检测的金标准,但因为设备昂贵,操作繁琐,不符合国情。而免疫诊断方法具有费用低、检测快捷等优点被市场广泛应用,但解决假阳性的问题仍需要各方积极努力。
综上所述,经本研究组的临床比对,虽然3个厂家不同检测原理的17α-OHP检测试剂盒在临床相关性不能达成一致,但与临床诊断的符合率较高,具有等效性,在现有金标准不能广泛应用开展的前提下,能够满足临床检测要求。临床使用单位可根据操作繁杂度及其他性价比等选择适宜本单位的优质试剂产品。
[1]吕萌萌,朱宇皇,张跃峰,等.先天性肾上腺皮质增生症筛查的相关进展[J].分子诊断与治疗杂志,2015,7(5):351-356.
[2]胡亚美,江载芳.诸福棠实用儿科学[M].7版.北京:人民卫生出版社,2002:2022-2027.
[3]Kashimada K,Ishii T,Nagasaki K,et al.Clinical,biochemical,and genetic features of non-classical 21-hydroxylase deficiency in Japanese children[J].Endocr J,2015,62(3):277-282.
[4]Speiser PW,Azziz R,Baskin LS,et al.Congenital adrenal hyperplasia due to steroid 21-hydroxylase deficiency:an endocrine society clinical practice guideline[J].J Clin Endocrinol Metab,2010,95(11):5137.
[5]Falhammar H,Frisén L,Norrby C,et al.Increased mortality in patients with congenital adrenal hyperplasia due to 21-hydroxylase deficiency[J].J Clin Endocrinol Metab,2014,99(12):E2715-E2721.
[6]毛维玉,郭辉,闵娟,等.早产新生儿体重对CAH筛查中17-羟孕酮结果的影响分析[J].国际医药卫生导报,2008,14(7):11-14.
[7]Heather NL,Seneviratne SN,Webster D,et al.Newborn screening for congenital adrenal hyperplasia in New Zealand,1994-2013[J].J Clin Endocrinol Metab,2015,100(3):1002-1008.
[8]Cavarzere P,Samara-Boustani D,Flechtner I,et al.Transient hyper-17-hydroxyprogesteronemia:clinical subgroup of patients diagnosed at neonatal screening forcongenital adrenal hyperplasia[J].Eur J Endocrinol,2009,161(2):285-292.
[9]Nascimento ML,Cristiano AN,Campos TD,et al.Ten-year evaluation of a neonatal screening program for congenital adrenal hyperplasia[J].Arq Bras Endocrinol Metabol,2014,58(7):765-771.
[10]Honour JW.17-Hydroxyprogesterone in children,adolescents and adults[J].Ann Clin Biochem,2014,51(Pt 4):424-440.
[11]Li XM,Ji H,Li CJ,et al.Chemerin expression in Chinese pregnant women with and without gestational diabetes mellitus[J].Ann Endocrinol(Paris),2015,76(1):19-24.
[12]Bello R,Lebenthal Y,Lazar L,et al.Basal 17-hydroxyprogesterone cannot accurately predict non-classical congenital adrenal hyperplasia in children and adolescents[J].Acta Paediatr,2016,106(1):155-160.
[13]Meier U,Schnabel C,Kunz D,et al.Comparison of three commercial assays for the measurement of 17alpha-hydroxyprogesterone(17alpha-OHPR):limitations of the quality control system[J].Clin Chem Lab Med,2004,42(4):450-454.
[14]Ceglarek U,Kortz L,Leichtle A,et al.Rapid quanti fi cation of steroid patterns in human serum by on-line solid phase extraction combined with liquid chromatography-triple quadrupole linear ion trap mass spectrometry[J].Clinica Chimica Acta,2009,401:114-118.
[15]Fanelli F,Belluomo L,Cuomo G,et al.Serum steroid profiling by isotopic dilution-liquid chromatography-mass spectrometry:Comparison with current immunoassays and reference intervals in healthy adults[J].Steroids,2011,76:244-253.
The clinical comparison of three methods for 17α-OH-progesterone assay kit
QU Hai1,LV Mengmeng2,ZHU Yuhuang1,FU Guangyu1
(1.Autobio Diagnostics CO.,Ltd,Zhengzhou,Henan,China,450016;2.Department of Clinical Laboratory,the Sixth People’s Hospital of Zhengzhou City,Zhengzhou,Henan,China,450015)
Objective To compare the correlation and consistency of results of 17α-OH-progesterone assay kits from 3 different manufactures. Methods From February to October 2015,17α-OH-progesterone in serum samples collected from 120 patients with congenital adrenal hyperplasia and 120 healthy subjects were detected by 3 different manufactures.The results of 17α-OH-progesterone were statistically analyzed. Results The R2of results detected by the 3 kits were 0.82,0.76 and 0.77.The positive coincident rate were 100%,100%and 99.2%.The negative coincident rate were 97.5%,98.3%and 98.3%.The total coincident rate were 98.8%,99.2%and 98.8%.The value of 3 kits were without statistical difference(P〉0.05).Conclusion The performance of the 3 kinds of 17α-OH-progesterone assay kit might be equivalent,all of which could meet the requirements of clinical application.
17α-OH-progesterone;Immuno-radiametric assay(RIA);Enzyme-linked immunosorbent assay(ELISA);Chemiluminescent microparticle immunoassay(CMIA)
河南省重大科技专项(121100510200)
1.郑州安图生物工程股份有限公司,河南,郑州450016
2.郑州市第六人民医院检验科,河南,郑州450015
付光宇,E-mail:fuguangyu@autobio.com.cn

