磁性固相萃取-高效液相色谱法测定牛奶中4种磺胺类药物
王 露,汪 怡,杭学宇,冯晓青,宋 鑫,徐 瑞,王 芹
(淮安市疾病预防控制中心,淮安223001)
磁性固相萃取-高效液相色谱法测定牛奶中4种磺胺类药物
王 露,汪 怡,杭学宇,冯晓青,宋 鑫,徐 瑞,王 芹*
(淮安市疾病预防控制中心,淮安223001)
磺胺类药物(SAs)是一种含有对氨基苯磺酰胺结构的化学合成药物,可用于预防和治疗细菌性疾病,并广泛应用于畜牧业。由于人们不合理使用,磺胺类药物经各种途径进入人体,从而危害了人类的健康[13]。世界各国已经对磺胺类药物的残留危害相当重视,国际食品法典委员会(CAC)和欧美等许多国家也对磺胺类药物的残留量作了相关规定[45]。在分析复杂样品中的痕量物质时,目标物质的预富集对检测结果起了关键性的作用。传统的固相萃取(SPE)因其价格低廉,副产物少等优点而被广泛使用,但是SPE操作繁琐且不适合于复杂样品。近年来,基于磁性材料的固相萃取备受关注。
磁性固相萃取技术的最重要的组成部分是吸附剂,目前多种磁性材料已被实际应用[67]。石墨烯因其疏水非极性、极大的比表面积(2 630m2·g-1)、共轭体系,对含有苯环的物质如磺胺类药物产生吸附作用[89]。到目前为止,大部分磁性石墨烯都依托在四氧化三铁上,而CoFe2O4-石墨烯(CoFe2O4-G)磁性材料应用在电池和催化方面。磁性石墨烯复合材料可将石墨烯的强吸附性能与便捷的磁性分离相结合,有望成为一种高效型磁性吸附剂。
本工作将合成的CoFe2O4-G作为磁性固相萃取的吸附剂,应用于牛奶中磺胺类药物的富集,并结合高效液相色谱法(HPLC)测定牛奶中4种磺胺类药物的含量。
1 试验部分
1.1 仪器与试剂
Aglient 1260型高效液相色谱仪;KQ 218型超声波清洗器;PHS-25型酸度计;磁铁(20 mm× 5mm圆形磁铁)。
磺胺甲基嘧啶(SM1)、磺胺甲二唑(SMTZ)、磺胺多辛(SDX)、磺胺异噁唑(SIZ)标准溶液:100mg·L-1,称取适量的磺胺标准品,用甲醇稀释成1mg·L-1中间液,再用阴性基质溶液稀释成标准溶液系列。于-20℃冰箱中储存。
所用试剂为分析纯,试验用水为重蒸水。
1.2 仪器工作条件
色谱柱(250mm×4.6mm,5μm),柱温25℃;流动相为乙腈-0.5%(体积分数,下同)乙酸(25+75)混合液;流量为1.0mL·min-1,进样量20μL;检测波长268nm。
1.3 试验方法
1.3.1 氧化石墨烯的制备
氧化石墨烯(GO)的制备方法参照Hummers方法[10]。称取石墨粉1.0g和硝酸钠1.0g加到含33.0mL硫酸的500mL烧杯里,在冰浴中剧烈搅拌。当石墨粉完全溶解后,慢慢加入高锰酸钾6.0g使反应充分。然后将烧杯置于35℃水浴中搅拌90min后,加入水40mL,在95℃下搅拌35min。然后加入水100mL和过氧化氢6.0mL待溶液颜色由暗棕色变至亮黄色。最后,用水离心洗至中性为止。真空干燥60℃、24h,制得GO备用。
1.3.2 CoFe2O4-G的制备
称取GO 0.45g分散在200 mL水中,超声2h。用25mL水溶解六水合氯化铁0.568 0g和六水合氯化钴0.25g,然后逐滴加入上述溶液中,在室温下剧烈搅拌。再逐滴加入200g·L-1氢氧化钠溶液调节pH至11.0,加热溶液至85℃时,加入水合肼6mL继续搅拌至溶液变黑色。待溶液冷却至室温,分别用水和乙醇多次洗涤,用磁铁分离。于60℃温度下,真空干燥24h,备用[1112]。
1.3.3 样品的吸附与富集
整个磁性固相萃取过程见图1。

图1 磁性固相萃取的步骤Fig.1 Procedures of magnetic solid phase extraction
图1 中,CoFe2O4-G 15.0mg加入至10mL磺胺类药物溶液中,调节pH至4.0,充分振荡10min,用磁铁分离固液两相。取上层清液,加入水2mL洗涤CoFe2O4-G-SAs,用乙酸-甲醇(0.1+99.9)溶液1.0mL超声洗脱。用氮吹仪吹干后溶解在乙腈-0.5%乙酸(25+75)混合液0.5mL中,按仪器工作条件进行测定。
2 结果与讨论
2.1 色谱行为
空白牛奶样品和加标牛奶样品的色谱图分别见图2(a)和图2(b)。

图2 色谱图Fig.2 Chromatograms
2.2 CoFe2O4-G的磁性
CoFe2O4、CoFe2O4-G纳米粒子在293K下测定的磁滞回线,见图3。
由图3可知:二者的饱和磁化强度分别为46.5,38.9Am2·kg-1,都具有较强的磁性,在外在磁场的作用下,能够较好地进行磁性分离。在试验中可以看出,均匀分散的磁性纳米粒子能够在磁铁作用下,充分地分离开来;CoFe2O4-G纳米粒子能够均匀地分散在水溶液中并形成黑色悬浮液,在磁铁的作用下,磁性粒子能够快速被吸引到杯内壁的一侧。

图3 磁滞回线Fig.3 Hysteresis loops
2.3 磁性固相萃取条件的选择
2.3.1 样品溶液酸度
样品溶液的酸度会影响SAs的存在形式和表面官能团,从而影响SAs在CoFe2O4-G上的吸附率。试验考察了样品溶液的pH在2.0~10.0时对萃取效率的影响,结果表明:样品溶液的pH在4.0时,响应值最高。这几种SAs的pKa1为5~8,在pH为4.0时,大多数SAs以中性分子存在,有一小部分以质子形式存在。因此SAs可以靠π-π的作用力和疏水作用力吸附在CoFe2O4-G表面。试验选择样品溶液的pH为4.0。
2.3.2 萃取时间
试验考察了萃取时间为2~30min时对萃取效率的影响,结果表明:随着萃取时间的增加,响应值逐渐增大;当萃取时间为10min时达最大值,之后保持稳定。试验选择萃取时间为10min。
2.3.3 CoFe2O4-G用量
试验考察了CoFe2O4-G用量为5.0~25.0mg时对萃取效率的影响。结果表明:随着CoFe2O4-G用量的增大,SAs的回收率迅速增大,最大回收率出现在15.0mg。CoFe2O4-G用量大于15.0mg后,回收率几乎保持不变,说明CoFe2O4-G 15.0mg足以吸附这4种磺胺类药物。试验选择吸附剂CoFe2O4-G用量为15.0mg。
2.3.4 洗脱剂及其用量
试验考察了甲醇、乙腈、丙酮与乙酸的混合液作洗脱剂时对测定的影响,结果表明:乙酸-甲醇(0.1+99.9)溶液洗脱能力最好,测定的回收率高于其他洗脱剂。试验选择乙酸-甲醇(0.1+99.9)溶液为洗脱剂。
为了完全洗脱吸附在CoFe2O4-G的SAs,试验考察了洗脱剂用量对测定的影响,最后选择洗脱剂乙酸-甲醇(0.1+99.9)溶液的用量为1.0mL。
2.4 CoFe2O4-G吸附剂的重复性
良好的吸附剂不仅具有较高的吸附容量,还要具有良好的稳定性。CoFe2O4-G吸附剂的重复性试验结果见图4。

图4 吸附剂的重复性试验结果Fig.4 Results of test for reusability of the sorbent
由图4可知,试验中制备的CoFe2O4-G吸附剂能够重复使用100次。
试验选择相同质量浓度的溶液(1.0mg·L-1)以及相同质量(20mg)的吸附剂,通过逐渐增加溶液体积来考察吸附剂的最大吸附量。结果表明:CoFe2O4-G纳米粒子对SM1、SMTZ、SDX、SIZ的吸附容量分别为5.1,5.6,9.8,6.9mg·g-1。
2.5 标准曲线和检出限
按试验方法对4种磺胺类药物混合标准溶液进行测定,并绘制标准曲线。结果表明:4种磺胺类药物的质量浓度均在0.1~50μg·L-1内与其对应的响应值呈线性关系,线性回归方程和相关系数见表1。
以3倍信噪比计算方法的检出限(3S/N),其结果见表1。
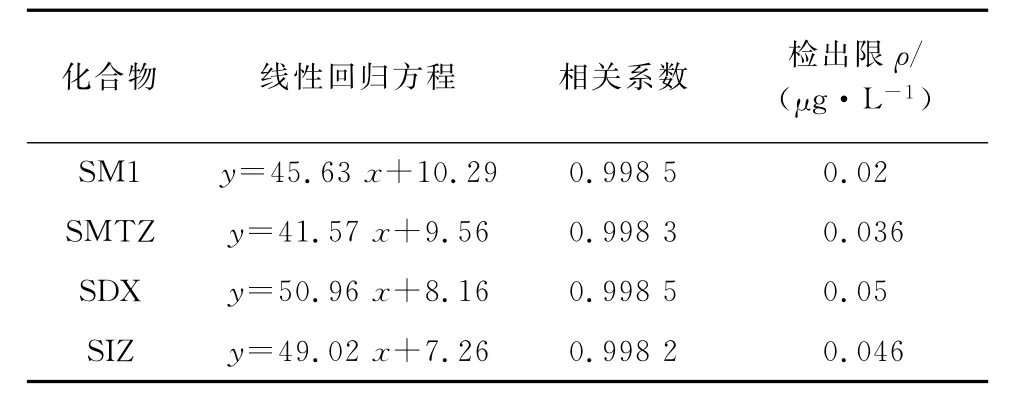
表1 线性回归方程、相关系数和检出限Tab.1 Linear regression equations,correlation coefficients and detection limits
2.6 精密度与回收试验
按试验方法对空白牛奶样品进行加标回收试验,精密度和回收试验结果见表2。

表2 精密度和回收试验结果(n=5)Tab.2 Results of tests for precision and recovery(n=5)
2.7 方法的比对
方法的检出限、线性范围和精密度与文献[11-16]方法的比较见表3。

表3 本法与其他文献方法的比较Tab.3 Comparison of the method with other literature methods
由表3可知:本方法具有较好的灵敏度、较高的富集倍数、较低的检出限,这归因于磁性石墨烯相对于其他吸附材料具有较大的表面积和较高的吸附效率。
本工作合成了磁性纳米材料CoFe2O4-G作为磁性固相萃取吸附剂富集牛奶中4种微量SAs,采用高效液相色谱法测定其含量。方法操作简便、灵敏度高、分析速率快。
[1] 耿士伟,曲斌,姜加华,等.QuEChERS-UPLC-MS/MS快速测定鸡肝中七种磺胺类药物残留[J].中国兽药杂志,2011,45(10):16-19.
[2] MARTINEZ J L.Environmental pollution by antibiotics and by antibiotic resistance determinants[J].Environmental Pollution,2009,157(11):2893-2902.
[3] ROSENBLATTFARRELL N.The landscape of antibiotic resistance[J].Environmental Health Perspectives,2009,117(6):244-250.
[4] HOMEM V,SANTOS L.Degradation and removal methods of antibiotics from aqueous matrices-a review[J].Journal of Environmental Management,2011,92(10):2304-2347.
[5] CHU Q,ZHANG D,WANG J,et al.Multi-residue analysis of sulfonamides in animal tissues by capillary zone electrophoresis with electrochemical detection[J].Journal of the Science of Food &Agriculture,2009,89(14):2498-2504.
[6] 胡文凌,张杰,余卫娟,等.磁固相萃取-高效液相色谱法测定环境水样中双酚A[J].理化检验-化学分册,2015,51(2):153-156.
[7] 连丽丽,郭亭秀,吴玉清,等.磁性固相萃取-液相色谱法测定环境水样中痕量的微囊藻毒素[J].分析化学,2015,43(12):1876-1881.
[8] YE N,SHI P,WANG Q,et al.Graphene as solidphase extraction adsorbent for CZE determination of sulfonamide residues in meat samples[J].Chromatographia,2013,76(9/10):553-557.
[9] WANG Y,LIU L,XIAO C,et al.Rapid determination of trace sulfonamides in milk by graphene oxidebased magnetic solid phase extraction coupled with HPLC-MS/MS[J].Food Analytical Methods,2016,9(9):2521-2530.
[10] MARCANO D C,KOSYNKIN D V,BERLIN J M,et al.Improved synthesis of graphene oxide[J].Acs Nano,2010,4(8):4806-4814.
[11] YAO Y,YANG Z,ZHANG D,et al.Magnetic CoFe2O4-graphene hybrids:facile synthesis,characterization,and catalytic properties[J].Industrial &Engineering Chemistry Research,2012,51(17):6044-6051.
[12] LI B,CAO H,SHAO J,et al.Co3O4@graphene composites as anode materials for high-performance lithium ion batteries[J].Inorganic Chemistry,2011,50(5):1628-32.
[13] 崔晓君,武小鹰,徐立恒,等.固相萃取-高效液相色谱测定奶粉中磺胺类抗生素残留[J].食品科技,2010(2):235-237.
[14] 吴银良,赵莉,刘勇军,等.固相萃取-高效液相色谱法同时测定牛奶中残留的9种磺胺类药物[J].色谱,2007,25(5):728-731.
[15] 邵金良,杨东顺,王丽,等.固相萃取-高效液相色谱法同时测定牛奶中13种磺胺残留[J].分析试验室,2014,33(11):1322-1325.
[16] 韩宝武.多壁碳纳米管固相萃取-液/质联用对牛奶中残留抗生素的检测[D].成都:成都理工大学,2008.
O652.63
B
1001-4020(2017)05-0562-04
10.11973/lhjy-hx201705015
2017-07-01
江苏省卫计委预防医学科研课题(Y2015033);江苏省卫计委预防医学科研课题(Y2015035);淮安市科技局科技支撑(社会发展)项目(HAS2015030)
*通信联系人。hacdcwq@sina.com

