妇科恶性肿瘤合并癌性腹水患者应用腹腔热灌注化疗的疗效观察
董学彩,杨 静,段树锋
(新乡市中心医院妇瘤科,河南 新乡 453000)
妇科恶性肿瘤合并癌性腹水患者应用腹腔热灌注化疗的疗效观察
董学彩,杨 静,段树锋
(新乡市中心医院妇瘤科,河南 新乡 453000)
目的 观察妇科恶性肿瘤合并癌性腹水患者应用腹腔热灌注化疗的疗效。方法 选取60例妇科恶性肿瘤伴有癌性腹水患者,给予体外循环热灌注化疗后,观察患者恶性腹水量及相关肿瘤标志物的情况。结果 16例患者腹水减少程度高于90.00%,37例患者腹水减少程度高于50.00%,治疗总有效率为88.33%;治疗后患者血红蛋白水平及腹水最大直径均优于治疗前(P均<0.05),而白细胞计数及血清白蛋白水平均未见明显改变(P均>0.05);相关肿瘤标志物水平均较治疗前降低(P均<0.05)。不良反应较轻,仅有11.67%患者出现恶心、呕吐等不良反应。结论 妇科恶性肿瘤合并癌性腹水患者应用腹腔热灌注化疗的疗效较为理想,安全性高,且患者耐受性较佳,临床上值得进一步推广和应用。
恶性肿瘤;癌性腹水;腹腔热灌注化疗;肿瘤标志物
腹水作为多发于妇科恶性肿瘤的并发症,其液体的大量产生,会对患者的食欲、体力情况造成严重的影响,使得其生活水平难以提高[1-3]。因此,如何更为有效治疗腹水等并发症以缓解妇科恶性肿瘤患者的临床症状,进一步改善其生活质量等意义重大。近年来,腹腔热灌注化疗逐渐成为治疗浆膜腔积液的先进手段[4-5]。多项研究[6-9]报道指出,腹腔热灌注化疗在肺癌、卵巢癌及结肠癌等不同肿瘤引起的胸腹腔恶性积液中发挥着显著的临床疗效。因此,本研究就我院60例妇科恶性肿瘤伴有癌性腹水患者进行探讨,分析其应用腹腔热灌注化疗的疗效。
1 资料与方法
1.1 一般资料 利用随机数字表法选取我院2013年1月至2016年6月60例妇科恶性肿瘤伴有癌性腹水患者,年龄40~68(54.07±4.33)岁;卵巢癌35例,宫颈癌12例,子宫内膜癌8例,输卵管癌1例,恶性畸胎瘤4例。全部患者均严格按照相应恶性肿瘤诊断标准入选。
1.2 腹腔热灌注化疗方法 通过B超探查患者腹水最大直径位置或CF-ABC12Ga型深静脉管于患者左下腹进行置管操作,穿刺置管操作方法按照常规腹腔穿刺进行。采取HGGZ-102型体腔热灌注治疗机,进行腹腔连接置管,若患者腹水量过多,则按照其实际情况可排放约1 000 mL腹水,并将1 000~1 500 mL氯化钠注射液加温至43~44 ℃,以较慢的速度注入腹腔,同时保留10~15 min,注入过程中实时观察受试者血压、心率、氧饱和度等情况。接着将1 000 mL缓慢放出,且检测回流腹水温度应高于41 ℃。重复以上操作3次,总时间约为2 h,然后于患者腹腔内将30 mg·m-2顺铂注入。腹腔热灌注化疗的频次为1次/5 d,15 d为1疗程。
1.3 肿瘤标志物检测 采集患者治疗前后的腹水3 mL,-5 ℃,无抗凝剂,经4 500 r·min-1低温离心后,分装上清液,并于-75 ℃保存。通过电化学发光免疫法对CA125、CA199、CA153、CA242及CEA进行检测,检测严格根据试剂盒说明指南完成,建议肿瘤标志物检测参考值:CA125、CA153、CA199均低于35 u·mL-1,CA242低于1.5 u·mL-1,CEA低于5 ng·mL-1。
1.4 观察指标 治疗前后腹水减少程度,治疗总有效率;治疗前后相关肿瘤标志物的变化;血红蛋白(hemoglobin,Hb)、白细胞(white blood-cell,WBC)及血清白蛋白(serum albumin,ALB)水平等情况;恶心、呕吐等并发症发生情况。在同一体位下,经床旁B超对患者最大腹水直径进行检测,治疗前检测3次后取其均值,治疗后每3 d进行1次B超检测,观察患者腹水情况,共15 d。

2 结果
2.1 临床疗效 治疗15 d后,16例患者腹水减少程度高于90.00%,37例患者腹水减少程度高于50.00%,7例未见显著变化,治疗总有效率为88.33%。
2.2 治疗前后Hb、WBC等指标变化情况 治疗后患者Hb水平及腹水最大直径均优于治疗前(P均<0.05),而WBC、ALB水平均未见明显改善(P均>0.05)。见表1。
2.3 治疗前后相关肿瘤标志物检测情况 CA125、CA199、CA153、CA242及CEA等相关肿瘤标志物水平均较治疗前低(P均<0.05)。见表2。
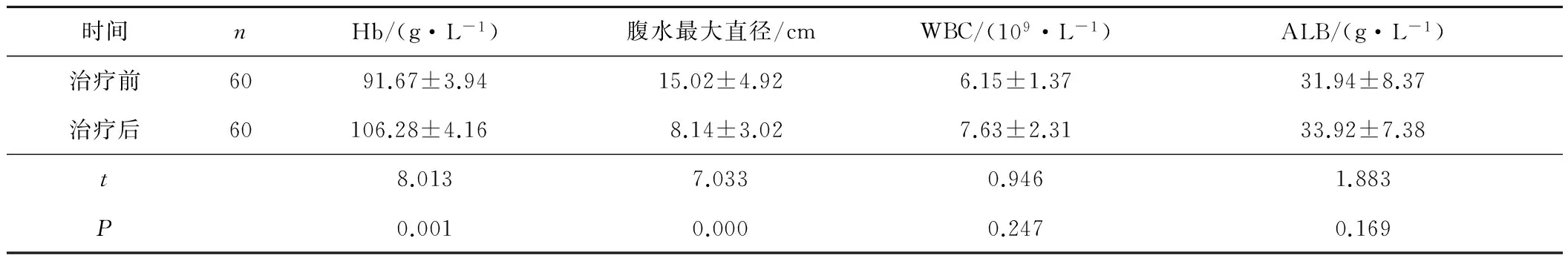
表1 治疗前后各指标变化情况
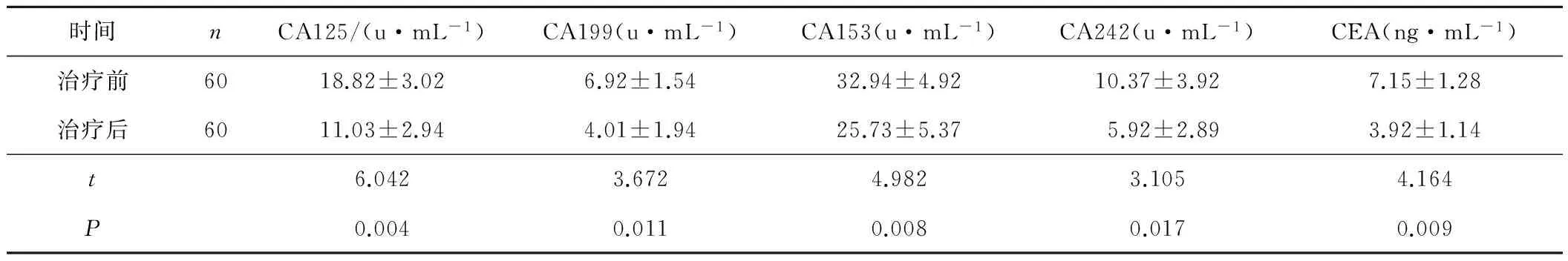
表2 治疗前后相关肿瘤标志物检测情况
2.4 治疗后不良反应发生情况 仅有7例(11.67%)患者出现恶心、呕吐等不良反应,其他患者均未见不适感。
3 讨论
研究[10]表明,组织细胞可耐受48 ℃高温并维持1 h,但肿瘤细胞于42 ℃维持1 h会产生不可逆损害情况。有研究[11-12]认为,肿瘤细胞对热敏感度要较正常细胞高出2倍。若温度不低于43 ℃,则每提高1 ℃,其杀伤细胞能力会提升2倍;在43 ℃的条件下增加作用时间1倍,亦会引起其杀伤细胞能力提升2倍。腹腔热灌注化疗是基于肿瘤细胞热敏感性的治疗方法之一,热疗的直接物理作用表现在细胞、组织、基因或分子等各种方面对患者肿瘤细胞造成一定的影响[13-15],具体体现在:引起患者肿瘤内部的微血管栓塞情况的出现,造成肿瘤细胞营养摄入受阻;溶酶体得以激活,使得肿瘤细胞及胞核遭受破坏,引起化疗药物与DNA直接交联,使得S期与M期细胞凋亡的情况发生;诱导促细胞凋亡基因包括肿瘤坏死因子、野生型P53的表达下降等情况。而温度不低于45 ℃或作用时间增加时,可能会导致患者脏器灼伤[16]。因此,应用腹腔热灌注化疗期间,应当对温度引起足够重视,起先灌注、腔内温度降低相对较快,此时可以适当提升灌注速度;而温度上升至最大治疗温度或患者无法承受时,应当降低灌注速度。
应用腹腔热灌注化疗时,较常用的药物顺铂是一种周期非特异性广谱抗肿瘤药物,有显著的水溶性,能够与不同化疗药物形成协同作用,特别是局部用药时,顺铂药物有效浓度可于患者体腔内保持较长时间,能够将局部各周期的肿瘤细胞有效杀灭[17-18]。并且,当在温度43 ℃的环境下,热灌注与顺铂结合治疗,能够取得良好的协同增敏效果,进而提升其抗肿瘤作用。目前,关于腹腔内灌注的药物与剂量的看法不一,而普遍认为应用腹腔热灌注化疗的治疗机制在很大程度上由化疗药物细胞毒性与温热对肿瘤细胞杀伤的双重效果决定。较多通过加温的含药溶液可以显著分布于患者腹腔的不同部位,引起其腹腔内微小癌灶较长时间浸泡于较高浓度的化疗药物中,同时通过其腹腔内危险静脉较长时间的吸收后,能够直接杀死门静脉系统内部的肿瘤细胞。并且,患者腹腔内灌注的抗肿瘤药物于肝脏代谢呈现无毒的特征后进入其血液中,能够有效减轻化疗药物的全身不良反应。从本次研究结果中发现,恶心、呕吐是其出现较多的不良反应,共有7例(11.67%)患者出现,但症状较轻微,经常规止呕等治疗后得到明显改善,其他患者均未见不适感。
本次研究结果发现,治疗15 d后,16例患者腹水减少程度高于90.00%,37例患者腹水减少程度高于50.00%,仅有7例未见显著变化,治疗总有效率为88.33%。治疗后患者Hb水平及腹水最大直径均优于治疗前,而WBC计数及ALB水平均未见明显差异。CA125、CA199、CA153、CA242及CEA等相关肿瘤标志物水平均较治疗前降低。可见,应用腹腔热灌注化疗后,患者腹水、Hb水平等指标能够明显改善;并且,检测相关肿瘤标志物可在腹腔热灌注化疗的疗效评估中起着一定的预测作用。
综上所述,妇科恶性肿瘤合并癌性腹水患者应用腹腔热灌注化疗的疗效较为理想,安全性高,方法方便可行,对患者创伤较轻,且患者耐受性较佳,有着较高的应用价值。
[1] 白艳艳.细胞减灭术联合腹腔热灌注化疗治疗腹膜癌的围术期规范化护理[J].癌症进展,2016,14(9):926-928.
[2] KUSAMURA S,TORRES MPA,CABRAS A,et al.The Role of Ki-67 and Pre-cytoreduction Parameters in Selecting Diffuse Malignant Peritoneal Mesothelioma (DMPM) Patients for Cytoreductive Surgery (CRS) and Hyperthermic Intraperitoneal Chemotherapy (HIPEC)[J].Ann Surg Oncol,2016,23(5):1468-1473.
[3] 詹高房,雷建,陈劲松.腹腔热灌注化疗联合 XELOX 方案治疗胃肠癌恶性腹腔积液的效果[J].广东医学,2014,(17):2732-2734.
[4] PASSOT G,VAUDOYER D,VILLENEUVE L,et al.What made hyperthermic intraperitoneal chemotherapy an effective curative treatment for peritoneal surface malignancy: A 25-year experience with 1,125 procedures[J].J Surg Oncol,2016,113(7):796-803.[5] 燕海姣,吴骏,孙文辉.吉西他滨联合腹腔热灌注顺铂治疗复发性卵巢癌的临床观察[J].肿瘤基础与临床,2014,(6):479-481,482.
[6] 陈勇.卡铂联合5-氟尿嘧啶腹腔热灌注治疗恶性腹腔积液临床研究[J].河北医科大学学报,2013,34(3):270-272.
[7] HONORÉ C,GOÉRÉ D,MACOVEI R,et al.Peritoneal carcinomatosis from unusual cancer origins:Is there a role for hyperthermic intraperitoneal chemotherapy?[J].J Visc Surg, 2016,153(2):101-107.
[8] 温爱萍.腹腔热灌注化疗治疗胃癌合并恶性腹腔积液的临床观察[J].河北医药,2013,(18):2814-2816.
[9] 杨越,张蕾,崔瑶,等.全身化疗联合腹腔热灌注化疗并射频热疗治疗晚期卵巢癌[J].肿瘤基础与临床,2014,(3):213-214.
[10]王琳,苏英花,侯孟君.腹腔热灌注联合化疗治疗恶性腹水46例临床护理[J].齐鲁护理杂志,2012,18(26):86-87.
[11]李明天,吴枚禅,卢云媚.卵巢癌病人使用腹腔热灌注机化疗术中护理[J].全科护理,2014,12(2):162-163.
[12]王增会.腹腔热灌注化疗药物及常温灌注生物制剂治疗癌性腹腔积液疗效观察[J].实用心脑肺血管病杂志,2012,20(6):1052-1052.
[13]IHEMELANDU C,BIJELIC L,SUGARBAKER PH.Iterative cytoreductive surgery and hyperthermic intraperitoneal chemotherapy for recurrent or progressive diffuse malignant peritoneal mesothelioma: clinicopathologic characteristics and survival outcome[J].Ann Surg Oncol,2015,22(5):1680-1685.
[14]HELM JH,MIURA JT,GLENN JA,et al.Cytoreductive surgery and hyperthermic intraperitoneal chemotherapy for malignant peritoneal mesothelioma: a systematic review and meta-analysis[J].Ann Surg Oncol,2015,22(5):1686-1693.
[15]POLANCO PM,DING Y,KNOX JM,et al.Institutional learning curve of cytoreductive surgery and hyperthermic intraperitoneal chemoperfusion for peritoneal malignancies[J].Ann Surg Oncol,2015,22(5):1673-1679.
[16]万凌.腹腔热灌注联合靶向药物化疗治疗恶性腹水的临床护理路径及体会[J].实用临床医药杂志,2014,18(4):33-35.
[17]BHAGWANDIN SB,Salti GI.Hepatocellular carcinoma with peritoneal metastasis treated with cytoreductive surgery plus hyperthermic intraperitoneal chemotherapy[J].Tumori,2015,101(1):e1-e3.
[18]陈祖龙,吴印兵,唐鸿生,等.腹腔热灌注化疗联合静脉化疗治疗恶性腹水的临床疗效观察[J].实用医学杂志,2014,(18):2950-2952.
Clinical Observation of Hyperthermic Intraperitoneal Chemotherapy in the Treatment of Gynecological Malignant Tumor Complicated with Malignant Seroperitoneum
DONG Xuecai,YANG Jing,DUAN Shufeng
(DepartmentGynecologicOncology,XinxiangCentralHospital,Xinxiang453000,China)
Objective To observe the curative effects of hyperthermic intraperitoneal chemotherapy in the treatment of gynecological malignant tumor complicated with malignant seroperitoneum.Methods Sixty cases of gynecological malignant tumor complicated with malignant seroperitoneum were selected,and the changes in volume of seroperitoneum and tumor markers were observed after extracorporeal circulation hyperthermic intraperitoneal chemotherapy.Results The degree of reduction in the amount of seroperitoneum was significantly higher than 90.00% in the cases,higher than 50.00% in the 37 cases,and the total effective rate was 88.33%; after treatment,the hemoglobin content and the maximum diameter of seroperitoneum were better than before treatment (P<0.05),white the white blood-cell count and serum albumin showed no significant difference (P>0.05); the levels of tumor markers were lower before treatment (P<0.05); only 11.67% of patients had nausea and vomiting.Conclusion Intraperitoneal hyperthermic chemotherapy in the treatment of gynecological malignant tumor complicated with malignant seroperitoneum has obvious effect,and has the high safety and tolerance.
malignant tumor; malignant seroperitoneum; hyperthermic intraperitoneal chemotherapy; tumor marker
董学彩(1970-),女,硕士,副主任医师,主要从事妇科肿瘤相关研究。E-mail:niee58765@163.com
10.3969/j.issn.1673-5412.2017.03.007
R737.3;R730.6
A
1673-5412(2017)03-0206-04
2016-09-22)

