层级纳米花环状Bi2O3/(BiO)2CO3复合材料光催化降解罗丹明B
宋强 李莉*,, 罗鸿祥 刘越 杨长龙(齐齐哈尔大学材料科学与工程学院,齐齐哈尔6006)(齐齐哈尔大学化学与化学工程学院,齐齐哈尔6006)(黑龙江省高校精细化工重点实验室,齐齐哈尔6006)
层级纳米花环状Bi2O3/(BiO)2CO3复合材料光催化降解罗丹明B
宋强1,2李莉*,1,2,3罗鸿祥2刘越2杨长龙1
(1齐齐哈尔大学材料科学与工程学院,齐齐哈尔161006)
(2齐齐哈尔大学化学与化学工程学院,齐齐哈尔161006)
(3黑龙江省高校精细化工重点实验室,齐齐哈尔161006)
通过程序升温水热法制备了层级纳米花状结构Bi2O3/(BiO)2CO3复合材料(简称BO/BCO)。采用X射线衍射(XRD)、紫外-可见漫反射吸收光谱(UV-Vis/DRS)、X射线光电子能谱(XPS)、扫描电子显微镜(SEM)、透射电子显微镜(TEM)和氮气吸附-脱附测定等方法对上述合成材料的晶型结构、组成、光吸收性质、形貌和表面物理化学性质进行了表征。结果表明,该复合材料中(BiO)2CO3的晶型为四方相,Bi2O3的晶型为单斜相,复合后的材料同时具有两者晶型结构。并且,合成时随着OH-的引入与反应时间的增加,复合材料中(BiO)2CO3的特征衍射峰强度逐渐降低,Bi2O3的特征衍射峰强度逐渐增加,证明了Bi2O3在样品中所占比例的增加。从UV-Vis/DRS吸收光谱分析结果显示,与单体(BiO)2CO3和单体Bi2O3相比,合成的BO/BCO复合材料的吸收边带发生偏移,且Bi2O3的引入有效增加其可见光区吸收。同时,样品由片状(BiO)2CO3生长为层级纳米花环状结构的BO/BCO-0.5,而层级结构的形成导致BO/BCO-0.5的带隙能变窄,且对于光电子的反射与散射发生改变,从而有利于光生电荷的转移与光的吸收效率。另外,以罗丹明B为模型分子,通过不同光源照射下的光催化活性实验,循环实验以及捕获实验对复合材料BO/BCO的光催化活性进行了研究。结果表明,与其他体系(单体Bi2O3和P25)相比,BO/BCO-0.5活性有明显提高,并且在多次循环实验后依然保持良好的稳定性。此外,根据捕获实验结果推测了BO/BCO复合材料可能的光催化反应机理。
程序升温水热法;氧化铋;碳酸氧铋;层级纳米花环状结构;光催化降解;罗丹明B
0 引言
近年来,经济全面快速增长的同时出现了严重的环境污染问题,而水污染尤为严重。目前,工业处理废水的方法有多种,如沉淀法、物理吸附、膜过滤技术、电解法、化学氧化法、微生物处理法等,这些方法存在能耗高、效率低、易产生二次污染等缺陷。半导体光催化技术由于绿色、环境友好等优点,已被人们不断研究和拓展[1-4]。然而,单纯的半导体材料由于存在带隙较宽、光利用率低等缺陷,一定程度上限制了其光催化技术的实际应用[5]。为此,研究者越来越多地致力于探索半导体新材料,同时着眼于材料改性的研究,包括:半导体掺杂(Ag,Au,Pt和Pd等贵金属,N等非金属,Bi半金属等的掺杂)[6-8],半导体复合[9-10],使用模板剂优化产物形貌和性能[11],从而进一步改善材料的光催化效率。
Bi系层状化合物由于其独特的层状异质结结构,有利于光致电荷分离,从而提高量子效率。近年来,大量关于含Bi元素的半导体,其中包含:BiVO3、Bi2O3、BiOI、Bi2S3等以及包含它们的复合材料被研究,并应用到光催化降解领域[12-14]。(BiO)2CO3首次报道于1984年,主要应用于微电极和医药领域,而对于其合成和光催化性能一直鲜有报道[15]。(BiO)2CO3晶体结构为正交晶体,由[Bi2O2]2+和[CO3]2-层垂直交替组装而成。纯的(BiO)2CO3与P25相比,具有良好的光催化活性[16]。然而,(BiO)2CO3带隙较宽,只能被紫外光激发,一定程度上限定了它的光应用范围。因此,研究者开展了针对(BiO)2CO3的改性研究,包括Bi-(BiO)2CO3,CO32--(BiO)2CO3,Bi2S3/(BiO)2CO3,BiOI/ (BiO)2CO3等的制备与性能测试[17-18]。相比于单体(BiO)2CO3,改性后Bi系材料的光吸收范围扩展到可见光区,一定程度上提高了(BiO)2CO3的量子效率,例如,董帆教授[17]制备了Bi半金属掺杂的(BiO)2CO3可以有效增强在可见光区的吸收效率;Huang等[18]通过制备掺杂CO32-的(BiO)2CO3,将CO32-自掺杂入(BiO)2CO3的晶格内,将(BiO)2CO3的吸收范围从紫外光区扩展到可见光区。
据此,本文开展了Bi2O3与(BiO)2CO3的复合,主要是因为它们都是铋系半导体,复合方式简便,并且两者带隙能不同,导带与价带的电势位置存在梯度差异。与单体相比,形成的复合材料能增强光生电子-空穴的转移途径,延长光生电荷的寿命,从而有利于光催化反应。研究中,以柠檬酸铋作为铋源,以碳酸钠,氢氧化钠作为原料,在程序升温水热法下合成得到BO/BCO复合材料。同时,复合材料的生成源自于反应中OH-的引入,在水热条件下一定程度上控制系统中Bi2O3的生成,从而改变(BiO)2CO3的量。研究中通过考察固定氢氧化钠的量,延长反应时间,制备了不同反应时间下的复合产物,并且较为系统地研究了其性质变化规律。同时,通过不同光源照射进一步深入讨论了复合产物BO/BCO光催化活性,以及其降解罗丹明B与单体Bi2O3,(BiO)2CO3和P25降解罗丹明B的结果进行对比,获得了其催化效果明显提高的结论。
1 实验部分
1.1 试剂
柠檬酸铋(99.99%)购于深圳市迈瑞尔化学技术有限公司,对苯醌、乙二酸四乙酸二钠、无水乙醇,氢氧化钠(96.0%),无水碳酸钠(99.8%)购于天津凯通化学试剂有限公司,罗丹明B(RhB)、龙胆紫(CV)、甲基橙(MO)、水杨酸(SA)和刚果红(CR)购于北京化工厂,所有试剂均为AR分析纯。全部实验用水均为二次蒸馏水。
1.2 Bi2O3与(BiO)2CO3材料制备
(BiO)2CO3制备:Na2CO3(0.217 molL-1)溶液中加入1.6 g柠檬酸铋,搅拌30min。然后,160℃水热条件下保持24 h。最后,将所得产品用去离子水和乙醇洗涤,于60℃下干燥12 h得到样品。
Bi2O3制备:柠檬酸铋(0.210mol·L-1)溶液中滴加定量的NaOH(1 mol·L-1NaOH)溶液,搅拌3 h后,160℃水热条件下保持24 h。最后,将所得产品用去离子水和乙醇洗涤,于60℃下干燥12 h得到样品。
1.3 Bi2O3/(BiO)2CO3复合材料的制备
取二次蒸馏水60 mL 4份,分别加入0.46 g Na2CO3,使其充分溶解。再加入1.6 g柠檬酸铋,搅拌30min。待溶液澄清后,逐滴加入定量的NaOH(0.2 g NaOH,5mL去离子水)溶液,继续搅拌,搅拌时间分别为3、2、1、0.5 h,使其完全反应。将上述混合溶液转移到聚四氟乙烯反应釜中,在160℃水热条件下保持24 h。然后,将所得产品用去离子水和乙醇洗涤后,在60℃下干燥12 h,得到样品根据反应时间分别标记为BO/BCO-3、BO/BCO-2、BO/BCO-1和BO/BCO-0.5。实验中作为对比样品,纯的(BiO)2CO3采用与BO/BCO-0.5相同的制备条件,没有NaOH加入;对比样品纯的Bi2O3的制备条件是加入足量NaOH,用相同水热条件制备。
1.4 仪器及表征条件
样品的XRD表征采用德国Bruker-AXS(D8) X射线衍射仪进行分析,条件为Cu靶,Kα线(λ= 0.154 06 nm),管电压40 kV,防散射狭缝0.6°,发射狭缝0.6°,扫描范围10°~80°,扫描速度1°·min-1;样品的形貌采用扫描电子显微镜(SEM,HitachS-4300,工作电压为5 kV)与透射电子显微镜(TEM,JEM-2100F,加速电压为100 kV。具体方法是:样品被分散到乙醇溶液中,超声5min,然后将其滴加在铜网上,干燥后用于透射电镜观察)进行分析;样品的XPS谱采用VG-ADES400X射线光电子能谱仪测定,Mg Kα(hν=1 486.6 eV)作为激发源,真空度为1× 10-8Pa。以样品中的碳氢C1s(Eb=284.6 eV)作为能量校正,AlK-ADES源,残留气体压力小于10-6Pa时测试;紫外-可见漫反射吸收光谱(UV-Vis/DRS)由普析通用TU-1901分光光度计(波长范围为190~900 nm,光度范围为-4.0~4.0 Abs)记录得到;样品溶液的吸光度由北京普析通用公司生产的TU-1901型紫外-可见分光光度计测定;样品的N2吸附-脱附由美国康塔公司的Quan-tachrome NoveWin2型物理吸附仪,测定温度为77 K,以氮气为吸附质,在液氮下测得。测定前样品在160℃下真空脱气3 h。
1.5 光催化实验
光催化实验装置由圆柱形石英外管和石英玻璃套环绕的内置光源构成,可见光光源为400W Xe灯(主要发射线大于410 nm,内套管采用11号玻璃制作以滤去Xe灯发射的紫外光);紫外光源为125 W高压Hg灯(主要发射线的波长大约在313.2 nm);模拟日光光催化反应由BL-GHX-V光催化反应仪构成,光源为1 000W外置Xe灯(主要发射线与太阳光光谱接近),灯与反应液大约距离8.5 cm,通过恒温乙醇循环保持反应体系温度恒定。实验中反应液(如罗丹明B,RhB)的浓度为50mg· L-1,可见光催化时催化剂用量为0.3 g,反应液体积220mL;紫外光催化时催化剂用量为0.15 g,反应液体积为90mL。光催化反应过程:将催化剂分散于罗丹明B溶液中,形成悬浮液,超声10min,避光搅拌30min,达到吸附-脱附平衡。将光强度稳定后的光源置于反应液中,每间隔一定时间取样(3 mL),离心分离后,用TU-1901紫外-可见分光光度计在罗丹明B的λmax=554 nm处测定吸光度。
2 结果与讨论
2.1 XRD表征
通过X射线衍射(XRD)分析方法对合成的(BiO)2CO3,Bi2O3和不同反应时间的BO/BCO复合材料的晶相结构与组成进行表征。图1分别是合成的Bi2O3单体,(BiO)2CO3单体、BO/BCO-3、BO/BCO-2、BO/BCO-1、BO/BCO-0.5的XRD图。首先,通过水热合成法得到的单体(BiO)2CO3可以被准确地索引到纯的四方相(BiO)2CO3(JCPDSNo.41-1488)[19]。实验中当引入OH-后,水热处理可形成黄色的Bi2O3粉末。该产物经过XRD分析测试后的结果,如图1所示。由图1可见,所合成的单体Bi2O3的衍射峰位置与标准Bi2O3的PDF卡片相比完全一致(JCPDS No. 65-2366)[20]。所合成的2种单体谱图中的曲线没有杂质峰,初步证明为单体(BiO)2CO3与单体Bi2O3。在(BiO)2CO3合成实验中,引入OH-,反应时间3 h并水热处理后得到比单体Bi2O3颜色浅的材料,与颜色为亮橙的单体Bi2O3相比,颜色为中等黄色,因此将反应时间减小,最终得到一系列的BO/BCO材料,其颜色变化随反应时间的延长,由白色(BO/BCO-0.5)变为中等黄色(BO/BCO-3),见图2。
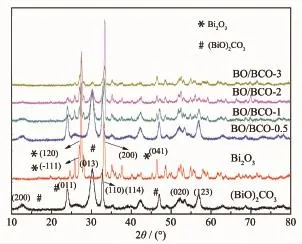
图1 单体Bi2O3,单体(BiO)2CO3,BO/BCO-0.5,BO/BCO-1,BO/BCO-2和BO/BCO-3复合材料的XRD图Fig.1 XRD patterns of the pure Bi2O3,(BiO)2CO3,BO/ BCO-0.5,BO/BCO-1,BO/BCO-2,and BO/BCO-3 composites
从图1可以看到,样品BO/BCO的XRD结果与合成的单体(BiO)2CO3与单体Bi2O3的XRD分析结果相比较发现,样品BO/BCO的XRD图上的衍射峰与2种单体的各衍射峰相接近,初步确定BO/BCO复合材料的形成。同时,所合成的单体(BiO)2CO3的晶胞参数为a=0.386 5 nm,b=1.367 5 nm,而复合材料中检测到(BiO)2CO3的晶胞参数为a=0.387 7 nm,b=1.399 8 nm,晶胞参数在复合产物形成后改变,进一步证明合成的材料为2种半导体复合[21]。且单体(BiO)2CO3与BO/BCO-0.5复合材料的XRD分析结果对比后,可以发现复合材料中(BiO)2CO3的(013)衍射峰的半峰宽为0.914,大于(BiO)2CO3的半高峰宽0.883,与之对应的是单体(BiO)2CO3的晶粒尺寸复合后由9.26增加到9.64(晶粒尺寸由谢勒公式计算得到),BO/BCO-0.5复合材料晶粒尺寸增加归因于Bi2O3的复合。

图2 不同BO/BCO复合材料的实物照片Fig.2 Real pictures of different BO/BCO composites
同时,为了研究随着反应时间的变化,Bi2O3/ (BiO)2CO3复合材料衍射峰的变化,在复合过程中,引入OH-形成Bi(OH)3,并且随着反应时间的增加,在程序升温水热下得到BO/BCO-0.5、BO/BCO-1、BO/BCO-2、BO/BCO-3复合材料。由图1所示,从BO/BCO-0.5到BO/BCO-3可见,图中属于Bi2O3的衍射峰强度增加,属于(BiO)2CO3的衍射峰强度降低。强度的变化从侧面说明物质在复合材料中的含量随反应时间延长后的变化。反应时间在0.5 h时,得到的样品BO/BCO-0.5中,(BiO)2CO3为主要成分,而在反应时间为3 h的复合材料中,Bi2O3为主体。
2.2 紫外-可见漫反射分析
为了表征复合材料的光学性质,进行了单体Bi2O3,单体(BiO)2CO3与不同反应时间的BO/BCO复合材料的紫外-可见漫反射光吸收性能分析,如图3 a所示。在图3 a可以看到,样品的吸收峰随着反应时间的延长,吸收边发生明显红移,并且在波长范围为360~450 nm中吸收峰强度明显增加,且在可见光区的光吸收高于单体(BiO)2CO3。并且随着OH-的引入,反应时间的增加,Bi2O3在复合材料中占有的含量增加,吸收强度逐渐增强。纯(BiO)2CO3的吸收主要存在于波长低于400 nm的紫外区。而单体Bi2O3的吸收扩展至可见区[22]。根据XRD分析表明,随着反应时间增加,复合材料中单体Bi2O3的含量逐渐增加,(BiO)2CO3的含量逐渐减少。因此,得到的不同反应时间的复合材料吸收边光响应增加。同时,随着反应时间的增加以及OH-的引入,BO/BCO复合材料可见光区吸收不断增加。结果表明,Bi2O3的增加在一定程度上增强了复合材料的可见光吸收,从而提高复合材料的光催化活性。在图3 b中,由于两种单体都是直接间隙半导体(n=1/2),根据(αhν)1/2与hν做图,得到所合成的单体以及复合材料的带隙能[23]。根据图3 b中的切线截到横坐标的数值,得到单体Bi2O3、单体(BiO)2CO3和BO/BCO-0.5的带隙能,结果见表1。复合后的样品与单体(BiO)2CO3对比,Eg值降低,因此,复合材料随着Bi2O3的生成其光学性质发生改变,降低了复合材料的带隙能,从而复合材料具有一定的可见光活性。
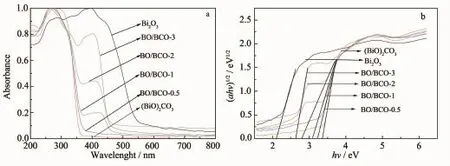
图3 不同样品的UV-Vis/DRS吸收光谱(a)与Kubelka-Munk函数与能量关系图(b)Fig.3 UV-Vis/DRS spectra(a)and Kubelka-Munk energy curves(b)of different samples
2.3 XPS测定
为了研究所合成复合材料的化学组成,确定复合材料中物质的信息,对BO/BCO-0.5复合材料进行了XPS分析,如图4。由图4a可以看到样品的全谱显示有Bi,O,C元素的存在。在图4 b可以看出,样品中Bi元素的最高峰位置的结合能分别在164.2 eV与159.05 eV,分别对应Bi4f5/2和Bi4f7/2,峰高中心的间距是5.15 eV,结果证明Bi在样品中为+3价[24]。图4 c为C1s的高分辨X射线光电子能谱,其中,在结合能284.9 eV位置的峰,对应于测试带来的偶然外来C元素所造成。在结合能288.6 eV位置的峰,归因于样品包含的(BiO)2CO3中的CO32-[25]。图4d为O1s的X射线光电子能谱,结合能位置在529.2、530.0、528.8 eV处的峰分别归因于样品中(BiO)2CO3中BiO+的Bi-O键,CO32-的C-O键以及Bi2O3中的Bi-O键。同时,529.0、533.1与531.8 eV分别归因于晶格氧、羟基氧和吸附氧[26]。另外,通过XPS分析了BO/BCO-0.5复合材料中次表面元素的组分与含量,Bi2O3与(BiO)2CO3的比例约为1∶3.3。
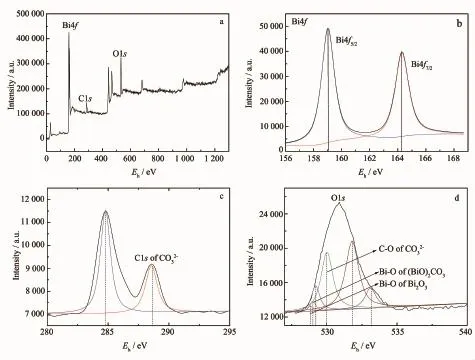
图4 复合材料BO/BCO-0.5的XPS谱图Fig.4 XPSspectra of BO/BCO-0.5 composite(a)full spectrum,(b)Bi4f,(c)C1s,and O1s(d)
2.4 扫描电镜
采用扫描电镜(SEM)分析了不同样品的形貌,如图5所示。图5a是单体(BiO)2CO3的扫描电镜图像,可以看到整体形貌结构为分散的片状,尺寸不均一,且有聚集现象,这与Bi系半导体的性质有关。(BiO)2CO3晶体结构为正交晶体结构,由[Bi2O2]2+和[CO3]2-垂直交替组装而成,并且Bi系层状化合物由于其独特的薄层状结构,有利于光致电荷分离,从而提高量子效率[27]。图5b是单体Bi2O3的扫描电镜图像,整体形貌为10μm棒组成的板状结构。当合成中添加OH-,体系中引入Bi2O3,从而形成BO/BCO复合材料,其扫描电镜如图5c,d,e所示。图5c为BO/BCO-0.5的形貌,经过OH-的引入与水热反应中Bi2O3的生成,BO/BCO-0.5自组装产生层级结构,外形整体为层级花环状,尺寸大约在200~400 nm。复合物形成过程中,由于Sillén结构,[BiO]22+层与CO32-层混合导致纳米片的形成。该结构的形成是由于水热条件下,(BiO)2CO3半导体形成,同时在(BiO)2CO3表面上Bi(OH)3在水热条件下分解为Bi2O3,并且体系中的(BiO)2CO3在碱性环境中生成少量的Bi2O3。由图5a中(BiO)2CO3纳米片的自然聚集,双晶核在形成中的相互作用影响了整体形貌,使(BiO)2CO3表面出现聚集,重叠,最终形成特殊的层级花环状结构的BC/BOC-0.5。并且从图5a中可以看到纳米片之间相互聚集,这也有利于层级结构的形成。层级结构的形成,有利于复合材料对光的反射与散射,从而有效利用光能,有利于光催化活性的提高[28]。然而,当反应时间增加,溶液中产生的Bi(OH)3增加,程序升温中形成的Bi2O3增多,如图5d所示。BO/BCO-0.5产物的形貌被破坏,生成具有大小不均一、圆滑的纳米片。同时,随着反应时间进一步增加,所形成的复合物以Bi2O3为主体,整体为70 nm棒状结构。Bi2O3的增加导致形貌的变化,从而对复合物的性质产生一定的影响。根据实验过程以及XRD结果,本文推测了(BiO)2CO3与Bi2O3可能的转换机理,如图6所示。

图5 (BiO)2CO3(a),Bi2O3(b),BO/BCO-0.5(c),BO/BCO-1(d)与BO/BCO-2(e)的扫描电镜照片Fig.5 SEM images of(BiO)2CO3(a),pure Bi2O3(b),BO/BCO-0.5(c),BO/BCO-1(d)and BO/BCO-2(e)
另外,BO/BCO-0.5复合材料的形貌结构与晶体结构被HR-TEM进一步分析,如图7所示。图7a,b是层级花环状结构BO/BCO-0.5复合材料的TEM图像。由图7a可见,层级结构的组成是由纳米片自组装形成,纳米片围绕圆心在四周叠加、组装、交叉,形成层级结构。通过Gatan Digital Micro Group软件分析图7c原件,得到多种晶格条纹,通过计算得到其中的晶格间距分别为3.31、3.28、3.75和1.93 nm,分别对应Bi2O3的(111)和(120)晶面,(BiO)2CO3的(011)和(020)晶面。并且根据晶面的分布,Bi2O3在水热过程中与(BiO)2CO3复合,大部分集中在纳米片的边缘位置,以静电引力,使复合了Bi2O3的(BiO)2CO3围绕圆心排列、叠加,从而形成独特的层环状纳米结构,详细的形貌由图7a,b所示。
2.5 N2吸附-脱附分析
图8a,b和c分别给出了单体Bi2O3,单体(BiO)2CO3和BO/BCO-0.5复合材料的氮气吸附-脱附等温线以及孔径分布曲线。单体Bi2O3的等温线类型为Ⅲ型,H1型滞后环。Ⅲ型等温线以向相对压力轴凸出为特征,这种等温线在有宏孔的固体上发生弱的气-固相互作用时出现。从图8b,c看出,单体(BiO)2CO3和复合物BO/BCO-0.5均为Ⅳ型等温线,H3型滞后环,表现为典型的介孔结构吸附等温线,这种等温线的结构与滞后环是由结构中颗粒的聚集所引起的。H1型滞后环表现为孔径分布较窄的孔径材料,H3型滞后环表示形貌为片状固体[29]。氮气吸附-脱附分析表明,复合物中Bi2O3的引入,导致BO/BCO-0.5的比表面积增加,孔体积增加,这有效地增加了样品BO/BCO-0.5的实际效果。同时,从等温线与滞后环得到的结果,片状的单体(BiO)2CO3中被掺入Bi2O3后,依然呈现H3型滞后环,Ⅳ型等温线,少量Bi2O3的引入有效促进样品的形貌发生变化,比表面积与孔体积增加,这有利于反应中为染料分子与光生基团提供更多的活性位,从而有效增加光催化效果。但随着Bi2O3的增加,复合材料的比表面积减小,平均孔径与微分孔体积在BO/BCO-0.5样品后逐渐降低,与Bi2O3类似,这表明Bi2O3的复合量太大会在一定程度上影响比表面积并导致光催化活性下降,该结果与后续2.6光催化实验结果一致。

图6 (BiO)2CO3与Bi2O3可能的转换机理Fig.6 Possible conversionmechanism of(BiO)2CO3and Bi2O3
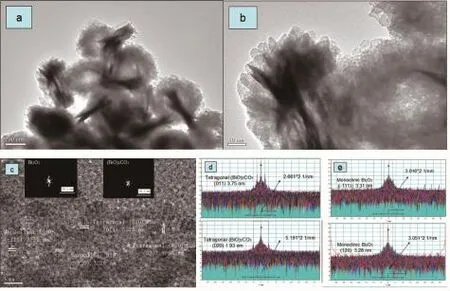
图7 复合材料BO/BCO-0.5的高分辨率透射电子显微镜电镜照片与FFT分析Fig.7 HR-TEM images(a,b,c),FFT line plot(d,e)and FFT(inset images in Fig 6 c)of BO/BCO-0.5 composite
2.6 光催化实验
为了考察BO/BCO系列复合材料在不同光源下对罗丹明B降解效果,进行了不同光催化活性对比实验,包括:紫外光(图9a),可见光(图9c),模拟日光(图9d)。结果显示,BO/BCO-0.5复合材料的催化活性高于罗丹明B的直接光催化降解以及P25,单体(BiO)2CO3的光催化结果,这证明随着适量Bi2O3的引入形成的BO/BCO复合材料,其活性有效增加。但是,随着搅拌反应时间的增加BO/BCO复合材料中Bi2O3的比例增加,反而抑制光催化活性。说明随着半导体Bi2O3与(BiO)2CO3复合,光学性能优于单体,且适量Bi2O3的引入有效增加光催化。在紫外光条件下,BO/BCO-0.5降解效果最佳,在反应进行到60 min时已经降解大部分,比单体(BiO)2CO3降解的更加迅速。如图9b所示,紫外光催化活性实验的反应动力学的结果表明,-ln(Ct/C0)与反应时间t基本呈线性关系,这说明对染料罗丹明B的光催化降解遵循准一级反应动力学。经计算,P25,Bi2O3,(BiO)2CO3,BO/BCO-0.5,BO/BCO-1,BO/BCO-2和BO/BCO-3的紫外光催化降解罗丹明B的表观反应速率常数分别为0.002 15、0.006 2、0.005 49、0.021 9、0.033 3、0.016 05、0.005 57、0.002 15 min-1。由此可知,催化剂的活性顺序为:BO/BCO-0.5>(BiO)2CO3>BO/BCO-1>P25>BO/BCO-2>Bi2O3>BO/BCO-3>紫外光直解降解,导致这样结果的原因:BO/BCO-0.5与其他样品相比,具有特殊的层级纳米花环状形貌,并且从物理化学性质方面分析具有较大的比表面积与孔径,这些优势增加了其光吸收效率[30-31]。
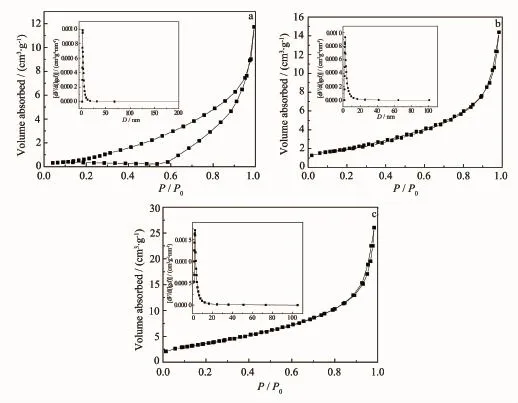
图8 不同催化剂的氮气吸附-脱附等温线和孔径分布曲线Fig.8 N2adsorption-desorption isotherms and pore size distribution curves(inset images)of pure Bi2O3(a),pure(BiO)2CO3
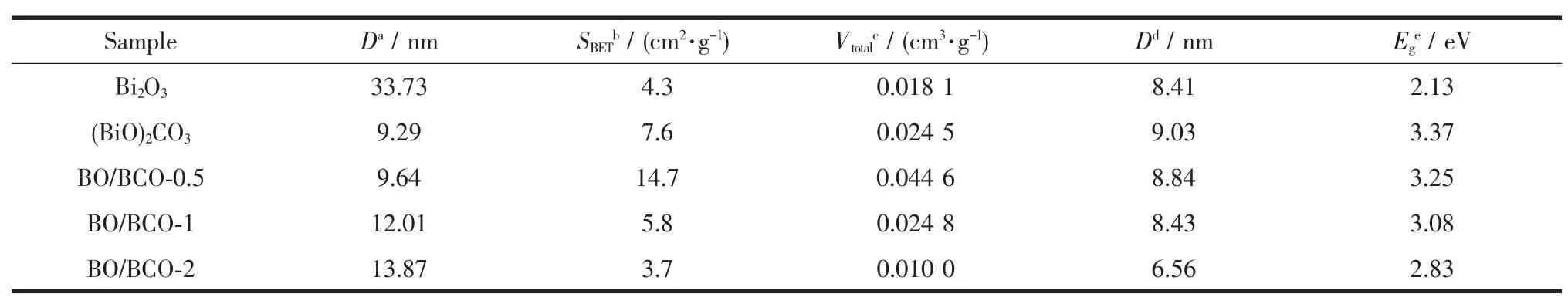
表1 Bi2O3、(BiO)2CO3、BO/BCO-0.5、BO/BCO-1和BO/BCO-2的晶粒尺寸、比表面积、孔体积、平均孔径和带隙能Table 1 Crystallite sizes,BET surface areas,pore volumes and average pore diameters and band gap energy of Bi2O3, (BiO)2CO3,BO/BCO-0.5,BO/BCO-1 and BO/BCO-2
为考察本文所合成复合材料的光催化活性,一方面研究了Bi2O3的引入对(BiO)2CO3材料的光催化活性的影响,另一方面也研究了随着反应时间的增加,Bi2O3在产物中所占的比例增加对复合材料的光催化活性的影响,从而进行了不同光源照射下的光催化对比实验,结果如图9所示。为了证明光催化材料在光催化反应中的稳定性,本文对样品进行光催化循环实验,催化剂循环使用过程如图10a所示。其中,每次重复实验均回收上一次光催化使用的催化剂,并分别进行去离子水、无水乙醇3次洗涤与干燥过程。循环实验结果显示,所合成的BO/BCO-0.5复合材料循环3次后的降解效果,虽然有所降低,依然保持较高的活性,其稳定性较好。其光催化活性的部分降低是由于循环过程中催化剂经搅拌以及光催化反应有可能造成材料表面形貌的变化,从而导致材料比表面积减小,以至于光催化活性降低;同时,循环过程中材料表面微量的残留污染物也是造成活性降低的原因之一。在催化剂回收过程中,虽经过去离子水、乙醇洗涤与干燥过程,但仍旧会有染料等吸附在催化剂表面,造成催化剂的孔隙被堵塞,从而导致催化剂表面活性位点降低,进而降解效果下降。另外,针对不同有机污染物(罗丹明B(RhB)、龙胆紫(CV)、甲基橙(MO)、水杨酸(SA)和刚果红(CR))(图10b),BO/BCO-0.5在紫外光下分别光催化降解上述5种反应物均呈现不同程度的降解效果,表明其催化效果具有普遍性。
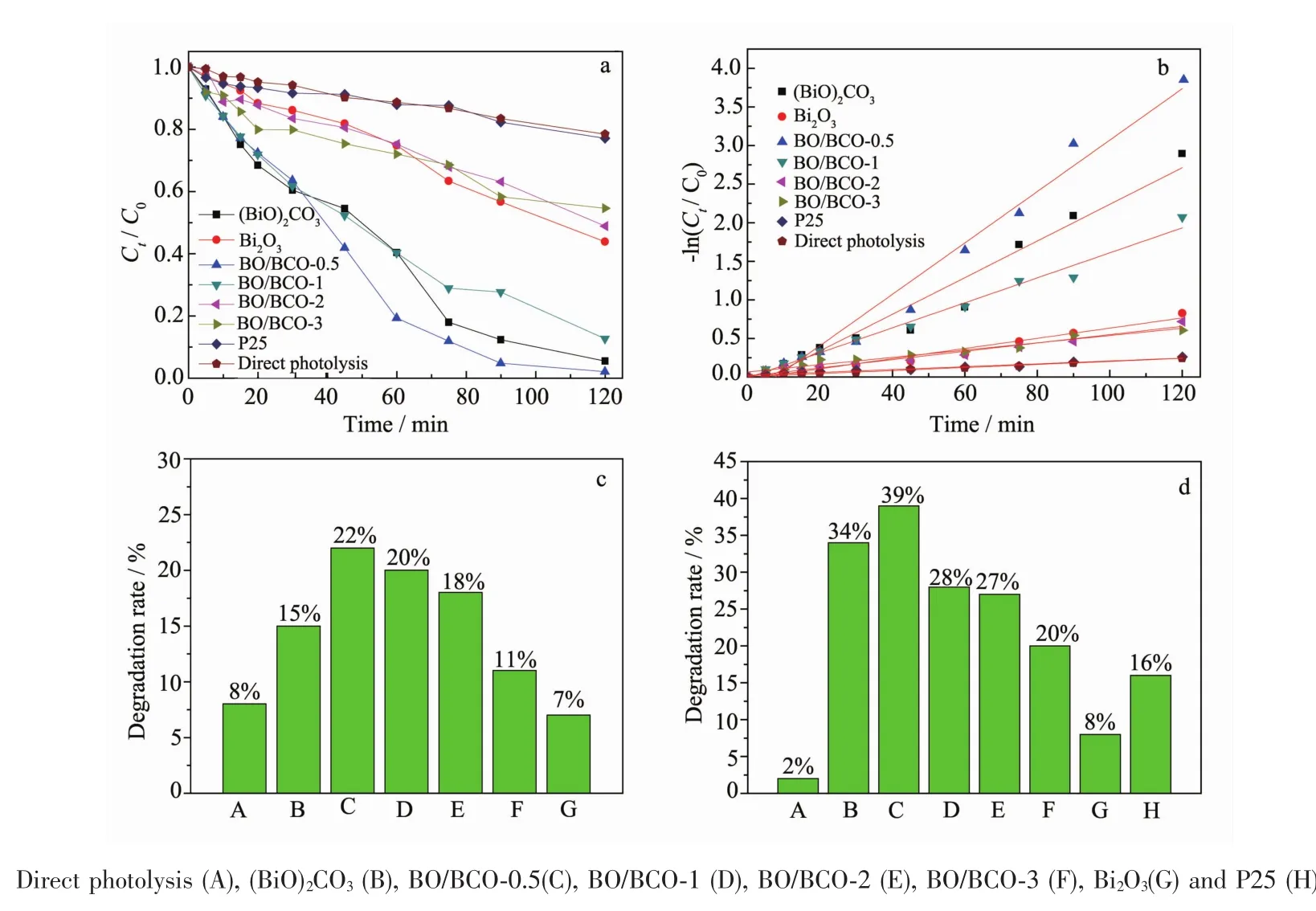
图9 不同复合材料在不同光源照射下的光催化活性实验结果Fig.9 Photocatalytic degradation of different catalystsunder UV light(a),visible light(c),simulated solar light(d)and kinetics results of photocatalytic degradation under UV light(b)
2.7 捕获实验以及可能的光催化机理
光催化过程中反应活性物质的检测是认识光催化反应机理的关键,本文通过检测反应活性物质推测了BO/BCO-0.5可能的光催化机理,结果如图11所示。实验分别利用乙二胺四乙酸二钠(EDTA,捕获h+)、异丙醇(IPA,捕获·OH)和对苯醌(BQ,捕获·O2-)作为捕获剂[32],紫外光下分别加入到RhB溶液中,并加入BO/BCO-0.5样品,研究捕获剂对复合材料紫外光下催化降解RhB活性的影响。由图11可知,光催化降解RhB实验时加入IPA、BQ后,光催化活性降低,光催化效果被抑制,证明其中的活性基团数量减少被捕获,因此推测·OH和·O2-在光催化降解体系中具有一定的作用。并且,加入h+捕获剂EDTA后,光催化活性几乎消失,说明光催化体系中的大部分h+被捕获剂捕获,导致半导体光催化材料的降解下降。因此,在BO/BCO-0.5紫外光下催化降解罗丹明B的光催化反应体系中,h+占主导地位,同时还存在一定的·OH以及·O2-。这些活性基团是光催化降解污染物的依据,从而推测出可能的光催化反应机理。
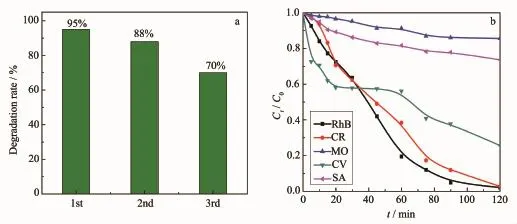
图10 BO/BCO-0.5复合材料的光催化循环与实用性实验结果Fig.10 Results of UV photocatalytic degradation for RhB after three cycleswith BO/BCO-0.5(a)and curves of different dyes with BO/BCO-0.5 by UV light irradiation
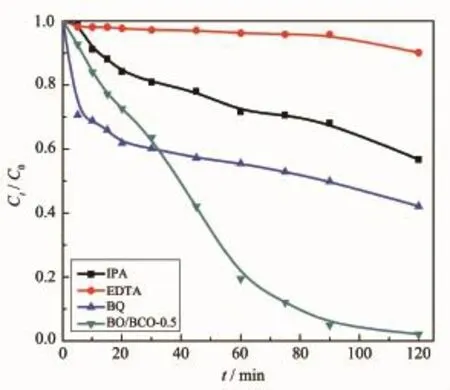
图11 BO/BCO-0.5复合材料紫外光下捕获实验结果图Fig.11 Capture experiment results of BO/BCO-0.5 under UV irradiation
图12 为BO/BCO-0.5纳米复合材料可能的光催化反应机理图。根据公式ECB=X-4.5-0.5Eg分别计算得出Bi2O3、(BiO)2CO3两种物质的导带和价带位置[33],如表2所示。复合材料中半导体Bi2O3(2.13 eV)和(BiO)2CO3(3.37 eV)带隙不同,(BiO)2CO3的带隙能大于Bi2O3,通过·OH-的引入形成的BO/BCO复合材料,可有效降低(BiO)2CO3半导体的带隙能,降低光激发条件。光催化过程时,2种半导体材料导带位置有一定差异,致使光生电子发生转移。另外,由于(BiO)2CO3的价带位置比Bi2O3的价带位置高,导致(BiO)2CO3的光生空穴可向Bi2O3的价带发生转移,光生空穴的转移在一定程度上增加了载流子的传递途径,从而降低了光生电子-空穴对的复合效率。少量Bi2O3与(BiO)2CO3的复合,引起光生空穴在Bi2O3价带聚集,提高了染料的降解效果。在反应中,吸附在催化剂表面的氧气分子接受电子形成超氧自由基,价带上产生的空穴与H2O接触形成·OH,还有价带上聚集的具有强氧化性质的h+都能与染料分子发生反应并将之分解成H2O与CO2,从而达到提高光催化活性的目的[34]。
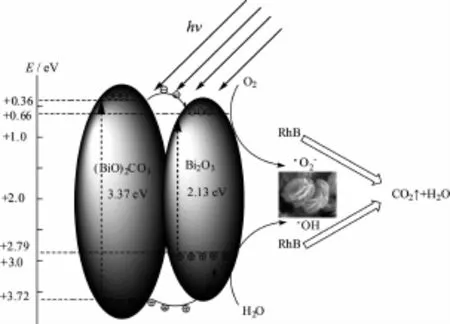
图12 BO/BCO复合材料可能的光催化反应机理图Fig.12 Possible photocatalytic reactionmechanism of BO/BCO composite

表2 Bi2O3和(BiO)2CO3的导带和价带Table 2 Calculated CB and VB of Bi2O3and(BiO)2CO3
3 结论
以柠檬酸铋作为铋源,以无水碳酸钠、NaOH作为原料,通过程序升温水热法制备了层级纳米花环状BO/BCO复合材料。同时,随着反应时间的增加,得到不同Bi2O3含量的复合物。根据活性实验得到,BO/BCO-0.5在多模式光催化的实验中具有最好的光催化活性。导致这种情况出现的原因是:合成的纳米复合产物中,适量的窄带隙Bi2O3降低了(BiO)2CO3的带隙能,从而降低光激发条件;Bi2O3的加入,造成吸收边红移,增加了可见光响应;增加的比表面积为染料分子提高更多的活性位点;层级纳米花状结构的形成有利于光的反射与散射,光的多重利用增加光的利用率;Bi2O3与(BiO)2CO3的导带与价带的电势位置的差异同样增加了光生电子-空穴对的转移途径,增加其分离时间,从而在一定程度上提高光催化活性。并且,该复合材料对5种不同的有机污染物都具有降解活性,展示出一定应用的广泛性。
参考文献:
[1]Li TY,Liu Y H,Chitara B,et al.J.Am.Chem.Soc.,2014, 136(8):2986-2989
[2]CHEN Xi(陈熙),LI Li(李莉),ZHANGWen-Zhi(张文治), etal.Chinese J.Inorg.Chem.(无机化学学报),2015,31(10): 1971-1980
[3]Jiang Y,Deng JG,Xie SH,et al.Ind.Eng.Chem.Res., 2015,54(3):900-910
[4]Kumar M,Deka S.ACSAppl.Mater.Interfaces,2014,6(18): 16071-16081
[5]Knauf R R,Kalanyan B,Parsons G N,et al.J.Phys.Chem. C,2015,119:28353-28360
[6]Li L,Huang X D,Zhang JQ,etal.J.Colloid Interface,2015, 443:13-22
[7]GAO Yu(高宇),LILi(李莉),YIChun-Xiong(易春雄),et al. Chinese J.Inorg.Chem.(无机化学学报),2016,32(3):405-413
[8]Merrill N A,Sethi M,Knecht M R.ACS Appl.Mater. Interfaces,2013,5(16):7906-7914
[9]ZHUO Na(禚娜),LILi(李莉),GAO Yu(高宇),etal.Chinese J.Inorg.Chem.(无机化学学报),2013,29(5):991-998
[10]Park S,Kim S,Sun G J,et al.ACSAppl.Mater.Interfaces, 2015,7:8138-8146
[11]Dong F,Wang Z Y,Li Y Y,et al.Environ.Sci.Technol., 2014,48:10345-10353
[12]LiW T,Zheng Y F,Yin H Y,et al.Nanopart.Res.,2015, 17:271
[13]Ali R,Selim A S S,Gwan H C,et al.ACS Sustainable Chem.Eng.,2015,10:2-27
[14]Jiang SQ,Wang L,HaoW C,etal.J.Phys.Chem.C,2015, 119:14094-14101
[15]Cao X F,Zhang L,Chen X T,et al.Cryst.Eng.Commun., 2011,13:1939-1945
[16]Dong F,Sun Y J,Fu M,etal.Langmuir,2012,28:766-773
[17]Huang H W,Li X W,Wang J J,et al.ACSCatal.,2015,5: 4094-4103
[18]Dong F,Li Q Y,Sun Y J,et al.ACSCatal.,2014,4:4341-4350
[19]Tang J L,Zhao H P,Li G F,et al.Ind.Eng.Chem.Res., 2013,52:12604-12612
[20]Ma JJ,Zhu S J,Shan Q Y,et al.Electrochim.Acta,2015, 168:97-103
[21]Cen W L,Xiong T,Tang C Y,et al.Ind.Eng.Chem.Res., 2014,53:15002-15011
[22]Chen Y F,Huang W X,He D L,et al.ACS Appl.Mater. Interfaces,2014,6:14405-14414
[23]Li M H,Maria E N T,Nereyda N M,et al.J.Environ.Sci. Technol.,2011,45:8989-8995
[24]Liu W J,Cai J Y,Li Z H.ACS Sustainable Chem.Eng., 2015,3:277-282
[25]Huang H W,Li X W,Wang J J,et al.ACSCatal.,2015,5: 4094-4103
[26]Cen W L,Xiong T,Tang C Y,et al.Ind.Eng.Chem.Res., 2014,53:15002-15011
[27]Sunita K,Simanta K,Amitava P,etal.J.Phys.Chem.C,2013, 117:5558-5567
[28]Prashant R K,Lee Y J,Geunjae K,et al.J.Phys.Chem.C, 2014,118(38):21975
[29]ZhaoW R,Zhang M,Ai ZY,etal.J.Phys.Chem.C,2014, 118:23117-23125
[30]Cheng H F,Huang B B,Yang K S,et al.ChemPhysChem, 2010,11(10):2167-2173
[31]Liu Y Y,Wang Z Y,Huang B B,et al.Appl.Surf.Sci., 2010,257(1):172-175
[32]Xu L,Ellen M P S,Sara E S.J.Phys.Chem.C,2012,116: 871-877
[33]Xu Y,Martin S.Am.Mineral.,2000,85:543-556
[34]Chen Xu,Rangaiah G P,Zhao X S.Ind.Eng.Chem.Res., 2014,8:1024-1036
Hierarchical Nanoflower-Ring Structure Bi2O3/(BiO)2CO3Com posite for Photocatalytic Degradation of Rhodam ine B
SONGQiang1,2LILi*,1,2,3LUO Hong-Xiang2LIU Yue2YANG Chang-Long1
(1College ofMaterials Science and Engineering,Qiqihar University,Qiqihar,Heilongjiang 161006,China)
(2College of Chemistry and Chemical Engineering,Qiqihar University,Qiqihar,Heilongjiang 161006,China)
(3College of Heilongjang Province Key Laboratory of Fine Chemicals,Qiqihar,Heilongjiang 161006,China)
Hierarchicalnanoflower-ring structure Bi2O3/(BiO)2CO3(BO/BCO)compositewas successfully synthesized by the temperature-programmed hydrothermal treatment.X-ray diffraction(XRD),UV-Vis diffuse reflectance spectroscopy(UV-Vis/DRS),X-ray photoelectron spectroscopy(XPS),Scanning electron microscopy(SEM), Transmission electron microscopy(TEM)and N2adsorption-desorption tests were employed to characterize the crystalline phase,chemical composition,optical absorption properties,morphology and surface physicochemical propertiesofas-synthetizedmaterial.The results showed that the crystalline phase of(BiO)2CO3was tetragonal phase, and the crystalline phase of Bi2O3was themonoclinic phase in as-composite Bi2O3/(BiO)2CO3which had both as-crystal structures.Moreover,with the introduction of OH-and reaction time increasing in synthesis process,the intensity of characteristics diffraction peak of(BiO)2CO3was gradually decreased,meanwhile,that of Bi2O3was gradually increased,showing that the proportionsof Bi2O3were increased in the samplewith reaction time increased. The results of UV-Vis/DRSanalysis showed that the absorption edge ofas-synthetized composite BO/BCO had shift compared to pure Bi2O3and pure(BiO)2CO3,and the absorption was effectively increased in the visible light region with the introduction of Bi2O3.At the same time,(BiO)2CO3nanolayerwas changed to the hierarchical nanoflowerring structure BO/BCO-0.5 composite,and the formation of specialmorphology leads to narrowed band gap and change the reflection and scattering ofphotoelectrons,whichwere conducive to the absorption efficiency of lightand transfering of photogenerated charges.In addition,the photocatalytic activities of as-composites BO/BCO were studied by degradation photocatalytic experimentsofRhB as themodelmolecule underdifferent light irradiation,the cycle experiment and the capture experiment.The results of photocatalytic activity experiment showed that the activity of BO/BCO-0.5 was significantly higher than that of other systems(Bi2O3and P25),and the photocatalytic activity of BO/BCO-0.5 was kepteven after three cycles.Meanwhile,according to the capture experimental results, the possible photocatalytic reactionmechanism of BO/BCO compositewasspeculated.
temperature-programmed hydrothermal treatment;bismuth oxide;bismuth subcarbonate;hierarchical nanoflower-ring structure;photocatalytic degradation;rhodamine B
O614.53+2
A
1001-4861(2017)07-1161-11
10.11862/CJIC.2017.139
2016-12-20。收修改稿日期:2017-03-16。
国家自然科学基金(21376126),黑龙江省自然科学基金(B201106、B201314),黑龙江省教育厅科学技术研究项目(12511592),黑龙江省政府博士后资助经费(LBH-Z11108),黑龙江省普通高校绿色化工技术重点实验室开放课题资助项目(2013年),黑龙江省政府博士后科研启动金(LBH-Q13172)和齐齐哈尔大学大学生创新创业训练计划项目(201610221112)。
*通信联系人。E-mail:qqhrll@163.com;Tel:0452-2738206;会员登记号:S06N2317M1508。

