盐酸西替利嗪巴布膏剂的药动学和生物利用度研究
韩 璐,原永芳
·药学研究·
盐酸西替利嗪巴布膏剂的药动学和生物利用度研究
韩 璐,原永芳
目的 研究盐酸西替利嗪巴布膏剂在大鼠体内的药代动力学特征,并与口服给药的药动学进行比较,考察生物利用度。方法 选用SD大鼠,分为巴布膏剂组和口服给药组,采用高效液相色谱法测定血药浓度;并剥取剩余的西替利嗪巴布膏剂,测定剩余药量。结果 西替利嗪巴布膏剂组的Tmax为2.35 h,Cmax为2.68 μg/mL,AUC为21.01 μg·h/mL,MRT为23.26 h;西替利嗪口服组的Tmax为1.11 h,Cmax为11.65 μg/mL,AUC为35.62 μg·h/mL,MRT为12.13 h。扣除巴布膏剂中的剩余药量,按照实际进入皮肤的剂量计算得西替利嗪巴布膏剂相当于片剂的生物利用度为30.81%;不扣除巴布膏剂中的剩余药量,西替利嗪巴布膏剂相当于片剂的生物利用度为14.75%。结论 西替利嗪巴布膏剂的血药浓度平稳而持久,具有缓释的特征。
西替利嗪;巴布膏剂;药动学;生物利用度
0 引言
盐酸西替利嗪(Cetirizine hydrocloride,CET)是一种高选择性的H1受体拮抗剂,用于治疗过敏性疾病。与其他抗组胺药相比,CET中枢神经系统的活性虽然较低,但仍有嗜睡、头晕等不良反应[1]。其具有一个独特的药理作用,即除在过敏反应早期阻断H1受体外,还对过敏反应后期起重要作用的嗜酸性粒细胞有强大的抑制作用。目前常用的CET多为口服制剂,研究表明,其在给药24 h后血药浓度已经很低,但仍具有较好的抗皮肤过敏的效果,并维持较长时间[2]。因此,笔者将其开发成西替利嗪巴布膏剂[3],以水溶性高分子材料为基质,载药量大,对皮肤无刺激,且透皮效果好;不仅能保持良好的治疗效果,还可以降低中枢抑制作用[4]。CET巴布膏剂的药动学研究选用SD大鼠,通过眼眦静脉丛采血方式,进行体内血药浓度的测定,并与CET口服给药组进行对比,考察生物利用度和药动学参数。
1 仪器和材料
SHIMADZU LC-10A高效液相色谱仪(日本岛津公司);低速离心机(上海医用分析仪器厂);TGL-16G型高速离心机(上海安亭科学仪器厂);涡旋混合器(上海琪特分析仪器有限公司)。
枸橼酸钠、枸橼酸、乙酸乙酯、磷酸、磷酸二氢钠、三乙胺、十二烷基硫酸钠、磷酸氢二钠、磷酸二氢钾、氯化钠,以上试剂均为分析纯,购于上海化学试剂公司。西替利嗪原料药(江苏联环药业股份有限公司);乙腈(英国MERCK),色谱纯;CET巴布膏剂(自制);脱毛膏(日本Kanebo)。
SD大鼠(西普尔-必凯动物有限公司,动物生产许可证号:SCXK沪2008-0016,使用许可证号:SYXK沪2008-0050)。
2 方法和结果
2.1 大鼠血样中CET含量测定方法的建立
2.1.1 血浆样品的预处理 精密量取大鼠血浆0.5 mL于10 mL具塞离心管中,加入pH 5.5的枸橼酸缓冲液0.5 mL,涡旋振荡0.5 min后,精密加入乙酸乙酯5 mL,涡旋振荡3 min后,3 000 r/min离心10 min,精密吸取上层乙酸乙酯4 mL于另一具塞离心管中,再加入乙酸乙酯5 mL提取1次,合并乙酸乙酯液,在乙酸乙酯液中加入1.7%磷酸溶液100 μL反提后,涡旋3 min,3 000 r/min离心5 min,弃去乙酸乙酯层,取磷酸溶液20 μL进样。
2.1.2 色谱条件 色谱柱:Hypersil ODS C18柱(200 mm×4.6 mm,5 μm);流动相:乙腈-0.02 mol/L NaH2PO4-三乙胺(50∶50∶0.15),pH=3.1±0.1,内含SDS 0.007 mol/L;流速:1.0 mL/min;检测波长:231 nm;柱温:室温;灵敏度:0.01 AUFS;进样量:20 μL。
2.1.3 标准曲线 精密称取CET原料药0.100 9 g于100 mL容量瓶中,加蒸馏水至刻度定容,得到1.009 mg/mL的CET储备液。
精密量取上述储备液0.02、0.1、0.2、1、2、4 mL,分别于100 mL容量瓶中,加蒸馏水至刻度定容,得到浓度为0.201 8、1.009、2.018、10.09、20.18、40.36 μg/mL的CET标准溶液。
分别于0.5 mL大鼠空白血浆中加入上述CET标准溶液0.5 mL,得到终浓度为0.100 9、0.504 5、1.009、5.045、10.09、20.18 μg/mL的标准血浆样品系列。并按照血浆样品预处理步骤和HPLC测定方法进行操作,典型图谱见图1。以测得的血浆中CET的浓度C为纵坐标、相应的峰面积A为横坐标,得标准曲线C=6×10-5A+0.023 6(r2=0.999 8)。当信噪比(S/N)=3时,最低检测限为0.5 ng。

图1 CET大鼠血浆样品色谱图
2.1.4 方法回收率 按照“2.1.3”项下的操作方法配成低、中、高浓度的CET标准血浆样品,并按照血浆样品预处理步骤和HPLC测定方法进行操作,所得的测定结果代入标准曲线方程得出理论浓度,与实际浓度比较,计算方法回收率,见表1。
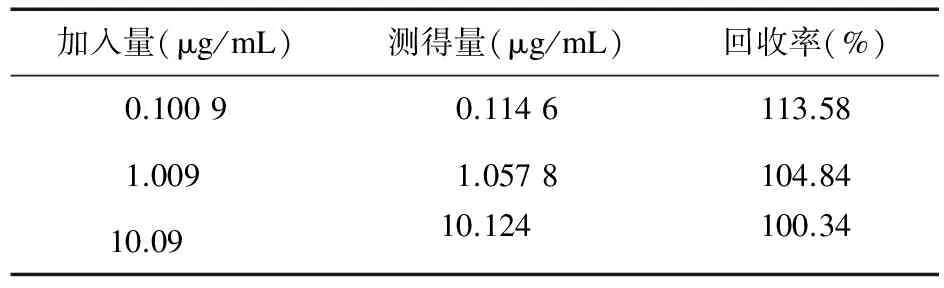
表1 血浆样品中CET测定的方法回收率(n=5)
2.1.5 绝对回收率 从上述1.009 mg/mL的CET储备液中精密量取0.01、0.1、1 mL分别于100 mL容量瓶中,加蒸馏水至刻度定容,得到浓度为0.100 9、1.009、10.09 μg/mL的CET标准溶液,直接通过HPLC进行测定,得出相应的峰面积。并与“2.1.3”项下的上述3个浓度的峰面积进行比较,即得CET在血样提取中的绝对回收率,见表2。
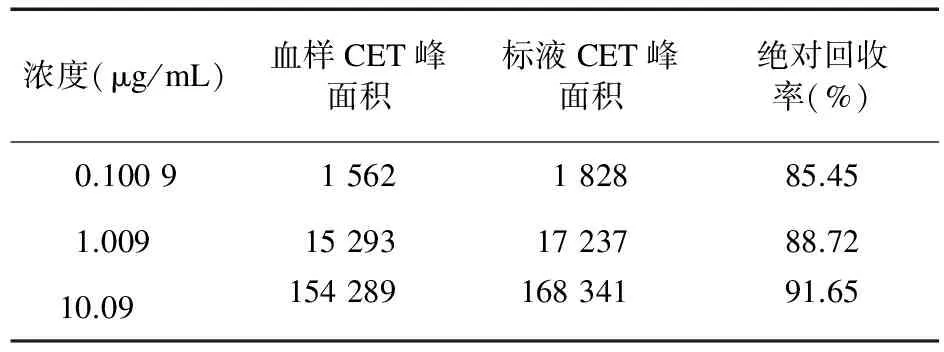
表2 CET在血样提取中的绝对回收率(n=5)
2.1.6 精密度实验 按照“2.1.3”项下的操作方法配成低、中、高浓度的CET标准血浆样品,分别于日内4、6、8 h和日间1、2、3 d测定其浓度,根据标准曲线计算理论浓度和变异系数,得出平均日内RSD为4.59%,平均日间RSD为5.88%,见表3。

表3 血浆样品中CET测定的方法精密度(n=5)
2.2 实验设计和样本采集
2.2.1 实验设计 CET巴布膏剂组:SD大鼠60只,雌雄各半,体重(200±20) g,随机分为12组,每组5只。实验前禁食饲养1 d,腹部用脱毛膏脱毛,温水洗净,饲养过夜。在腹部贴自制的CET巴布膏剂1贴,4 cm×4 cm,剂量为40 mg/kg,用纱布及胶布缠绕固定。于给药后0.5、1、2、3、4、5、6、8、10、12、24、48 h眼眦静脉丛取血于预先肝素化的离心管中,6 000 r/min离心10 min后,取上层血清置于-20 ℃冰箱中储存备测。每个取血点采用1组,即5只大鼠,取血后直接处死,并剥取剩余巴布膏剂,测定其中CET含量。
CET口服组:SD大鼠60只,雌雄各半,体重(200±20) g,随机分为12组,每组5只。口服灌胃给予CET水溶液,剂量为10 mg/kg,于给药后15 min、30 min、45 min、1 h、2 h、3 h、4 h、6 h、8 h、12 h、24 h、48 h眼眦静脉丛取血于预先肝素化的离心管中,并采用6 000 r/min离心10 min后,取上层血清置于-20 ℃冰箱中储存备测。每个取血点采用1组,即5只大鼠,取血后直接处死。
2.2.2 血药浓度的测定 按照血浆样品预处理步骤和HPLC测定方法进行操作,并根据血药浓度测定的标准曲线计算血浆样品中CET的含量。
2.2.3 CET巴布膏剂中剩余药量的测定 将剥取的剩余CET巴布膏剂(4 cm×4 cm)剪碎,置于100 mL容量瓶中,加蒸馏水至刻度定容,超声30 min,浸泡过夜,并进行适当稀释,3 000 r/min离心后进HPLC。按照含量测定标准曲线计算CET的含量。
2.3 实验结果
2.3.1 药时曲线 大鼠的血药浓度为纵坐标、相应的取样时间为横坐标,绘制药时曲线,见图2。

图2 CET巴布膏剂组与口服组的药时曲线(n=5)
2.3.2 药动学参数 巴布膏剂组药动学数据采用非参数法计算,口服组药动学数据用3P97软件处理,药动学参数见表4。
CET口服给药后平均1.11 h达到峰值,Cmax为11.65 μg/mL,MRT为12.13 h,体内药动学行为符合一级吸收二室模型。CET巴布膏剂组的Tmax为2.35 h,Cmax为2.68 μg/mL,较口服组明显减少,在达到药效的同时,可减轻中枢抑制作用,MRT为23.26 h,比口服组显著延长,血药浓度在24 h仍可以测到,说明该贴剂具有缓释的特点。
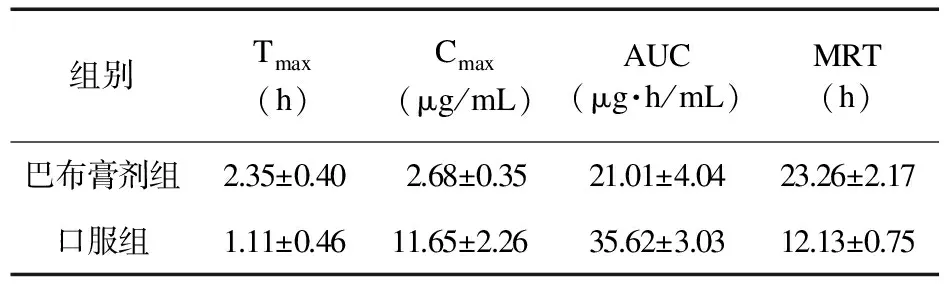
表4 CET药动学参数(n=5)
2.3.3 巴布膏剂中剩余药量 将巴布膏剂中的剩余药量对时间作图,见图3。
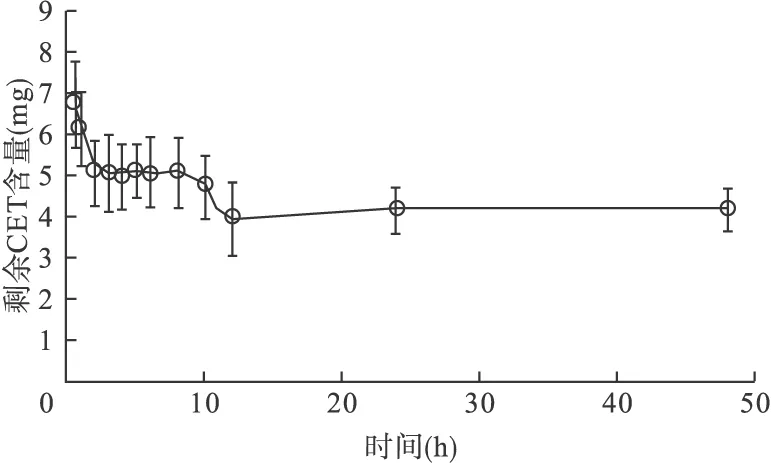
图3 CET巴布膏剂中剩余药量与给药时间的关系(n=5)
从图中可以看出,2 h前巴布膏剂的剩余药量呈递减趋势,2 h后逐步趋于稳定。
2.3.4 巴布膏剂的相对生物利用度 扣除巴布膏剂中的剩余药量,按照实际进入皮肤的剂量计算得CET巴布膏剂相当于片剂的生物利用度为30.81%;不扣除巴布膏剂中的剩余药量,CET巴布膏剂相当于片剂的生物利用度为14.75%。
3 讨论
3.1 血浆样品的处理及流动相中的添加剂 血浆样品的预处理用乙醚提取虽然较为干净,但是提取率较低,用乙酸乙酯提取率较高但是蛋白等杂质较多,因此采用稀磷酸溶液反提,在保证提取回收率的前提下,使体内样品提取色谱干扰减少,并在强洗脱流动相条件下使血浆样品中的西替利嗪组分快速出峰[5]。
对于碱性药物的高效液相色谱测定,离子对反相高效液相色谱是常用的方法[6]。在西替利嗪血药浓度测定方法中,文献采用短链昂贵的离子对试剂辛烷磺酸钠,基于对分析成本的考虑和血浆样品的复杂性,本实验选择国产SDS作为离子对试剂,较好地实现了血浆样品中西替利嗪的分离分析,而且SDS具有的蛋白增溶作用,使反相色谱柱的寿命大大提高[7]。
西替利嗪的叔胺结构存在与固定相表面游离硅醇基之间的离子交换或氢键作用,使西替利嗪的色谱峰拖尾,保留时间延长甚至于柱内滞留。在流动相中加入一定比例的有机胺扫尾剂,可以竞争、抑制或掩蔽固定相表面的游离硅醇基活性,使碱性药物易于出峰,改善峰形[8]。经优化考察,三乙胺是较理想的扫尾剂,且以0.007mol/L浓度为宜。
3.2 药动学试验采血及给药剂量的确定 本试验采用SD大鼠作为实验动物,考虑到大鼠的血量有限,不能反复采集;因此每只大鼠只采血1次,每个时间点采用一组大鼠,取血后直接处死。
药动学实验中巴布膏剂组的给药剂量是根据药效实验的结果得出的[4]。药效试验中,巴布膏剂高剂量组的抑制率最明显,因此,选择高剂量作为药动试验的巴布膏剂组给药剂量。口服组的给药剂量根据药理学实验方法中人与大鼠的剂量换算得出。
3.3 巴布膏剂的剩余药量及生物利用度 每个时间点的大鼠处死后,剥离巴布膏剂测定剩余含药量,结果表明,2h后巴布膏剂的剩余药量比较稳定。药动学参数也显示,巴布膏剂的Tmax约为2h,因此,我们认为体内血药浓度达峰后,巴布膏剂以稳定的透皮速率进入体内,因为其中的含药量远远大于血中的药量,可以保证用药时间内的浓度梯度,以维持一定的释药速度。
由于经皮给药制剂是一类吸收不完全的产品,即在规定的用药时间内仅有部分药量被吸收,因此在计算生物利用度时,将巴布膏剂中的剩余药量扣除来计算,与口服相比的生物利用度为30.81%,平均药物吸收百分比为47.88%;如果不扣除其中的剩余药量,与口服相比的生物利用度为14.75%。
CET巴布膏剂使药物的吸收和消除都较口服缓慢而持久,血药浓度平稳,但生物利用度较低,这主要是由药物在巴布膏剂中的被动扩散渗透机制所决定的。敷贴于皮肤表面时,药物从基质中释放出来的速率越慢,透过皮肤进入血循环的药物量就越少,需要增加巴布膏剂中药物的剂量来进行补偿以保证有效的血药浓度,透皮给药的生物利用度低于口服给药。因此,深入研究贴剂中药物基质控释系统的处方组成,减少贴剂中药物剂量,使药物起效迅速,有望提高药物的相对生物利用度。
[1]KappA,WediB.Chronicurticaria:clinicalaspectsandfocusonanewantihistamine,levocetirizine[J].JDrugsDermatol,2004,3(6):632-639.
[2]DayJH,EllisAK,RafeiroE.Levocetirizine:anewselectiveH1receptorantagonistforuseinallergicdisorders[J].DrugsToday(Barc),2004,40(5):415-421.
[3] 韩璐,华拯敏,俞晓艳,等.西替利嗪巴布膏剂的制备及体外评价[J].中国药物与临床,2012,12(9):1151-1153.
[4] 韩璐,原永芳.西替利嗪巴布膏剂被动皮肤过敏反应的实验研究[J].中南药学,2015,10(13):1045-1047.
[6] García-Alvarez-Coque MC,Ruiz-Angel MJ,Berthod A,et al.On the use of ionic liquids as mobile phase additives in high-performance liquid chromatography.A review[J].Anal Chim Acta,2015,883:1-21.
[7] Freiser HH,Newlan MP,Gooding DL,et al.Reversed phase high performance liquid chromatography of basic drugs on a silanol deactivated supported[J].J Lip Chromatogr,1998,12(5):827.
[8] Kiel JS,Morgan SL.Computer-assisted optimization of a high performance liquid chromatographic separation for chlorpromazine and thirteen metabolites[J].J Chromatogr,1998,485(1):827.
Research on the pharmacokinetics and bioavailability of cetirizine cataplasm
HAN Lu,YUAN Yong-fang
(Department of Pharmacy,No.9 People′s Hospital Affiliated to Shanghai Jiaotong University of Medicine,Shanghai 201999,China)
Objective To study the pharmacokinetics and bioavailability of cetirizine (CET) cataplasm.Methods SD rats were divided into CET cataplasm group and CET oral group.The content of CET in the rat plasma and the content in the CET cataplasm were detected using HPLC.Results Pharmacokinetic parameters of CET cataplasm group were as follows:Tmax2.35 h,Cmax2.68 μg/mL,AUC 21.01 μg·h/mL,MRT 23.26 h;while the pharmacokinetic parameters of CET oral group were as follows:Tmax1.11 h,Cmax11.65 μg/mL,AUC 35.62 μg·h/mL,MRT 12.13 h.The relative bioavailability was 30.81%.Conclusion Blood drug concentration of CET cataplasm was stable and lasting,and CET cataplasm has the characteristics of slow release.
Cetirizine;Cataplasm;Pharmacokinetics;Bioavailability
2016-09-14
上海交通大学医学院附属第九人民医院药剂科,上海 201999
上海高校选拔培养优秀青年教师科研专项基金(jdy-09070)
10.14053/j.cnki.ppcr.201706022

