唑来膦酸联合吉西他滨治疗非小细胞肺癌疗效观察
陈晓华,龚惠莉,邱晓平(.上海市浦东新区肺科医院药房,上海0000;.上海市浦东新区肺科医院呼吸科,上海0000;.上海市浦东新区人民医院肿瘤科,上海0000)
唑来膦酸联合吉西他滨治疗非小细胞肺癌疗效观察
陈晓华1,龚惠莉2,邱晓平3(1.上海市浦东新区肺科医院药房,上海200030;2.上海市浦东新区肺科医院呼吸科,上海200030;3.上海市浦东新区人民医院肿瘤科,上海200030)
目的观察唑来膦酸联合吉西他滨治疗非小细胞肺癌(NSCLC)的临床效果。方法选择上海市浦东新区肺科医院2015年1月至2016年3月收治的92例预计生存期大于3个月的NSCLC患者,采用随机数表法分为两组,每组46例,对照组患者接受标准一线化疗GP方案,观察组患者在此基础上给予唑来膦酸治疗,3周为一个周期,共治疗3个周期。治疗前、治疗3个周期后评价患者疼痛缓解情况、健康状况、骨转移灶疗效及不良反应。结果治疗后观察组和对照组患者的NRS评分分别为(3.32±0.84)分和(4.92±1.13)分,均明显低于各组治疗前的(6.03±1.26)分和(6.12±1.54)分,且观察组低于对照组,差异均有统计学意义(P˂0.05);治疗后观察组和对照组患者的Karnofsky评分分别为(71.29±12.47)分和(65.82±11.29)分,均明显高于各组治疗前的(54.07±9.46)分和(53.22±10.84)分,且观察组高于对照组,差异均有统计学意义(P˂0.05);观察组患者的治疗总有效率为60.87%,明显高于对照组的26.09%,差异有统计学意义(P˂0.05);两组患者的不良反应比较差异无统计学意义(P>0.05)。结论唑来膦酸与吉西他滨联合应用可能产生协同作用,治疗NSCLC疗效显著,安全性好。
唑来膦酸;吉西他滨;非小细胞肺癌;协同作用
肺癌是全球发病率最高的恶性肿瘤之一,特别是我国近年来肺癌的发病率迅速增加,成为城市人口恶性肿瘤死亡原因之首[1]。非小细胞肺癌(NSCLC)是最常见的类型,占80%~85%[2],晚期NSCLC患者中大多数会出现顽固性疼痛、病理性骨折等,而骨性疼痛的根本原因是原发癌骨转移,严重影响患者的预后和生活质量[3]。目前非小细胞肺癌治疗的方法主要是以铂类为基础进行联合化疗[4],虽然目前尚不能治愈,但减轻症状,减少并发症,提高患者生存质量是治疗的主要方向。唑来膦酸是目前作用最强的第三代双膦酸盐类药物,对缓解骨性疼痛,改善癌症骨转移引起的并发症方面作用良好[5],本文旨在探讨唑来膦酸联合吉西他滨治疗NSCLC的协同作用,并观察其治疗效果,现报道如下:
1 资料与方法
1.1 一般资料选取上海市浦东新区肺科医院2015年1月至2016年3月92例预计生存期大于3个月且符合以下纳入和排除标准的NSCLC患者,采用随机数表法分为对照组和观察组各46例,对照组中男性31例,女性15例;年龄40~72岁,平均(58.9±10.5)岁。观察组中男性32例,女性14例;年龄41~75岁,平均(59.5±11.4)岁。两组患者的年龄、性别等比较差异均无统计学意义(P>0.05),具有可比性。本研究经院医学伦理委员会批准。
1.2 纳入标准①确诊为NSCLC,且经骨扫描、X线、CT等检查证实伴骨转移患者;②Karnofsky功能状态评分≥50分,并伴有相应部位骨痛,部分患者伴有肢体或躯体活动障碍;③预计生存期≥3个月;④肝、肾功能、血常规、心电图无明显异常者。
1.3 治疗方法对照组患者给予标准一线化疗GP方案,即1 000 mg/m2吉西他滨(浙江豪森制药)加入0.9%生理盐水中静滴30~60 min,第1天、第8天,25 mg/m2顺铂第1天~第3天静滴(配合水化),每3周为一个周期,共治疗3个周期;观察组患者先给予4 mg唑来膦酸+100 mL生理盐水静脉滴注15 min,1周后给予GP方案治疗3个周期,治疗方法同对照组。
1.4 观察指标与评价方法治疗前、3个周期后采用Karnofsky功能状态评分评价患者健康状态[6],采用国际通用的数字疼痛强度量表(NRS)评价患者疼痛情况[7]。0分:无痛;1~3分:轻度疼痛;4~6分:中度疼痛;≥7分:重度疼痛。同时记录治疗期间不良反应,评价骨转移灶疗效。
1.5 疗效评价标准根据WHO骨转移灶疗效评价标准,完全缓解(CR):原有转移灶消失或完全钙化持续4周以上;部分缓解(PR):成骨性病灶密度降低,溶骨性病灶部分钙化或缩小,持续4周以上;稳定(NC):病灶无明显变化;进展(PD):骨转移灶体积增大或出现新病灶[8]。有效率=CR+PR。
1.6 统计学方法应用SPSS13.0统计软件进行数据分析,计量资料以均数±标准差(x-±s)表示,组间比较采用t检验,计数资料比较采用χ2检验,均以P˂0.05为差异有统计学意义。
2 结果
2.1 两组患者治疗前后的疼痛和健康状态比较两组患者治疗前的NRS评分、Karnofsky评分比较差异均无统计学意义(P>0.05)。两组患者治疗后的NRS评分均低于治疗前,Karnofsky评分高于治疗前,且观察组的NRS评分较对照组更低,Karnofsky评分较对照组更高,差异均具有统计学意义(P˂0.05),见表1。
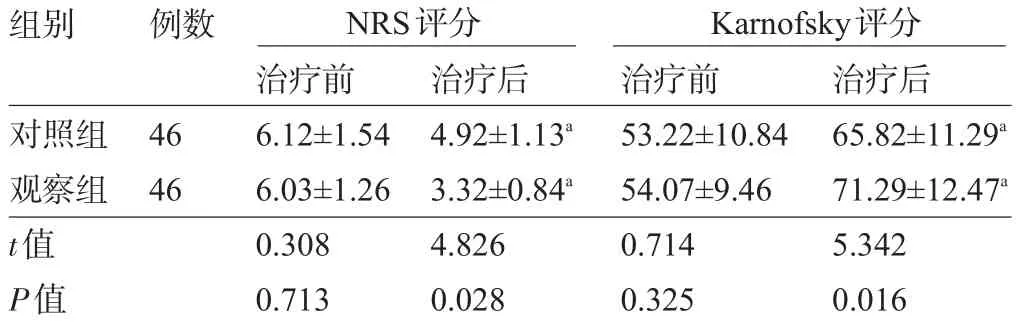
表1 两组患者治疗前后的NRS和Karnofsky评分比较(x-±s)
2.2 两组患者的骨转移灶疗效比较观察组患者的治疗总有效率为60.87%,明显高于对照组的26.09%,差异具有统计学意义(χ2=10.874,P˂0.05),见表2。

表2 两组患者的骨转移灶疗效比较(例)
2.3 两组患者的不良反应比较对照组发生Ⅲ度以上脱发、胃肠道反应、粒细胞减少、皮疹等不良反应9例,发生率为19.57%;观察组发生Ⅲ度以上脱发、胃肠道反应、粒细胞减少、皮疹等不良反应10例,发生率为21.74%,另有1例出现低热、肌肉酸痛,1例一过性骨痛加重,经对症治疗后症状缓解,两组不良反应发生率比较差异无统计学意义(χ2=0.728,P=0.302)。
3 讨论
吉西他滨是广谱抗肿瘤活性药物,作为新一代胞嘧啶核苷衍生物已在各器官肿瘤的治疗中广泛应用,单药和与铂类联合治疗NSCLC对肺癌的原发灶和转移灶均有效,能延长患者生存期,提高生存质量。但骨骼是癌症最常见的转移部位之一。肺癌患者中约有50%扩散至骨骼,晚期肺癌患者骨转移的发生率更高。NSCLC患者骨转移灶约75%以上呈溶骨性,仅少数骨转移灶为成骨性。唑来膦酸是目前作用最强的第三代双膦酸盐类药物,含氮杂环双膦酸盐,药理作用是通过结合骨内羟基磷灰石,吸附于骨小梁表面并形成保护膜,发生抑制骨钙释放,抗骨吸收作用。唑来膦酸与骨有高度的亲和力,使用后可优先被转运到骨吸收或形成加速部位,沉积于骨表面可抑制破骨细胞的活性,诱导破骨细胞凋亡,对多种癌细胞引起的骨转移有效。同时唑来膦酸抑制破骨细胞前列腺素和释放和合成,缓解骨性疼痛;而且研究还发现,唑来膦酸还具有直接的抗肿瘤作用,可抑制肺腺癌细胞A549生长和诱导凋亡[9-10]。
本研究结果显示,治疗后观察组和对照组患者的NRS评分均明显低于各组治疗前评分,且观察组低于对照组,差异均有统计学意义(P˂0.05);治疗后观察组和对照组患者的Karnofsky评分均明显高于各组治疗前评分,且观察组高于对照组,差异均有统计学意义(P˂0.05)。说明吉西他滨与铂类联合,吉西他滨与唑来膦酸联合均可缓解疼痛,提高健康状态。但观察组治疗后NRS评分降低幅度明显大于对照组,Karnofsky评分升高幅度明显高于对照组,差异有统计学意义。说明在吉西他滨与唑来膦酸联合在缓解疼痛,提高患者健康状态方面作用更加明显。两组骨转移灶疗效评价显示,观察组患者的治疗总有效率为60.87%,明显高于对照组的26.09%,差异有统计学意义(P˂0.05),与相关研究结果相符,说明吉西他滨与唑来膦酸联合应用可能具有协同作用,从而大大提高了NSCLC患者骨转移灶疗效。
吉西他滨可影响癌细胞S周期向G2/M期的转变,从而将肺癌细胞阻滞在S期,减少G2/M期癌细胞数目,达到抑制肿瘤生长的目的。唑来膦酸可将肺癌细胞阻滞于G0/G1期,减少S期、G2/M期癌细胞数目,阻碍细胞有丝分裂的进行。两种药物的作用机制均是通过干扰肺癌细胞DNA的合成来达到减少癌细胞数目,抑制肿瘤的生长和转移。两种药物联合时,唑来膦酸将肺癌细胞阻滞于G0/G1期,阻碍细胞有丝分裂的进行,使癌细胞对吉西他滨的敏感性增加,因此可明显增强其抑制作用,从而使骨转移灶疗效有大幅度提高。
综上所述,唑来膦酸与吉西他滨联合治疗NSCLC在缓解疼痛、提高患者健康状态和骨转移灶疗效方面作用明显,说明两者可能有协同作用,而且唑来膦酸临床使用毒副作用小,可推荐临床推广应用。
[1]周洋,荆薇,马洁韬,等.唑来膦酸与吉西他滨体外协同抑癌作用的实验研究[J].山西医药杂志,2015,44(20):2365-2368.
[2]梁研,郭进华.唑来膦酸联合化疗治疗非小细胞肺癌骨转移效果观察[J].肿瘤研究与临床,2016,28(5):345-347.
[3]赵铎,高宝安.中晚期非小细胞肺癌联合治疗研究进展[J].海南医学,2016,27(3):438-441.
[4]张靖宇,蒋华,刘明环,等.血液中KRAS基因状态与非小细胞肺癌骨转移患者治疗疗效的相关性[J].中国急救医学,2015,35(z2):287-289.
[5]李建,王阁,肖何,等.放疗联合唑来膦酸治疗NSCLC骨转移的疗效分析及影响因素[J].重庆医学,2015,44(12):1629-1632.
[6]虞晓林,申泓.唑来膦酸联合化疗治疗非小细胞肺癌骨转移的疗效观察[J].实用临床医药杂志,2016,20(11):156-158.
[7]张建群.吉西他滨联合康艾注射液在30例非小细胞肺癌化疗中的应用观察[J].山东医药,2013,53(31):87-88.
[8]谢忠海,沈琦斌,李鸿伟,等.多西紫杉醇联合吉西他滨和顺铂治疗非小细胞肺癌的临床研究[J].中国临床药理学杂志,2016,32(11):972-974.
[9]曲莉莉,刘晓晴,王伟霞,等.胞浆-5'-核苷酸酶-Ⅱ在非小细胞肺癌组织中的表达及其临床意义[J].中国肿瘤临床,2015,42(1):56-60.
[10]全吉钟,冯燕,王冬旭,等.吉西他滨联合洛铂或顺铂一线治疗老年晚期非小细胞肺癌患者的疗效[J].中国老年学杂志,2014,34(5):1181-1182.
Collaborative action research of azole phosphonic acid and gemcitabine for the treatment of non-small cell lung cancer.
CHEN Xiao-hua1,GONG Hui-li2,QIU Xiao-ping3.
1.Pharmacy,the Pulmonary Hospital of Pudong New Area, Shanghai 200030,CHINA;2.Department of Respiratory,the Pulmonary Hospital of Pudong New Area,Shanghai 200030, CHINA;3.Department of Oncology,the People's Hospital of Pudong New Area Shanghai,Shanghai 200030,CHINA
ObjectiveTo observe the curative effect of azole phosphonic acid combined with gemcitabine in the treatment of non-small cell lung cancer(NSCLC).MethodsA total of 92 cases of NSCLC patients with an expected survival of more than 3 months,who admitted to the Pulmonary Hospital of Pudong New Area from January 2015 to March 2016,were selected and divided into the two groups by using random number table,with 46 cases in each group. The control group patients
standard first-line chemotherapy GP,and the observation group was treated with azole phosphonic acid on the basis of the control group's treatment.Three weeks for one treatment course,all the patients were treated for three courses.The pain relief,health,bone metastases curative effect and adverse reactions of the pa-tients before and after the three courses were evaluated.ResultsAfter the treatment,the numeric rating scale(NRS) scores of the observation group and the control group were respectively(3.32±0.84)and(4.92±1.13),which were significantly lower than(6.03±1.26)and(6.12±1.54)before the treatment;After the treatment,the NRS score of the observation group was significantly lower than the control group(P˂0.05).After the treatment,the Karnofsky scores of the observation group and the control group were respectively(71.29±12.47)and(65.82±11.29),which were significantly higher than(54.07±9.46)and(53.22±10.84)of before the treatment,and the observation group is significantly higher than the control group(P˂0.05).The total effective rate of treatment in the observation group was 60.87%,which was significantly higher than 26.09%in the control group(P˂0.05).There was no significant difference between the two groups in adverse reactions(P>0.05).ConclusionThe combined application of azole phosphonic acid and gemcitabine may have significant synergistic effect on the treatment of NSCLC with obvious therapeutic effect and good safety.
Azole phosphonic acid;Gemcitabine;Non-small cell lung cancer(NSCLC);Synergistic effect
R734.2
A
1003—6350(2017)11—1744—03
2016-11-09)
10.3969/j.issn.1003-6350.2017.11.008
陈晓华。E-mail:fkyyyjk@163.com

