T-FMSAC制备及其催化臭氧氧化去除p-CBA效能研究
卢思颖,孙中恩,封 莉,张立秋(北京林业大学环境科学与工程学院,北京 100083)
T-FMSAC制备及其催化臭氧氧化去除p-CBA效能研究
卢思颖,孙中恩,封 莉,张立秋*(北京林业大学环境科学与工程学院,北京 100083)
以污泥基活性炭为基质,采用化学共沉淀法制备了不同过渡金属(Mn、Co和Cu)掺杂的铁磁污泥基活性炭(T-FMSAC, T=Mn、Co、Cu),重点考察了过渡金属种类及其掺杂比例对T-FMSAC催化臭氧氧化去除水中对氯苯甲酸(p-CBA)效能的影响,并对臭氧与T-FMSAC催化剂的最佳投量进行了研究确定.结果表明,在臭氧投加量为1mg/L,催化剂投加量为40mg/L条件下,反应进行40min后,Mn-FMSAC的催化活性最高,其催化臭氧氧化对 p-CBA的去除率为 76%,高于 Co-FMSAC(72%)及 Cu-FMSAC(65%).并且,随着金属掺杂比例的增加(100:1,50:1,25:1,10:1(污泥量:金属掺杂量,W:W)),T-FMSAC催化臭氧氧化对p-CBA的去除率逐渐降低.在100:1掺杂比例下,催化剂不仅能够简单地通过磁铁分离,且具备最佳催化活性.100:1Mn-FMSAC催化臭氧氧化工艺对p-CBA的去除率随臭氧浓度的增加而增加;当臭氧投加量为1mg/L时,100:1Mn-FMSAC催化剂的最佳投量为40mg/L.叔丁醇的加入显著抑制了100:1Mn-FMSAC 催化臭氧氧化降解p-CBA的效能,表明该反应过程遵循羟基自由基反应机制.
铁磁污泥基活性炭;过渡金属;臭氧催化氧化;对氯苯甲酸
城市污水处理厂剩余污泥含碳量高且富含Fe、Mn、Cu、Zn等金属,通过一定程度的活化热解处理,可将其转化为污泥基活性炭(SAC).研究表明,SAC不仅具有较好的吸附去除重金属性能,还可高效催化臭氧氧化去除水中具有较高稳定性的有机污染物[1-4].因此,利用城市污泥来制备 SAC已成为污泥资源化利用的有效途径[5-7].但目前制备的SAC多为粉末状,在实际应用过程中存在回收困难、易造成粉尘污染等缺点,使其在环境领域的应用受到一定程度的限制.
磁分离作为一种简单高效的分离方法,可分离磁性或可磁化的吸附剂、各类载体等.因此,近年来已有学者致力于研究具有高效催化效果、成本低廉的负载型磁性催化剂[8-10].化学共沉淀铁氧体法是负载型磁性催化剂制备的一种常用方法,具有磁性可调节、毒性低、能耗低等优点而采用铁氧体负载的磁性催化剂在非均相催化臭氧氧化中表现出了良好的活性[13-15].因此,对SAC进行磁性负载不仅能够解决其分离回收问题,还有可能提高其催化臭氧氧化除污染效能.对氯苯甲酸(p-CBA)是农药、药物和染料的重要中间体,且难于生物降解、易在生物体内积累,易对环境和人类的健康产生危害.另一方面,p-CBA与⋅OH自由基反应速率快(k·OH=5.2×109L/(mol·s),而与臭氧分子的反应速率很低[ko3<0.15L/ (mol·s)],非常适合用来考察催化剂的催化活性.因而,在本研究中采用p-CBA作为目标污染物.
本研究将以SAC为载体,3种具备催化臭氧氧化效果的过渡金属(Mn、Co、Cu)[16-18]为掺杂剂,采用化学共沉淀法分别制备不同种类过渡金属掺杂的铁磁污泥基活性炭(T-FMSAC,T=Mn、Co、Cu),考察过渡金属种类及其掺杂比例对本研究所选目标物—p-CBA降解效能的影响,以期在实现T-FMSAC高效磁分离的前提下,还可提高其催化臭氧氧化去除有机物的效能.
1 材料与方法
1.1 材料
实验中所需溶液均由超纯水配置,由 ELGA LabWater 公司生产的超纯水设备制得.p-CBA购自美国Sigma公司,纯度高于99%;其他所用试剂均为分析纯.剩余污泥取自北京高碑店污水处理厂未经消化的脱水污泥.
1.2 T-FMSAC催化剂的制备
T-FMSAC采用化学共沉淀法制备,SAC制备采用文献报道方法[1].本实验将制备3种过渡金属(Mn、Co、Cu)掺杂的T-FMSAC,每种过渡金属设置 4种掺杂比例(10:1,25:1:,50:1,100:1(污泥:金属掺杂量,W:W)),共制备12种T-FMSAC.具体步骤为:①分别称取一定量的 FeSO4⋅7H2O、FeCl3⋅6H2O和过渡金属盐(Co(NO3)2⋅6H2O、CuCl2或 MnSO4记为 T2+) 使得 Fe3+:Fe2+摩尔比为2:1,Fe3+及Fe2+总含量与T2+摩尔比为2:1,并采用超纯水配制成40mL水溶液;②称取1g SAC放入上述水溶液中,并在 70℃下磁力搅拌(380r/ min)30min;③保持磁力搅拌条件,向混合溶液中滴加NaOH (10mL,5mol/L)直至溶液pH值达到10;④将pH值为10的水溶液放入93℃水浴锅中陈化 3h;⑤将陈化后的溶液倾倒掉上清液,并采用超纯水将残留固体材料洗至滤液pH值为中性,再用磁铁从水中分离具有磁性的颗粒;⑥最后,将具备磁性的颗粒放入 50℃烘箱烘干 24h,取粒径小于0.15mm的部分作为T-FMSAC催化剂待用.
1.3 实验方法
本实验采用的臭氧发生器(3S-A5,北京同林科技)是以高纯氧为气源.臭氧采用液态储备液形式注入催化反应体系中,其液态储备液的制备方法为向-20℃的超纯水体系鼓入气态臭氧(臭氧浓度在25~32mg/L).
催化臭氧氧化降解p-CBA的实验在一个容积为500.0mL的圆柱形玻璃反应器中进行.向反应器中加入250.0mL、pH值为6的磷酸盐缓冲溶液(1.0mmol/L),然后加入一定量的 p-CBA储备液使得反应体系内p-CBA初始浓度为1mg/L.同时加入0.01g上述制备的T-FMSAC催化剂和一定量的液态臭氧储备液使得液态臭氧在反应体系浓度为 1mg/L.与此同时,开启磁力搅拌器(RCT B S25,德国IKA公司)使其混合均匀(转速为 380r/min).反应开始后在设定的时间点取样,采样后立即加入0.2mL Na2SO3(24mmol/ L)终止臭氧与p-CBA的反应,样品经过0.22μm滤膜过滤去除杂质,待测.叔丁醇抑制实验亦按上述实验条件进行,并添加50mg/LTBA,考察T-FMSAC催化氧化去除p-CBA的反应机制.
此外,通过改变臭氧投加量(0.25、0.5、1.0、1.2mg/L)和T-FMSAC投加量(20、40、60mg/L),来考察T-FMSAC催化臭氧氧化去除p-CBA的最佳工艺条件.
1.4 分析方法
液态臭氧浓度用靛蓝法测定[19].水中p-CBA采用高效液相色谱(Agilent HPLC 1260,美国Agilent公司)进行测定,检测波长为 234nm,色谱柱 为 Agilent Poroshell 120EC-C18(4.6mm× 50mm,2.7μm,美国 Agilent公司),流动相为甲醇:乙腈:0.002% 醋酸溶液(V:V:V)=25:20:55,流速为0.5mL/min,柱温为30℃.
2 结果与讨论
2.1 T-FMSAC催化臭氧氧化去除p-CBA效能T-FMSAC吸附和T-FMSAC催化臭氧氧化去除p-CBA的效能如图1所示.可以看出,反应进行至 40min时,不同掺杂比例下 Mn-FMSAC、Co-FMSAC及Cu-FMSAC对p-CBA的吸附去除率为 14%~18%,说明过渡金属种类及其掺杂比例对T-FMSAC吸附去除p-CBA的效果影响不大.
图1(a)为不同负载量的Mn-FMSAC催化臭氧氧化去除p-CBA的效能.当污泥与金属掺杂量比为 10:1,25:1,50:1 和 100:1(W:W)时,Mn-FMSAC催化臭氧氧化对p-CBA的去除率分别为64%、69%、73%、76%.由此可见,Mn掺杂比例为 100:1时所得的催化剂(100:1Mn-FMSAC)具有最佳催化活性.有文献报道,过多的金属负载会引起空间位阻现象的发生且会减少催化剂本身的比表面积从而降低其催化性能[20-22],这可能是100:1Mn-FMSAC具备最佳催化效果的原因.图 1(b)及图 1(c)分别为不同负载量的 Co-FMSAC、Cu-FMSAC催化臭氧氧化去除p-CBA的效能图,其结果表明Co、Cu掺杂比例为100:1时所得到的催化剂具备最佳催化效果,进一步证实了以上结论.

图1 T-FMSAC吸附及其催化臭氧氧化去除p-CBA效能Fig.1 The performance of different kinds of T-FMSAC adsorption and catalytic ozonation on the removal of p-CBA
图 1(d)为 3种过渡金属掺杂制备的 100:1T-FMSAC催化臭氧氧化去除p-CBA的效能对比图.可以看出,100:1Mn-FMSAC具有最佳的催化臭氧去除p-CBA效果,去除率达到76%,高于100:1Co-FMSAC (72%)和 100:1Cu-FMSAC (65%).综合考虑催化剂活性、磁分离性能及应用前景,在后续试验中选择100:1Mn-FMSAC作为主要的催化剂.
2.2 臭氧浓度对100:1Mn-FMSAC催化臭氧氧化去除p-CBA效能的影响
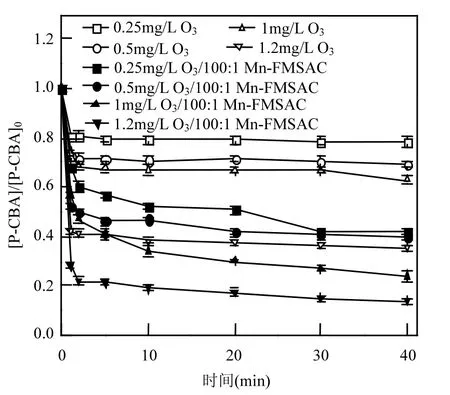
图2 臭氧浓度对100:1Mn-FMSAC催化臭氧氧化去除p-CBA的影响Fig.2 Effect of ozone concentration on p-CBA removal efficiency by catalytic ozonation with 100:1Mn-FMSAC
不同臭氧浓度下,单独臭氧氧化和100:1Mn-FMSAC催化臭氧氧化去除p-CBA的效能如图2所示.当臭氧初始浓度分别为 0.25、0.5、1.0和1.2mg/L时,反应 40.0min后,100:1Mn-FMSAC催化臭氧氧化工艺对 p-CBA的去除率分别为58.3%、60.6%、76%和 86.2%,而单独臭氧氧化对p-CBA的去除率分别为21.7%、31.2%、37.1%和64.7%.可见,随着水中臭氧初始浓度的增加,单独臭氧氧化和 100:1Mn-FMSAC催化臭氧氧化对p-CBA的去除率均随之增高.并且在相同臭氧浓度下(以1.2mg/L为例),100:1Mn-FMSAC催化臭氧氧化去除 p-CBA的效果(86.2%)优于 100: 1Mn-FMSAC吸附去除效果(18%)和单独臭氧氧化去除效果(64.7%)之和.
2.3 100:1Mn-FMSAC 投加量对其催化臭氧氧化去除p-CBA效能的影响

图3 100:1Mn-FMSAC催化剂投量对其吸附和催化臭氧氧化去除p-CBA效能影响Fig.3 Effect of catalyst dosage on p-CBA removal efficiency by adsorption of 100:1Mn-FMSAC and catalytic ozonation with 100:1Mn-FMSAC
分别考察了 100:1Mn-FMSAC催化剂在 3种投量(20、40、60mg/L)下吸附和催化臭氧氧化去除p-CBA的效能,结果如图3所示.可以看出,反应 40min后,随着催化剂投加量的增加,其对p-CBA的吸附去除率分别为14.1%,18%和21%,而其相应的催化臭氧氧化去除p-CBA的效率分别为56%,76%和83.1%,说明催化剂投加量的增加会显著提高 100:1Mn-FMSAC催化臭氧氧化工艺对p-CBA的去除效果.随着催化剂投加量的增加,催化剂表面的活性位点也会相应增加,有利于臭氧和反应物之间的反应以及催化臭氧分解产生活性物质(如⋅OH)[23].值得注意的是,当催化剂投加量由40mg/L增长至60mg/L时,p-CBA的去除率只有小幅增加,说明当臭氧投加量为1mg/L时,40mg/L的催化剂投量已经足够,在高催化剂投量下,虽然能够提供更多的活性位点,但此时水中溶解性臭氧含量已是提高p-CBA去除速率的限制因素.
2.4 叔丁醇对100:1Mn-FMSAC催化臭氧氧化去除p-CBA效能的影响
为进一步研究其反应机理,本研究进行了叔丁醇(Tertiary butyl alcohol,TBA)抑制⋅OH 试验.TBA的加入对臭氧单独氧化和 100:1Mn-FMSAC催化臭氧氧化p-CBA的影响如图4所示.当反应体系中加入TBA后, p-CBA的去除率明显降低,反应40min后,去除率由原来的76%下降到 26.3%,可见 TBA的加入明显抑制了 100:1Mn-FMSAC催化臭氧氧化p-CBA的效能,证明了在该体系中存在⋅OH,反应遵循羟基自由基反应机理.

图4 叔丁醇对100:1Mn-FMSAC催化臭氧氧化去除p-CBA效能影响Fig.4 Effect of the presence of TBA on p-CBA removal efficiency by catalytic ozoantion with 100:1Mn-FMSAC
由 TBA抑制实验结果可知,在 100:1Mn-FMSAC催化臭氧氧化去除p-CBA反应过程中产生了活性物种⋅OH.为了进一步说明反应体系中⋅OH贡献率(f⋅OH),通过以下公式计算得到:

式中:f⋅OH:⋅OH贡献率;fo3:分子臭氧贡献率;kTBA:叔丁醇抑制⋅OH 反应速率常数;koverall:催化臭氧氧化反应速率常数.
通过图4中数据,计算100:1Mn-FMSAC催化臭氧氧化去除 p-CBA 实验过程中 koverall及 TBA 抑制过程中 kTBA可知,kTBA=0.0055min-1, koverall=0.0256min-1代入公式(1)可知f⋅OH为78.5%,表明在该反应体系中以⋅OH反应为主,即 100:1Mn-FMSAC催化剂主要通过促进臭氧分解产生更多的⋅OH去除p-CBA.
3 结论
3.1 过渡金属种类及其掺杂比例对于 TFMSAC吸附去除p-CBA效果影响较小,而其对T-FMSAC催化臭氧氧化去除p-CBA影响效果较大;100:1Mn-FMSAC具有最佳的催化臭氧氧化去除p-CBA效果.
3.2 随着臭氧浓度的增加,100:1Mn-FMSAC催化臭氧氧化去除p-CBA的效率显著增强.综合考虑催化效果及原材料成本,当臭氧投加量为1mg/L时,催化剂的最佳投加量为40mg/L.
3.3 叔丁醇的加入在很大程度上抑制了 100:1Mn-FMSAC催化臭氧氧化去除p-CBA的效能,说明该反应体系遵循羟基自由基反应机制,经计算得到⋅OH对p-CBA的去除贡献率为78.5%.
[1]李 璐,封 莉,张立秋.污泥基活性炭表面官能团对其催化臭氧氧化活性的影响 [J]. 环境化学, 2014,(6):937-42.
[2]王红娟,齐 飞,封 莉.污泥基活性炭催化臭氧氧化降解水中微量布洛芬的效能研究 [J]. 环境科学, 2012,33(5):1591-6.
[3]GuTI RREZ-SEGURA. Adsorprion of cadmium by Na and Fe modified zeolitic tuffs and carbonaceous material from pyrolyzed sewage sludge [J]. Journal of Environmental Management, 2012, 97(2):6-13.
[4]RAJPUT S. Modeling and evaluation of chromium remediation from water using low cost bio-char,a green adsorbent [J]. Journal of Hazardous Materials, 2011,188(1-3):319-33.
[5]Bandosz T J. Effect of pyrolysis temperature and time on catalytic performance of sewage sludge/industrial sludge-based composite adsorbents [J]. Applied Catalysis B Environmental, 2006,67(1/2):77-85.
[6]Hwang H R. The perparation of an adsorbent from mixtures of sewage sludge and coal-tar pitch using an alkaline hydroxide activation agent [J]. Journal of Analytical & Applied Pyrolysis, 2008,83(2):220-6.
[7]Qian Q. Removal of copper from aqueous solution using ironcontaining adsorbents derived from methane fermentation sludge[J]. 2009,172(2/3):1137-44.
[8]李长波,赵国峥,王 飞.负载型臭氧氧化催化剂研究进展 [J].当代化工, 2014,(3):453-6.
[9]任百祥,范晶莹,杨春维.磁性活性炭催化臭氧氧化降解水中甲基橙 [J]. 化工环保, 2015,35(4):409-13.
[10]莫冰玉,唐玉斌,陈芳艳.磁性活性炭的制备及其对水中甲基橙的吸附 [J]. 环境工程学报, 2015,9(4):1863-8.
[11]Kwon J H. Synthesis and characterization of magnetite and actived carbon binary composites [J]. Synthetic Metals, 2014, 197(4):8-17.
[12]Shao L. Facile synthesis, characterization of a MnFe2O4/activated carbon magnetic composite and its effectiveness in tetracycline removal [J]. Materials Chemistry & Physics, 2012,135(1):16-24.
[13]Qiang Z. Kinetics and mechanism for omethoate degradation by catalytic ozonation with Fe(III)-loaded activated carbon in water [J]. Chemosphere, 2013,90(6):1966-72.
[14]LI H. Degradation of bezafibrate in wastewater by catalytic ozonation with cobalt doped red mud:Efficiency, intermediates and toxicity [J]. Applied Catalysis B Environmental, 2014,s152-253(1):342-51.
[15]LAN B. Catalytic ozonation of p-chlorobenzoic acid in aqueous solution using Fe-MCM-41as catalyst [J]. Chemical Engineering Journal, 2013,219(3):346-54.
[16]SUI M. Heterogeneous catalytic ozonation of ciprofloxacin in water with carbon nanotube supported manganese oxides as catalyst [J]. Journal of Hazardous Materials, 2012,s227-228(227-228):227-36.
[17]LI M. Influence of modification method and transition metal type on the physicochemical properties of MCM-41catalysts and their performances in the catalytic ozonation of toluene [J]. Applied Catalysis B Environmental, 2011,107(3/4):245-52.
[18]Zhao L. Enhancement Mechanism of Heterogeneous Catalytic Ozonation by Cordierite-Supported Copper for the Degradation of Nitrobenzene in Aqueous Solution [J]. Environmental Science & Technology, 2009,43(6):2047-53.
[19]Bander H. Determination of ozone in water by the indigo method [J]. Water Research, 1981,15(4):449-56.
[20]LI L. Catalytic ozoantion of dimethyl phthalate over cerium supported on activated carbon [J]. Joural of Hazardous Materials, 2009,170(1):411-6.
[21]Huang R. Catalytic activity of Fe/SBA-15for ozonation of dimethyl phthalate in aqueous solution [J]. Applied Catalysis B Environmental, 2011,106(1/2):264-71.
[22]FELLENZ N A. Influence of Bronsted and Lewis acid sites on the catalytic activity and selectivity of Fe/MCM-41system [J]. Applied Catalysis A General, 2012,s435-436(17):187-96.
[23]LIU H. Activated carbon and cerium supported on activated carbon applied to the catalytic ozonation of polycyclic aromatic hydrocarbons [J]. Journal of Molecular Catalysis A Chemical, 2012,363-364(11):101-7.
Preparation of T-FMSAC and its catalytic ozonation performance on the removal of p-CBA in water.
LU Si-ying,SUN Zhong-en, FENG Li, ZHANG Li-qiu*(Beijing Key Lab for Source Control Technology of Water Pollution, College of Environmental Science and Engineering, Beijing Forestry University, Beijing 100083, China). China Environmental science, 2017,37(6):2139~2144
Basing on the activated carbon prepared from sludge, different transition metals (Mn, Co, and Cu) doped ferromagnetic sludge-based activated carbons (T-FMSAC, T= Mn, Co, and Cu) were prepared by chemical coprecipitation method. The effects of metal species and doping ratio on the removal efficiency of p-chlorobenzoic acid (p-CBA) in water by T-FMSAC catalytic ozonation were investigated, and the optimal dosages of initial ozone and T-FMSAC catalyst were further determined. Experimental results showed that, after 40minutes of ozonation, Mn-FMSAC exhibited the highest catalytic activity under the initial ozone and catalyst dosage of 1mg/L and 40mg/L respectively, and the removal efficiency was 76%, higher than that for Co-FMSAC (72%) or Cu-FMSAC (65%). In addition, the removal efficiency of p-CBA decreased with the increase in the doping ratio from SAC: metal=100:1 to 10:1. With the doping ratio of 100:1, the T-FMSAC exhibited the optimal magnetic separation property and catalytic activity. The optimal condition for 100:1Mn-FMSAC catalytic ozonation was determined to be [O3]0= 1mg/L and [FMSAC]0= 40mg/L. Besides, the inhibition of p-CBA degradation by tertiary butyl alcohol (TBA) indicated that this process followed the hydroxyl radical reaction mechanism.
ferromagnetic sludge-based activated carbon;transition metal;catalytic ozonation;p-chlorobenzoic acid
X703
A
1000-6923(2017)06-2139-06
卢思颖(1992-),女,内蒙古乌海人,硕士研究生,主要研究方向为环境功能材料研发及高级氧化技术处理技术.
2016-10-21
北京市教委共建项目(2015GJ-02);国家自然科学基金项目(51178046)
* 责任作者, 教授, zhangliqiu@163.com

