丙戊酸钠神经保护作用机制及其应用研究
刘全乐 李天富 王保国*
(1.首都医科大学三博脑科医院麻醉科,北京 100093; 2.首都医科大学三博脑科医院神经内科,北京 100093)
· 麻醉学与神经科学 ·
丙戊酸钠神经保护作用机制及其应用研究
刘全乐1李天富2王保国1*
(1.首都医科大学三博脑科医院麻醉科,北京 100093; 2.首都医科大学三博脑科医院神经内科,北京 100093)
丙戊酸钠(sodium valproate)作为一种组蛋白去乙酰酶抑制剂,广泛应用于抗癫痫治疗以及精神分裂、双相障碍等精神疾病的治疗。丙戊酸钠还能对神经元的生长、变异、凋亡产生影响,发挥神经保护作用。丙戊酸钠的作用机制与神经传递和细胞内信号传导通路的调节有关。丙戊酸钠作为神经功能保护药物治疗神经损伤以及认知障碍有待于进一步研究。
丙戊酸钠;神经保护;信号传导;组蛋白去乙酰酶抑制剂
丙戊酸(valproic acid,VPA)是一种短支链脂肪酸,最初是由从植物中提取的缬草酸合成的[1]。常以丙戊酸钠(sodium valproate)的形式被用于治疗癫痫和双相情感障碍等疾病[1-2]。近年来,VPA以其良好的安全性[3]、合并症少[1]以及治疗剂量下几乎不对病人的意识产生影响等特性[4],日益受到神经外科医生的推崇,成为神经外科术后预防性抗癫痫治疗的首选药物。除此之外,VPA应用于一些急性神经系统损伤动物模型中,如创伤性脑损伤(traumatic brain injury,TBI)、脊髓损伤(spinal cord injury,SCI)、脑卒中(stroke)等,显示了良好的神经保护作用,在临床中的应用也越来越受重视。目前VPA的神经保护作用机制成为国内外研究的热点。本文就近年来VPA神经保护作用的相关机制和临床应用作一综述。
1 VPA抗癫痫作用机制
癫痫(epilepsy)是大脑神经元突发性放电,导致短暂的大脑功能障碍的一种慢性疾病。癫痫的发作主要是由于中枢神经系统兴奋与抑制的不平衡所致,与离子通道、神经递质及神经胶质细胞的改变有关。目前VPA治疗癫痫的作用与以下几方面有关:
1.1 作用于γ-氨基丁酸(γ-aminobutyric acid,GABA)能系统
VPA抗癫痫的作用机制与多种综合因素造成神经元兴奋性降低有关[5]。早在20世纪70年代,就有人提出VPA对于GABA能系统的作用。GABA是哺乳动物神经系统中重要的抑制性神经传递物质[6-7],癫痫的发生与GABA介导的抑制性突触传递作用降低有关。VPA主要通过作用于GABA的代谢途径进而影响GABA的水平,最终增强GABA介导的突触后抑制作用[8]。如图1所示,VPA通过作用于GABA的合成和分解代谢的关键酶发挥作用,最后总的结果是增加GABA的水平。近期一些研究[9-11]表明,VPA除了对于GABA代谢途径的影响外,还能够增强GABA受体的反应,能够通过与GABA-A受体苯二氮卓结合位点相互作用延长突触后抑制作用的时间。
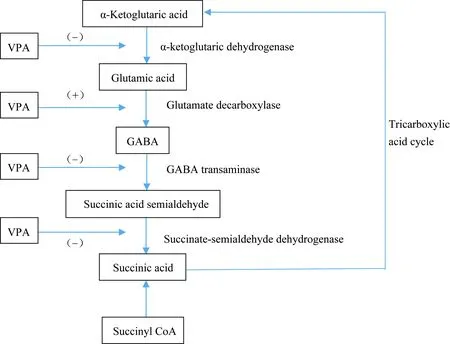
图1 VPA对GABA能系统作用示意图Fig.1 Schematic diagram of the effect of VPA on the GABA energy system
(+)shows the positive effect on the corresponding enzyme, and (-) indicates the negative inhibition of the corresponding enzyme;VPA: valproic acid;GABA: γ-aminobutyric acid.
1.2 作用于谷氨酸能系统
谷氨酸是一种兴奋性神经递质,对癫痫的诱发和发作起重要作用。研究[12]表明VPA能够降低大脑内谷氨酸和天冬氨酸的水平。但是近年来有一些实验[13]得出了相对矛盾的结果,VPA在脑内不同的区域对谷氨酸的作用是有差别的。例如在VPA慢性治疗的大鼠模型中,VPA能剂量依赖性地提高海马组织内谷氨酸的摄取能力,然而在额叶或者顶叶的皮质和小脑组织内却没有发现类似的结果[13]。VPA对谷氨酸的影响,在不同组织内得出了不同的观察结果可能与谷氨酸能系统的突触可塑性有关。
1.3 作用于离子通道
VPA的抗癫痫作用除了与上述两个神经递质系统有关外,还与VPA对细胞膜离子通道的作用有关。在早期的一项研究[14]中,研究者选取单个神经纤维的郎飞结,利用电压钳技术研究细胞膜钠钾电流,结果表明VPA能够同步阻滞钠和钾的传导,进而使细胞动作电位幅度、去极化最大速率降低,阈电位提高,最终导致了兴奋性的降低。N-甲基-D天冬氨酸(N-methyl-D-aspartic acid, NMDA)受体作为谷氨酸的受体之一,其拮抗剂被用于临床麻醉,逐步发展成为癫痫、卒中以及防止神经退行性损伤的治疗药物[15]。NMDA拮抗剂有明显的神经毒性,NMDA受体功能不良可能与神经退行性疾病(如阿尔茨海默病、双相情感障碍、精神分裂)有关。如图2所示,谷氨酸与GABA能神经元和去甲肾上腺素能神经元的NMDA受体结合能够维持这两种神经元对两种兴奋通路的紧张性抑制(tonic inhibitory)作用。NMDA拮抗剂能够消除这种抑制作用,从而受这两种通路支配的神经元将会处于极度活跃状态,进而导致多种细胞内通路的破坏,最终导致急性认知功能障碍等疾病的发生。VPA对钠通道的阻滞能够抑制NMDA拮抗剂相关的神经毒性作用。这也为VPA应用于临床麻醉,抑制由NMDA拮抗剂类的麻醉药物造成的神经毒性提供了理论依据。
2 VPA神经保护作用机制
组蛋白是真核生物体染色质中的碱性蛋白,是真核生物染色体基本结构蛋白,与带负电荷的双螺旋DNA结合成DNA-组蛋白复合物。染色质的局部重塑和动力学改变是基因表达的关键环节,进而影响细胞的变异、增生等功能[16]。其中影响染色质重塑的重要机制之一就是组蛋白N末端的乙酰化修饰。组蛋白的乙酰化作用由组蛋白乙酰转移酶(histone acetyltransferase,HAT)介导;组蛋白去乙酰化作用由组蛋白去乙酰酶(histone deacetylase,HDAC)介导。在组蛋白的去乙酰化过程中,HAT和HDAC的活性是相互平衡的[17]。HDAC能够影响细胞基因表达的修饰,VPA作为一种组蛋白去乙酰酶抑制剂(histone deacetylase inhibitor, HDACI),能够激活细胞生存因子Akt,进而发挥多种神经保护作用。下面就VPA的抗凋亡作用、抗炎作用、抗氧化作用等方面分别叙述VPA的神经保护作用及相关机制。
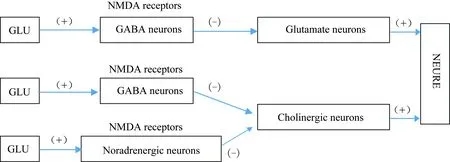
图2 VPA作用于谷氨酸和GABA代谢机制Fig.2 Mechanisms of VPA action on the glutamate and GABA metabolism
NMDA receptors are a unique dual gated channel that is controlled by both membrane potential and by other neurotransmitters. Mainly in the neural cells of the postsynaptic membrane, NMDA receptors is a class of important excitatory amino acid receptors. Glutamate acts on GLU nerve pathway and energetic pathway through the GABAergic neurons and NEergic neurons NMDA receptor. Glutamate binds to NMDA receptors of GABAergic neurons and norepinephrine neurons to maintain the inhibitory effects of these two neurons on the Glutamate nerve pathway and cholinergic nerve pathways, and thus effectively inhibit the excessive activity of the neurons. (+) indicates excitement, (-) indicates inhibition;VPA: valproic acid;Glu:glutamate; NMDA:N-methyl-D-aspartic acid;GABA: γ-aminobutyric acid.
2.1 抗细胞凋亡作用
研究[2]表明,对于一些急性中枢神经系统损伤性疾病,神经元凋亡机制不恰当的激活是造成其病理学表现的主要机制。VPA已经被证实能够在急性中枢神经系统损伤中抑制细胞的凋亡。VPA主要通过正向调节磷酸肌醇3激酶(phosphatidylinositol 3 kinase, PI3K)/Akt通路,如图3所示,磷酸化通路中的Akt和GSK-3β两个因子,最终抑制凋亡激酶的激活进而发挥抗凋亡的作用[18]。PI3K/Akt信号通路在介导神经元的生存机制中起到重要作用[19]。PI3K是一种细胞表面因子,能够激活Akt。Akt通过磷酸化多种酶、激酶和转录因子等作用调节细胞功能。TRB3和PTEN与PI3K的功能相反,可以减少Akt的活化。GSK-3β是一种与多种细胞生物过程有关的激酶,能够调节多种细胞骨架蛋白,在中枢神经系统中有重要作用。VPA能够抑制其活性,但是否可以直接抑制其活性仍然存在争议。β连环蛋白可以通过提高抗凋亡蛋白质如Bcl-2的水平改善细胞生存能力。VPA主要通过抑制TRB3和PTEN促进Akt的磷酸化,上调P-GSK-3β和β连环蛋白的方式促进细胞存活,抵抗细胞凋亡。
VPA的抗凋亡机制除了与上述的细胞通路有关,还与热休克蛋白70(heat shock protein70,HSP70)的诱导有关。热休克蛋白家族有强效的细胞保护作用[20]。HSP70通过多种机制抗细胞凋亡。caspase-3的激活具有细胞色素酶c依赖性。HSP 70可以抑制caspase-3的激活,并且抑制其下游的凋亡介导因子。HSP还可以使JNK失活,抑制其兴奋性细胞毒性作用,同时HSP作为分子伴侣,能够防止蛋白的聚集,减少细胞死亡。在短暂局灶性脑缺血的大鼠模型中,VPA能够上调大脑内HSP 70水平,减少缺血引起的大脑损伤[20]。除了HSP 70,VPA能够诱导多种神经保护蛋白(如BCL-2、葡萄糖转运蛋白78、脑源性神经营养因子等)的表达,但机制是否与VPA的组蛋白去乙酰酶抑制作用有关目前还尚不清楚。
除此之外,也有研究[21]表明VPA能够激活一些细胞外信号调节激酶类,反过来影响转录因子活性和基因的表达。在一项以外伤性脑损伤和失血性休克大鼠为模型的实验中,观察了VPA对脑部基因表达的影响,结果显示神经丝轻链基因(neurofilament light gene,NEFL)和SLX4两种基因在应用VPA的大鼠神经元中过度表达。这两种基因在神经元的再生、变异和成熟中有重要作用,并且与神经元凋亡的抑制有关。这些基因的表达对抑制细胞凋亡,提升神经元再生能力有重要作用[22]。
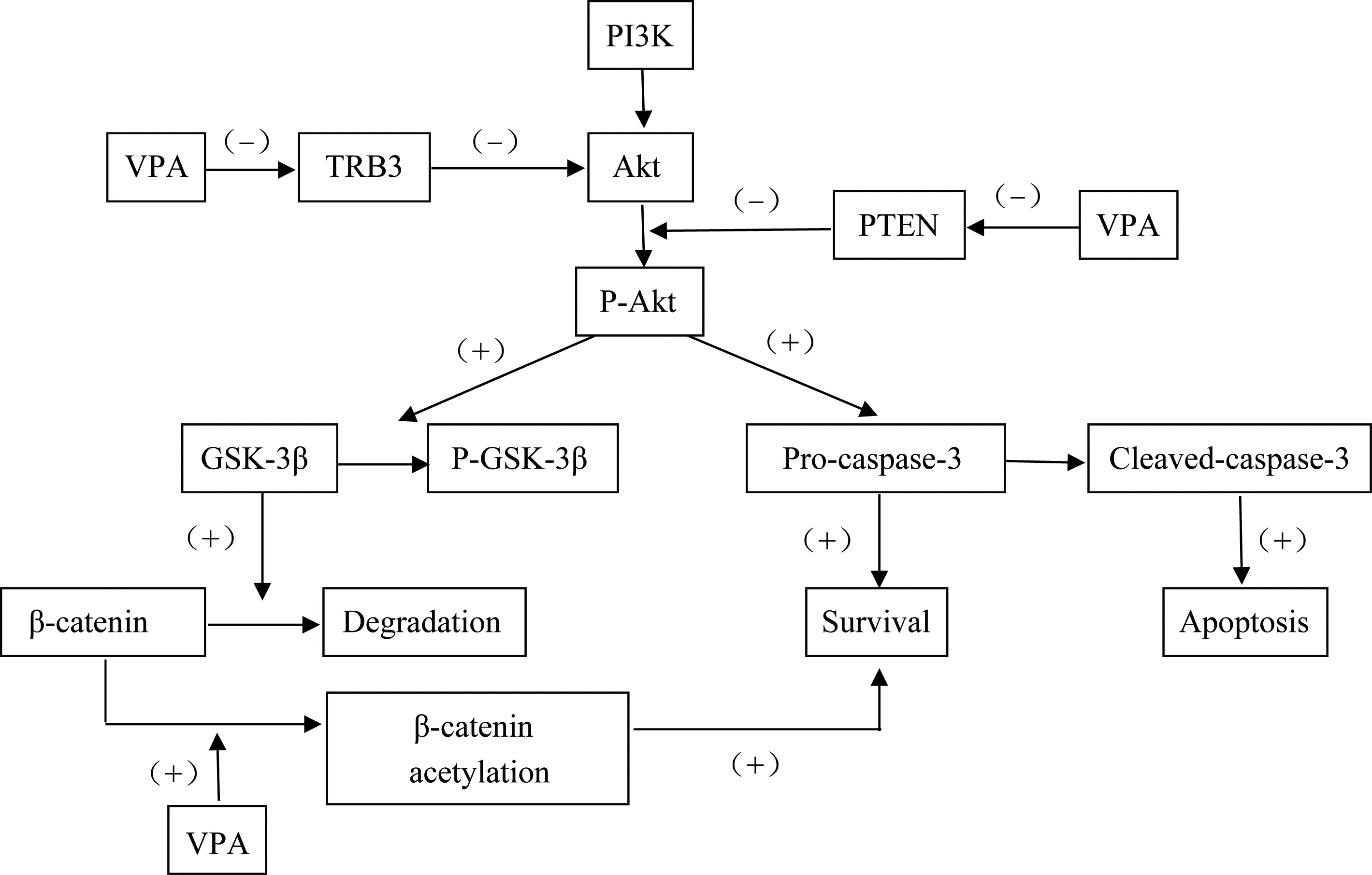
图3 VPA作用于PI3K/Akt通路机制Fig.3 VPA acting on PI3K/Akt pathway mechanism
(+) indicates excitement, (-) indicates inhibition; PI3K: phosphatidylinositol 3 kinase;Akt: serine/threonine kinase;TRB3: tribbles 3, a pseudo-kinase that controls stress, cell growth and metabolic processes;PTEN:phosphate and tension homology deleted on chromsome ten,PTENgene is a novel tumor suppressor gene whose product PTEN protein has lipid phosphatase activity and protein phosphatase activity;P-Akt: phosphorylated Akt;GSK-3β: glycogen synthase kinase-3β; P-GSK-3β: phosphorylated GSK-3β;Pro-caspase-3: Cysteine-3 precursor, caspase-3 is considered to be the most important terminal cleavage enzyme in apoptosis. Cleaved-caspase-3: caspase-3 cleaves into cleaved-caspase-3 after cleavage, which is the active form of the former.
2.2 抗炎性作用
神经炎性反应是中枢神经系统功能紊乱十分重要的发病机制,同时在脑部损伤中也起到重要作用[23-24]。在一些神经损伤模型中,VPA的抗炎作用得到证实[2]。小胶质细胞(microglial)作为一种普通免疫细胞,在神经元的生理活动中起着支持、营养、保护和修复的重要功能。在炎性反应刺激下,抗原性增强,功能活跃。研究[25]证实VPA能够抑制小胶质细胞的活性,并且在中脑神经元-神经胶质培养中,VPA能够保护多巴胺能神经元不受脂多糖引起的炎性损伤。在人类神经胶质的培养中发现,VPA改变了小胶质细胞的表现型,并且能够抑制小胶质细胞的吞噬作用[26]。在淋巴结中,VPA抑制Th1和Th7的反应但是能够对Th2和调节性T细胞的反应起到促进作用。在脑脊髓炎大鼠模型中,VPA减少巨噬细胞和淋巴细胞在脊髓内的积累[27]。VPA的抗炎作用主要是对炎性小体聚集和活性的抑制发挥作用。在众多炎性小体中,NLRP3是最近发现的胞质蛋白,主要参与免疫炎性应答反应。不论是内源性的还是外源性的刺激物都可以刺激NLRP3发生反应,NLRP3的激活涉及两个过程:1)NF-κB通路的激活能够启动NLRP3的转录,提高其数量并促进其聚集;2)多种刺激可以激活NLRP3,如细胞内低钾、增多的活性氧(reactive oxygen species, ROS)都能激活NLRP3炎性小体。参与免疫反应的早期和炎性反应各个阶段的分子都受到NF-κB的调控,VPA能够通过抑制NF-κB的活性进而减少NLRP3炎性小体的产生[28-33]。
2.3 神经营养作用
神经营养因子包括脑源性营养因子和胶质源性营养因子,对神经元的存活和功能都有重要作用。VPA能够上调这些营养因子。机制可能是VPA加强营养因子基因周围组蛋白的乙酰化,从而激活脑源性和胶质源性营养因子启动子并促进其转录[34-36]。
2.4 抗氧化防御作用
氧化应激(oxidative stress,OS)是指体内氧化与抗氧化作用失衡,倾向于氧化。OS是由自由基在体内产生的一种负面作用。VPA通过抑制脂质过氧化和蛋白质氧化对氧化应激起防御作用。众所周知,谷胱甘肽S-转移酶(glutathione S-transferases,GSTs)是谷胱甘肽结合反应的关键酶。GSTs能够清除体内氢过氧化物。GSTs同工酶能够清除脂类自由基,在抗脂质过氧化反应中起重要作用,是抗氧化的重要保护因子。VPA能够调节3种GST同工酶的表达。谷胱甘肽作为大脑内重要的抗氧化剂,在抗氧化防御中发挥重要作用。在培养的大鼠皮质细胞中,VPA既能够提高谷胱甘肽的水平,同时还能增加谷胱甘肽合成限速酶的表达。通过这种方式,VPA抑制了过氧化氢诱发的细胞死亡[37]。Shao等[38]发现,同样是在大鼠皮质细胞培养基中,VPA能够明显抑制谷氨酸盐诱发的细胞内游离钙的增加、脂质过氧化作用、蛋白质氧化作用、DNA的分裂和细胞死亡。有研究[39]表明,JNK信号通路在ROS介导的细胞死亡中发挥重要作用。VPA在含氧正常的细胞中对JNK没有激活作用,但是在低氧细胞中,能够显著抑制JNK的活性,这可能与上述的VPA对HSP 70的上调作用有关。VPA的抗氧化防御作用可能是其神经功能保护的主要作用机制。
2.5 保护血脑脊液屏障作用
一些急性神经系统损伤性疾病,如创伤性脑损伤(traumatic brain injury,TBI)造成的认知和行为异常,不仅与初始损伤有关,还与进行性的病理发展性损伤相关。其中血脑脊液屏障(blood-brain barrier,BBB)的破坏导致的脑内环境的紊乱,大量兴奋性神经递质的释放、神经元的炎性反应等都与大脑外伤后的二次损伤有关[40-44]。在TBI大鼠模型中,损伤后注射VPA可以减少血脑脊液屏障的渗透,改善血脑脊液屏障的完整性和功能[45]。该实验[45]还证实了损伤后早期注射VPA对于运动和认知功能的改善都有作用。有研究[46-47]表明脑卒中后导致血脑脊液屏障破坏和功能紊乱的重要调节因子是基质金属蛋白酶9。VPA能够降低这种蛋白质的活性,同时能够保护紧密连接,这也是其保护血脑脊液屏障的机制之一。
3 VPA的神经保护应用研究
VPA作为目前临床上一线广谱抗癫痫药物广泛应用于抗癫痫治疗中,其在神经外科术后以及颅脑损伤后预防和控制癫痫发作越来越受到关注。神经外科术后癫痫发生的主要原因是手术操作过程中分离病变以及脑板牵拉脑组织造成皮质脑组织的损伤。即使目前微创手术也是如此。这些损伤会引起皮质局部内环境的改变而诱发早期癫痫。术后预防性使用抗癫痫药物仍然存在争议。但是术后预防性应用VPA可以明显降低术后癫痫的发生率,而且在治疗剂量下使用不良反应小,安全性高。
一些临床前期的研究[2]显示,VPA在一些急性神经系统损伤中,如缺血性脑卒中(ischemic stroke)、颅内出血(intracerebral hemorrhage,ICH)、TBI和脊髓损伤(spinal cord injury,SCI),均能表现出神经保护作用,能从上述多个方面发挥其神经保护作用。对于一些神经性损伤的疾病,VPA的应用同样表现出了神经保护效应。例如皮下或经静脉注射VPA能够促进视网膜神经节细胞生存,使损伤的视神经重塑[48]。
4 前景与展望
通过以上对于VPA抗癫痫机制和神经保护作用机制的分析,以及一些VPA临床前期证据,都提示VPA在治疗急性中枢神经系统损伤中有重要作用。神经外科术后预防性应用VPA不仅能够有效抑制术后癫痫的发生,同时还能够有助于病人神经功能的恢复。这也为将丙戊酸钠的镇静作用和神经保护作用有机结合起来,应用于神经外科麻醉领域提供了一个新的思路。也有文献[49]报道,VPA对一些有认知障碍特点的神经退行性疾病有神经保护作用,并且可以加强记忆功能。越来越多的研究者投身于VPA抗阿尔茨海默病、帕金森病、亨廷顿舞蹈症和认知功能障碍的研究中。然而,因为VPA缺乏以其神经保护作用应用于临床的证据,以及药物本身产生的不良反应和毒性的限制,使VPA作为神经保护药物应用于临床还处于探索阶段。不同剂量的VPA能够发挥不同的药理效应,在临床上,100~120 mg/kg的剂量时能够发挥抗癫痫作用,高浓度的VPA(500 mg·kg-1·d-1)有组蛋白去乙酰酶抑制剂依赖性抗肿瘤作用,当VPA抑制组蛋白去乙酰化的作用提高细胞生存能力时,剂量范围是非常狭窄的,使VPA发挥促进组蛋白乙酰化作用需要很高的血药浓度,但是VPA的高浓度随之而来的就是其毒性反应的增加。
探索丙戊酸钠应用于临床的剂量,使其既发挥其神经保护作用,又能减少其不良反应和毒性反应还有很长的一段路要走,但无疑具有独特药理学优势的丙戊酸钠值得我们为之努力探索。
[1] Löscher W. Basic pharmacology of valproate: a review after 35 years of clinical use for the treatment of epilepsy[J]. CNS Drugs, 2002,16(10):669-694.
[2] Chen S, Wu H, Klebe D, et al. Valproic acid: a new candidate of therapeutic application for the acute central nervous system injuries[J]. Neurochem Res, 2014,39(9):1621-1633.
[3] Venkataraman V, Wheless J W. Safety of rapid intravenous infusion of valproate loading doses in epilepsy patients[J]. Epilepsy Res, 1999,35(2):147-153.
[4] Mattson R H, Cramer J A, Collins J F. A comparison of valproate with carbamazepine for the treatment of complex partial seizures and secondarily generalized tonic-clonic seizures in adults. The department of Veterans Affairs Epilepsy Cooperative Study No. 264 Group[J]. N Engl J Med, 1992,327(11):765-771.
[5] Löscher W. Valproate: a reappraisal of its pharmacodynamic properties and mechanisms of action[J]. Prog Neurobiol, 1999,58(1):31-59.
[6] Hu J, Quick M W. Substrate-mediated regulation of gamma-aminobutyric acid transporter 1 in rat brain[J]. Neuropharmacology, 2008,54(2):309-318.
[7] Chiu C S, Brickley S, Jensen K, et al. GABA transporter deficiency causes tremor, ataxia, nervousness, and increased GABA-induced tonic conductance in cerebellum[J]. J Neurosci, 2005,25(12):3234-3245.
[8] Monti B, Polazzi E, Contestabile A. Biochemical, molecular and epigenetic mechanisms of valproic acid neuroprotection[J]. Curr Mol Pharmacol, 2009,2(1):93-109.
[9] Harrison N L, Simmonds M A. Sodium valproate enhances responses to GABA receptor activation only at high concentrations[J]. Brain Res, 1982,250(1):201-204.
[10]Motohashi N. GABA receptor alterations after chronic lithium administration. Comparison with carbamazepine and sodium valproate[J]. Prog Neuropsychopharmacol Biol Psychiatry, 1992,16(4):571-579.
[11]Cunningham M O, Woodhall G L, Jones R S. Valproate modifies spontaneous excitation and inhibition at cortical synapses in vitro[J]. Neuropharmacology, 2003,45(7):907-917.
[12]Thurston J H, Hauhart R E. Valproate doubles the anoxic survival time of normal developing mice: possible relevance to valproate-induced decreases in cerebral levels of glutamate and aspartate, and increases in taurine[J]. Life Sci, 1989,45(1):59-62.
[13]Hassel B, Iversen E G, Gjerstad L, et al. Up-regulation of hippocampal glutamate transport during chronic treatment with sodium valproate[J]. J Neurochem, 2001,77(5):1285-1292.
[14]VanDongen A M, VanErp M G, Voskuyl R A. Valproate reduces excitability by blockage of sodium and potassium conductance[J]. Epilepsia, 1986,27(3):177-182.
[15]Farber N B, Jiang X P, Heinkel C, et al. Antiepileptic drugs and agents that inhibit voltage-gated sodium channels prevent NMDA antagonist neurotoxicity[J]. Mol Psychiatry, 2002,7(7):726-733.
[16]Göttlicher M, Minucci S, Zhu P, et al. Valproic acid defines a novel class of HDAC inhibitors inducing differentiation of transformed cells[J]. EMBO J, 2001,20(24):6969-6978.
[17]Li Y, Alam H B. Modulation of acetylation: creating a pro-survival and anti-inflammatory phenotype in lethal hemorrhagic and septic shock[J]. J Biomed Biotechnol, 2011,2011:523481.
[18]Bambakidis T, Dekker S E, Liu B, et al. Hypothermia and valproic acid activate prosurvival pathways after hemorrhage[J]. J Surg Res, 2015,196(1):159-165.
[19]Brunet A, Datta S R, Greenberg M E. Transcription-dependent and -independent control of neuronal survival by the PI3K-Akt signaling pathway[J]. Curr Opin Neurobiol, 2001,11(3):297-305.
[20]Ren M, Leng Y, Jeong M, et al. Valproic acid reduces brain damage induced by transient focal cerebral ischemia in rats: potential roles of histone deacetylase inhibition and heat shock protein induction[J]. J Neurochem, 2004,89(6):1358-1367.
[21]Yuan P X, Huang L D, Jiang Y M, et al. The mood stabilizer valproic acid activates mitogen-activated protein kinases and promotes neurite growth[J]. J Biol Chem, 2001,276(34):31674-31683.
[22]Dekker S E, Bambakidis T, Sillesen M, et al. Effect of pharmacologic resuscitation on the brain gene expression profiles in a swine model of traumatic brain injury and hemorrhage[J]. J Trauma Acute Care Surg, 2014,77(6): 906-912; discussion 912.
[23]Lucas S M, Rothwell N J, Gibson R M. The role of inflammation in CNS injury and disease[J]. Br J Pharmacol, 2006,147 Suppl 1:S232-240.
[24]Ahmad M, Graham S H. Inflammation after stroke: mechanisms and therapeutic approaches[J]. Transl Stroke Res, 2010,1(2):74-84.
[25]Chen P S, Wang C C, Bortner C D, et al. Valproic acid and other histone deacetylase inhibitors induce microglial apoptosis and attenuate lipopolysaccharide-induced dopaminergic neurotoxicity[J]. Neuroscience, 2007,149(1):203-212.
[26]Gibbons H M, Smith A M, Teoh H H, et al. Valproic acid induces microglial dysfunction, not apoptosis, in human glial cultures[J]. Neurobiol Dis, 2011,41(1):96-103.
[27]Zhang Z, Zhang Z Y, Wu Y, et al. Valproic acid ameliorates inflammation in experimental autoimmune encephalomyelitis rats[J]. Neuroscience, 2012,221:140-150.
[28]Bauernfeind F G, Horvath G, Stutz A, et al. Cutting edge: NF-kappaB activating pattern recognition and cytokine receptors license NLRP3 inflammasome activation by regulating NLRP3 expression[J]. J Immunol, 2009,183(2):787-791.
[29]Harder J, Franchi L, Muoz-Planillo R, et al. Activation of the Nlrp3 inflammasome by Streptococcus pyogenes requires streptolysin O and NF-kappa B activation but proceeds independently of TLR signaling and P2X7 receptor[J]. J Immunol, 2009,183(9):5823-5829.
[30]Segovia J, Sabbah A, Mgbemena V, et al. TLR2/MyD88/NF-κB pathway, reactive oxygen species, potassium efflux activates NLRP3/ASC inflammasome during respiratory syncytial virus infection[J].PLoS One,2012,7(1):e29695.
[31]Latz E, Xiao T S, Stutz A. Activation and regulation of the inflammasomes[J]. Nat Rev Immunol, 2013,13(6):397-411.
[32]Kwon K J, Kim J N, Kim M K, et al. Neuroprotective effects of valproic acid against hemin toxicity: possible involvement of the down-regulation of heme oxygenase-1 by regulating ubiquitin-proteasomal pathway[J]. Neurochem Int, 2013,62(3):240-250.
[33]Wang Z, Leng Y, Tsai L K, et al. Valproic acid attenuates blood-brain barrier disruption in a rat model of transient focal cerebral ischemia: the roles of HDAC and MMP-9 inhibition[J]. J Cereb Blood Flow Metab, 2011,31(1):52-57.
[34]Wu X, Chen P S, Dallas S, et al. Histone deacetylase inhibitors up-regulate astrocyte GDNF and BDNF gene transcription and protect dopaminergic neurons[J]. Int J Neuropsychopharmacol, 2008,11(8):1123-1134.
[35]Bredy T W, Wu H, Crego C, et al. Histone modifications around individual BDNF gene promoters in prefrontal cortex are associated with extinction of conditioned fear[J]. Learn Mem, 2007,14(4):268-276.
[36]Yasuda S, Liang M H, Marinova Z, et al. The mood stabilizers lithium and valproate selectively activate the promoter IV of brain-derived neurotrophic factor in neurons[J]. Mol Psychiatry, 2009,14(1):51-59.
[37]Cui J, Shao L, Young L T, et al. Role of glutathione in neuroprotective effects of mood stabilizing drugs lithium and valproate[J]. Neuroscience, 2007,144(4):1447-1453.
[38]Shao L, Young L T, Wang J F. Chronic treatment with mood stabilizers lithium and valproate prevents excitotoxicity by inhibiting oxidative stress in rat cerebral cortical cells[J]. Biol Psychiatry, 2005,58(11):879-884.
[39]Li Y, Yuan Z, Liu B, et al. Prevention of hypoxia-induced neuronal apoptosis through histone deacetylase inhibition[J]. J Trauma, 2008,64(4):863-870. discussion 870-871.
[40]Bramlett H M, Dietrich W D. Progressive damage after brain and spinal cord injury: pathomechanisms and treatment strategies[J]. Prog Brain Res, 2007,161:125-141.
[41]Kadhim H J, Duchateau J, Sébire G. Cytokines and brain injury: invited review[J]. J Intensive Care Med, 2008,23(4):236-249.
[42]Faden A I, Demediuk P, Panter S S, et al. The role of excitatory amino acids and NMDA receptors in traumatic brain injury[J]. Science, 1989,244(4906):798-800.
[43]Zhang X, Chen Y, Jenkins L W, et al. Bench-to-bedside review: Apoptosis/programmed cell death triggered by traumatic brain injury[J]. Crit Care, 2005,9(1):66-75.
[44]Raghupathi R. Cell death mechanisms following traumatic brain injury[J]. Brain Pathol, 2004,14(2):215-222.
[45]Dash P K, Orsi S A, Zhang M, et al. Valproate administered after traumatic brain injury provides neuroprotection and improves cognitive function in rats[J]. PLoS One, 2010,5(6):e11383.
[46]Sinn D I, Kim S J, Chu K, et al. Valproic acid-mediated neuroprotection in intracerebral hemorrhage via histone deacetylase inhibition and transcriptional activation[J]. Neurobiol Dis, 2007,26(2):464-472.
[47]Meaney D F, Ross D T, Winkelstein B A, et al. Modification of the cortical impact model to produce axonal injury in the rat cerebral cortex[J]. J Neurotrauma, 1994,11(5):599-612.
[48]Biermann J, Grieshaber P, Goebel U, et al. Valproic acid-mediated neuroprotection and regeneration in injured retinal ganglion cells[J]. Invest Ophthalmol Vis Sci, 2010,51(1):526-534.
[49]Bredy T W, Wu H, Crego C, et al. Histone modifications around individual BDNF gene promoters in prefrontal cortex are associated with extinction of conditioned fear[J]. Learn Mem, 2007,14(4):268-276.
编辑 陈瑞芳
Neuroprotective mechanism of sodium valproate and its application
Liu Quanle1, Li Tianfu2, Wang Baoguo1*
(1.DepartmentofAnesthesiology,SanboBrainHospital,CapitalMedicalUniversity,Beijing100093,China; 2.DepartmentofNeurology,SanboBrainHospital,CapitalMedicalUniversity,Beijing100093,China)
As an inhibitor of histone deacetylases,sodium valproate is often used in the treatment of neuropsychiatric disorders such as antiepileptic treatment,schizophrenia and bipolar disorder. Sodium valproate can also affect the growth,mutation and apoptosis of neurons and play a neuroprotective effect. The mechanism of neuroprotection of sodium valproate is related to the regulation of neurotransmission and intracellular signaling pathways. Sodium valproate as a neuroprotective drug for the treatment of nerve injury and cognitive impairment remains to be further studied.
sodium valproate;neuroprotection;signal transduction;histone deacetylase inhibitor
国家自然科学基金(81571275)。This study was supported by National Natural Science Foundation of China(81571275).
时间:2017-06-09 17∶50 网络出版地址:http://kns.cnki.net/kcms/detail/11.3662.r.20170609.1750.052.html
10.3969/j.issn.1006-7795.2017.03.008]
R971+.6
2017-03-20)
*Corresponding author, E-mail:wbgttyy@163.com

