不同肝血流阻断方式手术治疗原发性肝癌的临床体会
胡军 鲁光锐 鲁玲 郑军
·论著·
不同肝血流阻断方式手术治疗原发性肝癌的临床体会
胡军 鲁光锐 鲁玲 郑军
目的 比较4种入肝血流阻断手术方式治疗原发性肝癌的手术疗效及对术后肝功能的影响,筛选术中最佳肝血流阻断方案。方法 原发性肝癌患者137例,根据入肝血流阻断方式分为第一肝门连续阻断组(A组)、降低中心静脉压的第一肝门连续阻断组(B组)、降低中心静脉的的第一肝门间歇性阻断组(C组)以及降低中心静脉压的半肝阻断组(D组),比较4组患者的手术时间、肝脏缺血时间、术中出血量、术中输血量、术后肝功能恢复情况和术后并发症发生率。结果 A组和B手术时间分别为(194.0±31.3)min和(182.7±36.7)min,二者比较,差异无统计学意义(P>0.05),但两组手术时间均少于C组和D组。B组术中出血最少,为(497.8±146.3)ml,少于其他3组(P<0.05)。在丙氨酸氨基转移酶(ALT)和总胆红素(TBIL)恢复方面,C组和D组术后1周基本恢复正常,均优于其余两组。而4种手术方式术中输血率以及术后并发症比较,差异均无统计学意义(P>0.05)。结论 手术治疗原发性肝癌术中首选降低中心静脉压的半肝阻断方式,该方法尽可能保留了健侧肝脏血流,减少术中出血,对于围手术期肝功能的保护非常有效。其他各种肝脏血流阻断方法可以根据其特点,结合患者及医院条件进行合理选择,以保证手术成功率及患者安全。
原发性肝癌; 血流阻断; 缺血再灌注损伤
肝脏血供丰富,手术切除过程中创面出血是影响手术效果及术后患者恢复的重要因素。从全肝阻断理念到半肝阻断,肝血流阻断技术得到不断改良,但血流阻断技术在减少出血的同时所引起正常肝组织的缺血再灌注损伤是影响患者术后恢复的另一因素。各种阻断技术治疗原发性肝癌的手术效果及对患者术后肝功能方面的影响报道不一[1-2]。我们对137例原发性肝癌患者分别采用第一肝门连续阻断、降低中心静脉压(CVP)的第一肝门连续阻断、降低CVP的第一肝门间歇性阻断和降低CVP的半肝血流阻断4种手术方式进行治疗,观察4种不同肝血流阻断方式的临床效果。现将结果报道如下。
对象与方法
一、对象
2008年1月~2014年12月收治的原发性肝癌患者137例。排除标准:行胆肠吻合术及胃肠手术等联合脏器手术,以其他肝血流阻断方式手术治疗的原发性肝癌,因肿瘤破裂出血入院后急诊手术或行经导管肝动脉化疗栓塞术(TACE)后再手术,多发转移瘤。依据肝血流阻断方式分为经第一肝门连续阻断(A组)、联合降低CVP的第一肝门连续阻断(B组)、联合降低CVP的第一肝门间歇性阻断(C组)和联合降低CVP的半肝血流阻断(D组)4组。其中,A组17例,男11例,女6例;B组21例,男13例,女8例;C组56例,男39例,女17例;D组43例,男28例,女15例。4组患者性别、年龄、肿瘤直径、术前肝功Child 分级、血红蛋白、凝血酶原时间、合并肝硬化率等比较,见表1。患者术前均经彩超、CT 和(或)MRI 检查。各组患者的肝切除范围见表2。各组患者年龄、性别、术前Child分级、血红蛋白、凝血酶原时间、肿瘤大小、合并肝硬化率及肝切除类型等比较差异无统计学意义(P>0.05)。所有患者术前给予3~7天的护肝及改善凝血功能等治疗。
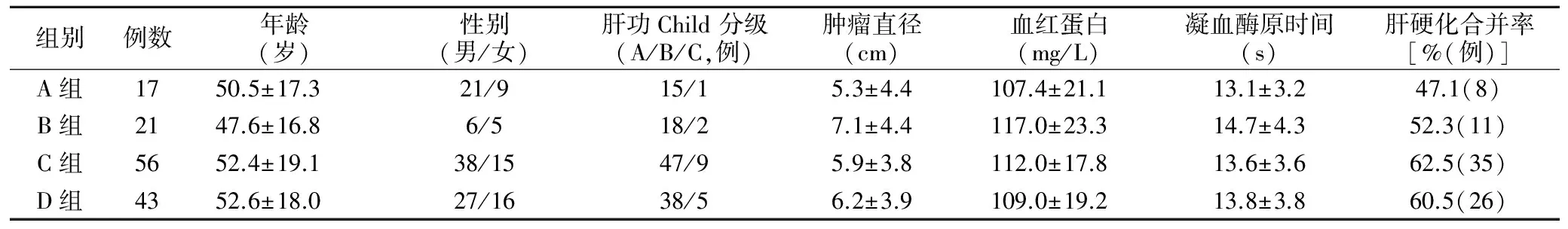
表1 患者基本情况比较

表2 患者肝切除范围比较(例)
二、方法
1.麻醉管理:4组患者均在全麻下手术。其中B组、C组、D组患者于麻醉后行右颈内静脉穿刺,置入双腔导管,其中一通路接换能器行连续CVP监测,另一通路用于输注液体,桡动脉穿刺连续测动脉血压。肝切除术过程中控制CVP在2~4 mmHg,收缩压>90 mmHg。术中快速查血红蛋白,低于80 g/L时即输注浓缩红细胞悬液,肿瘤切除并充分止血后,用晶体和胶体液恢复容量。
2.不同肝血流阻断方式 :A组:采用经典的Pringle法,以阻断带(乳胶管或8号导尿管)扎紧肝十二指肠韧带以阻断肝动脉及门静脉后行连续行操作,阻断时间控制在45分钟内。B组:以阻断带(乳胶管或8号导尿管)扎紧肝十二指肠韧带以阻断肝动脉及门静脉后降低CVP再行连续性操作,阻断时间控制在45分钟内。C组:以阻断带(乳胶管或8号导尿管)扎紧肝十二指肠韧带以阻断肝动脉及门静脉后降低CVP,手术操作过程中采取阻断入肝血流15分钟,复流5分钟的循环阻断方式,直至断肝完成,总阻断时间不超过60分钟。D组:在开腹探查腹腔及肝脏并判断无手术禁忌证后,在Glission鞘外分离肝蒂分叉部,用阻断带(乳胶管或8号导尿管)阻断患侧半肝的入肝血流,随后降低CVP,根据阻断后肝脏表面分界线行半肝切除术,总阻断时间不超过60分钟。 4组患者术中及术后均未使用防止缺血性损伤药物。
3.观察指标:记录4组患者的手术时间、肝脏缺血时间、术中出血量、术中输血量、术后肝功恢复情况以及术后并发症发生率。
三、统计学方法
应用SPSS 19.0 软件对数据进行分析,计数资料采用χ2检验,计量资料采用t检验。P<0.05为差异有统计学意义。
结 果
1.不同肝血流阻断技术对原发性肝癌患者手术效应的影响:A组、B组手术时间短于C组和D组,差异有统计学意义(P<0.05);B组术中出血量和术中输血量少于C组和D组,差异有统计学意义(P<0.05);余各组之间上述指标比较,差异无统计学意义(P>0.05)。术中肝脏阻断时间比较差异无统计学意义(P>0.05)。见表3。A组、B组、C组和D组患者的4组患者术中输血率分别为64.7%、61.9%、75.0%和67.4%,4组间比较,差异无统计学意义(P>0.05)。
2.不同肝血流阻断技术对原发性肝癌患者肝功能恢复的影响见表4。A组、B组术后肝功能恢复慢于C组和D组,差异有统计学意义(P<0.05)。其余各组间上述指标比较,差异无统计学意义(P>0.05)。

表3 各组患者术中指标比较
注:与C组和D组比较,aP<0.05,bP<0.05

表4 各组患者术前术后肝功能比较
注:与C组和D组比较,aP<0.05
3.不同肝血流阻断技术对原发性肝癌患者术后并发症的影响:4组术后并发症总体发生率比较,差异无统计学意义(P>0.05)。见表5。
讨 论
在肝切除手术过程中,如何控制术中出血以及减少缺血再灌注对肝细胞的损害,一直是研究的焦点。控制出血的肝切除术式应该术中血流阻断彻底,手术视野简洁清晰;同时操作简单、快捷、易学、易普及。为
减少肝脏缺血再灌注损伤,肝切除术中血流动力学应该稳定,术中安全性好,同时个性化差异契合性好;选择性甚至高选择性阻断拟被切除的肝叶或肝段,尽量保留健侧肝脏血流正常,从而尽可能保护残肝功能。降低CVP的半肝血流阻断是目前肝部分切除手术的首选方式,其优点表现在以下几个方面:(1)手术视野清晰,肝切线明了,增加了手术的便捷性,病损切除更为彻底;(2)术中血流动力学稳定,手术安全的同时不影响残肝血供,减小缺血再灌注损伤,有利于肝切除术后患者肝功能的恢复;(3)肠系膜血流可通过健侧肝脏回流至体循环,保证了胃肠道血流的通畅,避免了黏膜屏障受损及肠道菌群和内毒素的易位,使得术后患者肝功能恢复较快、减少并发症发生[1-4];(4)该方式尤其适用于术前肝功能较差或病灶局限于半肝内的原发性肝癌患者;(5)对其他脏器干扰较小。但因肝癌患者多合并肝硬化或不同程度的门静脉高压,肝门部解剖难度系数较高,对实行该方式的单位技术条件和手术医生熟练程度要求较高,基层医院难以推广普及。
第一肝门连续阻断因其具有解剖及阻断肝门简单及无需反复行阻断-放开循环等优点,使得手术时间较降低CVP的第一肝门间歇性阻断及降低CVP的半肝阻断用时少,但因其未降低CVP,未减少出肝静脉血液反流,使得术中出血量及术中输血量较其他各组并无明显优势,反而因长时间肝门阻断影响人体血流动力学的稳定,造成残肝缺血性损害及胃肠道淤血,从而影
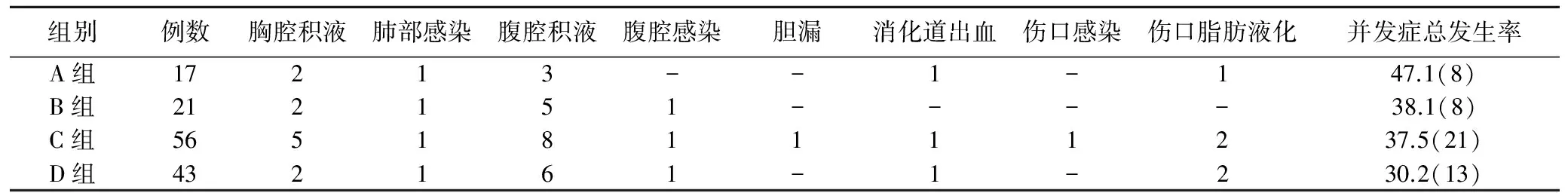
表5 各组患者术后并发症比较(例,%)
响患者术后肝功能恢复,尤其是对于肝脏本身存在基础病变的肝癌患者。有研究表明,因肝蒂阻断时间过长造成肠道血液回流不畅,引起肠道黏膜屏障损害和肠道细菌易位,引起全身内毒素血症,甚至引起急性肺损伤及胰腺功能损害等多个器官的功能不全[1-4]。有研究表明,因连续阻断第一肝门造成肝脏缺血再灌注损伤可能增加肿瘤转移的风险[5]。降低CVP的第一肝门连续性阻断在经典Pringl方法上改进了因出肝血液回流所致的创面出血,使得术中出血量进一步减少,术野清晰度增加,间接缩短了手术时间,但这种方式也未避免因缺血再灌注损伤对患者所造成的影响。除此之外,有研究表明,降低CVP的第一肝门连续阻断会增加气体栓塞的可能性[6-8]。本院实行这种方式的手术患者较少。降低CVP的间歇性第一肝门阻断较A、B两种方式需行反复阻断开放,延长了手术时间,但其减少了血流动力学不稳定因素,其优点是改善了缺血再灌注损伤对残肝所带来的不利影响,间歇阻断方式类似目前研究较多的肝脏缺血前处理和后处理的方法,以此尽量减轻氧自由基爆发对肝细胞的损伤。也有研究表明,反复阻断及开放入肝血流,可引起肝组织间隙压力的波动,导致肿瘤细胞的脱落,促进肿瘤细胞肝内转移,是原发性肝癌术后早期肝内复发的一项危险因素。以上3种方式各有利弊,本研究认为,在患者自身条件不佳,如合并严重肝硬化、门静脉高压、凝血机制障碍所造成解剖肝门困难的原发性肝癌患者,或机能状态较差术时不宜过长的原发性肝癌患者,以及本单位技术条件有限时,可根据实际情况,选择最适合患者的手术方式。
通过临床工作的总结,我们得到以下体会,应用联合序贯治疗,保证手术安全,减少术后并发症发生,促进术后肝功能恢复,这包括:(1)术前精确评估病情:术前选择恰当的方法评估肿瘤情况及肝功能的储备情况,其对手术方案的制定、术后风险的预防以及预后评估等具有重要意义[9]。(2)肝切除手术小组需密切配合,缩短手术时间,确保手术安全。(3)创面彻底快速止血,可酌情使用止血材料及器械[10]。
缺血预处理是预防缺血再损伤的有益探索,可使用药物或方式预见性减少肝脏缺血再灌注损伤。有研究表明,缺血预处理可缓解肝脏缺血-再灌注时血清肿瘤坏死因子(TNF-α)、高迁移率族蛋白1(HMGB1)的释放,减轻全身炎症反应,减轻肝脏缺血-再灌注损伤程度[11-12]。
微创是肝切除术中不断追求的理念,微创观念并不等同于小切口,而是着眼于降低患者在治疗过程中所受到的创伤的总和,自然也包括了小切口、愈合快、疗效佳。
解剖型肝切除因按照荷瘤肝段门静脉供应范围进行肝脏切除,可减少肿瘤早期门静脉分支播散的微转移灶,从而减少术后肿瘤复发[8,13]。
[1] Wijesurendere CN,Silva FH,Pathirana AA,et al.Pringle manoeuvre versus selective hepatic vascular exclusion:outcome of a case series in a tertiary referral centre[J].Ceylon Med J,2014,59(4):139-140.
[2] Sanjay P,Ong I,Bartlett A,et al.Meta-analysis of intermittent Pringle manoeuvre versus no Pringle manoeuvre in elective liver surgery[J].ANZ J Surg,2013,83(10):719-723.
[3] Si-Yuan FU,Yee LW,Li GG,et al.A prospective randomized controlled trial to compare Pringle maneuver,hemihepatic vascular inflow occlusion,and main portal vein inflow occlusion in partial hepatectomy[J].Am J Surg,2011,201(1):62-69.
[4] Furka A,Németh N,Pet K,et al.Data on liver enzyme and histological changes caused by intermittent clampings of the hepatoduodenal ligament in an experimental model.[J].Magyar Sebészet,2013,66(3):166-170.
[5] 郝胜华,杨湘武,杨文龙,等.间歇性肝门阻断是原发性肝癌术后早期肝内复发的一项危险因素[J].中华肝胆外科杂志,2013,19(5):321-324.
[6] Otsubo T.Control of the inflow and outflow system during liver resection[J].J Hepatobiliary Pancreat Sci,2012,19(1):15-18.
[7] 祁军安,江奎,朱海林,等.可控性低中心静脉压技术在肝切除术中的临床应用[J].肝胆胰外科杂志,2010,22(4):298-299.
[8] 黄志强.肝脏外科手术的难点[J].临床外科杂志,2010,18(1):1-2.
[9] 郭震,陈辉,钱群.肝癌术前肝脏储备功能评估的相关研究进展[J].临床外科杂志,2014,22(1):67-69.
[10]裴志强,程方贤,何毅明,等.肝癌切除术肝脏创面处理的体会[J].临床外科杂志,2011,19(1):64-65.
[11]Rodríguez A,Taurà P,Domingo M I G,et al.Hepatic cytoprotective effect ofischemic and anesthetic preconditioning before liver resection when using intermittent vascular inflow occlusion:A randomized clinical trial[J].Surgery,2015,157(2):249-259.
[12]李霞,龙小菊,胡衍辉,等.肢体远隔缺血预处理对肝脏手术中血清TNF-α和HMGB1水平的影响[J].临床麻醉学杂志,2015,31(12):1193-1195.
[13]Shindoh J,Mise Y,Satou S,et al.The intersegmental plane of the liver is not always flat--tricks for anatomical liver resection[J].Ann Surg,2010,251(5):917-922.
(本文编辑:杨泽平)
The clinical experience of different heaptic vascular exclusions in treatment of primary hepatocellular carcinoma patients
HUJun,LUGuangrui,LULing,etal.
(DepartmentofHepatopancreatobiliarySurgery,theFirstCollegeofClinicalMedicalScience,ChinaThreeGorgesUniversity,Yichang443003,China)
Objective To compare the effects of four kinds of heaptic vascular exclusions in treatment of primary hepatocellular carcinoma(HCC)and hepatic function,which was aimed to select the optimal treatment.Methods According to the different ways of hepatic vascular exclusions,137 hepatocellular carcinoma patients were divided into 4 groups,including the first hepatic hilum continuous exclusion group(group A),the first hepatic hilum continuous exclusion with low central venous pressure (LCVP)group(group B),the first hilum intermittent blockade with LCVP group(group C)and the semi-epatic vascular exclusion with LCVP group(group D).All data was collected and compared,incuding operative time,hepatic ischemia time,intraoperative blood loss,intraoperative blood transfusion volume,postoperative liver function recovery and postoperative complication rates.Results The operation time of group A and group B was(194.0±31.3)min and(182.7 ± 36.7)min,respectively,there was no significant difference between the two groups(P>0.05).While the operation time of the two groups wre less than the other groups(group C and D).The intraoperative blood loss of group B(497.8±146.3)ml was the least among the 4 groups.However,the group C and group D showed much better than group A and group B on the recovery of ALT and TBIL.There were no significant differences in the rate of blood transfusion and postoperative complication among 4 treatments(P>0.05).Conclusion The best way to treat patients with HCC is semi-epatic vascular exclusion with LCVP,this approach not only protects the contralateral hepatic blood flow,but also reduces intraoperative bleeding,it is conducive to the protection of liver function during perioperative period.According to the characteristics of other kinds of hepatic blood flow occlusion,we can choose the best treatment based on patients and hospital conditions,to ensure the success rates of surgery and patients safety.
primary hepatocellular carcinoma; vascular exclusion; ischemia-reperfusion injury
10.3969/j.issn.1005-6483.2017.03.009
443003 湖北省三峡大学第一临床医学院 宜昌市中心人民医院肝胆胰外科
郑军,Email:zhengjun1995@163.com
2016-11-02)

