(1-丁基-3,3-二苯基丙二烯基)二苯基氧膦的合成
陈 阳,孙 京,周明东
(辽宁石油化工大学 化学与材料科学学院,辽宁 抚顺 113001)
(1-丁基-3,3-二苯基丙二烯基)二苯基氧膦的合成
陈 阳,孙 京,周明东
(辽宁石油化工大学 化学与材料科学学院,辽宁 抚顺 113001)
报道了一种合成四取代二苯基膦氧类联烯化合物的方法。1,1-二苯基-2-庚炔-1-醇、二苯基氯化磷和无水三乙胺在无水四氢呋喃作为溶剂的体系中反应,以良好的收率得到目标产物(1-丁基-3,3-二苯基丙二烯基)二苯基氧膦。通过核磁共振(NMR)、红外光谱(FT-IR)、高分辨质谱(HRMS)等手段对目标产物的结构进行分析,确认目标产物的化学结构。
联烯; 膦氧化合物; 炔醇; 合成; 结构表征
联烯[1-10]是一类含有两个双键的累积烯烃,其本身具有独特的结构(见图1)[11]。在联烯化合物中,末端的两个碳sp2杂化轨道有剩下的未杂化p轨道,中间sp杂化的碳有两个互相垂直的p轨道,这两种p轨道相互交盖,从而形成两个相互垂直的π轨道。联烯的3个碳原子由于以上原因存在着不同的空间取向和电子云密度。联烯化合物能够连有不同的取代基团,但由于其取代基团具有不同的电子效应、立体效应或者是空间位阻效应等因素和性质,使得联烯化合物结构中的两个碳-碳双键具有不同的反应性能。同时,当联烯化合物中的两个sp2碳原子上的取代基连有不同的官能团时,联烯化合物表现出来的反应活性也不相同。
随着联烯化学的不断发展,其合成路线也越来越成熟。各种官能团化的联烯化合物合成方法也相继报道。但是,如何高效高收率地合成四取代联烯,到目前为止,还是一个比较困难的问题。本文提出了一种可以高效合成四取代联烯的简单方法,并以良好的收率得到目标产物。

图1 联烯独特的结构
1 实验部分
1.1 试剂及仪器
1-己炔、二苯甲酮、正丁基锂(2.5 mol/mL)、二苯基氯化膦、三乙胺、四氢呋喃,以上试剂均为分析纯,国药集团化学试剂有限公司。
AVANCE Ⅲ400型核磁共振仪1H-NMR,上海Bruker公司;AVATAR 360型红外光谱仪(FT-IR),美国Nicolet公司;APEXIII TME SI-FTI CRMS质谱仪HRMS,美国Bruker Daltonics公司。
反应中所加的溶剂需为无水溶剂,其处理方法如下:
①无水三乙胺:氩气保护,加入氢氧化钾回流,常压蒸出。
②无水四氢呋喃:氩气保护,钠丝存在下回流,以二苯甲酮为指示剂,溶液变蓝后蒸出。
1.2 实验方法
1.2.1 原料(1,1-二苯基-2-庚炔-1-醇)的合成 装有恒压滴液漏斗的250 mL的三口瓶,通过双排管对其进行抽换气操作3次,然后在氩气保护下,加入22 mmol的1-己炔(2.53 mL)和30 mL无水四氢呋喃,在恒压滴液漏斗中加入26.4 mmol的正丁基锂(10.56 mL),将整个反应装置放在-78 ℃的冷冻泵中搅拌30 min,滴加正丁基锂,滴加完毕后反应继续搅拌1 h,之后加入20 mmol的二苯甲酮(3.644 g),继续在-78oC搅拌,2 h之后将反应装置取出,室温下搅拌2 h。通过薄层色谱(TLC)监测反应,反应结束后,加水淬灭反应,用乙酸乙酯和饱和氯化钠溶液进行萃取,有机层用无水硫酸镁进行干燥,过滤,将滤液减压蒸馏去除溶剂,并利用硅胶柱层析(V(石油醚)/V(乙酸乙酯)=10∶1)将产品纯化,得到5.181 g产品,计算产物的分离收率。 反应方程式为:

1.2.2 目标产物(1-丁基-3,3-二苯基丙二烯基)二苯基氧膦的合成 装有恒压滴液漏斗的250 mL的三口瓶,通过双排管对其进行抽换气操作3次,然后在氩气保护下,加入10 mmol的1,1-二苯基-2-庚炔-1-醇(2.784 g)和30 mL无水四氢呋喃、14.4 mmol的无水三乙胺(2.0 mL),在恒压滴液漏斗中加入15 mmol的二苯基氯化膦(2.70 mL),将整个反应装置放在-78 ℃的冷冻泵中搅拌30 min,滴加二苯基氯化膦,滴加完毕后反应继续搅拌1 h,之后室温下搅拌1 h。通过TLC监测反应,反应结束后将沉淀物过滤,滤液减压蒸馏去除溶剂,并利用硅胶柱层析(V(石油醚)/V(乙酸乙酯)=1∶1)将产品纯化,得到3.787 g产品,计算产物的分离收率。反应方程式为:

2 原料及目标产物结构表征
2.1 原料的表征
原料的1H-NMR表征数据如下[12]:1H-NMR(400 MHz,CDCl3)δ7.59(d,J=7.2 Hz,4 H),7.32~7.21(m,6 H),2.83(s,1 H),2.33(t,J=7.2 Hz,2 H),1.59~1.53(m,2 H),1.48~1.39(m,2 H),0.92(t,J=7.2 Hz,3 H)。
图2为原料的核磁共振氢谱。

图2 原料的核磁共振氢谱
从图2中可以看出,化学位移为7.59处的双重峰和7.32~7.21处的重峰,归属于原料中苯环上的5个氢,化学位移为2.83处的单峰,归属于原料结构中的羟基氢,化学位移为2.33处的多重峰,归属于原料结构中正丁基官能团临近炔烃碳碳三键的碳上的两个氢,化学位移为1.59~1.53处和1.48~1.39处的多重峰,归属于原料结构中正丁基官能团中间两个碳上的4个氢,化学位移为0.917处的三重峰,归属于原料结构中正丁基官能团末端碳上的3个氢。
2.2 目标产物的表征
1H-NMR (400 MHz,CDCl3)δ7.68~7.59 (m,4 H),7.43 (t,J=6.8 Hz,2 H),7.35~7.24 (m,10 H),7.01~6.95 (m,4 H),2.49~2.40 (m,2 H),1.69~1.57 (m,2 H),1.38~1.25 (m,2 H),0.83 (t,J=7.4 Hz,3 H);13C-NMR (100 MHz,CDCl3)δ208.60 (d,JPC=6.1 Hz),135.10 (d,JPC=6.2 Hz),131.63 (d,JPC=103.5 Hz),131.61 (d,JPC=3.1 Hz),131.30 (d,JPC=9.9 Hz),128.20 (d,JPC=5.3 Hz),128.00,127.90 (d,JPC=3.1 Hz),127.50,112.50 (d,JPC=14.6 Hz),101.80 (d,JPC=98.0 Hz),30.40 (d,JPC=5.3 Hz),27.90 (d,JPC=6.1 Hz),22.20,13.60;31P-NMR (162 MHz,CDCl3)δ27.8; FT-IR(neat) 1 924、1 592、1 574、1 491、1 467、1 452、1 433 cm-1; HRMS (ESI) 计算为C31H30OP(M+H)+449.202 9,结果为 449.202 1。
2.2.1 核磁分析 图3为目标产物的核磁共振氢谱。
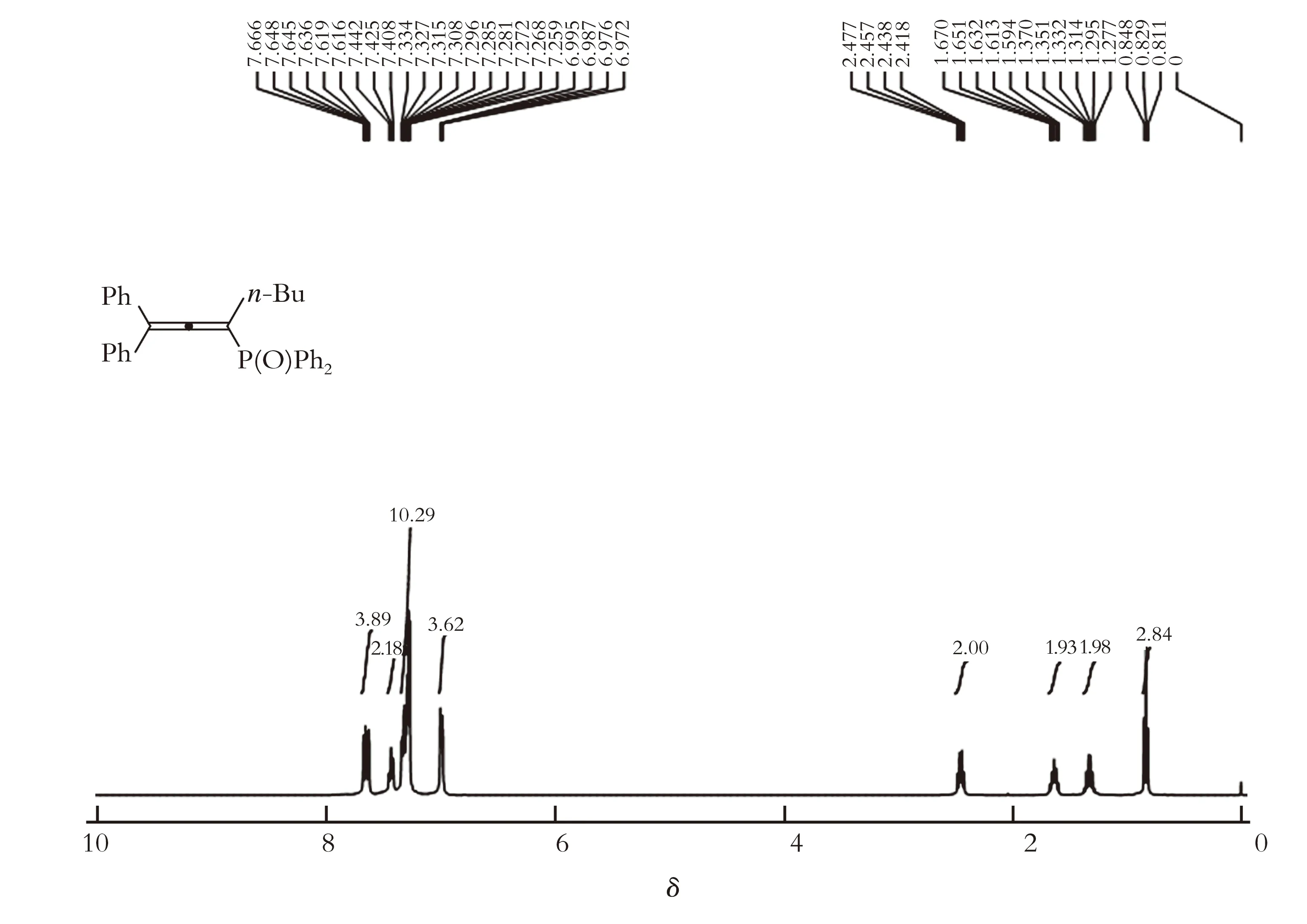
图3 目标产物的核磁共振氢谱
从图3中可以看出,化学位移为7.68~7.75处的多重峰、化学位移为7.43处的三重峰、化学位移为7.35~7.24处的多重峰和7.01~6.95处的多重峰,归属于目标产物结构中苯环上的20个氢,化学位移为2.49~2.40处的多重峰,归属于目标产物结构中正丁基官能团临近炔烃碳碳三键的碳上的两个氢,化学位移为1.69~1.57处和1.38~1.25处的多重峰,归属于目标产物结构中正丁基官能团中间两个碳上的4个氢,化学位移为0.917处的三重峰,归属于目标产物结构中正丁基官能团末端碳上的3个氢。
图4为目标产物的核磁共振碳谱。
由于目标产物的结构中含有磷元素,所以导致其碳谱中的峰会出现裂分的现象。从图4中可以看出,化学位移为208.60处有一个裂分峰,归属于联烯中间碳,和联烯化合物中间碳的峰出现在200左右处相吻合[13-15]。化学位移为135.10、131.63、131.61、131.30、128.20、127.90、127.50处均有一个裂分峰,化学位移为128.00处有一个单峰,以上8个峰归属于目标产物结构中苯环上的碳,因为产物结构中与联烯碳相连的两个苯环所处的化学环境相同,另外苯环具有对称性,所以在核磁共振碳谱中这两个苯环中的碳只会出现4个峰,而与磷相连的两个苯环由于同样的原因,在碳谱中也只会出现4个峰,这就解释了目标产物的核磁共振碳谱中只出现8个苯环碳的峰。化学位移为112.50和101.80处有一个裂分峰,这两处峰归属于目标产物结构中联烯的碳,由于化学位移为101.80处的峰耦合常数较大,所以此处裂分的峰归属于目标产物结构中与磷相连的联烯的碳。化学位移为30.4、27.9处均有一个裂分峰,化学位移为22.2、13.6处有一个单峰,这4处峰的化学位移都小于100,所以应归属于sp3类型碳,也就是目标产物结构中正丁基的4个碳。
图5为目标产物的核磁共振磷谱。

图4 目标产物的核磁共振碳谱

图5 目标产物的核磁共振磷谱
从图5中可以看出,化学位移为29.80处有一明显的单峰,归属于目标产物结构中的磷。
2.2.2 红外分析 图6为目标产物的红外谱图。

图6 目标产物的红外谱图
从图6中可以看出,1 924 cm-1处有一明显单峰,归属于目标产物结构中联烯的中间碳[13-15],1 592、1 574、1 491、1 467、1 452、1 433 cm-1处均有一个单峰,归属于目标产物结构中的苯环。
2.2.3 质谱分析 图7为目标产物的质谱谱图。

图7 目标产物的质谱谱图
从图7中可以看出,高分辨质谱中产物的相对分子质量为449.202 1,与目标产物的理论相对分子质量449.202 9相吻合,可以确定目标产物的相对分子质量。
3 结 论
发现了一种由1,1-二苯基-2-庚炔-1-醇、二苯基氯化膦、无水三乙胺在无水四氢呋喃作为溶剂的体系中以良好的收率合成四取代的联烯目标产物 (1-丁基-3,3-二苯基丙二烯基)二苯基氧膦的方法,同时通过核磁共振、红外光谱和高分辨质谱等手段确认了目标产物的结构。
[2] Bras J L,Muzret J.Palladium-catalysed inter-and intramolecular formation of C—O bonds from allenes[J].Chemical Society Reviews,2014,43(9):3003-3040.
[3] Tius M A.Allene ether nazarov cyclization[J].Chemical Society Reviews,2014,43(9):2979-3002.
[4] Yang W,Hashmi A S K.Mechanistic insights into the gold chemistry of allenes[J].Chemical Society Reviews,2014,43(9):2941-2955.
[6] Ye J,Ma S.Palladium-catalyzed cyclization reactions of allenes in the presence ofunsaturated carbon—carbon bonds[J].Accounts of Chemical Research,2014,47(4):989-1000.
[7] Krause N,Winter C.Gold-catalyzed nucleophilic cyclization of functionalized allenes:a powerful access to carbo-and heterocycles[J].Chemical Reviews,2011,111(3):1994-2009.
[8] Micalizio G C,Hale S B.Reaction design,discovery,and development as a foundation to function-oriented synthesis[J].Accounts of Chemical Research,2015,48(3):663-673.
[9] Kammerer C,Prestat G,Madec D,et al.Synthesis of γ-lactams and γ-lactones via intramolecular Pd-catalyzed allylic alkylations[J].Accounts of Chemical Research,2014,47(12):3439-3447.
[10] Neff R K,Frantz D E.Recent applications of chiral allenes in axial-to-central chirality transfer reactions[J].Tetrahedron,2015,71(1):7-18.
[11] 郭浩.联烯的一些加成反应研究[D].上海:中国科学院上海有机化学研究所,2008.
[12] Zhang X,Teo W T,Chan P W H.Ytterbium(III) triflate catalyzed tandem friedel-crafts alkylation/hydroarylation of propargylic alcohols with phenols as an expedient route to indenols[J].Organic Letters,2009,11(21):4990-4993.
[13] Guo H,Qian R,Guo Y,et al.Neighboring group participation of phosphine oxide functionality in the highly regio-and stereoselective iodohydroxylation of 1,2-allenylic diphenyl phosphine oxides[J].Journal of Organic Chemistry,2008,73(20):7934-7938.
[14] He G,Guo H,Qian R,et al.Studies on highly regio-and stereoselective selenohydroxylation reaction of 1,2-allenyl phosphine oxides with PhSeCl[J].Tetrahedron,2009,65(25):4877-4889.
[15] He G,Fu C,Ma S.Studies on highly regio-and stereoselective fluorohydroxylation reaction of 3-aryl-1,2-allenyl phosphine oxides with Selectfluor[J].Tetrahedron,2009,65(25):8035-8042.
(编辑 宋官龙)
Synthesis of 1,1-Diphenylhepta- 1,2-dien-3-yl Diphenyl Phosphine Oxide Compound
Chen Yang, Sun Jing, Zhou Mingdong
(CollegeofChemistryandMaterialScience,LiaoningShihuaUniversity,FushunLiaoning113001,China)
This article reported the method about the synthesis of a four-substituted diphenyl phosphine oxide type allene compounds. In the solvent system of anhydrous triethylamine, 1,1-diphenylhept-2-yn-1-ol reacted with chlorodiphenylphosphine in anhydrous tetrahydrofuran, it got the desired product (1,1-diphenylhepta-1,2-dien-3-yl diphenyl phosphine oxide compound) in good yield. The structure was analyzed by NMR, IR, HRMS to confirme the structures of the desired product.
Allene; Phosphine oxides; Acetylenic alcohols; Synthesis; Structural characterization
1672-6952(2017)03-0006-05 投稿网址:http://journal.lnpu.edu.cn
2016-05-03
2016-05-11
辽宁省自然科学基金项目“酸功能化离子液体在芳烃酰基化反应中的应用” (2015020196)。
陈阳(1989-),男,硕士研究生,从事有机合成化学研究;E-mail:544199578@qq.com。
周明东(1980-),女,博士,教授,从事分子催化与有机合成化学的研究;E-mail:mingdong.zhou@hotmail.com。
O621.3
A
10.3969/j.issn.1672-6952.2017.03.002

