利用铝厂污泥制备钛酸铝材料的热分解研究
沈阳
摘要: 在铝厂污泥和工业TiO2合成出的良好稳定性的钛酸铝材料基础上,探讨钛酸铝在750~1300℃温度范围内的热分解行为,为抑制钛酸铝的分解,合成高纯度钛酸铝材料,采取必要的措施提供动力学基础数据。采用XRD表征各试样的晶相结构;用Rietveld Quantification 法确定各试样中各晶相的含量。实验结果:不同分解温度下各试样均形成三个晶相:钛酸铝Al2TiO5、TiO2和Al2O3,其中钛酸铝Al2TiO5是主晶相;不同温度分解速率大小顺序为:1100℃>1200℃>1000℃>900℃;从扩散为控制步骤的动力学研究结果,开始阶段属于扩散为控制步骤,分解超过一定时间属非扩散为控制步骤。
Abstract: In this paper, the decomposition behavior of aluminum titanate from aluminum waste-residue and industrial TiO2 within the temperature range of 750~1300℃ was mainly discussed, which help us to obtain the high-purity product and to suppress the decomposition of aluminum titanate in theory. The crystalline phase structure of each sample were characterized with XRD methods; The content of each crystalline phase in each sample was confirmed with Rietveld Quantification method; The experimental results showed: There are three crystalline phases in each sample, corresponding to Al2TiO5,Al2O3 and TiO2 respectively; The order of the decomposition rates is 1100℃>1200℃>1000℃>900℃; Diffusion velocity is far less than Chemistry reaction velocity within the reaction interface at first, thus it is diffusion velocity that control the reaction process,but late it is not.
关键词: 铝厂污泥;钛酸铝;热稳定性;分解度
Key words: aluminum waste-residue;aluminium titanate;thermal instable;decomposition ratio
中图分类号:TB332 文献标识码:A 文章编号:1006-4311(2017)16-0242-04
0 引言
钛酸铝(Al2TiO5简称AT)是一种新型结构材料,具有高熔点和很低的膨胀系数,因此具有优良的抗热震性,可在剧烈的急冷急热条件下使用,广泛地应用于测温热电偶保护套、冶金工业用水口、过滤器、坩埚、通气管、汽车发动机排气管及汽车尾气净化处理用蜂窝状催化剂载体。通常钛酸铝合成方法基本都是利用工业Al2O3或Al(OH)3和工业钛白粉或使用相应的化学试剂,以传统烧结方法制备。但由于工业Al2O3成本较高,导致合成钛酸铝材料的成本较高。铝厂污泥中含有大量无定形体结构的γ-AlOOH形式存在,在高温下(1100℃以上)烧结会转变成α-Al2O3,其粒径约在0.1-1μm之间,活性高,企业通常做法是将其当成废渣直接排放,这样不仅造成资源的严重浪费,而且还会对环境造成污染。如若充分利用铝厂污泥中的Al2O3合成制备钛酸铝材料[1-4],不仅是含铝原料的最佳替代品,而且能降低原料成本,减少企业对环境的污染和资源的浪费。本论文正是上面思想指导的基础上,利用铝厂污泥和工业用TiO2,合成出具有良好稳定性的钛酸铝材料。在此基础上探讨钛酸铝在750~1300℃温度范围内的热分解行为[5-8],通过对其热分解率的分析讨论,使我们对钛酸铝的分解本质有更深一步的了解,为抑制钛酸铝的分解,采取必要的措施提供动力学基础数据,有助于指导我们材料工作者合成出高纯和稳定的钛酸铝材料。
1 实验
合成原料为铝型材厂污泥和TiO2,其中污泥化学组成(wt%):Al2O3 61.16%、 SiO2 2.34%、 Fe2O3 0.27%、 CaO 0.48%、MgO 0.37%、K2O 0.03%、Na2O 1.34%、L.O.I 34.26%。钛酸铝(Al2TiO5)理论质量百分比Al2O3/TiO2=1.27。根据钛酸铝理论化学组成配料,烧制成的钛酸铝试样(含量为90%),以已该烧制成的钛酸铝试样为基础,分別探讨试样在900℃,1000℃,1100℃,1200℃的热分解行为。将试样置于高温炉中,固定一个分解温度,分别保温3h,6h,9h,12h,15h,18h进行分解实验,分解产物应在分解温度时立即投入水中淬冷,低温下保持着高温状态,淬冷后产物经脱水烘干。
采用Philips Xpert-MPD型X射线衍射仪分析确定各分解试样形成的晶相,分析条件:Cu靶(Kα),管电压35KV,管电流20mA;用Rietveld Quantification软件计算确定各试样中各晶相的含量;根据分解数据计算钛酸铝材料的分解率。
2 实验结果与分析
2.1 晶相分析和分解率计算
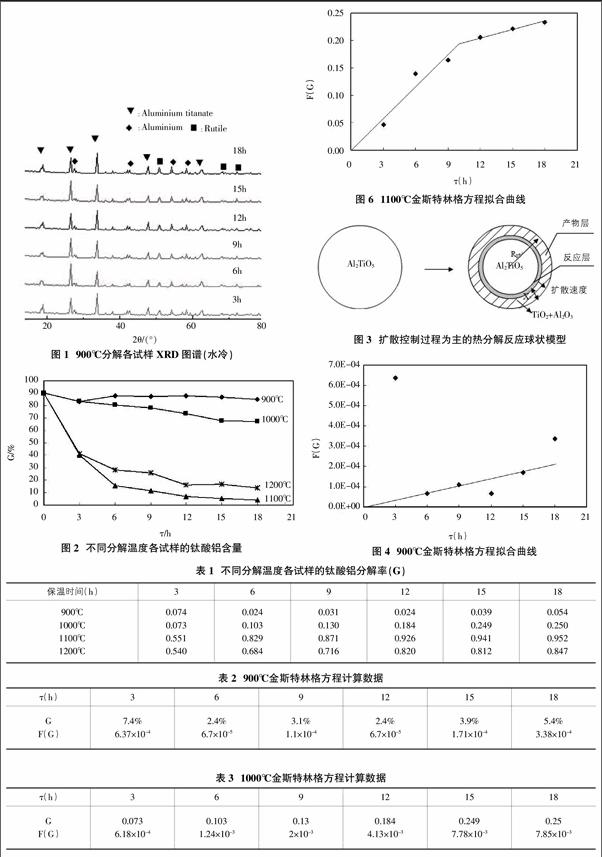
分解实验的各试样经XRD分析,分析数据采用Origin软件画出不同分解温度各试样对比衍射谱图,图1是900℃分解各试样的XRD谱图,根据图谱定性分析结果,各试样形成三个晶相:Al2TiO5、Al2O3、TiO2,其中Al2TiO5是主晶相,图中分别标注Al2TiO5、Al2O3、TiO2几条最强的衍射峰,用▼、■和◆表示;1000℃,1100℃,1200℃都有相似的衍射谱图,由于编幅的限制,尚未将三者衍射谱图列出。采用Rietveld Quantification法确定各分解温度下各晶相的含量,其中分别将不同分解温度各试样的钛酸铝含量以图2中的曲线表示。
在900℃,1000℃,1100℃,1200℃都存在钛酸铝晶体的分解和从玻璃相中析出钛酸铝晶体的过程,由于温度处在750~1300℃钛酸铝理论分解范围内。分解速度与温度有关,温度低分解产物的扩散速度慢,引起分解速度低,温度升高分解速度加快,分解速率提高;其中1100℃分解速率最高,3 h后钛酸铝晶体的含量从90%下降至40.4%,分解率为55.11%; 1200℃已达到Al2O3与TiO2反应形成Al2TiO5的温度,Al2TiO5的分解同时,有少量分解产生的Al2O3与Ti O2重新又反应形成Al2TiO5,使得1200℃分解速率反而比1100℃低;不同溫度分解速率大小顺序为:1100℃>1200℃>1000℃>900℃,在图2中可明显加于比较。
2.2 扩散控制AT分解过程的机理讨论
根据图2中的钛酸铝含量可以计算各试样钛酸铝分解率,设分解率为G,分解率G=[(W0-Wi)/ W0 ]×100%,式中W0、Wi分别代表分解时间为0小时和i小时试样的钛酸铝含量,将图2数据分别代入式中,计算出不同温度下分解3h,6h,9h,12h,15h,18h的分解率Gi,列于表1中。假设钛酸铝(AT)颗粒为球状的,分解反应可用球状模型加以解释,扩散控制模型如图3。化学反应速率>>扩散速率(KC0>>DC0/?啄),反应阻力主要来源于扩散速率,该固相反应属扩散动力学范围。
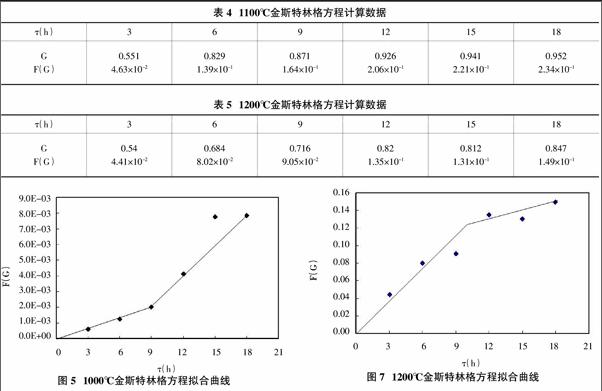
基于固相反应属扩散动力学范围,固可将分解温度为900℃、1000℃、1100℃、1200℃,分解时间分别为3-18 h各试样的G值代入金斯特林格方程F(G)=1-2G/3-(1-G)2/3=Kt中进行拟合,计算出方程的F(G)值列于表2、3、4、5中,以分解时间为横坐标,以F(G)值为纵坐标画出动力学方程的曲线,如图4、5、6、7所示。
钛酸铝的分解反应过程,涉及到二个重要的过程:钛酸铝在界面上进行分解反应,分解产物从界面向产物层扩散,其中之一必是控制步骤;若满足金斯特林格方程,则该过程属于扩散为控制步骤,属于稳定扩散;不满足金斯特林格方程,属于化学反应或其他为控制步骤的过程。
从图4~7可以看出,900℃时,其F(G)与τ成线性(通过原点)关系,符合金斯特林格方程,分解反应过程以扩散为控制步骤。1000℃的分解反应,其F(G)与τ形成关系在0-9 h内可近似为通过原点的直线,符合金斯特林格方程,分解反应时间大于9小时,直线不通过原点,不符合金斯特林格方程,所以开始阶段属于扩散为控制步骤,分解反应一定时间后,钛酸铝材料内部由于钛酸铝晶体分解加快,晶体晶型发生转变,液相含量的增加等过程,使分解反应动力学方程偏离金斯特林格方程,因此此时属于化学反应或其他为控制步骤的过程。
同样,1100℃和1200℃时,其分解反应的其F(G)与τ形成关系在0-10.5h内可近似为通过原点的直线,符合金斯特林格方程,分解反应时间大于10.5小时,其直线不通过原点,不符合金斯特林格方程,在此期间,由于温度的升高以及钛酸铝已大量分解,导致晶格松散,结构内部缺陷增多,其扩散和反应能力加强,所以此时扩散已不成为分解反应的主要控制步骤,此阶段属于化学反应或其他为控制步骤的过程。
因此反应开始时,可以用金斯特林格方程表征分解反应动力学过程,随着时间的加长需要再进一步的讨论AT热分解反应的机理,找到更精确的表征分解反应动力学的模型。
3 结论
①XRD分析表明各分解温度下试样形成Al2TiO5、Al2O3和TiO2三个晶相,其中Al2TiO5是主晶相。在900℃存在钛酸铝晶体的分解的过程;不同温度分解速率大小顺序为:1100℃>1200℃>1000℃>900℃。
②从扩散为控制步骤的动力学研究结果,开始阶段属于扩散为控制步骤,动力学方程符合金斯特林格方程;分解超过一定时间属非扩散为控制步骤。
参考文献:
[1]Y. Shen, Y. Z. Ruan et al. Key Engineering Materials, 2008, 368-72: 1538-40.
[2]Y. Shen, Y. Z. Ruan et al. Chinese J. Struct. Chem. 2009, 28(1):61-66.
[3]Y. Shen, Y. Z. Ruan et al. Chinese J. Struct. Chem. 2009, 28(2):228-234.
[4]Y. Shen, Y. Z. Ruan et al. Chinese J. Struct. Chem. 2009, 28(3).
[5]Xu G. ; Han G. R. Materials review, 2003, 17: 44-47.
[6]Parker F. J. J. Am. Ceram. Soc., 1990, 73: 929-932.
[7]Liu T. S.; Perera D. S. J. Mater. Sci., 1998, 33: 995-958.
[8]Djambazov S.; LePkova D. J. Mater. Sci., 1994, 29: 2521.

