微波加热法所制Ag/Cu双金属纳米粒子的表征及其抗菌性能分析
李培义,宋述鹏,王今朝,张远卓,万 天
(1. 武汉科技大学省部共建耐火材料与冶金国家重点实验室,湖北 武汉,430081;2. 武汉科技大学材料与冶金学院,湖北 武汉,430081;3. 湖北大学材料科学与工程学院,湖北 武汉,430062)
微波加热法所制Ag/Cu双金属纳米粒子的表征及其抗菌性能分析
李培义1,2,宋述鹏1,2,王今朝3,张远卓2,万 天2
(1. 武汉科技大学省部共建耐火材料与冶金国家重点实验室,湖北 武汉,430081;2. 武汉科技大学材料与冶金学院,湖北 武汉,430081;3. 湖北大学材料科学与工程学院,湖北 武汉,430062)
以AgNO3和Cu(CH3COO)2·H2O为前驱体,PVP为分散剂,分别以乙醇和乙二醇为还原剂,采用微波加热法制备Ag/Cu双金属纳米粒子,利用XRD、TEM、XPS等技术对其进行表征,并分析反应温度、n(Ag+)∶n(Cu2+)等因素对Ag/Cu双金属纳米粒子微观形貌及抗菌性能的影响。结果表明,以乙二醇为还原剂,当反应温度为169 ℃、n(Ag+)∶n(Cu2+)为4∶1时,所制Ag/Cu双金属纳米粒子粒径小且分散均匀,粒子粒径在20~60 nm范围内,并呈现出各种多面体结构,其对大肠杆菌具有良好的抗菌效果。
Ag/Cu;双金属;纳米粒子;醇还原;微波加热;抗菌性能
纳米级粒子由于具有独特的物理、化学和生物性质,已成为材料研究的热点之一,而由不同金属组成的双金属合金纳米颗粒更是备受关注[1]。双金属是将两种金属材料在纳米尺度上进行复合,形成核壳、空心等结构的纳米粒子,能提高材料的物理化学性能。双金属纳米材料可应用于催化、抗菌、电化学传感器、水处理、生物传感等诸多领域[2]。双金属纳米材料的制备方法主要有置换法[3]、激光烧蚀法[4]、化学还原法[5]、多元醇法[6]、水热法、微波法[7]、化学气相沉积法[8]、胶体晶种法等,不同方法合成的双金属纳米材料具有不同的微观形貌和物理化学性能[9]。
微波加热与传统加热方式相比具有独特的优势,微波加热是通过被加热物体内部偶极分子高频往复运动,产生“内摩擦热”而使被加热物质温度升高,不需任何热传导过程,就能使物料内外部同时加热、同时升温,不存在温度梯度,加热速度快且均匀,而且能耗仅需传统加热方式的几分之一甚至几十分之一[10]。徐伟等[11]采用微波加热法,数分钟内制备出平均粒径在50 nm左右且分散均匀的球状纳米镍。Wang等[12]采用多元醇还原法,制备出平均粒径小于3 nm,具有核壳结构的Pt/Pd双金属纳米颗粒,其催化活性远远高于Pt、Pd单金属纳米颗粒。为此,本文以AgNO3和Cu(CH3COO)2·H2O为前驱体,PVP为分散剂,分别以乙醇和乙二醇为还原剂,采用微波加热法制备Ag/Cu双金属纳米粒子,利用XRD、TEM、XPS等技术对其进行表征,并分析反应温度、n(Ag+)∶n(Cu2+)等因素对Ag/Cu双金属纳米粒子微观形貌及抗菌性能的影响,以期为新型双金属纳米材料的制备提供参考。
1 试验
1.1 试剂及仪器
主要试剂有硝酸银(AgNO3,99.8%)、一水合乙酸铜(Cu(CH3COO)2·H2O,99.0%)、无水乙醇(CH3COOH,99.0%)、乙二醇(C2H6O2,99.0%),以上均为分析纯。聚乙烯吡咯烷酮(PVP,Mw = 30000)为国产优级纯试剂,试验用水均为二次去离子水。
主要仪器有WBFY-201型微波化学反应器、H1850型台式高速离心机、CJJ79-1磁力加热搅拌器、KX-1730QT超声波清洗机。
1.2 试样制备与表征
Ag/Cu双金属纳米粒子试样制备方案如表1所示。首先,配置浓度为12 mmol/L(或48 mmol/L)硝酸银的醇溶液,向其中加入一定量的PVP分散剂,磁力搅拌至完全溶解后,将溶液放入微波反应器中,在500 W功率下反应2 min,制得纳米银溶胶。然后将浓度为12 mmol/L醋酸铜的醇溶液分别与上述制得的纳米银溶胶混合,置于微波反应器中,在500 W功率下反应3 min,自然冷却至室温,得到银铜双金属纳米溶胶。再将所制银铜双金属纳米溶胶以13000 r/min转速离心15 min,倒掉上层清液后,将沉淀物置于无水乙醇和丙酮的混合液中,超声分散15 min,再以13000 r/min转速离心15 min,收集沉淀物。重复上述离心过程两次,将最终沉淀物真空干燥后分散到去离子水中,配制成不同浓度的纳米溶胶。最后将纳米溶胶超声分散后滴在碳微栅支持膜上,室温干燥,使用FEI Tecnai G20型透射电镜(TEM)对试样进行组织形貌观察和选区电子衍射分析,用XRD、XPS、UV-Vis等技术对所制银铜双金属纳米粒子进行表征。
表1 Ag/Cu双金属纳米粒子试样制备方案
Table 1 Preparation scheme of Ag/Cu bimetallic nanoparticle samples

试样n(Ag+)∶n(Cu2+)反应温度/℃溶剂和还原剂1#1∶178乙醇2#1∶1169乙二醇3#4∶1169乙二醇
1.3 Ag/Cu双金属纳米材料抗菌性能测试
采用肉汤稀释法对Ag/Cu双金属纳米粒子试样进行最小抑菌浓度(MIC)的测定,并用滤纸片法测试Ag/Cu双金属纳米材料的抗菌性能。首先,采用稀释平板计数法,将大肠杆菌的浓度稀释到1×107cfu/mL数量级,并均匀涂布在LB固体培养基上,然后将不同浓度的溶胶接种到培养基上,在37 ℃恒温下培养24 h后,观察培养基中菌落生长情况,以不形成菌落的最低溶胶浓度作为试样的最小抑菌浓度(MIC)值。最后将直径为6 mm浸有Ag/Cu双金属纳米溶胶的小圆纸片点入接种有大肠杆菌的培养基中,在37 ℃恒温下培养24 h后,观察滤纸片周围抑菌环的大小。
2 结果与分析
2.1 XRD分析
图1为3种Ag/Cu双金属纳米粒子试样的XRD谱图。从图1中可以看出,在2θ为38.26°、44.38°、64.67°和77.54°处出现的衍射峰分别对应面心立方Ag的(111)、(200)、(220)、(311)晶面;在2θ为43.55°、50.57°、74.23°处出现的衍射峰分别对应面心立方Cu的(111)、(200)、(220)晶面,由此可见,2#、3#试样主要成分是单质Ag和单质Cu,而1#试样中只有单质Ag,没有单质Cu生成。从图1中还可看出,1#、2#、3#试样中均未出现明显的杂峰,表明Ag/Cu双金属纳米材料中没有CuO、Cu2O等杂质。铜纳米粒子在常温下极易被氧化,而所制Ag/Cu双金属纳米粒子却未被氧化,这是因为,在银和铜的团簇中,活性较高的铜原子被银原子取代,改变了团簇中原有的电子状态与几何构型,使团簇对氧分子发生化学吸附的活化能升高,从而导致其团簇抗氧化性能的提高[13]。

图1 3种Ag/Cu双金属纳米粒子试样的XRD谱图
Fig.1 XRD patterns of three Ag/Cu bimetallic nanoparticle samples
2.2 TEM分析
图2依次为3种Ag/Cu双金属纳米粒子试样的TEM照片和粒径分布图。从图2中可以看出,1#试样的纳米粒子粒径范围为30~120 nm,呈现出不规则的片状三角形、六边形及十面体等多面体形状,且纳米粒子没有明显的团聚现象;2#试样的纳米粒子粒径范围为20~100 nm,粒子形状主要是棒状、三角片状和球状,分散均匀;3#试样的纳米粒子以片状三角形、球形、短棒状、十面体以及其它多面体形状存在,分散均匀,纳米粒子的粒径范围为20~60 nm。由此可见,与1#、2#试样相比,3#试样中纳米粒子有较小的粒径分布和较规则的形状,且分散更加均匀,这可能是因为3#试样在制备过程中,体系中的Ag+含量和反应温度相对较高,反应过程中形成Ag晶核的数量多且成核速率快,更易形成分散的、粒径较小的纳米粒子。

(a)

(b)

(c)
图2 3种Ag/Cu双金属纳米粒子试样的TEM照片和粒径分布图
Fig.2 TEM images and particle size distributions of three Ag/Cu bimetallic nanoparticle samples
图3为3种Ag/Cu双金属纳米粒子试样的选区电子衍射照片。从图3中可以看出,1#试样呈现单个纳米银颗粒的选区电子衍射花样,2#、3#试样呈现多晶环选区电子衍射花样,每个衍射环照片中箭头所示分别对应面心立方Ag和面心立方Cu的不同晶面。从图3中还可看出,2#试样的衍射环有较明显的弥散现象,3#试样的衍射环基本无弥散,表明3#试样较2#试样纳米粒子的平均粒径更小且结晶效果更好。

(a) 1#

(b) 2#

(c) 3#
图3 3种Ag/Cu双金属纳米粒子试样的选区电子衍射照片
Fig.3 Electron diffraction patterns on selected areas of three Ag/Cu bimetallic nanoparticle samples
2.3 紫外可见光谱分析
图4为3种Ag/Cu双金属纳米粒子试样的紫外可见光谱图。从图4中可以看出,1#试样中只有在波长为400 nm附近出现银的吸收峰,而2#、3#试样在波长为400、600 nm附近分别出现银和铜的吸收峰,表明1#试样中只有银纳米粒子,2#、3#试样中不仅有银纳米粒子,还有铜纳米粒子。比较三条曲线峰的形状和位置可以发现,3#试样银的半峰宽最小,表明3#试样中粒子的粒径分布范围更小;3#试样中银峰的位置相对其它两条曲线发生了蓝移并在360 nm处有一个峰肩,表明3#试样中粒子分散更均匀,粒子形状更加多样化。
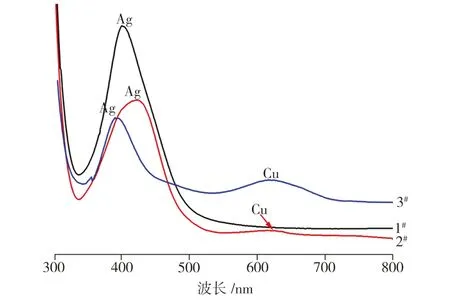
图4 3种Ag/Cu双金属纳米粒子试样的紫外可见光谱图
Fig.4 UV-Vis patterns of three Ag/Cu bimetallic nanoparticle samples
2.4 XPS分析
图5为Ag/Cu双金属纳米粒子的XPS谱图。从图5(a)中可以看出,在结合能为367.8、373.8 eV处出现两个峰,两峰间距为6.0 eV,对这两个峰进行分峰拟合后,在结合能为368.2、374.2 eV处出现的峰分别对应Ag 3d3/2和Ag 3d5/2的光电子峰,其它两个分峰是Ag2O的光电子峰。从图5(b)中可以看出,在结合能为932.6、952.2 eV处出现的峰分别对应Cu 2p3/2和Cu 2p1/2的光电子峰,其它峰分别是CuO和Cu2O的光电子峰。由此可见,试样中有单质Ag、单质Cu、Ag2O、Cu2O和CuO,而图1中的XRD图谱显示试样中只有单质Ag和单质Cu,这可能是由于试样在干燥过程中表面被部分氧化生成Ag2O、Cu2O和CuO所致。

(a) Ag

(b) Cu
微波加热醇还原法制备Ag/Cu双金属纳米粒子的反应方程式为:

(1)

(2)

(3)

(4)

(5)
醇在高温下发生热分解反应,释放出有机自由基和自由电子,此时溶液中的银离子和铜离子得到电子,被还原成单质银或铜。Cu2+/Cu0对的标准氧化还原电位(+0.34 eV)低于Ag+/Ag0对的标准氧化还原电位(+0.78 eV),因此,Cu2+的还原比Ag+缓慢。同时,银离子与单质铜发生置换反应生成单质银,而纳米银的存在又能促进铜离子吸附在其表面并得到电子,被还原成单质铜,从而推动整个反应进一步进行,最终生成Ag/Cu双金属纳米粒子[14]。
2.5 Ag/Cu双金属纳米材料抗菌性能分析
表2为Ag/Cu双金属纳米溶胶试样的MIC测定结果。其中,对不加纳米溶胶的菌悬液进行培养作为阳性对照,阴性对照则只加纳米溶胶而不加菌悬液。从表2中可以看出,1#试样MIC值为64 μg/mL,2#、3#试样的MIC值均为32 μg/mL,由此表明,2#、3#试样对大肠杆菌的抑菌效果比1#试样好。

表2 3种Ag/Cu双金属纳米溶胶试样的MIC测定结果
注:“-”表示无菌生长,“+”表示有菌生长。
图6为Ag/Cu双金属纳米材料对大肠杆菌的抑菌效果图片。从图6中可以看出,1#、2#、3#试样都出现了大小不同的抑菌环,并且抑菌环直径越大,表明其抑菌效果越明显,这是因为,具有极大比表面积的纳米尺度的粒子,其表面原子具有很高的活性而极不稳定[15],而Ag/Cu纳米材料可以释放出有较高氧化还原电位的Ag+和Cu2+,这些离子与带负电的细胞壁通过库仑引力紧密结合,并与膜蛋白结合使细菌结构发生变化,导致细菌死亡。结合图2中的TEM照片,可知本试验的抑菌效果与Ag/Cu双金属纳米粒子的粒径大小、形状和分散程度均有关,粒子粒径越小、形状越规则、分散越均匀以及比表面积越大,则其抗菌性能越好。另外,Ag+还可以进入菌体内,取代氧代谢酶(—SH)中的H+,形成大量稳定的—SAg基团,影响菌体内蛋白质的活性和DNA的复制,从而使细胞丧失分裂增殖能力而死亡[16]。2#、3#试样抑菌环直径比1#试样的大,这是由于纳米铜粒子也具有抗菌性,且与纳米银粒子产生协同抗菌作用,使Ag/Cu双金属纳米粒子比单金属纳米粒子具有更加优异的抗菌性能。对比图6(c)和图6(d)可知,当n(Ag+)∶n(Cu2+)为4∶1时,所制Ag/Cu双金属纳米材料的抗菌性能较n(Ag+)∶n(Cu2+)为1∶1时所制材料强,由此表明,在制备Ag/Cu双金属纳米材料时,适当增加银离子的摩尔浓度,可以使双金属纳米材料的抗菌性能增强。

(a) 未加纳米溶胶 (b)1#(c)2#(d)3#
图6 Ag/Cu双金属纳米溶胶的抑菌环图片
Fig.6 Bacteriostatic ring diagrams of Ag/Cu bimetallic colloidals
3 结论
(1)以硝酸银和醋酸铜为前驱体、乙二醇为还原剂,采用微波辅助加热法,可快速制备出Ag/Cu双金属纳米粒子。
(2)当反应温度为169 ℃、n(Ag+)∶n(Cu2+)为4∶1时,所制Ag/Cu双金属纳米粒子的粒径小且分散均匀,粒子粒径在20~60 nm范围内,并呈现出各种多面体结构,其对大肠杆菌具有良好的抗菌效果。
[1] 王小凤,黄自力,张海军. 双金属纳米颗粒的制备方法[J]. 稀有金属材料与工程,2013,42(8): 1751-1755.
[2] Singh H P, Gupta N, Sharma S K, et al. Synthesis of bimetallic Pt-Cu nanoparticles and their application in the reduction of rhodamine B[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2013, 416: 43-50.
[3] Sun Y, Mayers B T, Xia Y. Template-engaged replacement reaction: a one-step approach to the large-scale synthesis of metal nanostructures with hollow interiors[J]. Nano Letters, 2002, 2(5): 481-485.
[4] Barcikowski S, Compagnini G. Advanced nanoparticle generation and excitation by lasers in liquids[J]. Physical Chemistry Chemical Physics, 2013, 15(9): 3022-3026.
[5] Zhang J, Yuan Y, Xu X W, et al. Core/shell Cu@Ag nanoparticle: a versatile platform for colorimetric visualization of inorganic anions[J]. ACS Applied Materials and Interfaces, 2011, 3(10): 4092-4100.
[6] Czaplinska J, Sobczak I, Ziolek M. Bimetallic AgCu/SBA-15 system: the effect of metal loading and treatment of catalyst on surface properties[J]. The Journal of Physical Chemistry C, 2014, 118(24):12 796-12 810.
[7] Miyakawa M, Hiyoshi N, Nishioka M, et al. Continuous syntheses of Pd@Pt and Cu@Ag core-shell nanoparticles using microwave-assisted core particle formation coupled with galvanic metal displacement[J]. Nanoscale, 2014, 6(15): 8720-8725.
[8] Liu Z, Bando Y. A novel method for preparing copper nanorods and nanowires[J]. Advanced Materials, 2003, 15(4): 303-305.
[9] Ghosh Chaudhuri R, Paria S. Core/shell nanoparticles: classes, properties, synthesis mechanisms, characterization and applications[J]. Chemical Reviews, 2011, 112(4): 2373-2433.
[10]Tsuji M, Hashimoto M, Nishizawa Y, et al. Microwave-assisted synthesis of metallic nanostructures in solution[J]. Chemistry—A European Journal, 2005, 11(2): 440-452.
[11] 徐伟, 何宝林, 刘光荣,等. 微波法纳米镍的制备[J]. 中南民族大学学报:自然科学版, 2006, 25(4): 1-4.
[12]Wang Y, Toshima N. Preparation of Pd-Pt bimetallic colloids with controllable core/shell structures[J]. The Journal of Physical Chemistry B, 1997, 101(27): 5301-5306.
[13]其木苏荣,赵永芳,井孝功,等. 在重金属铜、银和金的团簇中电子相关作用的定量估算[J]. 原子与分子物理学报, 2003, 20(3):413-416.
[14]Tsuji M, Hikino S, Tanabe R, et al. Syntheses of Ag/Cu alloy and Ag/Cu alloy core Cu shell nanoparticles using a polyol method[J]. Crystal Engineering Communications, 2010,12(11): 3900-3908.
[15]Nowak A, Szade J, Talik E, et al. Physicochemical and antibacterial characterization of ionocity Ag/Cu powder nanoparticles[J]. Materials Characterization, 2016, 117: 9-16.
[16]Hundakova M, ValškovM, Tomšek V, et al. Silver and/or copper vermiculites and their antibacterial effect[J]. Acta Geodynamica et Geomaterialia, 2013, 10(1): 97-104.
[责任编辑 张惠芳]
Characterization and antibacterial properties of Ag/Cu bimetallic nanoparticles prepared by microwave heating method
Li Peiyi1,2, Song Shupeng1,2, Wang Jinzhao3, Zhang Yuanzhuo2, Wan Tian2
(1.State Key Laboratory of Refractories and Metallurgy, Wuhan University of Science and Technology,Wuhan 430081,China; 2.College of Materials Science and Metallurgical Engineering, Wuhan University of Science and Technology,Wuhan 430081, China; 3.School of Materials Science and Engineering, Hubei University, Wuhan 430062, China)
With AgNO3and Cu(CH3COO)2·H2O as the precursors, PVP as dispersing agent, ethylene glycol and ethanol as reductants respectively, Ag/Cu bimetallic nanoparticles were synthesised by microwave heating method. XRD, TEM, XPS, etc. techniques were applied to characterize Ag/Cu bimetallic nanoparticles. At the same time, the effects of reaction temperature,n(Ag+)∶n(Cu2+), etc. on morphology and antibacterial properties of Ag/Cu bimetallic nanoparticles were investigated. The results show that, with ethylene glycol used as the reduction agent ,when the reaction temperature is 169 ℃ andn(Ag+)∶n(Cu2+) is 4∶1, Ag/Cu bimetallic nanoparticles prepared have small particle size and uniform dispersion, the particle size is in the range of 20~60 nm, showing a variety of polyhedral structures with good antibacterial properties againstEscherichiacoli.
Ag/Cu; bimetal; nanoparticle; polyol reduction; microwave heating; antibacterial property
2017-01-05
国家自然科学基金资助项目(50901053);湖北省自然科学基金资助项目 (2014CFB799).
李培义(1991-),男,武汉科技大学硕士生.E-mail: 15671616389@163.com
宋述鹏(1979-),男,武汉科技大学副教授,博士.E-mail: spsong@wust.edu.cn
10.3969/j.issn.1674-3644.2017.03.004
O614
A
1674-3644(2017)03-0178-06

