高效液相色谱法测定养阴降糖片4种成分的含量
姜 晖,李开智,王绍志,付连浩,张熙洁,刘晓红△
(1.河北省唐山市工人医院,河北 唐山 063000; 2.河北省唐山市第二医院,河北 唐山 063000)
·检验检测·
高效液相色谱法测定养阴降糖片4种成分的含量
姜 晖1,李开智2,王绍志1,付连浩1,张熙洁1,刘晓红1△
(1.河北省唐山市工人医院,河北 唐山 063000; 2.河北省唐山市第二医院,河北 唐山 063000)
目的 建立同时测定养阴降糖片中葛根素、虎杖苷、阿魏酸和大黄素含量的高效液相色谱(HPLC)法。方法 色谱柱采用Agilent Zorbax Eclipse XDB-C18柱(150mm×4.6mm,5μm),流动相为乙腈(A)-甲醇(B)-0.5%H3PO4溶液(C),梯度洗脱(0min时A 10%,B 5%,C 85%;10 min时A 20%,B 5%,C 75%;20 min时A 25%,B 5%,C 70%;30 min时A 30%,B 7%,C 53%;40 min时A 50%,B 30%,C 20%;55min时A 50%,B 30%,C 20%),流速为0.6mL/min,柱温为30℃,进样量为10μL,检测波长为250,306,254,320 nm。结果 葛根素、虎杖苷、阿魏酸和大黄素质量浓度分别在42.43~678.91,150.00~2 400.00,0.39~6.26,62.50~1 000.00μg/mL范围内与峰面积积分值线性关系良好,平均回收率为98.59%,99.12%,98.70%,98.89%,RSD分别为0.30%,0.52%,1.79%,0.61%(n=6)。结论 该方法分离效果好,操作简便,能较好地控制产品质量。
中药制剂;高效液相色谱法;含量测定;葛根素;虎杖苷;阿魏酸;大黄素
养阴降糖片收载于2015年版《中国药典(一部)》[1],由黄芪[2]、党参、葛根、枸杞子、玄参、玉竹、地黄、知母、牡丹皮、川芎、虎杖[3]、五味子等12味中药组方,具有养阴益气、清热活血的功效,用于治疗糖尿病。虎杖中的虎杖苷[4]具有镇咳、去痰、平喘、抗菌、清除自由基、调血脂、降低胆固醇及抗菌作用。大黄素[5]具有抗肿瘤活性,抗微生物生长作用,免疫抑制作用,解痉、止咳作用,对心血管系统的作用,利尿作用及泻下作用等。葛根中的葛根素[6]具有提高免疫。增强心肌收缩力、保护心肌细胞、降低血压、抗血小板聚集等作用。川芎中含有的阿魏酸(阿魏酸钠)具有抗血小板聚集、增强前列腺素活性、镇痛、缓解血管痉挛等作用。本研究中选取虎杖[7]、葛根及川芎中的活性成分虎杖苷[8-9]、大黄素、葛根素[10]和阿魏酸,建立同步测定4种指标成分含量的分析方法,分离效果好,操作简便,能达到较好地控制产品质量的目的。现报道如下。
1 仪器与试药
1.1 仪器
Agilent1200系列HPLC仪(包括G1311A四元泵,G1322A脱气机,G1316A柱温箱,G1329A自动进样器,G1315D-DAD检测器,HPRev.B.0302化学工作站,美国Agilent公司);摩尔纯水机;真空抽滤泵(大连依利特公司);Sartorius CP225D分析天平(德国 Sartorius公司);80-2型离心沉淀机 (上海手术器械厂);FS-150型超声提取器(上海生析超声仪器有限公司);索氏提取装置。
1.2 试药
虎杖苷对照品(批号为111575-200502),大黄素对照品(批号为110756-200110),葛根素对照品(批号为 110752-200511),阿魏酸对照品(批号为 0773-9910),均购于中国食品药品检定研究院;养阴降糖片(陕西方舟制药有限公司,批号为 130301,130801,140201);乙腈(色谱纯,美国Fisher公司);甲醇(色谱纯,天津市协和昊鹏色谱科技有机限公司);磷酸溶液(分析纯,天津市北方天医化学试剂厂);冰乙酸(分析纯,天津市永大化学试剂有限公司);甲酸(分析纯,天津市博迪化工有限公司);无水乙醇(分析纯,天津市天大化工实验厂);水为超纯水。
2 方法与结果
2.1 色谱条件与系统适用性试验
色谱柱:AgilentZorbaxEclipseXDB-C18柱(150mm× 4.6 mm,5μm);流动相:乙腈(A)-甲醇(B)-0.5% H3PO4溶液(C)[11],梯度洗脱[12](见表1);流速:0.6m L/min;柱温:30℃;进样量:10μL;检测波长:虎杖苷306 nm[13],葛根素250 nm[14],大黄素254 nm[15],阿魏酸320 nm[16]。
分别精密吸取2.2项下对照品贮备液Ⅱ溶液及供试品溶液与阴性对照品溶液,按拟订色谱条件进样,记录色谱图,见图1。可见,在该色谱条件下,养阴降糖片中的4种待测成分可达到基线分离,分离度在相应检测波长下均大于1.5,理论板数均大于3 000,分离效果良好。

表1 流动相梯度洗脱表
2.2 溶液制备
对照品溶液:精密称定对照品葛根素、虎杖苷、阿魏酸和大黄素适量,用甲醇溶解并稀释成质量浓度分别为2 715.64,9 600.00,25.04,4 000.00μg/m L的单一成分对照品贮备液。分别精密量取葛根素对照品贮备液、虎杖苷对照品贮备液、阿魏酸对照品贮备液、大黄素对照品贮备液各1m L置容量瓶中即得混合对照品贮备液Ⅰ(葛根素678.91μg/mL,虎杖苷2 400.00μg/mL,阿魏酸6.26μg/m L,大黄素1 000.00μg/m L),精密量取混合对照品贮备液Ⅰ1mL,精密加取色谱级甲醇3m L,即得混合对照品贮备液Ⅱ(葛根素169.73μg/mL,虎杖苷600.00μg/m L,阿魏酸 1.56μg/m L,大黄素250.00μg/m L)。
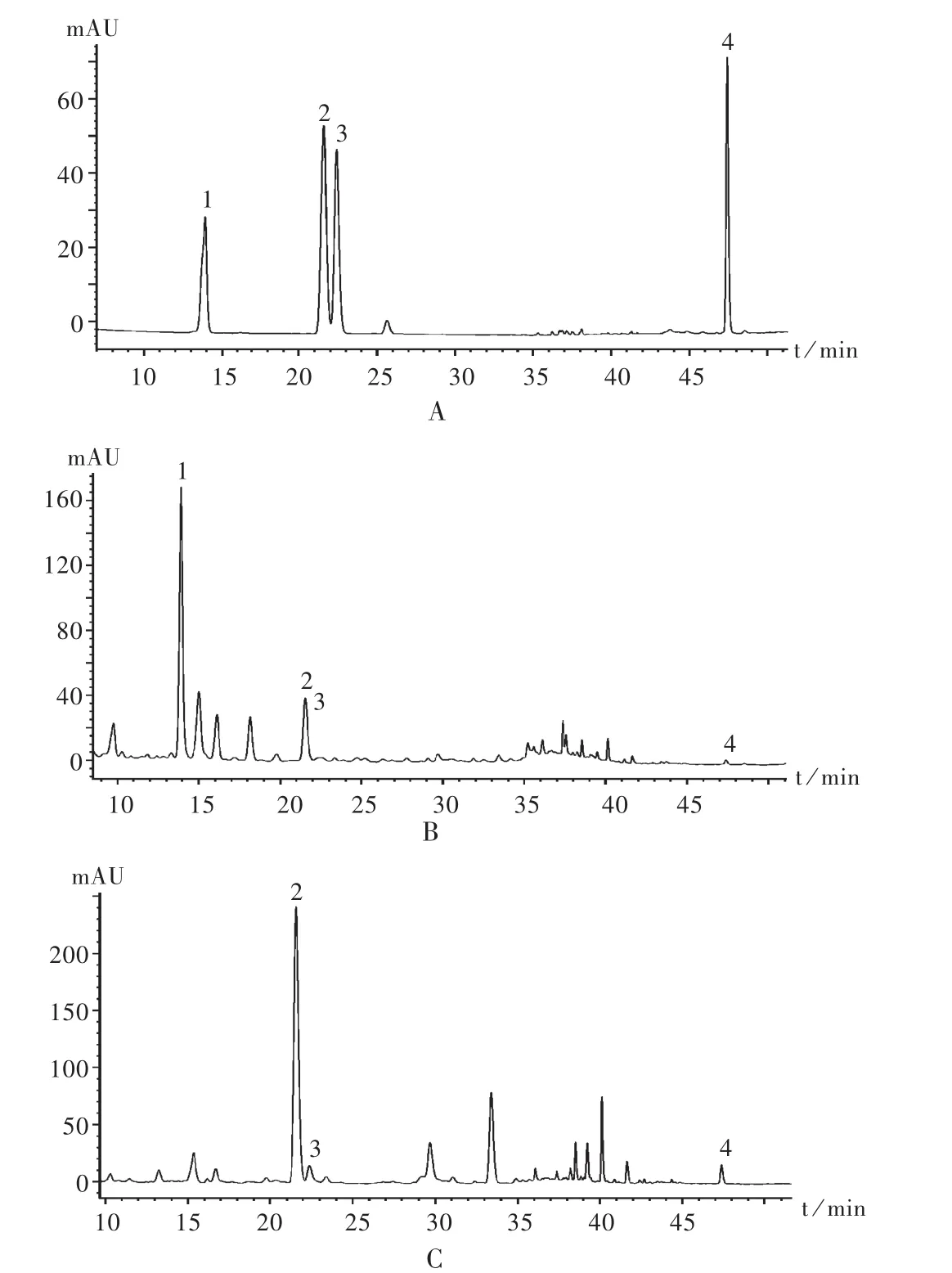
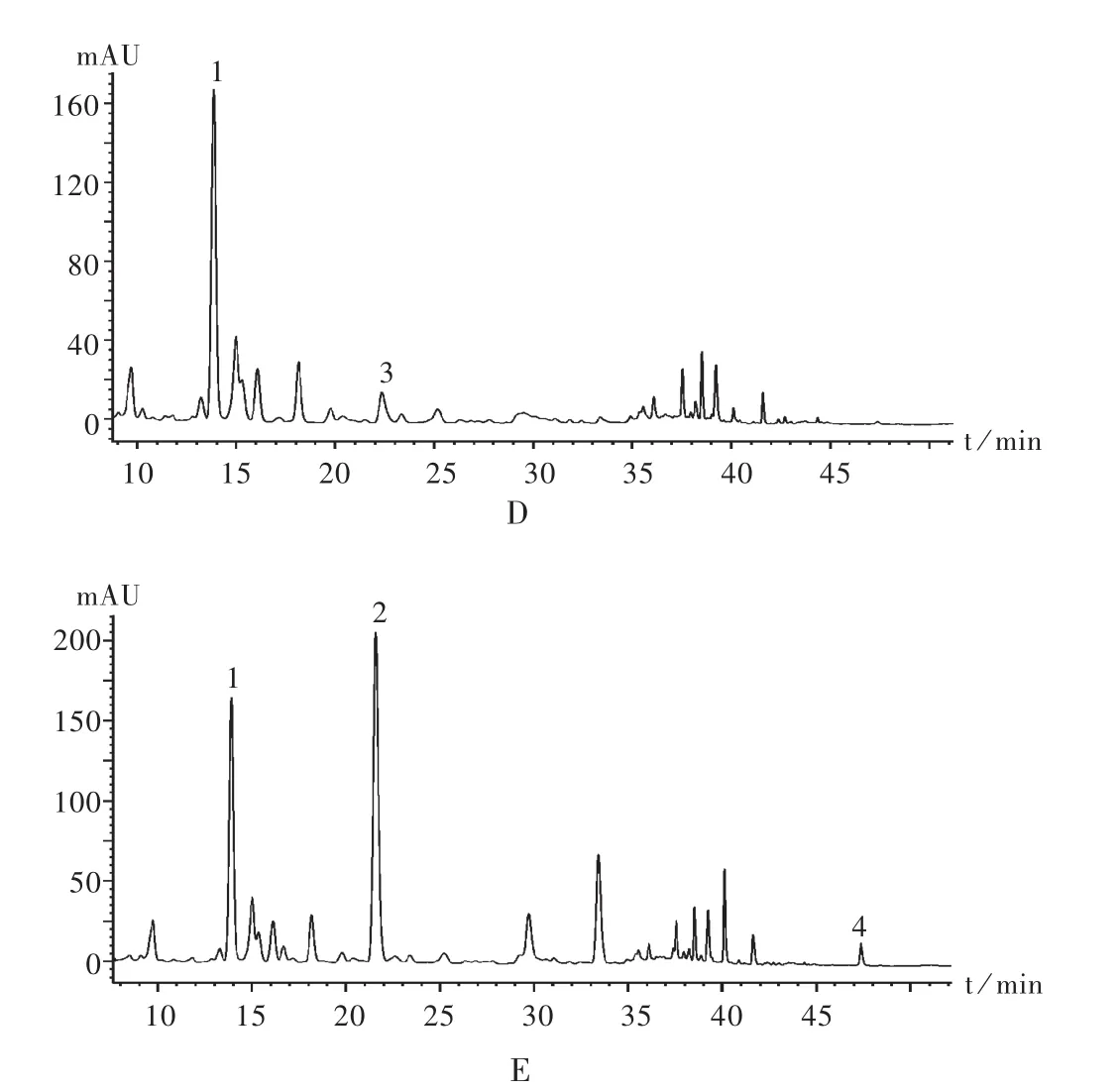
1.葛根素 2.虎杖苷 3.阿魏酸 4.大黄素A.对照品溶液 B.供试品溶液 C.缺葛根阴性对照品溶液 D.缺虎杖阴性对照品溶液 E.缺川芎阴性对照品溶液图1 高效液相色谱图
供试品溶液:取本品约0.3 g,精密称定,置10 mL容量瓶中,加超纯水溶解,超声30min,静置冷却至室温后用超纯水补足容量,离心,0.45μm的微孔滤膜过滤,取续滤液,即得。
阴性对照品溶液:用免煎颗粒按处方工艺制备不含葛根、虎杖、川芎药材的阴性样品,依法制备阴性对照品溶液。
2.3 方法学考察
线性关系考察:精密量取贮备液Ⅰ适量,制备葛根素(42.43,84.86,169.73,339.46,678.91μg/m L)、虎杖苷(150.00,300.00,600.00,1 200.00,2 400.00μg/mL)、阿魏酸(0.39,0.78,1.56,3.13,6.26μg/m L)和大黄素(62.50,125.00,250.00,500.00,1 000.00μg/m L)的系列溶液。再分别精密吸取10μL注入色谱仪,以峰面积(Y)对质量浓度(X,μg/m L)进行线性拟合。得回归方程,见表2。
检测限及定量限:精密吸取贮备液Ⅱ,采用倍比稀释的方法,检测限按照信噪比(S/N)大于3,定量限按照信噪比(S/N)大于10的要求检测。结果见表2。
精密度试验:精密吸取贮备液Ⅱ10μL,重复进样6次,测定峰面积。葛根素、虎杖苷、阿魏酸和大黄素峰面积的RSD分别为 0.35%,0.96%,1.60%,1.14%(n=6),表明仪器精密度良好。详见表3。
稳定性试验:精密吸取同一供试品溶液10μL,分别于0,2,4,6,8,12,24 h时进样,测定峰面积。葛根素、虎杖苷、阿魏酸和大黄素峰面积的 RSD分别为0.23%,0.81%,1.55%,1.44%(n=7),表明供试品溶液在24 h内稳定。详见表4。
重复性试验:取同一批(批号为130301)样品,依法平行制备供试品溶液6份,测定峰面积。葛根素、虎杖苷、阿魏酸和大黄素峰面积的 RSD分别为 0.80%,1.30%,1.73%,1.43%(n=6),表明方法重复性良好。详见表5。
加样回收试验:取已知含量的样品6份,每份约0.3 g,分别精密加入一定量的葛根素、虎杖苷、阿魏酸和大黄素对照品,依法制得供试品溶液,测定含量,计算回收率,结果见表6。
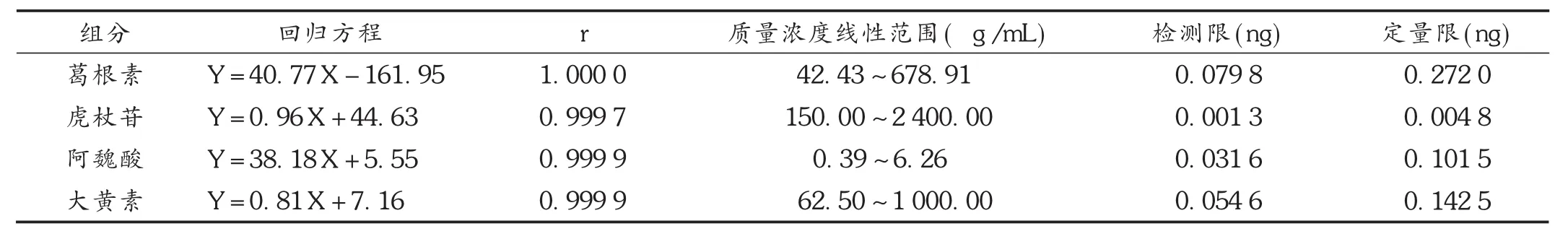
表2 线性关系考察结果

表3 精密度试验结果(n=6)
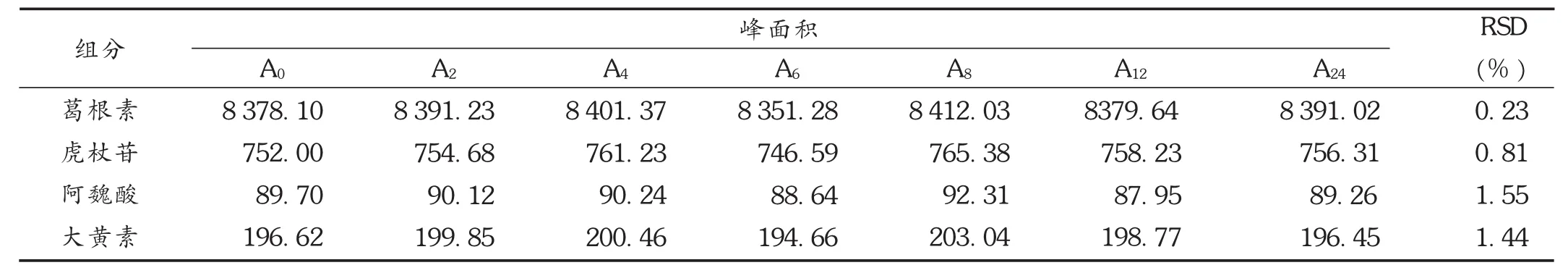
表4 稳定性试验结果(n=7)
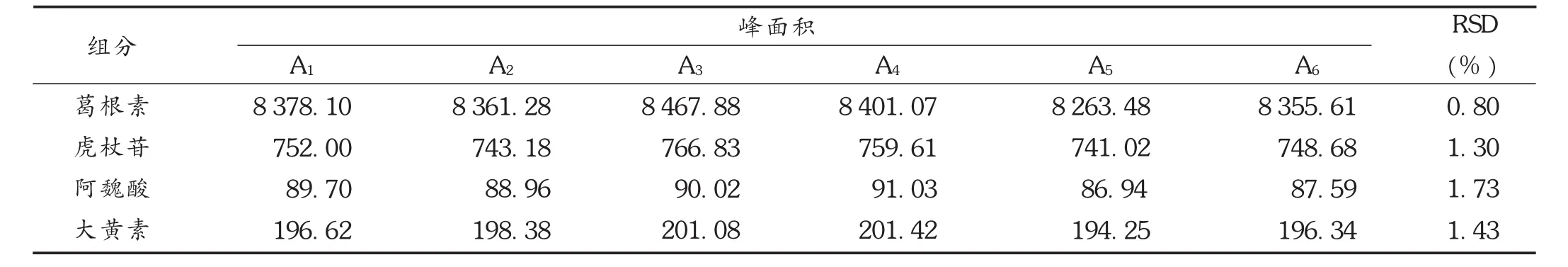
表5 重复性试验结果(n=6)
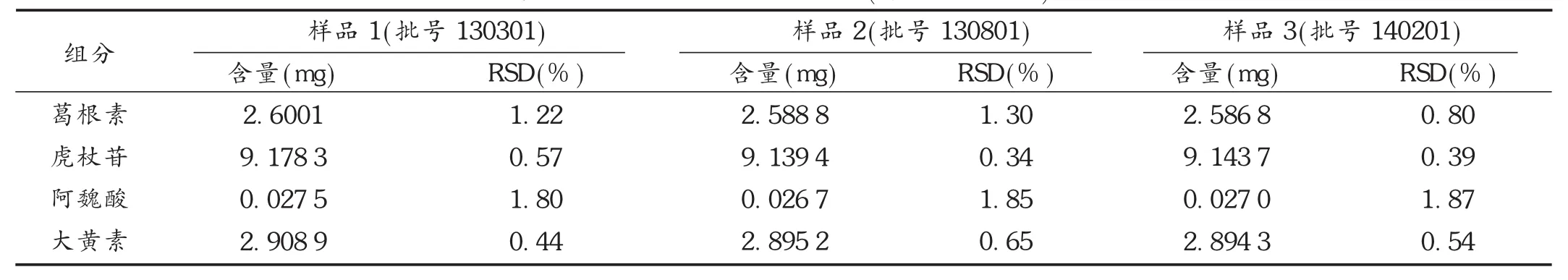
表6 3批样品含量测定结果(每片平均含量)
2.4 样品含量测定
取样品3批,依法分别制成供试品溶液,按拟订色谱条件进样,测定峰面积,按外标法计算样品含量。结果见表7。
3 讨论
3.1 提取方法选择
曾比较索氏提取和超声提取方法,结果在相同提取时间下索氏提取法的提取率与超声提取法无明显区别,超声提取简单、方便,安全性更高,故试验中用超声提取。
3.2 超声提取时间选择
曾选择超声提取10,20,30,40,50,60 min,结果提取率相差不大,葛根素在40min的提取率相对较大,虎杖苷、阿魏酸和大黄素在30min的提取率相对较大,故本试验中选用30min超声提取。
3.3 提取溶剂选择
考察了 50%甲醇、75%甲醇、甲醇、50%甲醇-0.5%磷酸、75%甲醇-0.5%磷酸,甲醇-0.5%磷酸提取。结果以75%甲醇提取的干扰较小,且峰型也较好,磷酸的加入对色谱图无明显影响,故选用75%甲醇提取。
3.4 流动相选择
流动相考察甲醇-水、甲醇-醋酸溶液、甲醇-甲酸溶液、甲醇-磷酸溶液、乙腈-磷酸溶液、甲醇-乙腈-磷酸溶液。结果乙腈-磷酸溶液和甲醇-乙腈-磷酸溶液对5种成分均有较好的分离,但乙腈毒性和成本高,故选择甲醇-乙腈-磷酸溶液进行梯度洗脱。
3.5 阴性对照品的制备
按2015年版《中国药典(一部)》中养阴降糖片的制作工艺来制作阴性对照品,用免煎颗粒制作的阴性对照品的高效液相图谱与生产工艺的阴性对照图谱虽有差异,但影响不大,考虑某些阴性对照品不易找到,按处方工艺制备阴性对照品程序比较烦琐,所用设备不齐全及试验用量较少,用免煎颗粒制作阴性对照品方法简单,且不影响试验结果,故本试验用免煎颗粒制作阴性对照品。
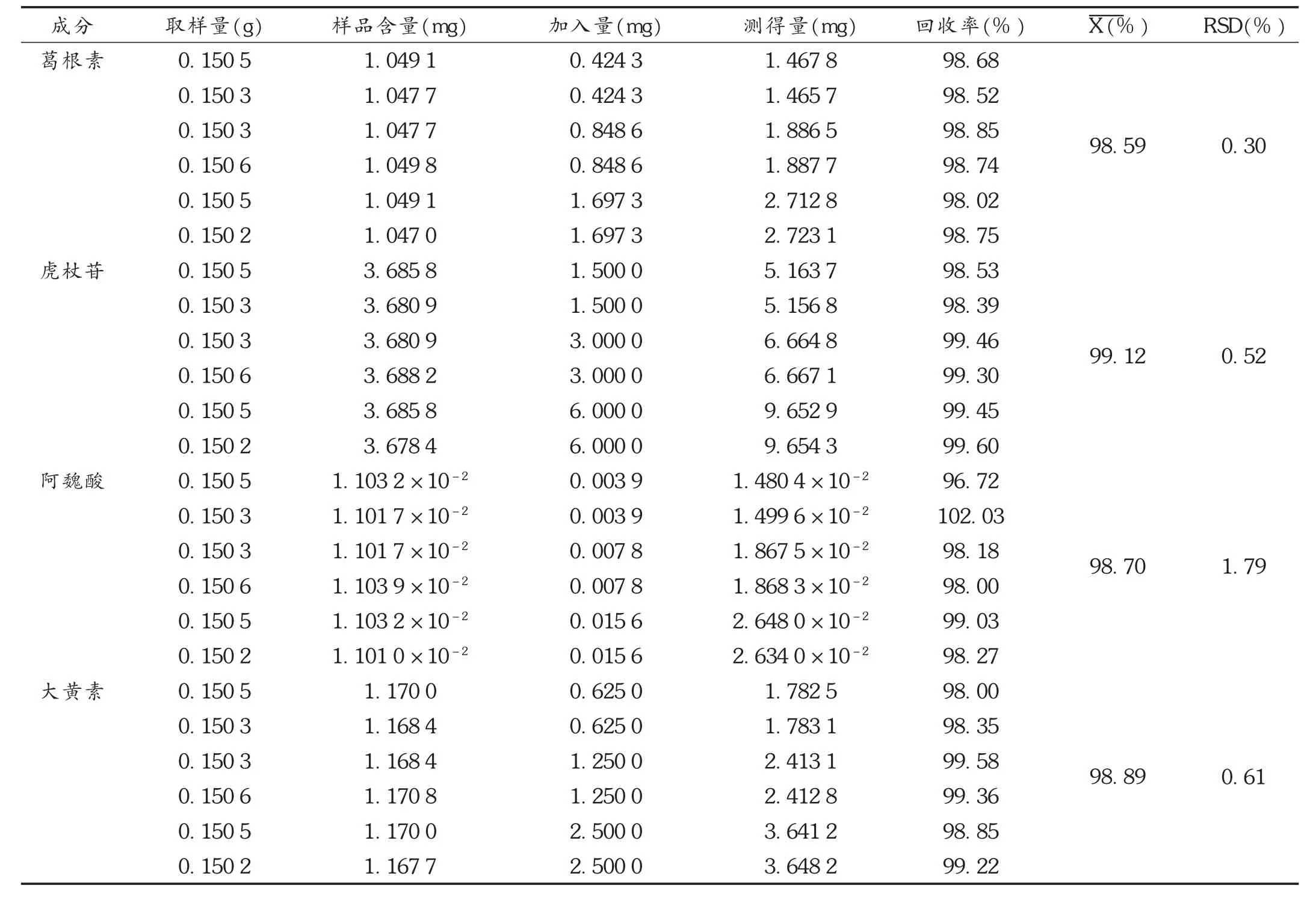
表7 加样回收试验结果(n=6)
综上所述,建立了同步测定养阴降糖片中虎杖苷、大黄素、葛根素和阿魏酸4种有效成分含量的HPLC法,经试验证明,该方法精密度、准确性良好,完全符合药品检测要求,可用于养阴降糖片的质量监测及有关研究。
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:1283-1284.
[2]孙志云.HPLC-ELSD法测定养阴降糖片中黄芪甲苷含量[J].中国实验方剂学杂志,2003,9(6):8-9.
[3]Chen S,Zhou GH,Pi XW,et al.Comparison of differentmethods for the detection of polydatin in polygonuncus pidatum Sieb.et Zucc[J].Medicinal Plant,2012,3(3):18-20.
[4]张 明,鞠 楷,孙 琴,等.西南5个产区虎杖中虎杖苷和白藜芦醇含量比较[J].中国药房,2012,23(39):3723-3725.
[5]李 英,黄清松,罗建明,等.超临界流体萃取-HPLC法测定虎杖中的大黄酸、大黄素及大黄素甲醚的含量[J].中药材,2013,36(5):764-766.
[6]车彦忠,王培智,陈浩英,等.HPLC测定护肝宁丸中虎杖苷的含量[J].中国临床研究,2013,5(19):27-28.
[7]覃开羽,吴 敏.葛根素的药理作用及不良反应分析[J].中国药业,2007,16(3):60-61.
[8]Li YJ,Li Q,Ma J,et al.Validation of HPLCmethod for the determination of polydatin in giant knotweed rhizome[J].Acta Pharmaceutica Sinica,2013,48(4):536-540.
[9]张海欢,缪 红.HPLC法测定疏风解毒胶囊中虎杖苷[J].中成药,2013,35(10):2281-2283.
[10]朱益利,谭浩军.养阴降糖片的质量标准研究[J].世界中西医结合杂志,2009,4(5):321-323.
[11]谢文健,钟 军,黄 婷,等.通腑醒神胶囊中虎杖苷的含量测定[J].中国药师,2011,14(11):1703-1704.
[12]张 蕾,郭晏华,黄 婷,等.虎杖生品及不同炮制品中虎杖苷、白藜芦醇和大黄素含量[J].辽宁中医药大学学报,2013,15(11):56-58.
[13]陈 刚.高效液相色谱法测定清肝利胆排石丸中虎杖苷含量[J].中国药业,2015,24(1):46-47.
[14]屈金凤.高效液相色谱法测定益阴降糖胶囊中葛根素含量[J].中国药业,2012,21(18):43-44.
[15]巩长芹.反相高效液相色谱法测定保婴镇惊丸中大黄素和大黄酚含量[J].中国药业,2014,23(22):58-59.
[16]周赛妮,刘明平,文 艺,等.HPLC同时测定川芎-天麻药对中4种指标性成分的含量[J].中国实验方剂学杂志,2016,22(3):53-56.
Content Determ ination of 4 Com ponents in Yangyin Jiangtang Tab lets by HPLC
Jiang Hui1,Li Kaizhi2,Wang Shaozhi1,Fu Lianhao1,Zhang Xijie1,Liu Xiaohong1
(1.Tang Shan Workers Hospital,Hebei,Tangshan,China 063000;2.The Second Hospital of Tangshan City,Hebei,Tangshan,China 063000)
Ob jective To establish an HPLC method for content determination of puerarin,polydatin,ferulic acid and emodin in Yangyin Jiangtang Tablets.M ethods The Agilent Zorbax Eclipse XDB-C18(150 mm×4.6 mm,5μm)chromatographic separation column was used,mobile phase were composed of acetonitrile(A)-methanol(B)-0.5%H3PO4(C)solution in a linear gradient elution mode(0 min: A 10%,B 5%,C 85%;10 min:A 20%,B 5%,C 75%;20 min:A 25%,B 5%,C 70%;30 min:A 30%,B 7%,C 53%;40 min: A 50%,B 30%,C 20%;55 min:A 50%,B 30%,C 20%).The flow rate was 0.6 m L/min,and the column temperature was set at 30℃,the injection volume was 10μL.The detection wave length were set at 250,306,254,320 nm.Resu lts There was a good linear relationship in a range of 42.43-678.91μg/m L for puerarin,150.00-2 400.00μg/m L for polydatin,0.39-6.26μg/mL for ferulic acid,62.50-1 000.00μg/mL for emodin,respectively.The average recovery were 98.59%,99.12%,98.70%,98.89%,respectively,the RSDs were 0.30%,0.52%,1.79%,0.61%(n=6),respectively.Conclusion The method has good separation effect,it is simple,convenient,and can control the quality of Yangyin Jiangtang Tablets.
preparations of traditional Chinese medicine;HPLC;content determination;puerarin;polydatin;ferulic acid;emodin
2016-08-22;
2016-10-23)
10.3969/j.issn.1006-4931.2017.07.010
姜晖,硕士研究生,副主任药师,研究方向为药理学、药物分析学,(电话)0315-3722840(电子信箱)jianghui910@163.com。
刘晓红,博士研究生,硕士研究生导师,主任药师,研究方向为药理学、临床药学和药物分析学,(电话)0315-3722435(电子信箱)13930520000@163.com。
R284.1
A
1006-4931(2017)07-0032-05

