乙烯基改性聚碳硅烷热分解动力学研究
李博弘,曹先启,陈泽明,2,贾晓莹,王 超,2*,王 勃,2,王文博,徐 鑫
(1.黑龙江省科学院 石油化学研究院,黑龙江 哈尔滨 150040;2.黑龙江省科学院 高技术研究院,黑龙江 哈尔滨 150020)
乙烯基改性聚碳硅烷热分解动力学研究
李博弘1,曹先启1,陈泽明1,2,贾晓莹1,王 超1,2*,王 勃1,2,王文博1,徐 鑫1
(1.黑龙江省科学院 石油化学研究院,黑龙江 哈尔滨 150040;2.黑龙江省科学院 高技术研究院,黑龙江 哈尔滨 150020)
使用红外分析仪分析了乙烯基聚碳硅烷(PVCS)热分解前后的结构,采用热重分析法(TG),在空气气氛下分别以10,20,30,40,50℃/min的升温速率对PVCS的热分解进行了分析。实验结果表明PVCS在空气中1000℃失重率为6.7%~9.3%,主要热失重的温度范围为310~800℃;采用Kissinger方程和Flynn-Wall-Ozawa方程对PVCS热分解动力学常数进行了计算,分别得出PVCS的热分解活化能为158.39kJ/mol和164.65kJ/mol。
乙烯基聚碳硅烷;热分解;动力学;先驱体聚合物
前言
随着科技的飞速发展,对材料及其制备工艺提出了越来越高的要求。纤维(碳化硅纤维或碳纤维)增强碳化硅复合材料是目前最有发展前景的高温结构材料之一,其在高温条件下仍具有高强度、韧性好、耐腐蚀等优点,被广泛应用于航空、航天、军事、能源以及通讯等领域[1~3]。目前国内制备纤维增强碳化硅复合材料主要采用先驱体聚合物浸渍工艺,先驱体聚合物通常为聚碳硅烷(PCS)及其衍生物。而PCS及其大多数衍生物均为固体,需溶解在二甲苯、四氢呋喃等溶剂中再进行浸渍工艺,影响了浸渍效率,致使生产工艺繁杂、生产周期长,影响了纤维增强碳化硅复合材料的生产效率[4]。
乙烯基聚碳硅烷(PVCS)室温为液态,在160~ 400℃进行自交联固化反应,高温裂解后能得到近化学计量比的SiC材料,且具有较高的陶瓷化产率[5~7]。使用PVCS制备纤维增强碳化硅复合材料省去了溶解及除溶剂步骤,简化了生产工艺,缩短了生产周期[8]。本文采用Kissinger法和Flynn-Wall-Ozawa法计算了PVCS热分解动力学参数,为制备纤维增强碳化硅复合材料提供了理论基础。
1 实验部分
所使用的PVCS是黑龙江省科学院石油化学研究院生产的PVCS-601,其Mn=752,Mw=1442,Mw/Mn= 1.92,固化工艺为180℃保温3h。使用美国OHAUS公司AR1140/C型精密电子天平对样品进行称量。使用美国PE公司TG/DTA6300型热失重分析仪研究了在空气气氛下,升温速率分别为10、20、30、40、50℃/min,升温范围为常温~1000℃条件下固化后的PVCS的热失重情况。并通过TG-DTG曲线分析了PVCS的热分解特性。使用德国Bruker公司Vector22型红外分析仪对PVCS及1000℃处理30min的PVCS(升温速率:10℃/min)进行了红外特性分析。
2 结果与讨论
2.1 PVCS热分解过程的TG曲线分析
图1是固化后PVCS样品的TG-DTG谱图,从图中曲线可以看出,固化后PVCS空气气氛下1000℃热失重率为6.7%,其热失重分为两个阶段,第一阶段为150℃~240℃,失重率为0.8%,对应DTG曲线中在200℃左右的失重峰,分析认为该阶段的热失重主要为体系中低分子或未交联的PVCS逸出引起的,基本不存在热分解反应;第二阶段为310℃~800℃,失重率为5.9%,对应DTG曲线中在560℃左右的失重峰,分析认为该阶段的热失重主要为PVCS受热后,分子链发生断裂与重排反应,大量CH4、H2生成并逸出引起的。
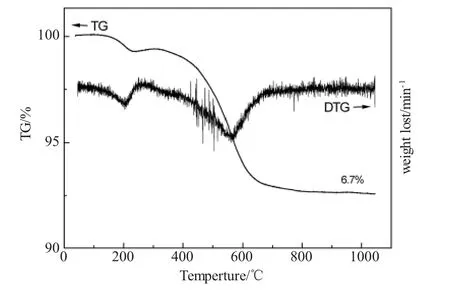
图1 PVCS固化后TG-DTG谱图Fig.1 The TG-DTG curves of cured PVCS
图2是PVCS和经1000℃处理30min后的IR曲线。图中PVCS曲线中3050cm-1、3020cm-1处对应的是不饱和C-H的反对称伸缩振动峰;2950cm-1、2900cm-1处对应Si-CH3中C-H的伸缩振动峰;2100cm-1处为Si-H的伸缩振动峰;1600cm-1处对应C=C的伸缩振动峰;1400cm-1处对应的是Si-CH3中的C-H变形振动峰;1360cm-1处为Si-CH2-Si中C-H的面外振动峰;1250cm-1处对应的是Si-CH3的变形振动峰;1080cm-1处对应Si-O-Si的伸缩振动峰;1010cm-1处对应的是Si-CH2-Si中Si-C-Si骨架振动峰。1000℃处理后的PVCS曲线中有机基团特征吸收峰基本消失,仅1100cm-1附近出现一宽峰,对应的是Si-C和Si-O的相叠加的振动峰,说明PVCS经1000℃处理后,已向无机物转变。
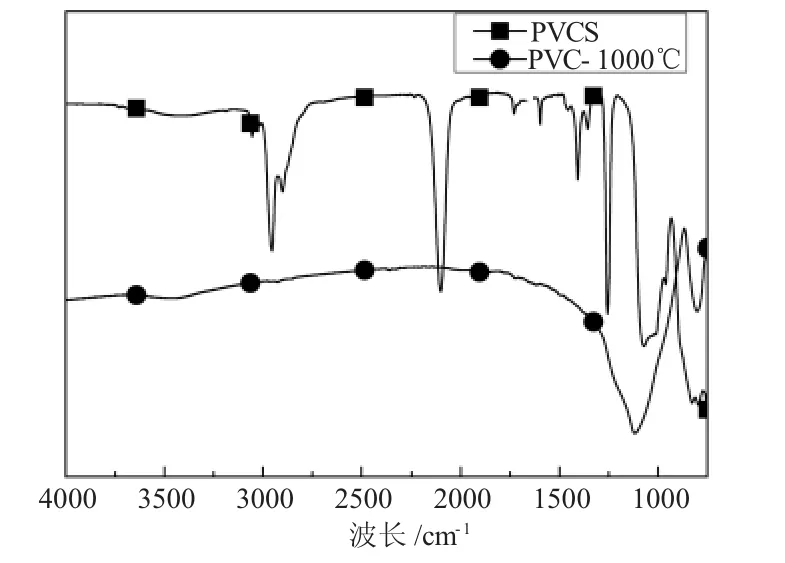
图2 PVCS的IR谱图Fig.2 The IR spectrum of PVCS
图3和图4分别是固化后PVCS样品不同升温速率的TG谱图和DTG谱图。

图3 不同升温速率PVCS的TG谱图Fig.3 The TG curves of PVCS at different heating rates

图4 不同升温速率PVCS的DTG谱图Fig.4 The DTG curves of PVCS at different heating rates
2.2 PVCS热分解动力学分析
热分解动力学计算对聚合物的应用有重要的指导意义。热分解动力学的处理方法包括Kissinger、Friedman、Freeman-Carrol、Flynn-Wall-Ozawa、Chang、Coats-Redfern等一系列方法。本文主要用Kissinger方法和Flynn-Wall-Ozawa方法对样品热分解动力学进行了处理。
2.2.1 Kissinger方法
Kissinger方法的优点在于无需了解确切的反应机理,就可以用ln(β/Tp2)对1000/Tp作图得一直线,直线的斜率经计算后即可求出热分解活化能E。Kissinger[9]方程为:
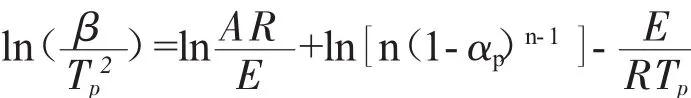
式中:β为升温速度,Tp为热失重曲线上失重速率最大时对应的温度,A为指前因子,αp为最大失重速率时的转化率,n为反应级数。
根据Kissinger方程,用ln(β/Tp2)对1000/Tp作图,得到如图5所示的数据点及拟合直线,线性回归常数R值为0.97,直线斜率为-19.05,即-E/R= -19.05,由此计算出 PVCS的热分解活化能为158.39kJ/mol。
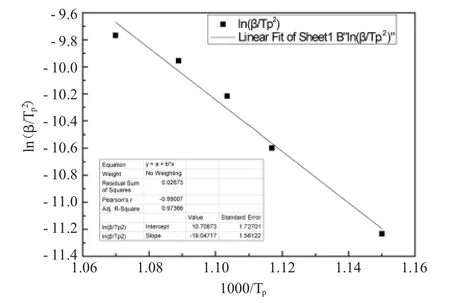
图5 PVCS依据Kissinger方程ln(β/Tp2)对1000/Tp关系图Fig.5 The plot of ln(β/Tp2) VS 1000/Tp according to Kissinger’s equation of PVCS
2.2.2 Flynn-Wall-Ozawa方法
利用Doyle近似理论,可以得到Flynn-Wall-Ozawa方法[10,11]的表达式:
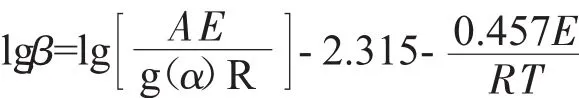
式中:β为升温速度,T为从热失重曲线上得到的不同转化率α对应的温度,A为指前因子。
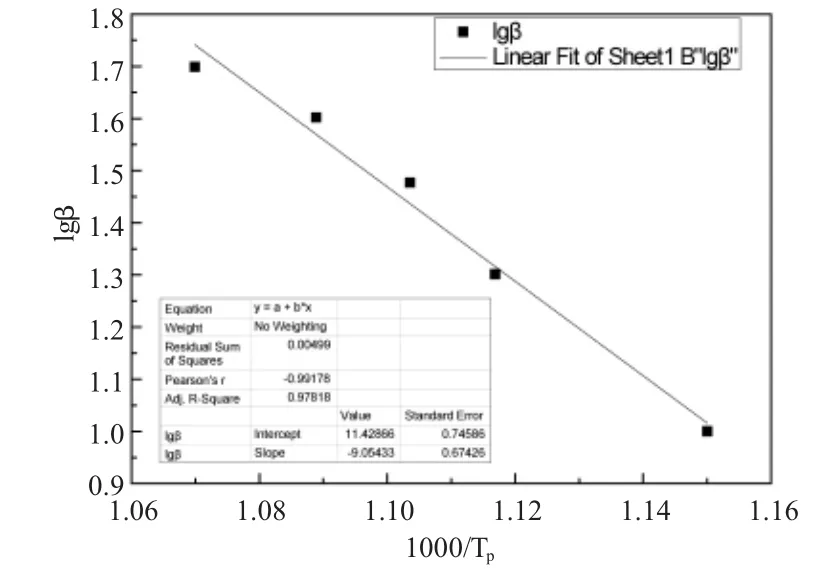
图6 PVCS依据Flynn-Wall-Ozawa方程lgβ对1000/Tp关系图Fig.6 The plot of lgβ VS 1000/Tp according to Flynn-Wall-Ozawa’s equation of PVCS
Flynn-Wall-Ozawa方法无需了解详细的反应机理即可以求出热分解活化能E,但要计算指前因子A则需要了解g(α)的详细表达式。
根据Flynn-Wall-Ozawa方程,在不同升温速率PVCS的TG谱图上读取失重率为5%的温度Tp,用lgβ对1000/Tp作图,得到如图6所示的数据点及拟合直线,线性回归常数R值为0.98,直线斜率为-9.05,即-0.457E/R=-9.05,由此计算出PVCS的热分解活化能为164.65kJ/mol。
3 结论
(1)通过对PVCS的TG-DTG曲线分析得出PVCS在空气中1000℃失重率为6.7%~9.3%,主要热失重的温度范围为310~800℃。
(2)采用Kissinger方程和Flynn-Wall-Ozawa方程对PVCS热分解动力学常数进行了计算,得出PVCS的热分解活化能分别为 158.39kJ/mol和164.65kJ/mol。
[1] JOHNSON D W,EVANS A G,GOETTLER R W,et al.Ceramic fibers and coatings advanced materials for the twenty-first century[M].Washington D.C:National Academy Press,1998:1~49.
[2] 冯春祥,宋永才,王应德.高性能陶瓷纤维的研究进展[M].北京:化学工业出版社,1997:395~400.
[3] 程祥珍,谢征芳,宋永才,等.高压合成聚碳硅烷的分子量分布于可纺性[J].高分子材料科学与工程,2005,21(5):59~62.
[4] 张剑锋.新型液态SiC-C陶瓷先驱体的研究[D].长沙:国防科技大学,2007.
[5] YAJMA S,HAYASHI J,OMORI M,et al.Development of tensile strength silicon carbide fiber using organo-silicon precursor[J].Nature,1976,273(5663):525~528.
[6] WHITMARSH C K,INTERRANTE L V.Carbosilane polymer precursors to silicon carbide ceramics:US,5153295[P].1992-10-06.
[7] INTERRANTE L V,JACOBS J M,SHERWOOD W,et al.Fabrication and properties of fiber and particulate-reinforced SiC matrix composites obtained with(A)HPCS as the matrix source[J].Key Engineering Materials,1997,127:271~278.
[8] 王彦桥,宋永才.含乙烯基的液态聚碳硅烷的结构与性能表征[J].有机硅材料,2010,24(2):85~88.
[9] KISSINGER HE.Reaction kinetics in differential thermal analysis[J].Analytical Chemistry,1957,29(11):1702~1706.
[10] 陈镜泓,李传儒.热分析及其应用[M].北京:科学出版社.1985:120~134.
[11] ABATE L,CALANNA S,POLICINO A,et al.Thermal stability of a novel poly(ether ether ketone ketone)[J].Polym.Eng.Sci., 1996,36(13):1782~1788.
Study on Thermal Decomposition Kinetic Parameters of Vinyl-Polycarbosilane
LI Bo-hong1,CAO Xian-qi1,CHEN Ze-ming1,2,JIA Xiao-ying1,WANG Chao1,2,WANG Bo1,2,WANG Wen-bo1and XU Xin1
(1.Institute of Petrochemistry,Heilongjiang Academy of Sciences,Harbin 150040 China;2.Institute of Advanced Technology,Heilongjiang Academy of Sciences,Harbin 150020,China)
The molecular structures of vinyl-polycarbosilane(PVCS)before and after thermal decomposition were analyzed by IR.The pyrolysis characteristics and dynamics of PVCS was studied with the thermogravimetric analysis at different heating rates(10,20,30,40 and 50℃/min).The result showed that the thermal weight loss of vinyl-polycarbosilane in air at 1000℃ was 6.7%to 9.3%.The thermal decomposition temperature was 310℃to 800℃.The thermal decomposition kinetic constant of PVCS was calculated by Kissinger’s equation and Flynn-Wall-Ozawa’s equation.And the thermal decomposition activation energy of PVCS was 158.39kJ/mol and 164.65kJ/mol.
Vinyl-polycarbosilane;thermal decomposition;kinetic;precursor polymers
TQ323.7;O634.41
A
1001-0017(2017)02-0102-03
2016-10-24
李博弘(1986-),男,黑龙江哈尔滨人,研究实习员,主要从事高分子功能材料研究。
*通讯联系人

