UFLC-MS/MS法测定急进高原前后大鼠体内左氧氟沙星含量及其药代动力学差异*
王 昌, 贾正平,2, 李文斌, 鹿 辉, 罗冰峰,2, 刘晶晶,2, 张明霞,2, 王 荣,2△
1兰州军区兰州总医院全军高原环境损伤防治重点实验室,兰州 7300502兰州大学药学院,兰州 730000
UFLC-MS/MS法测定急进高原前后大鼠体内左氧氟沙星含量及其药代动力学差异*
王 昌1, 贾正平1,2, 李文斌1, 鹿 辉1, 罗冰峰1,2, 刘晶晶1,2, 张明霞1,2, 王 荣1,2△
1兰州军区兰州总医院全军高原环境损伤防治重点实验室,兰州 7300502兰州大学药学院,兰州 730000
目的 建立高效液相色谱-串联质谱测定大鼠血浆左氧氟沙星含量的方法,并研究急进高原前后大鼠体内左氧氟沙星的药代动力学变化情况。方法 采用超快速液相色谱串联质谱(UFLC-MS/MS)法,以Gemini 3u C18柱(75 mm×3 mm,3 μm)分离,以乙腈∶水∶甲酸(体积比55∶45∶0.1)为流动相进行洗脱,流速0.4 mL/min,柱温30℃,进样10 μL,电喷雾正离子电离(ESI)模式、多反应监测(multiple reaction monitoring,MRM)模式进行检测。12只大鼠被随机分为平原组与高原组(n=6),实验前禁食12 h。实验时,大鼠灌胃给予左氧氟沙星(20 mg/kg)。于给药前(0 h)和给药后0.25、0.5、0.75、1、1.5、2、4、6、8、12和24 h,由眼眶静脉丛采血0.2 mL,并采用UFLC-MS/MS法测定大鼠体内左氧氟沙星浓度。结果 左氧氟沙星的峰面积与其质量浓度在一定浓度范围内均呈良好的线性关系(r=0.999 5),该方法线性范围为5.00~2.00×105μg/L,最低检测限为5.00 μg/L。比较急进高原组与平原组大鼠体内左氧氟沙星药动学参数,发现其发生了显著变化,药时曲线下面积从(5 799.27±1 867.18)(μg·h)/L增大到(33 828.41±8 196.08)(μg·h)/L,峰浓度增大、体内平均驻留时间延长、总清除率降低,且差异均有统计学意义(均P<0.05)。结论 急进高原后,左氧氟沙星在大鼠体内代谢过程发生明显变化,研究结果为平原和急进高原后临床合理应用左氧氟沙星提供参考依据。
超快速液相色谱串联质谱; 左氧氟沙星; 血浆样品; 药代动力学; 急进高原
我国高原地区幅员辽阔,常驻海拔2 500 m以上人群达到6 000万~8 000万人。随着社会发展、旅游业的兴起、丝绸之路经济带的复兴,及国防事业的需要,越来越多的人前往高原地区工作与生活。高原环境具有低气压、低氧、低温、低湿度、强紫外线辐射等自然条件特点,会造成机体出现一系列的病理、生理性改变,这将在一定程度上改变高原患者体内药物的吸收、分布、代谢及排泄过程。国家食品药品监督管理总局于2015年7月公布的数据显示,1999年至2014年,全国药品不良反应监测网络累计收到《药品不良反应/事件报告表》近790万份。因此,了解药物的合理用药情况,降低药物不良反应发生率,非常重要。目前,高原地区的药物与平原地区的使用方式一致,那么,药物在急进高原人群的体内药代动力学参数与在平原时是否有差异?这一点有待研究解决。
左氧氟沙星属于喹诺酮类抗生素,具有广谱抗菌作用,抗菌效果强,临床上运用广泛。其口服吸收作用完全,相对生物利用度接近98%,体内吸收迅速,达峰时间约为1 h。由于吸收后能广泛分布于机体大多数组织,因此,左氧氟沙星能够用于大部分组织器官的抗感染治疗。本研究选择临床常用的药物——左氧氟沙星作为研究对象,观察实验大鼠由平原急进高原地区后,体内左氧氟沙星的药代动力学变化,为高原急进人群的合理用药提供参考。
作为临床常用的抗菌药物,左氧氟沙星的测定方法主要为高效液相色谱法[1-7]、拉曼光谱法[8]、荧光法[9]等,为缩短检测时间,提高分析效率,本实验在文献报道的基础上进一步研究,通过优化色谱和质谱条件,建立了一种简单、高效和灵敏的UFLC-MS/MS测定大鼠血浆中左氧氟沙星的方法,并将其应用于大鼠血浆左氧氟沙星的药代动力学研究中。
1 材料与方法
1.1 仪器与试剂
UFLC-20A高效液相色谱仪(Japan SHIMADZU CO.LTD);API3200三重四极杆串联质谱仪(American Applied Biosystems/MDS SCIEX Pte.LTD);高速离心机(上海安亭科技仪器厂);超声波清洗器(上海科导超声波仪器有限公司);快速混匀器(常州国华电器有限公司)。
左氧氟沙星标准品(中国食品药品检定研究院,批号:110136-201009);左氧氟沙星注射液(湖南五洲通药业有限公司,规格2 mL:0.2 g,批号:1508051);甲酸(美国DIMA公司,色谱纯);乙腈(德国Merk公司,色谱纯);灭菌注射用水(西安双鹤制药有限公司)。
1.2 样品分析方法
1.2.1 色谱质谱条件 色谱柱:Gemini 3u C18柱(75 mm×3 mm,3 μm),流动相为乙腈∶水∶甲酸(55∶45∶0.1),流速0.4 mL/min,柱温30℃,进样量10 μL,整个分析流程用时3 min。
质谱采用ESI正离子多反应(multiple reaction monitoring,MRM)方式检测:电喷雾离子源(electrospray interface,ESI)电压5.5 kV,温度(source temperature,TEM)300℃,解离电压(declustering potential,DP)30.0 psi,碰撞能量(collision energy,CE)25.0 psi。左氧氟沙星的检测离子对为m/z 362.2→m/z 318.2。
1.2.2 对照品溶液的制备 精密称取左氧氟沙星对照品0.002 g置于10 mL容量瓶,甲醇溶解定容至刻度,振荡混匀,获得浓度为2.00×106μg/L的左氧氟沙星储备液,并置于4℃冰箱中保存。使用大鼠空白血浆,将左氧氟沙星储备液按梯度稀释成5.00、0.10×102、0.50×102、1.00×102、2.50×102、5.00×102、1.00×103、2.50×103、5.00×103、1.00×104、2.50×104、5.00×104、1.00×105、2.00×105μg/L对照品溶液,置于4℃冰箱中保存,待用。
1.2.3 血浆样品处理 吸取100 μL血浆样品加入0.5 mL离心管中,加入300 μL乙腈,涡旋振荡30 s,沉淀蛋白,13 000 r/min离心10 min后,取上清液,进样量为10 μL。
1.3 药代动力学实验
1.3.1 动物分组及急进方式 实验所用动物均为健康雄性SPF级Wistar大鼠,共12只,购自上海斯莱克实验动物有限公司,合格证编号2007000525382,约8~9周龄,体质量(200±20)g。将大鼠随机分为平原组(上海,海拔55 m,大气压101.3 kPa)和急进高原组(青海玛多,海拔4 300 m,大气压60.2 kPa),每组各6只,两组大鼠均在平原海拔实验室适应性喂养1周。急进高原组在上海经航空托运至甘肃兰州后,立即由恒温厢式货车转运至青海玛多海拔4 300 m处[10]。大鼠禁食12 h后开始实验,药代动力学实验过程同平原组。
1.3.2 样品采集方式 各实验大鼠分别以20 mg/kg的剂量灌胃给药,于给药前(0 h)和给药后0.25、0.5、0.75、1、1.5、2、4、6、8、12和24 h各由眼眶静脉丛采血0.2 mL,置入含少量肝素钠的0.5 mL离心管中,3 000 r/min离心15 min,将获得的血浆样品放入-20℃保存。待实验结束后,置于-80℃超低温冰箱冻存,备用。
1.4 数据处理

2 结果
2.1 质谱分析
采取正离子方式检测,将左氧氟沙星对照品溶于流动相中,按“1.2.1色谱质谱条件”项操作,于一级全扫描质谱图中获得左氧氟沙星准分子离子峰[M+H]+m/z 362.2,选择该准分子离子峰进行碰撞诱导电离,生成主要的碎片离子峰m/z 318.2用于定量,其二级质谱图见图1。
2.2 方法学考察
2.2.1 方法的专属性 根据上述血浆样品处理方
法及检测条件,分析空白血浆样品、含药血浆样品(5.00×103μg/L)及给药大鼠的血浆样品(给药后0.5 h)。结果表明,血浆中杂质不干扰样品的测定。左氧氟沙星的保留时间为0.93 min(图2),表明本法具有较高的专属性。

图1 左氧氟沙星的二级质谱扫描图Fig.1 Two-stage mass spectrum graph of levofloxacin

A:空白血浆样品;B:空白血浆加对照品(5.00×103 μg/L);C:实验大鼠血浆给药后0.5 h样品图2 左氧氟沙星专属性实验结果Fig.2 Results of levofloxacin specialized experiments
2.2.2 线性关系考察 精密量取“1.2.2”项下浓度依次为5.00、0.10×102、0.50×102、1.00×102、2.50×102、5.00×102、1.00×103、2.50×103、5.00×103、1.00×104、2.50×104、5.00×104、1.00×105、2.00×105μg/L的对照品溶液,按样品处理项下操作。以左氧氟沙星峰面积对相应浓度值作线性回归分析,得到标准曲线方程:Y=29.4X-72.4(r=0.999 5),权重为1/x2。结果表明,左氧氟沙星检测质量浓度在5.00~2.00×105μg/L的范围内线性关系良好。以标准曲线的线性范围最低点浓度作为定量限,则最低定量限为5.00 μg/L。
2.2.3 提取回收率 取一定量的左氧氟沙星对照品储备液,加入空白血浆,分别配置低、中、高3个浓度(0.50×102、2.50×103、1.50×105μg/L)的标准血浆溶液,按“1.2.3”项下进行操作,结果高、中、低3个浓度的提取回收率分别为96.72%、95.08%、95.63%,RSD分别为3.61%、4.17%、4.85%,表明测定数据精密度好,实验方法可重现。
2.2.4 精密度和准确度考察 同上法配置低、中、高浓度的左氧氟沙星血浆样品,按照“1.2.3”项下平行操作,于日内分别测定5次,用工作曲线计算浓度,考察方法日内精密度;日间分别进行分析,连续测定3 d,考察日间精密度,计算日内和日间RSD,结果均小于4.50%,符合要求。
2.2.5 稳定性试验 同上法配置低、中、高浓度的左氧氟沙星血浆样品,将样品分为3组,每组5份,第1组在室温下放置24 h后测定浓度考察其室温稳定性,第2组在-20℃冰箱连续冻融3次后测定浓度考察其冻融稳定性,第3组冻入-80℃冰箱15 d后测定浓度考察其冷冻稳定性。供试品溶液在上述条件下稳定,结果见表1。
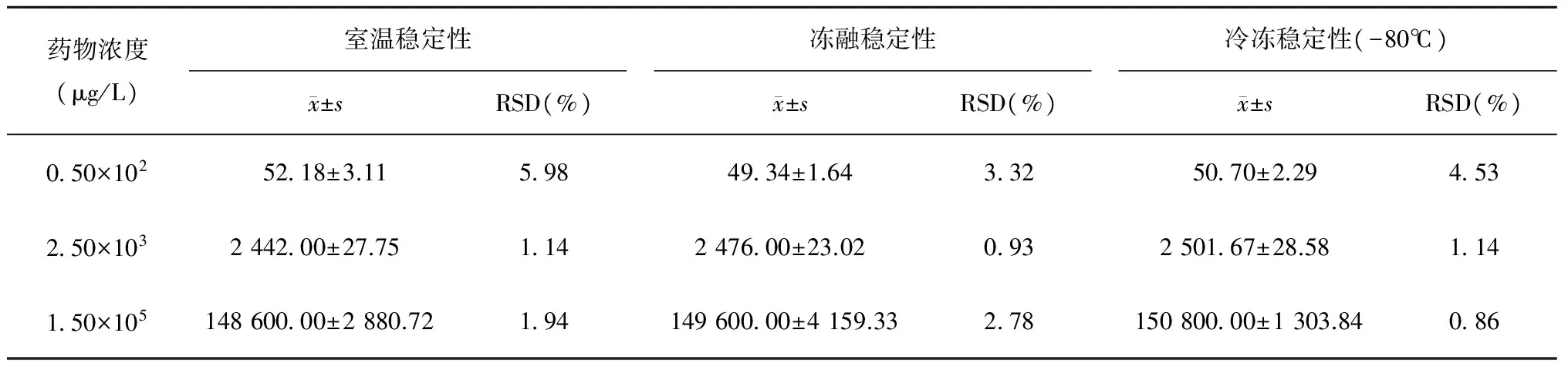
表1 左氧氟沙星的稳定性考察(n=5)
2.2.6 平均血药浓度-时间曲线 采用UFLC-MS/MS法测定Wistar大鼠单剂量(20.00 mg/kg)灌胃左氧氟沙星注射液后的左氧氟沙星血药浓度,其平均血药浓度-时间曲线见图3。

图3 大鼠左氧氟沙星的平均血药浓度-时间曲线Fig.3 Curves of the average levofloxacin concentration against time in rats
2.2.7 药代动力学参数 将灌胃给药后的血药浓度-时间数据用DAS 2.0软件处理进行拟合,得到其主要药代动力学参数见表2。
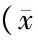
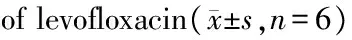
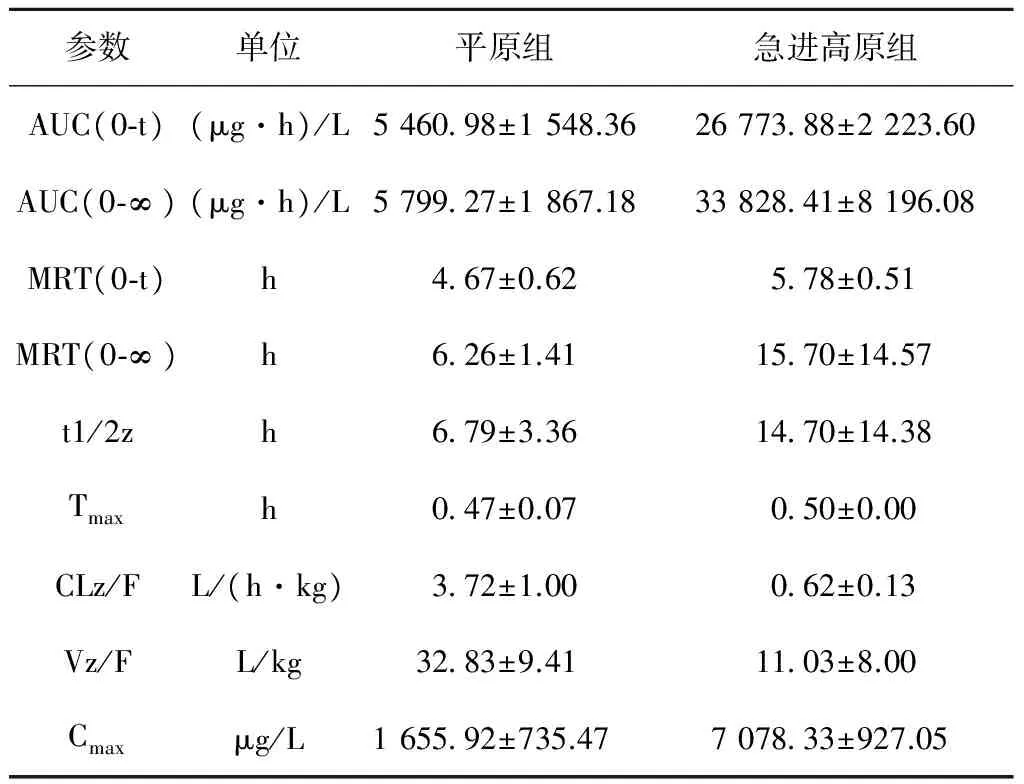
参数单位平原组急进高原组AUC(0⁃t)(μg·h)/L546098±1548.362677388±2223.60AUC(0⁃∞)(μg·h)/L579927±1867.183382841±8196.08MRT(0⁃t)h467±0.62578±0.51MRT(0⁃∞)h626±1.411570±14.57t1/2zh679±3.361470±14.38Tmaxh047±0.07050±0.00CLz/FL/(h·kg)372±1.00062±0.13Vz/FL/kg3283±9.411103±8.00Cmaxμg/L165592±735.47707833±927.05
AUC:药时曲线下面积;MRT:平均驻留时间;t1/2z:半衰期;Tmax:达峰时间;CLz/F:清除率;Vz/F:表观分布容积;Cmax:最大血药浓度
3 讨论
3.1 色谱条件的优化
本实验考察了流动相中不同浓度的甲酸对左氧氟沙星检测的影响,当甲酸的浓度为0.1%时,峰形、响应值均较好,所以实验时以乙腈∶水∶甲酸=55∶45∶0.1(V/V/V)为流动相,检测结果达到最佳。
3.2 质谱条件的优化
本实验选用1.00×103μg/L的左氧氟沙星对照品溶液进行条件优化,选择ESI+作为电离模式,分别对DP、射入电压(entrance potential,EP)、TEM、CE等参数进行优化。通过全扫描方式观察总离子流图,得到母离子峰,通过碰撞反应进行子离子扫描,确定其定量和辅助定性离子,然后分别对各离子对进行检测,经反复选用离子对,结合其断裂方式最后确定ESI+作为电离模式,以m/z 362.2→m/z 318.2为检测离子对,质谱仪的检测响应值达到最佳。
3.3 药代动力学参数差异
本研究采用UFLC-MS/MS联用技术,采用多反应监测模式测定大鼠血浆中左氧氟沙星的浓度,大大提高了检测灵敏度,最低定量限达到5.00 μg/L,可以满足大鼠体内左氧氟沙星的药代动力学研究要求。上述研究结果表明,急进高原后左氧氟沙星在大鼠体内的吸收、分布、代谢和排泄发生了一定的变化,由药代动力学参数的前后变化可以看出,急进高原后左氧氟沙星的清除率变小,半衰期延长,说明急进高原后左氧氟沙星的体内代谢和排泄均减慢。急进高原组的AUC和Cmax分别比平原组增加5.8倍和4.3倍,表明左氧氟沙星的吸收显著增加,这可能与高原缺氧环境对大鼠体内药物转运体的影响有关。课题组前期研究[11]表明,缺氧环境下药物转运体P-gp的蛋白含量显著升高,而左氧氟沙星由这2种蛋白转运,所以急进高原后其浓度显著增加。左氧氟沙星血药浓度的显著升高,将会在一定程度增加药物的不良反应风险。
药动学参数的变化会很大程度上影响药物的疗效和毒副作用[12],因此调整高原人群(包括急进高原、高原常驻及习服人群)药物用法和用量有重要意义。本研究结果对高原人群临床合理用药、避免药物不良反应和个体化用药起重要的参考作用。
[1] Carlos A J,Hernandez-Pineda J,Miguel J J,et al.Rapid and sensitive determination of levofloxacin in microsamples of human plasma by high-performance liquid chromatography and its application in a pharmacokinetic study[J].Biomed Chromatogra,2015,29(3):341-345.
[2] Carral N,Lukas J C,Oteo I,et al.Impact of poor compliance with levofloxacin and moxifloxacin on respiratory tract infection antimicrobial efficacy:A pharmacokinetic/ pharmacodynamic simulation study[J].Int J Antimicrob Agents,2015,45(1):79-83.
[3] Guillaume M,Garraffo R,Bensalem M,et al.Pharmacokinetic and dynamic study of levofloxacin and rifampicin in bone and joint infections[J].Med Mal Infect,2012,42(9):414-420.
[4] Zherdev V P,Litvin A A,Kolyvanov G B.Pharmacokinetic study of original and generic levofloxacin tablets[J].Moscow University Chemistry Bulletin,2013,68(5):251-255.
[5] Rajagopalan S,Shafiq N,Pandhi P.Effect of levofloxacin on lithium-a pharmacokinetic study in rabbits[J].Fundam Clin Pharmacol,2013,27(2):181-185.
[6] Srinivas N,Narasu L,Shankar B P,et al.Development and validation of a HPLC method for simultaneous quantitation of gatifloxacin,sparfloxacin and moxifloxacin using levofloxacin as internal standard in human plasma:application to a clinical pharmacokinetic study[J].Biomed Chromatogra,2008,22(11):1288-1295.
[7] Yusuke T,Hisashi N,Noriko K,et al.premarketing population pharmacokinetic study of levofloxacin in normal subjects and patients with infectious diseases[J].Biol Pharm Bull,1995,18(2):315-320.
[8] 陈斌,张少敏,余岳林,等.拉曼光谱快速检测盐酸左氧氟沙星注射液[J].药物分析杂志,2011,9:1715-1719.
[9] 刘奇,杨红瑞,王爱军.β-环糊精增敏亚甲基蓝荧光法测定左氧氟沙星[J].分析试验室,2012,5:6-9.
[10] 王昌,王荣,谢华,等.氨茶碱对急进高原大鼠部分生理病理变化的影响[J].中南大学学报:医学版,2015,4(1):39-45.
[11] Li W B,Li J,Wang R,et al.MDR1 will play a key role in pharmacokinetic changes under hypoxia at high altitude and its potential regulatory networks[J].Drug Metab Rev.2015.47(2).191-198.
[12] 李文斌,王荣,谢华,等.影响急进4010 m高原大鼠药动学参数的诸因素变化[J].国际病理科学与临床杂志,2012,32(3):185-191.
(2016-09-26 收稿)
UFLC-MS/MS Assay for Pharmacokinetics of Levofloxacinin Rats after Acute Ascent to High Altitude
Wang Chang1,Jia Zhengping1,2,Li Wenbin1etal
1PLAKeyLaboratoryofthePlateauoftheEnvironmentalDamageControl,LanzhouGeneralHospital,LanzhouMilitaryCommand,Lanzhou730050,China2SchoolofPharmacy,LanzhouUniversity,Lanzhou730000,China
Objective To measure the contents of levofloxacin in rats by UFLC-MS/MS in an attempt to examine the changes of pharmacokinetics of levofloxacin in rats after acute ascent to high altitude.Methods The plasma concentration of levofloxacin was detected by UFLC-MS/MS.The Gemini 3u C18 column(75 mm×3 mm,3 μm)was used for isolation,and acetonitrile-water-formic acid(volume ratio 55∶45∶0.1)as the mobile phase for elution.The flow rate of the mobile phase through the Gemini 3u C18 column was 0.4 mL/min,the column temperature was 30℃ and the adding sample was 10 μL.The MS/MS detection was performed in multiple reaction monitoring mode(MRM)with positive electrospray ionization(ESI).Twelve rats were randomly divided into plain group and high altitude group(n=6).After fasting for 12 h,levofloxacin at 20 mg/kg was given by gavage.Blood(0.2 mL)was collected from the orbital venous plexus before administration(0 h)and 0.25,0.5,0.75,1,1.5,2,4,6,8,12 and 24 h after administration,respectively,and the levofloxacin concentrations were determined in the rat plasma by UFLC-MS/MS.Results The peak area showed a good linear relationship with levofloxacin(r=0.999 5)in a certain concentration range.The linear range of levofloxacin was 5.00-2.00×105μg/L and the limit of quantification(LQ)was 5.00 μg/L.Pharmacokinetics of Levofloxacin was significantly different between the high altitude group and the plain group.The area under the curve increased from(5 799.27±1 867.18)(μg·h)/L in the plain group to(33 828.41±8 196.08)(μg·h)/L in the high altitude group.The Cmaxwas significantly higher and the average intracorporal residence time significantly prolonged and the total body clearance markedly lower in the high altitude group than in the plain group(P<0.05).Conclusion Theinvivometabolism of levofloxacin changed significantly in rats after acute ascent to high altitude,which provides references for clinical rational application of levofloxacin after acute high-altitude exposure.
UFLC-MS/MS; levofloxacin; plasma samples; pharmacokinetics; acute ascent to high altitude
*国家科技部重大专项(No.2008ZXJ09014-010);国家自然科学青年基金资助项目(No.81403004,No.81401552);全军后勤科研“十二五”重大项目(No.AWS14L0005);全军医学科研"十二五"重点项目(No.BWS12J012)
R917.1
10.3870/j.issn.1672-0741.2017.02.009
王 昌,男,1989年生,药师,E-mail:smith_003@163.com
△通讯作者,Corresponding author,E-mail:wangrong-69@163.com

