响应面试验优化低酸水解大豆蛋白生产工艺
郑姣姣,魏然,李永歌
(保定味群食品科技股份有限公司,河北 保定 071000)
响应面试验优化低酸水解大豆蛋白生产工艺
郑姣姣,魏然,李永歌
(保定味群食品科技股份有限公司,河北 保定 071000)
优化了在低酸条件下大豆蛋白的水解工艺,此工艺旨在降低水解蛋白中的氯化钠含量。以脱脂大豆作为原料,采用盐酸水解工艺,分析盐酸浓度、液固比、水解时间、水解温度对蛋白水解率影响的规律。结果表明:液固比、温度对蛋白水解率影响主效应显著,各因素对蛋白水解率影响程度的大小顺序为液固比>水解温度>水解时间>盐酸浓度。液固比与盐酸浓度、盐酸浓度与时间、盐酸浓度与温度、温度与液固比、时间与温度之间交互作用对水解率的影响均为极显著。优化得到的大豆蛋白水解工艺为盐酸浓度14%、液固比2∶1、水解时间31 h、水解温度105 ℃,在此条件下蛋白水解率为73.6%,所得水解蛋白液中氯化钠含量约为12.5%,较传统的水解工艺降低了22%~31%。
脱脂大豆;响应面设计法;水解工艺;蛋白水解率;氯化钠
酸水解植物蛋白调味液(acid-hydrolyzed vegetable protein seasoning,HVP)是以含有食用植物蛋白脱脂大豆、花生粕、小麦蛋白或玉米蛋白为原料,经盐酸水解、碱中和制成的液体鲜味调味品[1,2]。HVP生产周期短,含有丰富的氨基酸和小肽类物质,包括人体必需的8种氨基酸,其具有植物清香、清爽的氨基酸香味以及浓郁的类肉汤香气的食品调味料[3-5]。以往,HVP在调味品行业主要用于酱油和酱腌菜的生产;近年来,随着食品工业的发展,特别是在方便面、鸡精、鸡粉、休闲食品、香精香料等食品加工业中,HVP与其产品的需求量越来越大,成为公众的日常食用调味佳品[6,7],在食品工业领域中得到广泛的应用和广阔的市场前景。
HVP在使用盐酸作为催化剂、经酸碱中和后,势必生成较多的氯化钠(食盐)。但是,近年来“健康生活从低盐开始”的理念在国际上受到广泛关注,国内的营养学家正在倡导低盐饮食。“低盐”已经慢慢成为被人们所接受的健康膳食理念[8]。营养学家一直呼吁消费者在饮食中限盐,以减少钠的摄入。虽然许多天然食品里都含有钠成分,但盐是摄入钠的最主要来源。目前,国外一些食品企业已经在研究降低食品中的钠含量。
酸水解过程的控制是HVP生产的重点环节[9,10]。常规酸法水解植物蛋白生产工艺为了达到较高的蛋白水解率,水解所用盐酸浓度较高,所得水解液中盐含量往往很高,但在生产实践中,仍缺乏控制和降低氯化钠含量的良好工艺[11-13]。本文采用响应面设计法优化了低酸条件下水解大豆蛋白的工艺,旨在保证较高蛋白水解率的前提下,降低水解蛋白液中的氯化钠含量。
1 材料与方法
1.1 材料与试剂
脱脂大豆(食品级):金海粮油有限公司;盐酸(食品级)、液碱(食品级):滨化集团股份有限公司;纯碱(食品级):山东海化股份有限公司。
1.2 仪器与设备
K-360 BUCHI凯氏定氮仪 上海岛通应用科技有限公司;雷磁PHS-3E酸度计 上海仪电科学仪器股份有限公司;SHD-Ⅲ循环水式多用真空泵 保定高新区阳光科教仪器厂;JJ-1精密增力电动搅拌器 常州国华电器有限公司;98-I-B型电子调温加热套 天津市泰斯特仪器有限公司;JA51001电子精密天平 上海精天电子仪器有限公司。
1.3 方法
1.3.1 工艺流程
脱脂大豆、盐酸、水→水解→冷却→中和→过滤→HVP液[14-16]。
1.3.2 检测方法
氨基酸态氮(以N计,g/100 g):参照GB 5009.39-2003;
总氮(以N计,g/100 g):参照GB 5009.5-2010;
氯化钠(g/100 g):参照GB 5009.39-2003。
1.4 蛋白水解率计算

式中:A1为水解液中氨基酸态氮含量,g/100 g;A2为水解液中总氮含量,g/100 g。
1.5 单因素试验
1.5.1 液固比的确定
选取盐酸浓度15%、水解时间26 h、水解温度95 ℃,测定不同液固比1∶1,1.5∶1,2∶1,2.5∶1,3∶1条件下的蛋白水解率,重复试验3次。
1.5.2 盐酸浓度的确定
选取液固比2∶1、水解时间26 h、水解温度95 ℃,测定不同盐酸浓度12%,15%,17%,20%水平条件下的蛋白水解率,重复试验3次。
1.5.3 水解时间的确定
选取液固比2∶1、盐酸浓度15%、水解温度95 ℃,测定不同水解时间24,26,28,30,32 h水平条件下的蛋白水解率,重复试验3次。
1.5.4 水解温度的确定
选取盐酸浓度15%、液固比2∶1、水解时间30 h,测定不同水解温度90,95,100,105,110 ℃水平条件下的蛋白水解率,重复试验3次。
1.6 响应面优化试验
选取盐酸浓度、液固比、温度、时间为考察因子,以蛋白水解率为响应值,利用Design Expert 8.0.6进行Box-Behnken试验设计,试验因素水平设计见表1。

表1 Box-Behnken分析因素与水平
1.7 数据处理
采用SPSS 17. 0 统计分析软件对试验数据进行分析,试验结果为3次实验的平均值。
2 结果与分析
2.1 单因素试验结果
2.1.1 液固比对蛋白水解率的影响
液固比对蛋白水解率的影响见图1。

图1 液固比对蛋白水解率的影响
由图1可知,当液固比由1∶1增加至2∶1时,蛋白水解率呈显著增加(P<0.05),液固比继续增大,蛋白水解率增加缓慢。可能因为随着盐酸用量增大,脱脂大豆中的蛋白质与盐酸溶液接触得更加充分,蛋白更易被盐酸水解,蛋白水解率更高[17,18]。但是达到一定盐酸溶液量,蛋白已基本完全被水解,再增加盐酸溶液量,蛋白水解率增加得并不明显;同时液固比过高,会造成后期水解液成品含盐量高以及盐酸溶液的浪费;观察水解液的状态,在液固比2∶1生成的水解液氨基酸无明显的析出,溶液状态相对稳定。因此,选取液固比2∶1进行下一步实验。
2.1.2 盐酸浓度对蛋白水解率的影响
根据氯化钠生成机理,盐酸浓度是主要决定的因素之一,从控制蛋白水解液中盐含量角度出发,在蛋白水解率满足一定要求条件下,应尽量选择较低浓度盐酸[19-21]。盐酸浓度对蛋白水解率的影响见图2。

图2 盐酸浓度对蛋白水解率的影响
由图2可知,当盐酸浓度由12%升至15%,蛋白水解率显著增加(P<0.05)。盐酸浓度在15%~20%,随着盐酸浓度的提高,蛋白水解率增加程度变化缓慢。因此,选取盐酸浓度15%进行下一步试验。
2.1.3 水解时间对蛋白水解率的影响
水解时间对蛋白水解率的影响见图3。
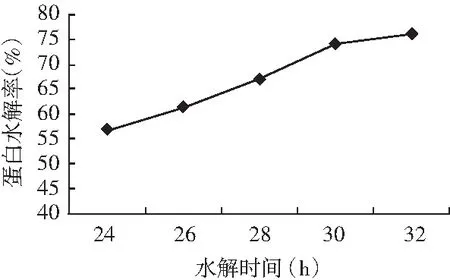
图3 水解时间对蛋白水解率的影响
由图3可知,蛋白水解率随水解时间延长而不断增加。在24~30 h内,随时间增加,蛋白水解率呈现显著升高(P<0.05);超过30 h,蛋白水解率增幅减小。水解开始时,随着时间的延长,蛋白迅速被水解,氨基酸被释放到溶液中,溶液中氨基酸态氮不断升高[22]。再延长水解时间,由于蛋白基本完全被水解,因此蛋白水解率不再增加或增加缓慢。因此,水解时间为30 h较为适宜。
2.1.4 水解温度对蛋白水解率的影响
水解温度对蛋白水解率的影响见图4。

图4 水解温度对蛋白水解率的影响
由图4可知,在90~105 ℃范围内,蛋白水解率随着温度的升高而逐渐增大(P<0.05),水解温度继续升高,蛋白水解率略有降低。可能因为随着水解温度升高,越来越多的游离氨基酸与原料中少量醛基发生了美拉德反应,反应产物可能会破坏水解液风味,从而降低水解液中游离氨基酸含量。温度过高,将消耗过多的能量,增加生产成本。
2.2 响应面设计法对蛋白水解条件的优化[23,24]
2.2.1 响应面试验设计与结果
试验方案及相应结果见表2。利用Design Expert 8.0.6对表2中试验数据进行多元回归拟合,回归分析结果见表3。

表2 Box-Behnken 试验设计及结果

表3 回归方程方差分析
由表3可知,蛋白水解率所建立的回归模型P<0.01,表明模型的拟合度较好。失拟项P>0.05,表明试验的误差较小,未控制因素对结果的干扰很小,拟合不足以被否定,可对回归模型进一步进行拟合检验;R2=0.9868,说明实际情况与该方程拟合良好,正确反映了各因素与蛋白水解率之间的关系。水解温度、液固比主效应显著,各因素对蛋白水解率的影响程度大小为X2(液固比)>X4(水解温度)>X3(水解时间)> X1(盐酸浓度),各因素二次项对蛋白水解率均有显著影响。经过拟合,回归方程为:
Y=71.06-0.092X1+3.65X2-0.47X3+2.06X4-1.87X1X2-4.60X1X3-0.88X2X3-3.75X2X4+3.48X3X4-3.05X12-3.46X22-6.71X32-0.90X42。
2.2.2 响应面分析
利用Design Expert 8.0.6做不同因素响应面图,结合方差分析表,盐酸浓度、水解时间、液固比、水解温度4个因素及其交互作用对蛋白水解率的影响见图5~图10。

图5 盐酸浓度与液固比的交互作用对蛋白水解率的影响
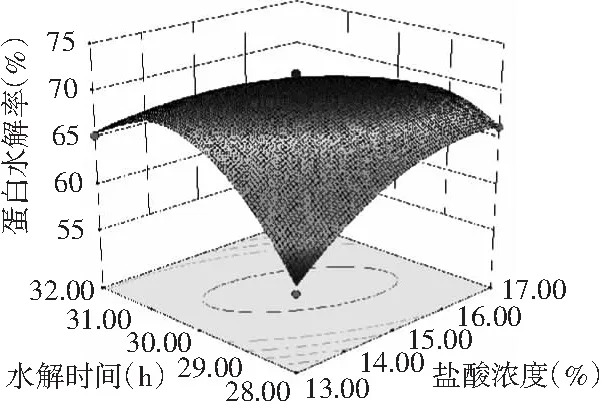
图6 水解时间与盐酸浓度的交互作用对蛋白水解率的影响
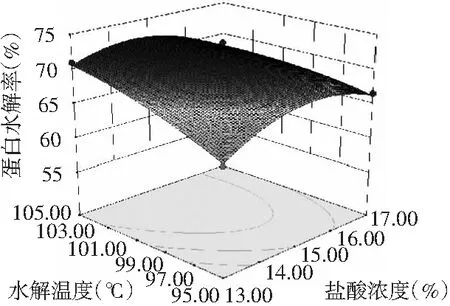
图7 水解温度与盐酸浓度的交互作用对蛋白水解率的影响
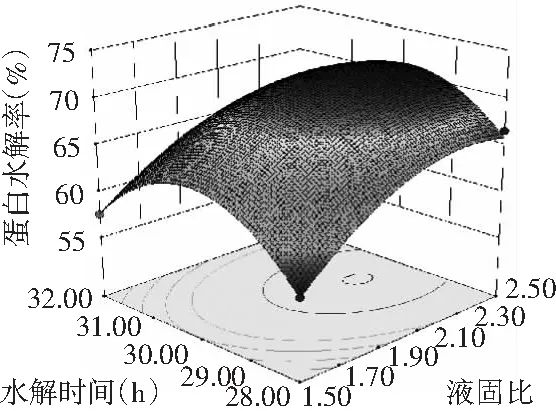
图8 液固比与水解时间的交互作用对蛋白水解率的影响

图9 水解温度与水解时间的交互作用对蛋白水解率的影响

图10 水解温度与液固比的交互作用对蛋白水解率的影响
由图5~图10可知,液固比与盐酸浓度、水解时间与盐酸浓度、水解温度与盐酸浓度、水解温度与液固比、水解温度与时间之间交互作用对蛋白水解率的影响均为极显著。
2.2.3 工艺条件优化与验证试验
利用Design Expert 8.0.6得到模型的极值点坐标,换算得到预测真实值,最终得出蛋白提取率最高的一组如下:盐酸浓度13.84%、液固比2.05∶1、水解时间30.84 h、水解温度105 ℃。为了实际操作方便,将水解条件修正为:盐酸浓度14%、液固比2∶1、水解时间31 h、水解温度105 ℃,在此条件下做3次重复试验,实际蛋白水解率为(73.6±0.03)%,与预测值73.3%接近,可以满足生产的要求,说明试验优化得到的蛋白水解条件具有实用价值。
在上述水解工艺条件下,对水解产品的氯化钠含量进行检测,得到此产品的氯化钠含量为(12.5±0.02)%,而常规水解工艺为16%~18%。由此可知,此低酸水解工艺使产品中的氯化钠含量较常规水解工艺降低了22%~31%。
3 结论
液固比、水解温度对蛋白水解率影响的主效应显著,各因素对蛋白水解率影响程度的大小顺序为:液固比>水解温度>水解时间>盐酸浓度。低酸水解大豆蛋白最佳优化工艺条件为:盐酸浓度14%,液固比2∶1,水解时间31 h,水解温度105 ℃,蛋白水解率为73.6%,此工艺可满足水解生产的要求。水解液中氯化钠含量约为12.5%,比传统的水解工艺要低很多。
[1]高文宏,李国基,于淑娟,等.水解植物蛋白[J].食品科学,2000,21(12):167-171.
[2]SB 10338-2000,酸水解植物蛋白调味液行业标准[S].
[3]Mahta M, Saeed M, Mohamad R E, et al. Purification and identification of antioxidant and ACE-inhibitory peptide fromSaccharomycescerevisiaeprotein hydrolysate[J].Journal of Functional Foods,2015,19:259-268.
[4]Kwok O W, Yock H C, Huay L S. 3-Monochloropropane-1,2-diol (3-MCPD)in soy and oyster sauces: occurrence and dietary intake assessment[J].Food Control,2006,17(5):408-413.
[5]Chanikan S, Natta L, Orapin K.Physicochemical and flavor characteristics of flavoring agent from mungbean protein hydrolyzed by bromelain[J].Journal of Agricultural and Food Chemistry,2011,59(15):8475-8483.
[6]Su G W, Zheng L, Cui C, et al. Characterization of antioxidant activity and volatile compounds of Maillard reaction products derived from different peptide fractions of peanut hydrolysate[J].Food Research International,2011,44(10):3250-3258.
[7]Koo S H, Bae I Y, Lee S Y, et al. Evaluation of wheat gluten hydrolysates as taste-active compounds with antioxidant activity[J].Journal of Food Science and Technology, 2011,51(3):535-542.
[8]高行恩, 赵敏, 季倩楠.健康饮食理念下调味方式的改革与创新[J].中国调味品,2015,40(1):128-130.
[9]Shinobu S, Ryosuke N, Reiko A, et al. Experimental assessments of the cross-reactivity of IgE from patients sensitised with acid-hydrolysed wheat protein in a cosmetic soap[J]. Clinical and Translational Allergy, 2015, 5(3):16.
[10]Martin A M. Influence of degree of hydrolysis on the functional properties of cowpea protein hydrolysates[J].Journal of Food Processing and Preservation, 2015, 39(6): 2386-2392.
[11]赵贵兴,陈霞.大豆水解蛋白调味料研制[J].大豆科学,2002,21(3):234-236.
[12]王辛,蒋蕴珍,周晔艳,等.酸水解小麦蛋白技术的研究[J].现代面粉工业,2009(3):42-44.
[13]严群芳,王恬, 张莉莉.酸水解大豆蛋白制取复合氨基酸水解液的研究[J].饲料工业,2006,27(11):18-19.
[14]刘立新,李永歌.加工工艺对酸水解植物蛋白液色泽的影响[J].中国调味品,2014,39(6):83-85.
[15]徐满苹.水解植物蛋白工艺[J].食品工业科技,2000(3):59.
[16]刘立新,李永歌,杨雪娟.酸水解植物蛋白热反应制备烤牛肉香基的工艺研究[J].中国调味品,2015,40(6):88-93.
[17]金青哲,刘元法,周伟.低含量3-氯-1,2-丙二醇的水解植物蛋白生产工艺优化[J].食品科学,2005,26(5):179-182.
[18]Rail A K, Nived C, Sakhare P Z, et al. Optimization of acid hydrolysis conditions of delimed tannery fleshings by response surface method[J].Journal of Scientific & Industrial Research,2009,68(11):967-974.
[19]魏然,陈义伦,邹辉,等.超声波提取条件对圆铃大枣多糖提取率的影响[J].食品与发酵工业,2013,39(11):120-126.
[20]周小双,王锦旭,杨贤庆,等.响应面法优化合浦珠母贝糖胺聚糖提取工艺[J].食品与发酵工业,2016,42(1):238-243.
[21]Choo W S, Kharidah M, Salmah Y, et al. The optimization of conditions for the production of acid-hydrolysed winged bean and soybean proteins with reduction of 3-monochloropropane-1,2-diol (3-MCPD)[J]. International Journal of Food Science and Technology,2004,39:947- 958.
[22]Kechaou E S, Berge J P, Pascal J, et al. Optimization of common cuttlefish (Sepiaofficinalis)protein hydrolysate using pepsin by response surface methodology[J].Journal of Aquatic Food Product Technology,2013,24(3):270-282.
[23]王欢,黄国清,肖军霞.玉米蛋白粉水解工艺的研究[J].粮油食品科技,2013,21(5):8-11.
[24]Zhang H Y, Tian T, Chen H. Optimization of enzymatic hydrolysis for protein from black bean by response surface methodology[J].Advanced Materials Research,2013,781:875-879.
Response Surface Optimization of Soybean Protein Production Technology with Low Hydrochloric Acid Concentration
ZHENG Jiao-jiao,WEI Ran,LI Yong-ge
(Baoding Waychein Food Science and Technology Co., Ltd., Baoding 071000,China)
Focus on the acid hydrolysis process of soybean protein under the conditions of low concentration of acid, on the purpose of reducing the content of NaCl. Analyze the influence of hydrochloric acid concentration, liquid-solid ratio, hydrolysis time and hydrolysis temperature on protein hydrolysis rate. The results indicate that the main effect of liquid-solid ratio and hydrolysis temperature is significant. The order of the influence on protein hydrolysis rate is liquid-solid ratio,hydrolysis temperature,hydrolysis time and hydrochloric acid concentration. The interaction between liquid-solid ratio and hydrolysis time is not significant. The influence of interaction between other factors on the protein hydrolysis rate is significant. The optimal hydrolysis conditions are hydrochloric acid concentration of 14%,liquid-solid ratio of 2∶1, hydrolysis time of 31 h and hydrolysis temperature of 105 ℃. Under such conditions, the hydrolysis rate of protein is 73.6%. The NaCl content in the hydrolysate is about 12.5%, and it is reduced by 22%~31% compared with the traditional hydrolysis process.
defatted soybean; response surface methodology; hydrolysis process; protein hydrolysis rate; sodium chloride (NaCl)
2016-11-18
郑姣姣(1979-),女,河北保定人,助理工程师,硕士,研究方向:调味品。
TS201.1
A
10.3969/j.issn.1000-9973.2017.05.018
1000-9973(2017)05-0084-06

