水溶性聚磷酸铵的合成工艺进展*
徐保明,徐思思,唐 强,许庆博,时 爽
(湖北工业大学,湖北武汉430068)
水溶性聚磷酸铵的合成工艺进展*
徐保明,徐思思,唐 强,许庆博,时 爽
(湖北工业大学,湖北武汉430068)
水溶性聚磷酸铵具有高效、经济、安全的特点,在工农业上有着重要的应用,研究其大规模生产成为磷化工产业的重要研究课题。综述了水溶性聚磷酸铵目前主流的生产方法:磷酸氨化法、聚磷酸氨化法、磷酸铵盐-五氧化二磷-氨气聚合法、磷酸尿素缩合法、磷酸铵盐尿素缩合法及磷酸脲法的生产工艺。归纳总结了各种生产方法的优缺点,指出尿素缩合法更优于氨气聚合法,并对未来发展进行了展望。
聚磷酸铵;水溶性;合成工艺
聚磷酸铵又称多聚磷酸铵或缩聚磷酸铵,简称APP。其分子式为:(NH4)n+2PnO3n+1[1],其中氮、磷元素含量较高。根据聚合度的大小,可分为低聚、中聚、高聚。聚合度越低其水溶性越高,反之水溶性越低,当n>20时,为水难溶的APP,当n<20时,为水溶性高的APP[1]。因其水溶性的不同,聚磷酸铵的应用也十分广泛。水溶性聚磷酸铵,由于其熔点和烧结点比较低,在较低温度下可以快速熔化,渗透到可燃物的气孔内,使可燃物与空气隔离,并进一步聚合再分解,形成膜状物,迅速覆盖在可燃物的各个层面,使火焰熄灭,从而达到灭火的目的[2]。因此可用于制作干粉灭火剂,应用于纸张、织物、木材等材料的灭火上。另外,由于其化学性质稳定,pH接近中性,溶解性好;且含植物所需氮、磷元素高,对金属离子有较强的螯合作用,也可用于制作液体复合肥料,并通过逐步水解,被植物很好地吸收利用,可作为一种缓溶性长效肥料[3]。
国外对水溶性聚磷酸铵的研究开始得比较早。20世纪70年代初,美国TVA公司在管式反应器中对P2O5质量分数为54%的湿法磷酸进行氨化,产品为含有水溶性聚磷酸铵的熔融体[4]。20世纪70年代末,日本、前苏联等国家开始大量生产水溶性聚磷酸铵并应用于农业上[5]。20世纪80年代末,印度RCE公司着手于开发颗粒状水溶性聚磷酸铵肥料工艺[6]。在中国,对这方面的研究相对较晚,20世纪80年代,开始了对水溶性聚磷酸铵的合成工艺及其应用的研究[7]。市场上出售水溶性聚磷酸铵的厂家较少,价格比较昂贵且产品性能也不是很稳定。对水溶性聚磷酸铵的纯化和精制还需要进一步研究。
目前国内外比较常用的水溶性聚磷酸铵的合成方法主要有氨气聚合法和尿素缩合法。其中氨气聚合法包括:磷酸氨化法、聚磷酸氨化法和磷酸铵盐-五氧化二磷-氨气聚合法;尿素缩合法包括:磷酸尿素缩合法、磷酸铵盐尿素缩合法和磷酸脲法。
1 氨气聚合法
1.1 磷酸氨化法
磷酸氨化法采用磷酸为原料,与无水氨按照一定的比例混合,聚合之后,经固化、冷却得到产品。
V.Archie等[8]以湿法磷酸[w(P2O5)=60%~70%]与无水氨为原料,在加长管式反应器内,加热至300℃,充分接触5~60 s,制得的产品聚磷酸铵质量分数为60%~90%,并且溶解度较高。该反应利用加长管式反应器来增加其氨化程度,加长管式反应器局部冷却可得到不黏易碎的固体产品,并且未反应的氨气能够得到循环利用。
H.Hahn[9]研究聚磷酸铵的合成时研制出多段下降薄膜式反应器。采用物质的量比约0.8~1.0的氨气与湿法磷酸[w(P2O5)=54%~74%]进行氨化反应,控制温度在260~310℃。在反应器内,液态的湿法磷酸由反应器上部加入,加热的气态氨由反应器底部进入,两者呈逆流状态,物料更充分地接触。接触过程中,磷酸与气态氨中和,产生的中和热用来浓缩磷酸,并使产物进一步缩聚,得到聚磷酸铵。在多段下降薄膜式反应器内,各段温度各不相同,从上往下温度逐渐降低,形成的液膜能够起到保护器壁,减少结垢的作用。
林明等[10]采用质量分数为30%~80%的湿法磷酸与氨气反应,加热到150~300℃,制得全水溶性低聚合度聚磷酸铵水溶液。该法能降低生产成本,得到的水溶性聚磷酸铵产品中水不溶物质量分数< 0.18%,可用于飞机喷洒森林灭火和液体肥料等方面。
磷酸氨化法生产的水溶性聚磷酸铵能用于制作干粉灭火剂、液体肥料及其他配制剂等,具有实现低成本大规模连续化生产的应用前景,但是由于产品的运输条件要求高,得到的产品会溶解少量氨气和不溶性聚磷酸铵,产品的聚合度不稳定,想要进一步扩展应用还要继续在提纯和浓缩上进行工艺改进。另外,中国湿法磷酸的工艺尚有不足,制得的产品所含杂质较高,杂质在反应过程中易形成沉淀或使容器表面结垢,使反应物难以聚合,不利于反应的进行。因此,目前在中国利用湿法磷酸氨化制水溶性聚磷酸铵的方法实施起来尚存在困难。
1.2 聚磷酸氨化法
聚磷酸一般含75%~85%(质量分数)的P2O5。聚磷酸与气态氨按一定的比例加入,在高温高压下进行聚合反应,制取聚磷酸铵产品。
P.H.Travis[11]提出了由聚磷酸直接氨化制聚磷酸铵的工艺流程。聚磷酸和无水氨分别经管道进入反应器,搅拌使聚磷酸与无水氨充分混合,进行聚合反应,产物经固化、冷却、粉碎即得产品,所得产品聚合度小于10,可用于制作灭火剂和液体肥料。反应过程中,产物的组成受温度、压力、反应时间和搅拌速度的影响,由于聚磷酸氨化放热,反应器内部需安装冷却管进行冷却,但温度不能过低,以防止产物粘在冷却管壁上。反应器内氨分压随着搅拌速度的加快而增加,氨分压增大,有利于反应进行,氨化程度也相应增大。随后对该工艺再次进行了优化,采用聚磷酸[w(P2O5)=83%~90%]为原料,其他条件相同,得到的熔融态的产物,静置冷却后,溶解、过滤、干燥得成品,滤液副产物可作为液体肥料。
古思廉等[12]开发了一种聚磷酸铵的生产工艺。聚磷酸铵与缩合剂以质量比为1∶1混合均匀加入反应器,在温度为100~500℃、压力为0.01~0.35 MPa的条件下,反应5~210 min,得到高纯度聚磷酸铵。随后改变聚磷酸纯度,选择适宜的缩合剂,并在适宜的条件下,制得工业需要的不同品质的聚磷酸铵。该方法生产控制方便,能耗低,产率高,有利于实现大规模连续生产。
聚磷酸氨化法采用聚磷酸为原料,产品质量稳定,带入系统的杂质量少,同时聚磷酸铵不含游离水,既保证了合成反应的进行又降低了能耗,还减轻了物料对设备材质的腐蚀。
1.3 磷酸铵盐-五氧化二磷-氨气聚合法
该法采用磷酸铵盐与五氧化二磷混合,并在氨气氛围中聚合,其原理为:
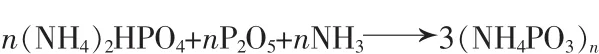
在氨气环境中,以磷酸铵盐与五氧化二磷混合,采用单一反应器,适当改变反应温度,可得到平均聚合度不同的产物[13]。张爱民等[14]研究了一种连续生产聚磷酸铵的工艺。将液氨在气罐中汽化,并在压力为0.05~1.5 MPa,温度为0~350℃的条件下通入长径比为20~100的螺杆挤出机。将物质的量比为0.1~10的五氧化二磷和磷酸氢二铵从反应器的侧加料口加入,在25~400℃、转速为5~600 r/min条件下,聚合0.5~60 min,通过气固分离器获得聚磷酸铵产品,该方法制得的聚磷酸铵包含水溶性聚磷酸铵和部分难溶的聚磷酸铵。
该法工艺路线短、操作较简便。采用五氧化二磷作缩合剂,无大量废气排出,得到产品质量较好。但是五氧化二磷的活性较大,反应不易控制。此外,由于氨气的存在,还要求反应容器为密闭体系且耐高温高压,能耗大,成本高。并且需安装搅拌装置,以防止反应过程中产生粘稠的中间产物,使产物产率降低,因此所需设备费用较高,不适宜大规模生产。
氨气聚合法中氨气参与缩合反应,要求反应体系密闭,对反应条件和设备的要求很高,能耗高,且安全性较低对于连续大规模的生产投资较大。不适宜于大规模生产水溶性聚磷酸铵。
2 尿素缩合法
2.1 磷酸尿素缩合法
磷酸和尿素按一定物料比例进行混合,加热、发泡、聚合、冷却和固化得到白色干燥的成品。其反应原理为:
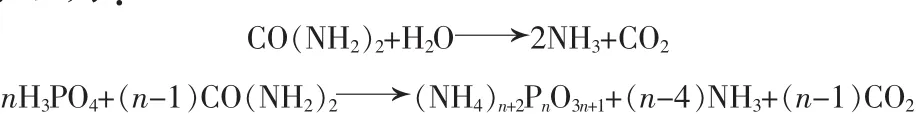
胡炳成等[15]以质量分数为85%的化学纯磷酸和尿素为原料,经聚合反应制得聚磷酸铵。反应过程中随着反应时间的增长、反应温度的升高,聚合度增加;随着反应物物质的量比的增加,聚合度增加趋缓,当反应物物质的量比[n(尿素)∶n(磷酸)]大于2.2时,产物聚合度下降,产物难以固化,影响产率。最终确定在尿素和磷酸物质的量比为2.0、反应温度为130℃的条件下,反应 14~16 min,得到平均聚合度约为9的产物,产物熔点为141℃,烧结点为183℃,可以用来制作干粉灭火剂。
张长水等[16]探讨了聚磷酸铵的合成工艺。采用磷酸与尿素进行正交实验,实验表明,若尿素用量过少,缩合反应不完全;尿素用量过多,则不易固化,且氨利用率较低。预聚合温度低于100℃时,反应较难进行,预聚合不充分;温度升高,反应速率加快,高于200℃则出现局部粘黏。固化时间太短、固化温度过低,聚磷酸铵不能充分发泡固化;固化时间过长、固化温度过高会使聚磷酸铵有轻微分解,二者都会引起聚磷酸铵聚合度降低。并且高温下尿素会迅速分解,生成大量的NH3和CO2等气体,使得反应装置中产生大量泡沫。造成装置溢料,导致产量过低,需另外设置较大的废气回收装置,使生产过程繁琐。实验确定最佳工艺为:尿素和磷酸物质的量比为1.7∶1、预聚合温度为180℃、固化温度为240℃、固化时间为160 min,得到产品为白色固体。
磷酸尿素法,工艺简单、过程参数易于控制、投资少、成本低且操作安全,是中小企业生产聚磷酸铵常用的方法。采用的磷酸原料中,含有一定量的水,使得产品聚合度较低,所得产品易溶于水,可用于生产水溶性聚磷酸铵,并用在工业灭火剂和液体肥料上。另外,由于尿素易分解,产生大量氨气和二氧化碳气体,使反应过程中大量发泡,易造成溢料,物料损失,影响生产效率,该方法还需要进一步改进。
2.2 磷酸铵盐尿素缩合法
将磷酸铵盐和尿素按一定比例进行混合,在高温下聚合,冷却、粉碎得到聚磷酸铵产品。其反应原理为:

K.O.Knollmueller[17]探究了聚磷酸铵合成工艺,以磷酸铵和尿素为原料,得到聚合度较低、水溶性好的聚磷酸铵。研究表明,当磷酸铵与尿素物质的量比高于1.2∶1时,主要产品是焦磷酸铵或三聚磷酸铵。而要得到聚合度大于6的水溶性聚磷酸铵,磷酸铵和尿素的物质的量比为(1~1.2)∶1,并在常压或减压、温度为145~160℃条件下进行反应。这为水溶性聚磷酸铵的生产提供了理论依据。
付秋菠等[18]采用正交实验研究合成聚磷酸铵的工艺条件,并对反应条件进行了优化。研究表明,反应温度对有效磷的含量和聚合度影响较小,对氨氮含量影响最大,选择最佳反应温度为160℃。反应时间对氨氮含量影响较小,对有效磷的含量和聚合程度的影响较小,保证反应完全,选择最佳时间为1.5h。原料配比对氨氮含量影响程度适中,对有效磷的含量和聚合度影响程度最大,选择原料配比为磷酸二氢铵和尿素物质的量比为1∶(1.1~1.2),得到的产物中氨氮质量分数为16.65%,有效磷质量分数为70.20%。
雷婷等[19]研究了不同反应器对聚磷酸铵缩合反应的影响,选取磷酸二氢铵和尿素为原料。分别采用微波炉和马弗炉为反应器,研究工艺条件对产物聚合度的影响。研究表明,采用微波反应器对缩合反应起到了强化作用,使缩合反应可以在相对较低的温度下进行,并缩短反应时间。加入物质的量比为1∶1.1的磷酸二氢铵和尿素,在200℃下,反应40 min,所得产品中P2O5的质量分数为69.05%,氮质量分数为14.13%。
磷酸铵盐尿素聚合过程中,产品质量和聚合度都较好,但反应温度高于磷酸与尿素的聚合,实际生产中需要的能耗大。而反应结束后,为了得到更纯的产品,还需脱除液体石蜡,反应步骤较复杂,生产成本较高,对技术要求也更高。
2.3 磷酸脲法
磷酸脲是磷酸与尿素制备磷酸铵的中间产物,以磷酸脲和尿素按一定比例混合制备低聚磷酸铵,其原理如下:

马赛等[20]以自制磷酸脲与尿素为原料制取聚磷酸铵。研究表明,随着磷酸脲与尿素物质的量比增大、反应时间增加及反应温度升高,聚磷酸铵的聚合度都呈现先升高后降低的趋势。最终得到的最佳合成条件为:磷酸脲与尿素的物质的量比为2.2∶1,温度为215℃,反应时间为50 min。在最佳条件下反应,所得到的产品聚合度为14.56,溶解度为0.018 3 g/g。可用于制作高浓度水溶性氮磷复合肥。尿素在此反应中作为缩合剂和氨化剂,尿素量过少,缩合反应不完全,产物的聚合度低,随着尿素量的增加,缩合反应逐渐完全,聚合度也随之升高;但当尿素过多时,加重了发泡的影响,并且可能有缩二脲等副产物的生成。
磷酸脲法以磷酸脲为原料,能得到纯度和聚合度较好的水溶性聚磷酸铵。有效地解决了常规方法以磷酸为原料导致的运输、储存问题,降低了成本和能耗,且比传统的加氨气聚合法更加安全环保,整个环节步骤简练容易操作,但是磷酸脲不易制得,且对条件要求严格。该法主要是通过物质的量比来控制聚磷酸铵合成的聚合度,所以对浓度比要求也高,成本也相应增加。
与氨气聚合相比,磷酸尿素缩合法、磷酸铵盐尿素缩合法、磷酸脲法等尿素缩合方法中,尿素既是氨源,维持反应体系的氨分压,防止聚磷酸铵分解;又起到缩合剂的作用,促进了原料的脱水缩合。尿素易分解生成大量氨气和二氧化碳气体,使聚合过程中形成大量泡沫造成溢料,因此反应过程中仍需适当控制气体的分压。另外,尿素缩合法对设备的要求较低,工艺比较简单,操作安全,且得到的产品是聚合度更低的短链APP,产品更适宜于制作农用产品。
3 结语
水溶性低聚磷酸铵目前通过氨气聚合法和尿素缩合法制备出的产品都能够满足市场要求,其中氨气聚合法由于原料需要使用氨气,故反应必须在密闭体系中完成,对生产设备及操作条件要求较高。而尿素缩合法工艺简单易行、设备要求低、操作简便、原料易得,更适于生产水溶性聚磷酸铵。由于国内对水溶性聚磷酸铵合成研发较晚,故今后的研究重点是研发以尿素缩合法为代表的、能有效环保的、低成本、适宜于大规模生产的新生产技术。使水溶性聚磷酸铵能够更广泛地应用到农业上和工业灭火剂上。
[1] 崔小明,聂颖.聚磷酸铵的生产工艺及改性技术进展[J].杭州化工,2007,37(4):14-17.
[2] 尚成新,杨帅.水溶性聚磷酸铵的纸张阻燃[J].杭州化工,2010,40(1):26-28.
[3] 王方进.低聚磷酸铵肥料的合成及其在土壤中的转化研究[D].山东:山东农业大学,2014.
[4] Meline R S,Lee R G.Process for the production of ammonium polyphosphate:US,3733191A[P].1973-05-15.
[5] 王连祥.农用肥料聚磷酸铵的制备与应用[J].磷肥与复肥,2008,23(2):49-50.
[6] 林明,印华亮.磷化工产业结构调整方向研究[J].无机盐工业,2016,48(5):6-8.
[7] 王连祥.新型肥料聚磷酸铵生产技术与应用初探[J].化肥工业,2008,35(4):16-17.
[8] Archie V,Donald W.Liquid fertilizer from batchwise ammoniation
of wet-process phosphoric acid:US,3264087A[P].1966-08-02. [9] Hahn H.Process for the manufacture of ammonium polyphosphate:US,4104362A[P].1978-08-01.
[10] 林明,印华亮.一种用湿法磷酸制取全水溶性聚磷酸铵水溶液的方法:中国,104528682A[P].2015-04-22.
[11] Travis P H.High-analysis ammonium polyphosphate fertilizer:US,3171733A[P].1965-03-02.
[12] 古思廉,李云东,马兆宁,等.一种聚磷酸铵的生产方法:中国,1651488A[P].2005-08-10.
[13] 张亨.聚磷酸铵的性质及合成研究进展[J].杭州化工,2012,42(1):22-27.
[14] 张爱民,李云勇,周涛,等.一种聚磷酸铵的连续生产方法:中国,1994873A[P].2007-07-11.
[15] 胡炳成,吕春绪,刘祖亮,等.低聚磷酸铵的合成及其在灭火剂中的应用[J].爆破器材,2001,30(6):30-33.
[16] 张长水,叶勇,何晓霞,等.正交法优化聚磷酸铵的合成工艺研究[J].应用化工,2008,37(6):592-594.
[17] Knollmueller K O.Anhydrous ammonium polyphosphate process:US,3333921A[P].1967-08-01.
[18] 付秋菠,苗红波,吕莉,等.聚磷酸铵合成工艺条件研究[J].无机盐工业,2006,38(3):28-29.
[19] 雷婷,李军,王珊.微波强化聚磷酸铵聚合的研究[J].无机盐工业,2008,40(11):24-25.
[20] 马赛,刘咏,化全县,等.水溶性聚磷酸铵的合成工艺研究[J].化工矿物与加工,2014,43(10):14-17.
Synthesis progress of water-soluble ammonium polyphosphate
Xu Baoming,Xu Sisi,Tang Qiang,Xu Qingbo,Shi Shuang
(Hubei University of Technology,Wuhan 430068,China)
Water-soluble ammonium polyphosphate has the characteristics of high efficiency,economy,and safety.It has important application in industry and agriculture,and its mass production has become an important research subject of phosphorus chemical industry.The current mainstream synthesis processes of water-soluble ammonium polyphosphate were summarized,which included phosphoric acid ammoniation method,poly-phosphoric acid ammoniation method,ammonium phosphate-phosphorus pentoxide-ammonia polymerization method,phosphoric acid-urea condensation method,ammonium phosphate-urea condensation method,and urea phosphate method.The advantages and disadvantages of each process were reviewed.The analysis showed that the urea condensation process was more superior to ammonia polymerization process.And the future development was prospected.
ammonium polyphosphate;water-soluble;synthesis process
TQ126.35
A
1006-4990(2017)04-0005-04
2016-10-23
徐保明(1966— ),男,硕士,教授,从事新材料合成技术与应用研究,获得中国授权发明专利7项,发表论文70余篇。
湖北省教育厅产学研重大项目(CXY2009A010);湖北省自然基金重点项目(2010CDA020)。
联系方式:xubaoming897@yeah.net

