油酸甲酯催化加氢制备生物烷烃的热力学分析
孙培永,李梦晨,刘森,戚琪,张胜红,姚志龙
油酸甲酯催化加氢制备生物烷烃的热力学分析
孙培永1,李梦晨2,刘森1,戚琪1,张胜红1,姚志龙1
(1北京石油化工学院化学工程学院,恩泽生物质精细化工北京市重点实验室,北京 102617;2中国石油天然气集团公司石油化工研究院,北京 102206)
采用Benson基团贡献法对油酸甲酯加氢脱氧、加氢脱羰和加氢脱羧制备生物烷烃的热力学进行了分析,计算了613~653 K温度区间内油酸甲酯加氢体系的反应热、反应熵变、反应Gibbs自由能变和标准平衡常数,在此基础上采用PRO/Ⅱ软件中的平衡反应器模型分析了温度对油酸甲酯加氢产物分布的影响并和实验数据进行了对比验证。结果表明,油酸甲酯加氢脱氧、加氢脱羧和加氢脱羰制备生物烷烃的反应均为放热反应,放热量依次递减,各反应在613~653K范围内均能够自发进行且反应完全。升高温度能够提高平衡产物中油酸甲酯加氢脱羰/羧产物的选择性,降低温度则有利于加氢脱氧产物的选择性,加氢脱氧与脱羰/羧产物选择性的比例随温度从613 K升高到653 K相应从1.92降低到0.56,与实验测得的反应数据变化趋势吻合。
油酸甲酯;加氢;生物烷烃;热力学;基团贡献法;模拟
引 言
可再生生物质的能源化利用是解决目前过度使用化石能源引发的环境恶化及未来化石能源短缺问题的一个重要方向[1-2]。其中,直接利用生物油脂(主要是植物油脂) 制备液态燃料是一个切实可行的方案,并且已经在欧盟获得大范围的推广[1]。植物油脂具有低硫、低氮、富氧等特点,燃烧热值低,不宜直接用作发动机燃料。但植物油脂,尤其是废弃植物油脂,经热裂解或催化加氢脱氧处理后能够获得在组成、结构和性能方面和传统液态燃料相似的生物烷烃,可直接用作发动机燃料;并且该生物烷烃具有不与民争利、低硫低氮、生产过程二氧化碳低排放、绿色可再生等特点[3]。
废弃植物油脂,由于其来源复杂且收集、运输、存储和加工过程中卫生状况得不到保障,往往含有大量无机盐、重金属粒子、胶质及其他物理杂质[4],不宜直接用作催化加氢的原料。初步除水、除(胶) 杂、脱色、脱臭和脱酸后的废弃油脂在酸或碱催化剂的存在下和甲醇发生酯交换反应可以制备脂肪酸甲酯(FAMEs, 第一代生物柴油)[5-7]。FAMEs的主要成分为油酸甲酯(C18:1FAME)、棕榈油酸甲酯(C16:1FAME) 及其氢化产物硬(软) 脂酸甲酯,和石化柴油相比具有含氧量高、黏度大、热值相对低等缺点[8],限制了其大范围的应用。但废弃油脂酯交换制备FAMEs的过程可以有效去除催化剂较为敏感的金属粒子、胶杂等组分,利于FAMEs的后续加氢脱氧制备生物烷烃[9-12]。相应地,废弃植物油脂经由甲醇酯交换制备FAMEs并以此为平台进一步催化加氢生产生物烷烃、脂肪醇等高附加值产品已经成为废弃油脂利用的一条重要途径。
目前,研究人员对油脂及其衍生物催化加氢制备生物烷烃的反应工艺、动力学和反应路径等内容已经进行了大量的研究[13-15]。相关研究结果表明:油脂及其衍生物在镍基催化剂上的加氢产物主要为直链烷烃,其中的偶数碳正构烷烃为加氢脱氧产物,奇数碳烷烃为加氢脱羧/羰基产物。但油脂及其衍生物催化加氢产物的分布差异较大,如NiMoS/Al2O3催化剂上十八烷的选择性随反应条件的改变可以在20%~80%之间波动。这种变化一方面依赖于催化剂特定的结构和加氢活性,另一方面也说明反应条件,如温度、氢压、空速等,能够显著影响反应的产物分布。而分析反应参数对产物分布的影响并优化反应工艺不仅需要理解反应的动力学和路径,更需要建立实际反应条件下各物质完整的热力学基础数据以从热力学的角度加深对油脂及其衍生物催化加氢反应的认知[16]。
在涉及油脂及其衍生物的化学反应的热力学方面,由于缺乏反应物和产物的基础热力学数据,研究内容鲜有涉及反应的热力学分析,尽管这些数据对化学反应平衡产物的分布、反应路径的分析及反应工艺的改进至关重要。马鸿宾等[17]、张继龙等[18]和李留等[19]在分析甘油三酸酯甲酯化制备油酸甲酯反应热力学的过程中分别采用Benson基团贡献法估算了甘油三酸脂和油酸甲酯的基础热力学数据,计算了甘油三酸酯分步酯交换反应的热力学和平衡常数,为甘油三酸酯制备FAMEs工艺指出了进一步的改进方向。Cheng等[20]利用Joback基团贡献法估算了油酸甘油酯热裂解的热力学,发现在低温下(< 573 K) 容易发生C—O键的断裂,而高温时(>673 K) 更容易发生位的C—C键断裂,与实验观测到的产物分布吻合。Smejkal等[16]采用Joback基团贡献法粗略地估算了菜籽油加氢脱氧制备直链烷烃反应的热力学,结果显示:随反应温度从543 K逐渐升高到623 K,C18产物的选择性从78%提高到82%,C17产物的选择性则从22%降低到18%。而实验结果[16]则证实在相同的反应条件下,C18产物的选择性从92%逐步降低到78%,理论估算结果和实验数据在趋势上的相悖表明在计算含有多种官能团且具有一定空间构型的大分子的热力学数据时Joback基团贡献法仍有待进一步完善。
相比于Joback基团贡献法简单地以官能团划分分子结构[21-22],Benson基团贡献法将物质视作理想气体,在计算其热力学数据时以原子(团) 为中心并兼顾相邻和次邻原子(团) 的影响,同时针对那些不能在基团参数中反映出来的因素(如顺反异构、交叉异构等) 在估算结果中另行修正,具有准确度较高且普适性广的特点[23-27]。为此,本文以油酸甲酯催化加氢制备生物烷烃为模型反应,采用Benson基团贡献法对油酸甲酯及其主要加氢产物的基础热力学数据进行估算,据此进一步计算油酸甲酯催化加氢体系的反应热并分析温度对反应产物分布的影响,为油酸甲酯及其他不饱和油脂催化加氢反应器的设计及相应工艺的优化提供理论依据。
1 实验部分
NiMoS/Al2O3催化油酸甲酯加氢制备生物烷烃的实验在固定床反应管内(20 mm×400 mm ) 进行。实验原料为不饱和脂肪酸甲酯工业品,其中油酸甲酯和棕榈油酸甲酯的含量分别为74%和21%,催化剂NiMoS/Al2O3为实验室自制[28],Ni、Mo和Al的摩尔比为1.00/0.145/3.12。催化剂经预硫化处理后在613~653 K温度区间进行反应,反应压力为2 MPa,原料空速为1 h-1,氢气和甲酯进料的体积比为1000/1 (氢气和油酸甲酯的摩尔比约为19/1),且在原料中添加0.1%(质量)的二硫化碳以维持催化剂的结构和活性稳定。反应产物采用配有HP-5ms (30 m×0.25 mm×0.25 μm) 毛细管色谱柱的Shimadzu 2010气相色谱仪进行分析,原料和反应产物中各组分的含量采用面积归一化法进行计算。
油酸甲酯加氢产物较为复杂,液相产品主要为油酸甲酯HDO产物十八烷,HDC产物十七烷,以及少量烯烃和异构化烷烃;气相产品中主要含有甲烷、水、H2S和CO,反应的总体碳平衡大于96%。油酸甲酯的转化率定义为转化的油酸甲酯的量与其进料量之间的比值,油酸甲酯HDO和HDC的选择性分别通过产品中C18烷烃和C17烷烃的量与转化的油酸甲酯的量比值进行计算。具体计算见式(1)~式(3)
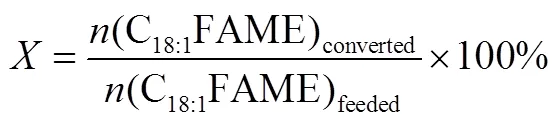


2 热力学计算
2.1 反应条件下物质的相态分析
油酸甲酯、十七烷和十八烷的正常沸点分别为617、575和590 K,其在613~653 K反应温度区间内的饱和蒸气压可以近似采用Antoine公式[29]进行估算,结果如图1所示。在实际反应体系中,若忽略加氢过程中物质的量改变带来的影响,油酸甲酯、十七烷及十八烷的最高可能分压均为111 kPa。而图1显示十七烷和十八烷的饱和蒸气压在613 K时分别为204和160 kPa,远高于其最高可能分压,表明在实际反应中二者均以气相形式存在。油酸甲酯的饱和蒸气压在613和623 K时分别为98和125 kPa,说明在613 K反应时少量的油酸甲酯可能以液相的形式存在,在623 K及更高温度反应时油酸甲酯主要以气相反应形式存在。由于实际反应体系中油酸甲酯存在液-气动态平衡并且气相油酸甲酯不断加氢转化,即使在613 K反应时油酸甲酯的气液分布对反应的影响也较为微弱。为简化分析,613~653 K温度区间内油酸甲酯的加氢反应可视作气、固两相催化反应。

图1 温度对十七烷、十八烷和油酸甲酯的饱和蒸气压的影响
2.2 气态条件下热力学数据的估算






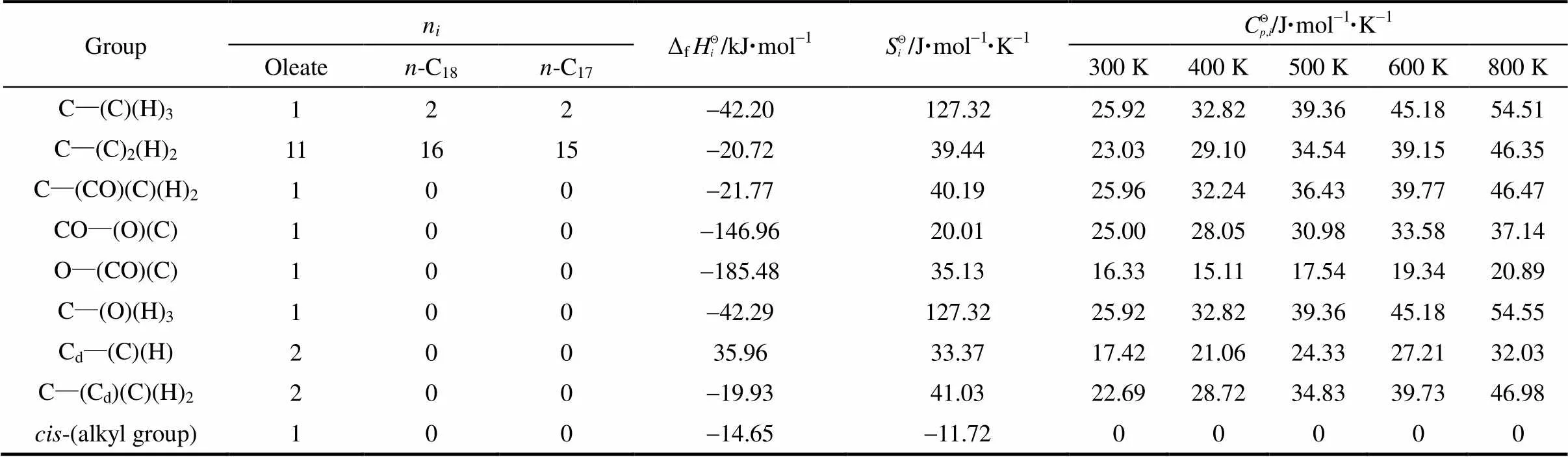
表1 油酸甲酯、十七烷和十八烷的热力学基团贡献值(Benson法)

表2 油酸甲酯及其加氢产物的热力学数据
2.3 油酸甲酯加氢反应热力学数据的估算
油酸甲酯催化加氢制备生物烷烃的反应网络复杂,包含以下几个主要反应:油酸甲酯直接加氢脱氧生成十八烷(HDO, 反应Ⅰ),油酸甲酯加氢脱羧基(HDCO2, 反应Ⅱ) 或加氢脱羰基(HDCO, 反应Ⅲ) 生成十七烷,CO2的甲烷化反应(反应Ⅳ),以及逆水汽迁移反应(RWGS, 反应Ⅴ)。由于甲烷化反应的存在,HDCO和HDCO2反应中只有1个为独立反应,二者可以合并称之为加氢脱羰/羧(HDC) 反应。
C17H33COOCH3+ 5H2= C18H38+ CH4+ 2H2O (Ⅰ)
C17H33COOCH3+ 2H2= C17H36+ CH4+ CO2(Ⅱ)
C17H33COOCH3+ 3H2= C17H36+ CO+ CH4+ H2O (Ⅲ)
CO2+ 4H2= CH4+ 2H2O (Ⅳ)
CO2+ H2= CO + H2O (Ⅴ)




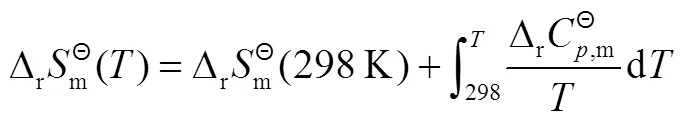



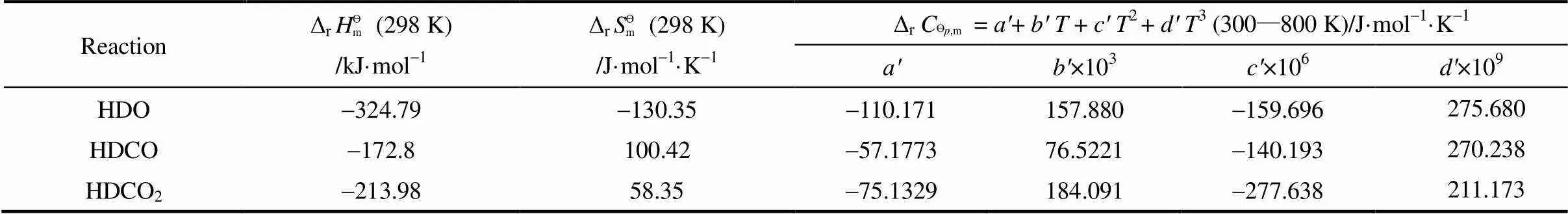
表3 298 K时油酸甲酯加氢反应的热力学数据
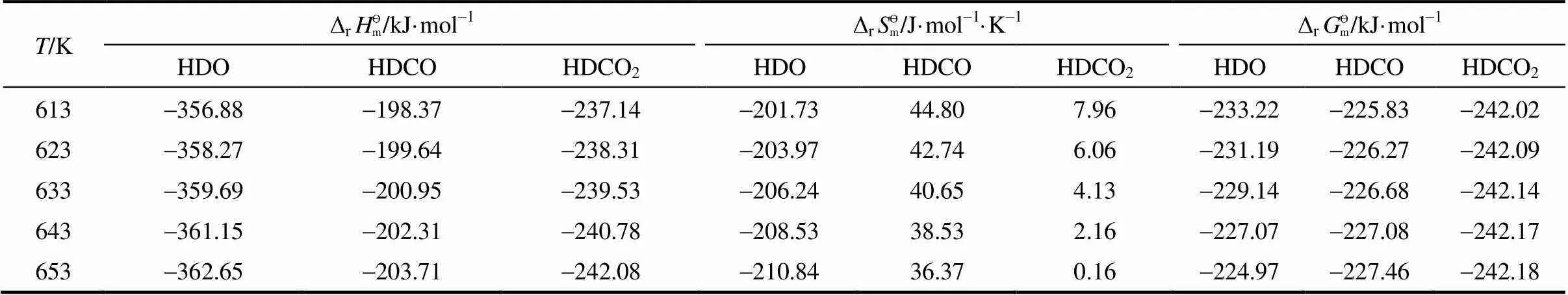
表4 不同反应温度下油酸甲酯加氢反应的热力学数据
3 反应热力学分析与讨论
NiMoS/Al2O3催化油酸甲酯加氢反应的实际体系中除主要产物十七烷和十八烷外,还观察到少量脂肪酸、异构烷烃、CH4和CO等产物,证实在613~653 K反应条件下存在油酸甲酯的水解、正构烷烃的异构化、CO甲烷化和RWGS等反应。这些共存的反应可能会影响油酸甲酯催化加氢反应的整体热效应和产物分布,为简化处理以下讨论中只考虑油酸甲酯HDO和HDC过程的热力学及主要产物十八烷和十七烷的选择性。
3.1 温度对反应热力学的影响


3.2 温度对化学平衡的影响
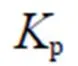
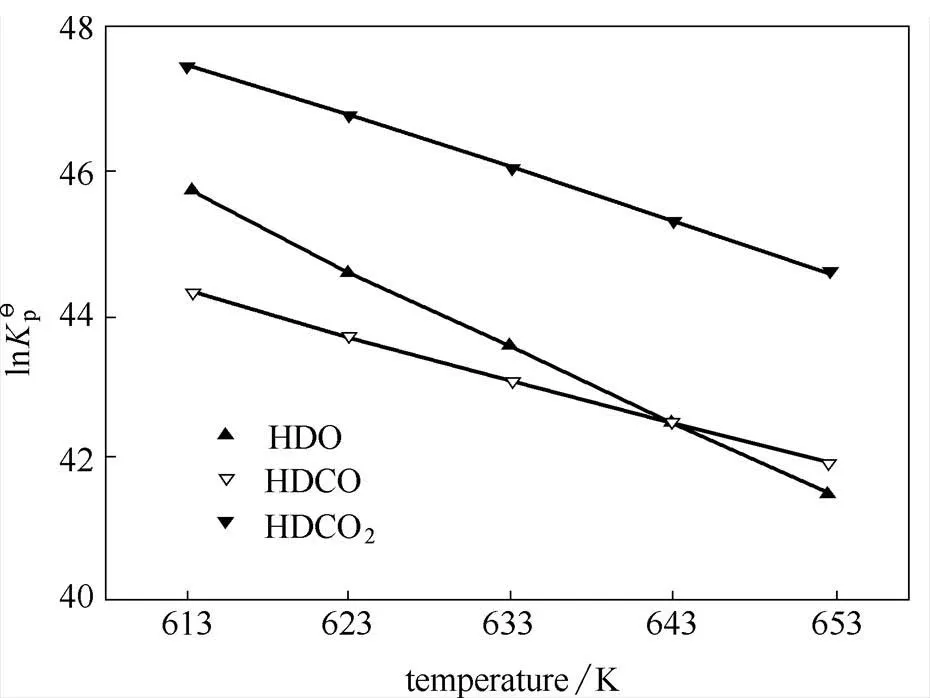
图2 温度对油酸甲酯加氢脱氧(HDO)、加氢脱羰(HDCO) 和加氢脱羧(HDCO2) 反应平衡常数的影响
3.3 温度对平衡产物分布的影响
油酸甲酯加氢产物的平衡分布采用PRO/Ⅱ软件中的平衡反应器模块基于表4中不同温度下的反应热力学数据进行模拟,模拟反应的绝对压力为2.1 MPa,氢酯摩尔比为19/1。为便于计算,忽略CO甲烷化、RWGS和直链烷烃异构化反应对平衡产物分布中正构烷烃的影响,模拟结果如图3所示。随反应温度从613 K升高到653 K,HDO产物十八烷的选择性从65.78% 逐步降低为35.84%,HDC产物十七烷的选择性则相应从34.22%上升到64.16%,HDO/HDC的比例也随之从1.92降低到0.56。这表明升高温度相对有利于油酸甲酯的HDC反应,与上述反应热力学分析和预测的趋势一致。

图3 温度对油酸甲酯加氢脱氧(HDO) 和加氢脱羰/羧(HDC) 选择性理论值的影响
为进一步证实温度对油酸甲酯加氢反应产物分布的影响,在低空速(1 h-1) 和高转化率(>99%) 的近平衡条件下通过实验手段分析了不同温度下NiMoS/Al2O3催化油酸甲酯加氢反应的产物选择性,结果如图4所示。随反应温度升高,十八烷的选择性从613 K时的69.28% 逐步降低到653 K时的67.53%,十七烷的选择性则从28.28%提高到29.92%,HDO/HDC的比值也相应从2.45降低为2.26,与图3中模拟结果的变化趋势一致,同时也与Smejkal等[16]在菜籽油加氢反应中观察到的高温有利于奇数碳烷烃选择性的实验现象吻合。

图4 温度对油酸甲酯加氢脱氧(HDO) 和加氢脱羰/羧(HDC) 选择性实验值的影响
基于化学平衡模拟得到的HDO/HDC比值和实验得到的数值大致相当,未出现数量级的偏差;在分析温度对油酸甲酯加氢产物选择性的影响方面,理论模拟结果的变化趋势上也符合实验数据,表明基于Benson基团贡献法估算的反应热力学数据有望用于分析温度、压力等参数对油酸甲酯催化加氢反应产物分布和反应路径的影响。但仍需注意的是,实际反应中的平衡产物分布受油酸甲酯加氢复杂的反应网络(如共存的甲烷化反应、逆水汽迁移反应、正构烷烃的裂解和异构化反应等)、氢酯摩尔比、氢气压力、催化剂的选择性及其他动力学因素的影响,在数值上和采用简化的热力学平衡反应器模型预测的理论值不可避免地存在差异。
4 结 论
通过Benson基团贡献法对油酸甲酯催化加氢制备生物烷烃反应体系中各物质的基础热力学数据进行估算,进而计算了613~653 K实际反应温度下油酸甲酯加氢反应的标准摩尔反应焓变、Gibbs自由能变和反应标准平衡常数。同时基于上述数据采用PRO/Ⅱ软件中的平衡反应器模型分析了温度对油酸甲酯加氢脱氧和加氢脱羰/羧产物分布及反应路径的影响,并与实验数据进行对比。结论如下。
(1)油酸甲酯加氢脱氧、加氢脱羧和加氢脱羰制备生物烷烃的反应均为放热反应,在633 K时的标准摩尔反应焓分别为-359.69、-239.53和-200.95 kJ·mol-1。上述反应在613~653 K温度区间均能够自发进行且反应完全。
(2)油酸甲酯催化加氢的反应热力学分析和平衡产物分布模拟结果表明:升高温度有助于提高平衡产物中油酸甲酯加氢脱羰/羧产物的选择性,降低反应温度则有利于油酸甲酯加氢脱氧产物的选择性,且加氢脱氧与脱羰/羧产物选择性的比例随温度从613 K升高到653 K相应从1.92降低到0.56。这与在近平衡条件下实验测得的反应数据变化趋势一致。
符 号 说 明

Cp,m——等压摩尔热容,J·mol-1·K-1 ΔG——Gibbs自由能变,kJ·mol-1 ΔH ——焓变,kJ·mol-1 K ——反应平衡常数 p ——反应压力,MPa R ——摩尔气体常数,J·mol-1·K-1 S ——熵,J·mol-1·K-1 T ——热力学温度,K ν ——反应物或产物系数 上角标 ϴ——标准态 下角标 f ——生成态 g ——气态 m ——摩尔 p ——等压 r ——反应
[1] MELERO J A, IGLESIAS J, GARCIA A. Biomass as renewable feedstock in standard refinery units. Feasibility, opportunities and challenges[J]. Energy & Environmental Science, 2012, 5(6): 7393-7420.
[2] 张家仁, 邓甜音, 刘海超. 油脂和木质纤维素催化转化制备生物液体燃料[J]. 化学进展, 2013, 25(2/3): 192-208. ZHANG J R, DENG T Y, LIU H C. Catalytic production of liquid biofuels from triglyceride feedstocks and lignocellulose[J]. Progress in Chemistry, 2013, 25(2/3): 192-208.
[3] 马冰, 张晶晶, 崔慧梅, 等. 油脂催化转化为绿色燃料的技术进展[J]. 中国科学:化学, 2015, 45(4): 350-360. MA B, ZHANG J J, CUI H M,Development in catalytic conversion of lipid to green fuels[J]. Scientia Sinica: Chimica, 2015, 45(4): 350-360.
[4] 吴才武, 夏建新. 地沟油的危害及其应对方法[J]. 食品工业, 2014, 35(3): 237-240. WU C W, XIA J X. Hazards and resolve methods of illegal cooking oil[J]. Food Industry, 2014, 35(3): 237-240.
[5] 陈锋亮, 钟耕, 魏益民. 废油脂预处理及制备生物柴油研究进展[J]. 化工进展, 2006, 25(8): 871-875. CHEN F L, ZHONG G, WEI Y M. Advances in waste oil pretreatment and biodiesel production[J]. Chemical Industry and Engineering Progress, 2006, 25(8): 871-875.
[6] 嵇磊, 张利雄, 徐南平. 利用高酸值餐饮废油脂制备生物柴油[J]. 化工进展, 2007, 36(4): 393-396. JI L, ZHANG L X, XU N P. Preparation of biodiesel from high acid value waste edible oil[J]. Chemical Industry and Engineering Progress, 2007, 36(4): 393-396.
[7] 张秋云, 杨松, 李虎. 制备生物柴油的固体酸催化剂研究进展[J]. 化工进展, 2013, 32(3): 575-584. ZHANG Q Y, YANG S, LI H. Research progress in the preparation of biodiesel with solid acid as the catalyst[J]. Chemical Industry and Engineering Progress, 2013, 32(3): 575-584.
[8] 熊良军, 李为民. 第二代生物柴油研究进展[J]. 化工进展, 2010, 29(5): 839-842. XIONG L J, LI W M. Advances in research for second generation biodiesel[J]. Chemical Industry and Engineering Progress, 2010, 29(5): 839-842.
[9] 翟西平, 殷长龙, 刘晨光. 油脂加氢制备第二代生物柴油的研究进展[J]. 石油化工, 2011, 40(12): 1364-1369. ZHAI X P, YIN C L, LIU C G. Advances in second generation biodiesel prepared by hydroprocessing of oils and fats[J]. Petrochemical Technology, 2011, 40(12): 1364-1369.
[10] KORDULIS C, BOURIKAS K, GOUSI M,Development of nickel based catalysts for the transformation of natural triglycerides and related compounds into green diesel: a critical review[J]. Applied Catalysis B-Environmental, 2016, 181: 156-196.
[11] 刘玉环, 刘英语, 王允圃, 等. 油脂催化裂解制备可再生烃类燃料研究进展[J]. 化工进展, 2013, 32(11): 2588-2592. LIU Y H, LIU Y Y, WANG Y P,Progress of production of hydrocarbon fuel by cracking non-edible oil[J]. Chemical Industry and Engineering Progress, 2013, 32(11): 2588-2592.
[12] COUMANS A E, HENSEN E J M. A model compound (methyl oleate, oleic acid, triolein) study of triglycerides hydrodeoxygenation over alumina-supported NiMo sulfide[J]. Applied Catalysis B: Environmental, 2017, 201: 290-301.
[13] HERMIDA L, ABDULLAH A Z, MOHAMED A R. Deoxygenation of fatty acid to produce diesel-like hydrocarbons: a review of process conditions, reaction kinetics and mechanism[J]. Renewable & Sustainable Energy Reviews, 2015, 42: 1223-1233.
[14] GOSSELINK R W, HOLLAK S A W, CHANG S W,Reaction pathways for the deoxygenation of vegetable oils and related model compounds[J]. ChemSusChem, 2013, 6(9): 1576-1594.
[15] ANAND M, FAROOQUI S A, KUMAR R,Kinetics, thermodynamics and mechanisms for hydroprocessing of renewable oils[J]. Applied Catalysis A-General, 2016, 516: 144-152.
[16] SMEJKAL Q, SMEJKALOVÁ L, KUBIČKA D. Thermodynamic balance in reaction system of total vegetable oil hydrogenation[J]. Chemical Engineering Journal, 2009, 146: 155-160.
[17] 马鸿宾, 李淑芬, 王渤洋, 等. 三油酸甘油酯与甲醇酯交换反应热力学分析[J]. 化学工程, 2010, 38(5): 55-58. MA H B, LI S F, WANG B Y,Thermodynamic analysis for transesterification of triolein with methanol[J]. Chemical Engineering(China), 2010, 38(5): 55-58.
[18] 张继龙, 赵志仝, 乔燕, 等. 酯交换制油酸甲酯的基团贡献法热力学分析[J]. 化工学报, 2012, 63(6): 1684-1690. ZHANG J L, ZHAO Z T, QIAO Y,Thermodynamic analysis on preparation of methyl oleatetransesterification by group-contribution method[J]. CIESC Journal, 2012, 63(6): 1684-1690.
[19] 李留, 陈盈, 林金清. 三油酸甘油酯与甲醇反应合成生物柴油的热力学分析[J]. 华侨大学学报(自然科学版), 2013, 34(4): 409-414. LI L, CHEN Y, LIN J Q. Thermodynamic analysis of triolein and methanol synthesis of biodiesel[J]. Journal of Huaqiao University (Natural Science), 2013, 34(4): 409-414.
[20] CHENG Z Y, JI X, LI S Y. Thermodynamics calculation of the pyrolysis of vegetable oils[J]. Energy Sources, 2004, 26(9): 849-856.
[21] JOBACK K G, REID R C. Estimation of pure-component properties from group-contributions[J]. Chemical Engineering Communications, 1987, 57(1/6): 233-243.
[22] 付丽丽, 蒋登高. 棕榈酸异丙酯合成反应的热力学分析[J]. 高效化学工程学报, 2016, 30(2): 398-403. FU L L, JIANG D GThermodynamic analysis of isopropyl palmitate synthesis[J]. Journal of Chemical Engineering of Chinese Universities, 2016, 30(2): 398-403.
[23] POLING B E, PRAUSNITZ J M, CONNEL J P O. The Properties of Gases and Liquids[M]. 5th ed. New York: McGraw-Hill Professional, 2001: 3.5-3.50.
[24] 王丽苹, 萧斌, 王公应. 碳酸酯与1,4-丁二醇酯交换合成聚碳酸酯二醇的热力学分析[J]. 石油化工, 2009, 38(9): 961-965. WANG L P, XIAO B, WANG G Y. Thermodynamic analysis for synthesis of polycarbonate diols by transesterification of carbonate and 1,4-butanediol[J]. Petrochemical Technology, 2009, 38(9): 961-965.
[25] 王琳琳, 陈建云, 梁杰珍, 等. 枞酸与甲醇酯化反应的基团贡献法热力学分析[J]. 化工学报, 2013, 64(6): 1900-1906. WANG L L, CHEN J Y, LIANG J Z,Thermodynamic analysis for esterification of abietic acid with methanol by group-contribution method[J]. CIESC Journal, 2013, 64(6): 1900-1906.
[26] 崔雪霞, 王桂荣, 赵茜, 等. 尿素法合成甲苯二氨基甲酸苯酯反应体系的热力学分析[J]. 化工学报, 2015, 66(9): 3367-3376. CUI X X, WANG G R, ZHAO Q,Thermodynamic analysis on synthesis of diphenyl toluene dicarbamateurea route[J]. CIESC Journal, 2015, 66(9): 3367-3376.
[27] 王修纲, 沈阳, 田冰虎, 等. 环丁烯砜合成反应的基团贡献法热力学分析[J]. 化工学报, 2016, 67(4): 1103-1109. WANG X G, SHEN Y, TIAN B H,Thermodynamic analysis on synthesis of sulfolene by group-contribution method[J]. CIESC Journal, 2016, 67(4): 1103-1109.
[28] 李梦晨. 脂肪酸甲酯加氢脱氧制备液体石蜡催化剂改性及工艺研究[D]. 北京: 北京化工大学, 2014.LI M C. Study on catalyst improvement for hydrodeoxygenating FAME into molten paraffin and corresponding reaction conditions[D]. Beijing:Beijing University of Chemical Technology, 2014.
[29] NIST Chemistry WebBook[EB/OL].[2016-12-24]. http://webbook. nist.gov/ chemistry/.
[30] 马沛生, 夏淑倩, 夏清. 化工物性数据简明手册[M]. 北京: 化学工业出版社, 2013. MA P S, XIA S Q, XIA Q. Concise Handbook of Chemical Property Data[M]. Beijing: Chemical Industry Press, 2013.
Thermodynamic analysis of catalytic hydrogenation of methyl oleate to produce bio-paraffins
SUN Peiyong1, LI Mengchen2, LIU Sen1, QI Qi1, ZHANG Shenghong1, YAO Zhilong1
(1Beijing Key Laboratory of Enze Biomass Fine Chemicals, College of Chemical Engineering, Beijing Institute of Petrochemical Technology, Beijing 102617, China;2Petrochemical Research Institute of CNPC, Beijing 102206, China)
The thermodynamic analysis of the hydrogenation of methyl oleate to bio-paraffinshydrodeoxygenation (HDO), hydrodecarbonylation (HDCO) or hydrodecarboxylation (HDCO2) routes was carried out by the Benson group-contribution method. Changes of enthalpy, entropy and Gibbs free energy, as well as the standard equilibrium constants, for each reaction were calculated in the temperature range of 613—653 K. The equilibrium distribution of products as a function of temperature was also simulated based on an equilibrium reactor of PRO/Ⅱsoftware and compared with the experimental data. The calculated thermodynamics indicates that HDO, HDCO and HDCO2of methyl oleate are exothermic processes, with the released heat decreasing in the order of HDO>HDCO2>HDCO, and each reaction can take place spontaneously and proceed completely. Moreover, improving temperature prefers HDC to HDO products at equilibrium, results in a decreasing HDO/HDC ratio from 1.92 to 0.56 as the temperature rises from 613 K to 653 K, consisting well with the experimental data collected in the catalytic hydrogenation of methyl oleate.
methyl oleate; hydrogenation; bio-paraffins; thermodynamic; group-contribution method; simulation
10.11949/j.issn.0438-1157.20161808
O 642.1
A
0438—1157(2017)06—2258—08
2016-12-26收到初稿,2017-03-10收到修改稿。
张胜红。
孙培永(1979—),男,讲师。
北京市属高等学校高层次人才引进与培养计划项目资助长城学者项目(20150316)。
2016-12-26.
ZHANG Shenghong, zshong@bipt.edu.cn
supported by the Changcheng Scholars Program of Beijing (CIT&TCD 20150316).

