双水相萃取系统相图制作新方法
高向阳, 穆洪涛, 方 颖
(1.华南农业大学 食品学院,广州 510642; 2.广东第二师范学院 生物与食品工程学院,广州 510303; 3.华南农业大学 公共基础课实验教学中心,广州 510510)
双水相萃取系统相图制作新方法
高向阳1, 穆洪涛2, 方 颖3
(1.华南农业大学 食品学院,广州 510642; 2.广东第二师范学院 生物与食品工程学院,广州 510303; 3.华南农业大学 公共基础课实验教学中心,广州 510510)

相图是研究双水相萃取分离过程的重要前提步骤,提出了清-浊点辅助相图制作方法,采用移液器微量滴定的方法绘制了PEGs/(NH4)2SO4的双水相相图,经准确度验证,此方法准确可靠。清-浊点辅助相图制作法具有操作简便、快速、准确和适用范围广等特点,为双水相系统相图制作提供了新的方法,可以用于双水相萃取的实验教学、科研及生产等领域。关键词:清-浊点辅助相图制作方法; 双节线; 微量滴定; PEG/(NH4)2SO4双水相系统
0 引 言
双水相萃取系统(Aqueous Two-phase Extraction,ATPS)是由两种化学结构不同的亲水性聚合物,或者一种亲水性聚合物和无机盐在水中以适当的浓度而形成互不相溶的两水相系统。由于其条件温和、容易放大、可连续操作,目前已广泛地应用于生物大分子的分离和纯化[1]。
目前,常用于双水相系统相图制作的方法大致有浊点法[2]和系线法[3]。浊点法制作相图操作简便,但由于在临界点判断上往往存在误差,故不同研究者制作的相图差异较大,降低了参考性[4-6]。系线法需要分析上、下相的组分的质量分数,操作繁琐,而且精确地做出相图要许多组数据,工作量大,增加了相图制作的困难。基于此,本文提出了清-浊点辅助相图制作法,此方法不仅对所有的双水相体系相图制作具有普遍适用性,而且其操作过程更加简易快捷,相图的精确度方面也较传统浊点法有较大程度的提高。
1 材料与方法
1.1 材料与仪器
材料:PEG400(聚乙二醇400),PEG1000,PEG2000,PEG6000购自阿拉丁试剂(上海)有限公司;硫酸铵购自国药集团化学试剂有限公司,去离子水产自Milli-Q Academic A10。
仪器:1/1000天平(METTLER TOLEDO PB203-N),20~200 μL、100~1 000 μL移液器(Eppendorf Research plus),漩涡振荡器(Essenscien v7),玻璃刻度离心管10 mL。
1.2 实验方法
1.2.1 溶液配制
将成相物质PEG配制成50%(质量分数)的浓溶液,(NH4)2SO4配制成40%(质量分数)的浓溶液,备用。
1.2.2 清-浊点的测定
浓溶液质量的标定:用微量移液器量取一定体积(1 mL 或100 μL)的50%PEG浓溶液或40%的(NH4)2SO4浓溶液,于电子天平上称量液体质量,每种浓溶液反复称量10次。
在刻度离心管中加入1 mL 50%PEG浓溶液,然后用移液器每次加入100 μL (NH4)2SO4浓溶液,振荡,至体系刚刚浑浊(浊点),记录加入(NH4)2SO4浓溶液的体积;再每次加入100 μL水,至体系刚刚澄清(清点),记录加入水的体积;同理依次交替加入(NH4)2SO4浓溶和水,记录加入体积并计算每个测试点含(NH4)2SO4和PEG的质量分数。
1.2.3 PEG/(NH4)2SO4双水相体系相图的建立
以硫酸铵的质量分数为横坐标,PEG的质量分数为纵坐标,绘制清点散点图和浊点散点图。由于理论上相图的双节线位于浊点散点图和清点散点图之间,故取相邻浊点坐标和清点坐标的中点所组成的系列散点制作双节线图,并对中点散点图进行曲线拟合。
1.2.4 相图精准度验证
根据对双节线的拟合结果,在双节线附近均匀选取验证点,根据所选的验证点坐标配制相应浓度的溶液体系,验证分相结果。
2 结果与分析
2.1 PEG1000/(NH4)2SO4双水相体系清-浊点的测定
PEG是双水相萃取分离中最常用的一种有机试剂,本研究着重以PEG1000/(NH4)2SO4双水相体系相图的制作为例,介绍清-浊点相图制作方法。由于备用硫酸铵浓溶液比重较大,需要对一定体积的浓溶液的质量(密度)进行标定,以便计算每个清-浊点的PEG和硫酸铵的质量分数。浓溶液质量标定参照移液器标定方法[7]。由表1可知,一定体积浓溶液质量标定结果的标准差及变异系数(CV<5%)为可接受范围。即可以用微量移液器来量取溶液进行清-浊点的制作。
向1 mL 50%的PEG1000溶液中以100 μL为单位滴加(NH4)2SO4或去离子水,记录达到每个浊点或清点所用的(NH4)2SO4和去离子水的份数(25 ℃)。在PEG1000/(NH4)2SO4双水相体系中共测定54个测试点,其中清点和浊点的个数均为27个。在54个测试点中,绝大数测试点(90.7%)只需滴加1份(100 μL);只有少数(7.4%)需滴加2份,仅有一个点需滴加4份。由此可见,此方法大大简化了传统相图的制作步骤。
计算每个浊点和清点处PEG1000和(NH4)2SO4的质量分数,并以(NH4)2SO4的质量分数为横坐标,PEG1000的质量分数为纵坐标绘制散点图(见图1)。图1中浊点散点和清点散点图大致平行,且距离紧密。
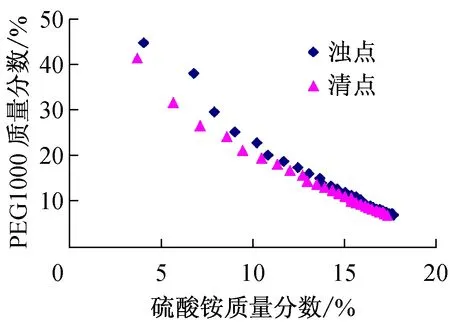
图1 PEG1000/(NH4)2SO4双水相体系测试点分布图
2.2 PEG1000/(NH4)2SO4双水相体系的相图制作及验证
由于每次加入(NH4)2SO4和H2O的体积大体相当,且每次加入的溶液相对整个体系来说较小,故选取相邻清点和浊点坐标的中点散点作为双节线的制作依据,所作的相图更加精确。依据中点散点图描出的平滑曲线即为PEG1000/(NH4)2SO4双水相体系的相图(见图2)。经回归分析获得中点散点图的拟合曲线公式:
y=9.971 2x2-4.708 1x+0.594 3
回归系数R2=0.996 5。
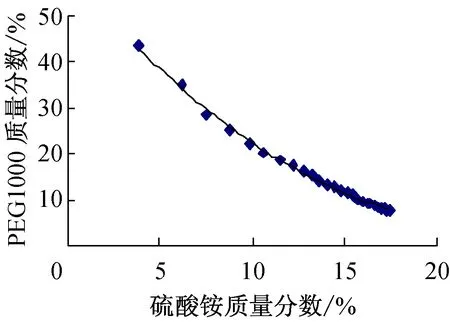
图2 PEG1000/(NH4)2SO4双水相体系相图
根据拟合的方程,在双节线上下均匀选取验证点各7个,并配制相应浓度的溶液体系,震荡后静止观察是否出现两相。各验证点的结果(见图3)显示,虽然双节线上下的验证点距离较近,但是上方的7个点均出现两相分层,下方的7个点均未出现两相分层(均相)。此结果表明,清-浊点辅助相图制作方法制作的相图精确。
2.3 其他型号PEG/(NH4)2SO4的相图制作
按照同样方法作出PEG400、PEG2000、PEG6000与(NH4)2SO4的双水相体系相图(见图4)。由此可知,清-浊点辅助相图制作方法同样适合其他型号或类型的双水相系统相图的制作。
3 讨 论
与其他方法相比,清-浊点辅助相图制作法样品用量少使体系能够快速平衡,从而在单位时间内能够采集更多相分离临界点,提高了相图的准确度,同时又大大地减少了相图制作时间并节约了测试试剂成本(见表2)。另外,由于本方法无需测定各成相组分的质量分数,故具有极高的通用性。由表2可知,传统浊点法依然是相图制作的主流方法。此种方法虽然具有操作简便快捷的优点,但在临界点判断上往往存在误差。浊度滴定法[12]是在传统浊点法的基础上,用回滴水或回滴有机相的方法对浊点加以确定。浊度滴定法虽在一定程度内提高了浊点的判定的准确度,但反复滴加和每管至多测定一个浊点,也在一定程度上增加了操作步骤的繁琐度。安建平等[6]用吸光度法和电导率法分别测定PEG和(NH4)2SO4的质量分数带替代传统的称重法,在临界点的判定上并没有做出改进。
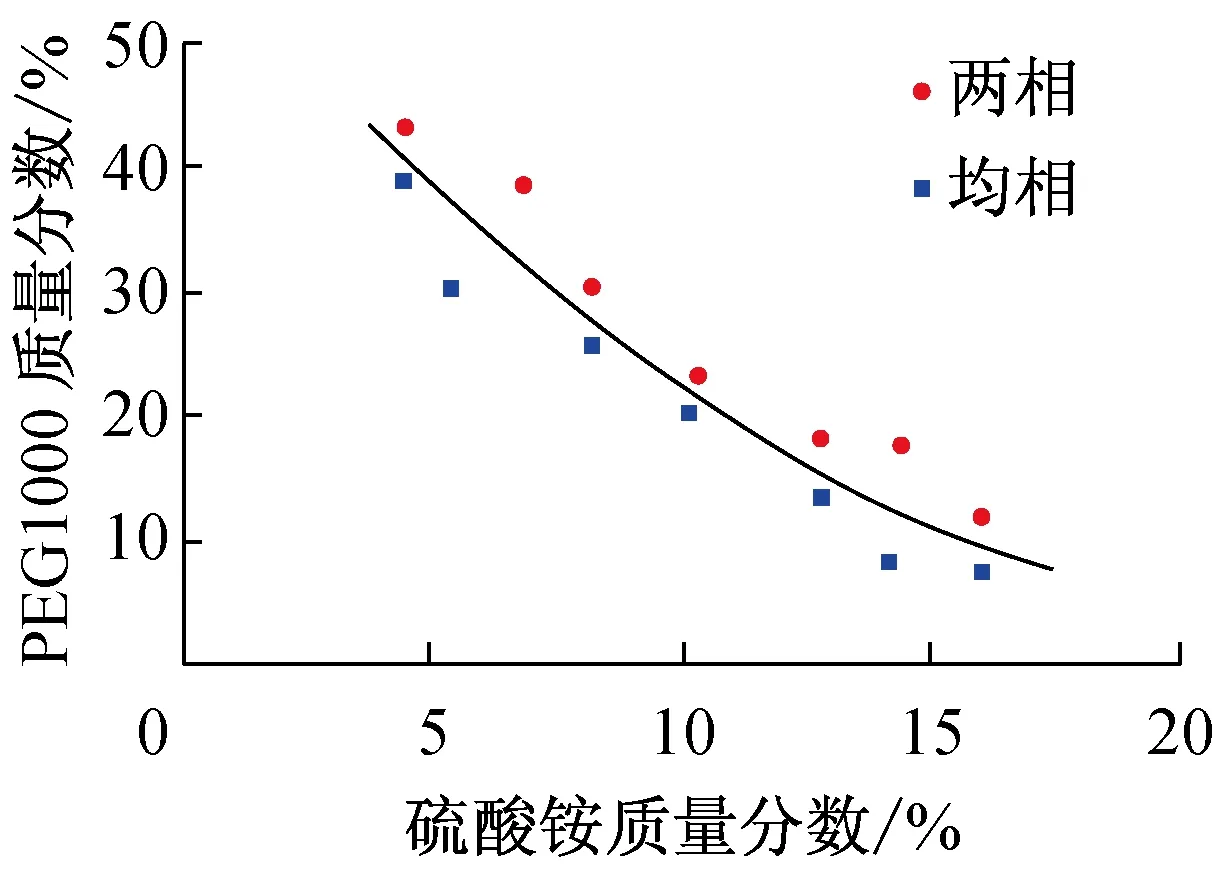
图3 相图精准度验证
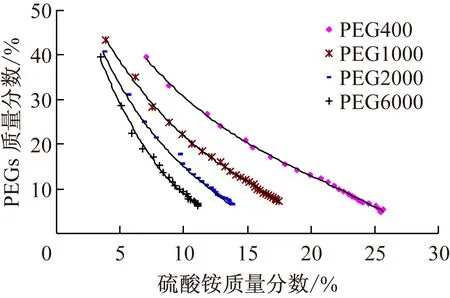
图4 PEGs/(NH4)2SO4的双水相体系相图

表2 清-浊点辅助相图制作法与其他相图制作方法的比较
4 结 语
本文提出的清-浊点辅助相图制作方法依据双节线的定义修正了传统上用浊点来表示临界点的方法,提高了临界点确定的准确度,具有快捷简便、试剂用量少和适用范围广等特点;另外,清-浊点辅助相图制作方法同时也传承了传统浊点法适用范围广的优点,即不仅适用于PEGs/(NH4)2SO4的双水相体系还适用于其他双水相萃取体系的相图制作,如高聚物-盐、高聚物-高聚物、表面活性剂、离子液体等组成的双水相体系。综上,清-浊点辅助相图制作法作为一种新型双水相系统相图制作方法,可以用于与双水相萃取相关的实验教学、科研及生产等领域。
[1] Molino J V D, Marques V, de Araújo D,etal. Different types of aqueous two-phase systems for biomolecule and bioparticle extraction and purification[J]. Biotechnol Prog, 2013, 29(6): 1343-1353.
[2] 孙 彦. 生物分离工程[M]. 北京: 化学工业出版社, 1998.
[3] 曹学君. 现代生物分离工程[M].上海: 华东理工大学出版社, 2007. 54-70.
[4] 冯自立, 马 娜. 无花果蛋白酶在PEG/(NH4)2SO4双水相体系中的分配行为[J]. 食品科学, 2010(19): 67-70.
[5] 杨 辉, 张 娟, 王 旭. PEG/(NH4)2SO4双水相体系萃取果胶酶[J]. 食品科学, 2007, 28(6): 124-127.
[6] 马伟超, 吕志民, 李一婧,等. PEG/(NH4)2SO4双水相相图制作新方法的研究[J]. 食品工业科技, 2010, 31(10): 113-115.
[7] 李 莉. 微量移液器的定期标定及校准方法[J]. 山西医药杂志, 2006, 34(12): 1077-1077.
[8] 杨 雪, 张志清, 李青莲,等. 响应面分析法优化麦麸酯酶双水相萃取的条件[J]. 食品工业科技, 2014, 35(19): 257-263.
[9] 龙文清.丙酮和乙醇双水相萃取、荧光法测定痕量维生素B2[J].光谱学与光谱分析,2007,27(10):2098-2101.
[10] 赵新颖,屈 锋,董 敏,等.双水相萃取结合液相色谱法分离蛋白质[J].分析化学,2012,40(1):38-42.
[11] 王 良,朱 红,孙艳涛,等.[Bmim]BF4-NaH2PO4双水相萃取-高效液相色谱法测定水中痕量氯酚类内分泌干扰物[J].分析化学,2011,39(5):709-712.
[12] 王志华,马会民,马泉莉,等.双水相萃取体系的研究[J].应用化学,2001,18(3):173-175.
[13] 陈建中,葛水莲,昝立峰,等.响应面试验优化双水相萃取大吴风草总黄酮工艺及抑菌活性测定[J].食品科学,2015,36(24):57-62.
[14] 梁云星,郑 颖,王 宁,等.双水相萃取的葛根黄酮搽剂对神经根型颈椎病大鼠的疗效[J].山西医科大学学报,2016,47(4):315-318.
[15] 范杰平,曹 婧,孔 涛,等.[Bmim]Br-K2HPO4双水相萃取与超声耦合法提取葛根中的葛根素及其优化[J].高校化学工程学报,2011,25(6):955-960.
A Novel Method for Construction Aqueous Two-phase System Phase Diagram: Clear-cloud Points Aid Phase Diagram Establishment
GAOXiangyang1,MUHongtao2,FANGYin3
(1. Food College, South China Agricultural University, Guangzhou 510642, China; 2. College of Biological and Food Engineering, Guangdong Education Institute, Guangzhou 510303, China; 3. Public Basic Course Experimental Teaching Center, South China Agrical Telrel University, Guangzhou 510510, China)
Phase diagrams are essential and important in the application of aqueous two-phase extraction technology. Conventional methods in the determination of phase boundaries are inaccurate, complicated and time consuming. In this paper, we proposed a novel method to overcome these imperfections. Using adjustable-volume pipettes and pipette calibration method, the method proposed could steadily provide accurate phase diagrams in a short time. It was tested in the phase diagram of PEG/(NH4)2SO4, and the result showed extensive reliability. This method can be used in area of experiment teaching, scientific research, and industrial manufacture which related to aqueous two-phase extraction technology.
clear-cloud points aid phase diagram establishment; bimodal; microtitration; PEG/(NH4)2SO4aqueous two-phase extraction system
2016-05-13
国家自然科学基金项目(6130425);华南农业大学校级教学改革项目(JG14110)
高向阳(1966-),女,湖南麻阳人,博士,副教授,研究方向:食品生物化学。Tel.:13310896601;E-mail:xin-198310@163.com
1006-7167(2017)03-0016-04
TP 212
A

