山茱萸的化学成分研究
叶贤胜+赫军+张佳琳+庞晓斌+张蕾+乔灏祎+潘雪格+张佳+刘淑娜+张维库+续洁琨
[摘要] 利用各种色谱技术对山茱萸的化学成分进行研究,从山茱萸水提取物中分离得到6个化合物,分别为6′-O-乙酰基-7α-O-乙基莫诺苷(1),(-)-isolariciresinol 3α-O-β-D-glucopyranoside(2),芹菜素(3),cirsiumaldehyde(4),对香豆酸(5),咖啡酸(6),其中化合物1为新化合物,化合物2~4为首次从山茱萸属植物中分离得到。利用MTT 法检测了化合物2~6对缺氧缺糖损伤的PC12细胞的保护作用,结果表明化合物4在1.0 μmol·L-1的浓度下,对OGD/R损伤的PC12细胞物有一定的保护作用。
[关键词] 山茱萸;化学成分;6′-O-乙酰基-7α-O-乙基莫诺苷;PC12细胞
[Abstract] To investigate the chemical compounds from the fruit of Cornus officinalis,six compounds were isolated and determined by extensive spectroscopic analysis as 6′-O-acetyl-7α-O-ethyl morroniside (1),(-)-isolariciresinol 3α-O-β-D-glucopyranoside(2),apigenin (3),cirsiumaldehyde(4), p-coumaric acid (5),caffeic acid (6). Compound 1 was a new iridoid glucoside,and compounds 2-4 were obtained from the Cornus genus for the first time. Compounds 2-6 were evaluated for the viability of PC12 cells when exposed in conditions of oxygen and glucose deprivation. The MTT results showed that compound 4 increased cell viability moderately in OGD/R treated PC12 cells at the concentration of 1.0 μmol·L-1.
[Key words] Cornus officinalis;chemical constituents;6′-O-acetyl-7α-O-ethyl morroniside;PC12 cells
doi:10.4268/cjcmm20162419
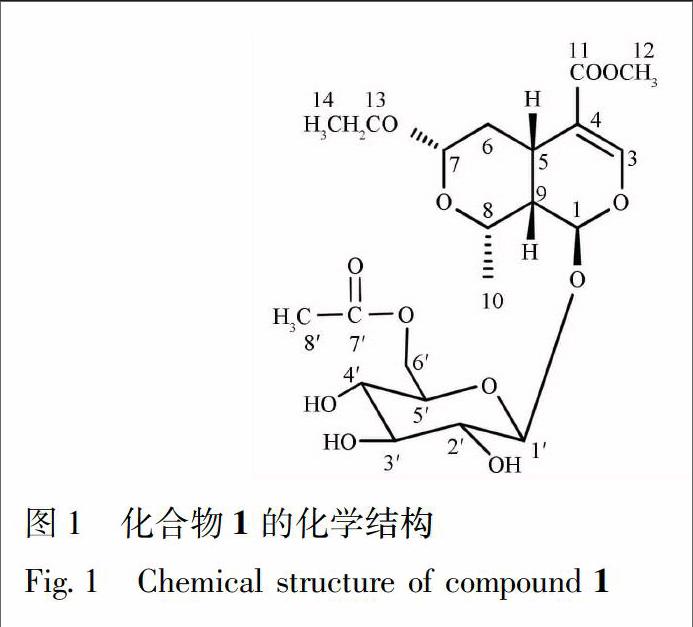
山茱萸为山茱萸科Cornaceae植物山茱萸Cornus officinalis Sieb. et Zucc.的干燥成熟果肉,主产于山西、陕西、河南等省[1],是我国传统的名贵滋补中药材。始载于《神农本草经》,其性酸、涩,微温,归肝、肾经,具有补益肝肾和涩精固脱之功效[2]。研究表明山茱萸的化学成分主要为环烯醚萜、鞣质、黄酮、三萜和苯丙素类等[3-5]。现代药理学研究表明山茱萸在降血糖,降血脂,抗炎、抑菌,抗心律失常,抗氧化,抗衰老,抗肿瘤,抗血栓等方面均表现出较好的活性[3,6-9]。目前关于山茱萸的化学成分研究还不够深入,为了更好的阐明其药效物质基础,本实验对山茱萸的化学成分进行了系统地研究,采用硅胶柱色谱、ODS柱色谱、Sephadex LH-20柱色谱和制备高效液相色谱等方法分离纯化得到6个化合物,根据理化性质和波谱数据分别鉴定为6′-O-乙酰基-7α-O-乙基莫诺苷(1),(-)-isolariciresinol 3α-O-β-D-glucopyranoside(2),芹菜素(3),cirsiumaldehyde(4),对香豆酸(5),咖啡酸(6)。其中化合物1为新化合物(图1),化合物2~4为首次从山茱萸属植物中分离得到。此外,还利用MTT法检测了化合物2~6对缺氧缺糖损伤的PC12细胞的保护作用,结果表明在化合物4在1.0 μmol·L-1的浓度下,对OGD/R损伤的PC12细胞物有一定的保护作用。
1 材料
JASCO P-2000 Polarimeter型旋光仪(JASCO公司);Nicolet 5700型FT-IR红外光谱仪(Thermo Fisher公司);Bruker AV-400/600型核磁共振仪(BrukerBiospin公司);Agilent 1200 LC/MSD TOF型液相色谱-质谱联用仪(Agilent公司);Agilent 1100型分析液相(DAD检测器);Waters制备液相(泵:Waters 515型,检测器:Waters 2487);岛津制备液相(泵:LC-20AR,检测器:SPD-20A);WFH-203三用紫外分析仪;Sartorius-BS223S电子分析天平;D101型大孔吸附树脂为沧州宝恩吸附材料科技有限公司生产;柱层析硅胶(100~200目,200~300目)为青岛海洋化工厂生产;硅胶GF254薄层预制板为烟台化学工业研究所产品;ODS(30~50 μm)为YMC公司生产;Sephadex LH-20型凝胶为Pharmacia公司生产;制备型HPLC色谱柱为ES Epic C18色谱柱(20 mm×250 mm,5 μm)和ES Sonoma C18色谱柱(20 mm×250 mm,5 μm);实验所用試剂均为分析纯(北京化工厂)和色谱纯(Honeywell)。
实验所用山茱萸为2013年11月采摘自陕西省佛坪县,由北京中医药大学续洁琨副教授鉴定为山茱萸科山茱萸属植物山茱萸C. officinalis的成熟果实,样本存放于中日友好医院临床医学研究所(No.20131106)。
2 提取分离
干燥的山茱萸果实(63 kg),水煎煮提取2次(600,500 L),每次2 h。合并提取液,减压浓缩得到总浸膏(约28.9 kg)。总浸膏用水混悬后经D101型大孔吸附树脂柱,依次用水,30%,55%,95%乙醇洗脱。30%乙醇洗脱部位浓缩后得浸膏2.8 kg,经硅胶柱色谱分离,氯仿-甲醇(100∶0,95∶5,9∶1,8∶2,7∶3,6∶4,1∶1)梯度洗脱,洗脱液经薄层色谱检测,合并相同组分,得组分Fr.A~Fr.E。
Fr. A经硅胶柱色谱分离,氯仿-丙酮(100∶0,95∶5,9∶1,6∶1,4∶1,3∶1,2∶1,1∶1)梯度洗脱,洗脱液经薄层色谱检测,合并相同组分,得组分Fr.A1~Fr.A4;Fr.A1经硅胶柱色谱分离,环己烷-乙酸乙酯(100∶0,9∶1,8∶1,6∶1,4∶1,3∶1,2∶1,1∶1)梯度洗脱,洗脱液经薄层色谱检测,合并相同组分,得组分Fr. A1-1~Fr. A1-8,其中Fr. A1-6经ODS柱色谱分离,依次用10%,18%,25%,33%,40%,50%,65%,85%,100%甲醇梯度洗脱,洗脱液经薄层色谱检测,合并相同组分,得组分Fr. A1-6-1~Fr. A1-6-8;Fr. A1-6-4在甲醇中结晶得到化合物4(24 mg)。Fr. A2经ODS柱色谱分离,依次用10%,20%,30%,40%,50%,60%,80%甲醇梯度洗脱,洗脱液经薄层色谱检测,合并相同组分,得组分Fr.A2-1~Fr.A2-6,其中Fr.A2-1经制备液相分离(色谱柱ES Epic C18;流动相30%甲醇;流速4.0 mL·min-1)得到化合物6(18 mg);Fr.A2-2经制备液相分离(色谱柱ES Epic C18;流动相18%乙腈;流速4.5 mL·min-1)得到化合物5(20 mg);Fr. A2-4经制备液相分离(色谱柱ES Epic C18;流动相15%甲醇;流速3.5 mL·min-1)得到化合物3(10 mg)。Fr.A3经ODS柱色谱分离,依次用10%,20%,30%,40%,50%,60%,75%甲醇梯度洗脱,洗脱液经薄层色谱检测,合并相同组分,得组分Fr.A3-1~Fr.A3-4,其中Fr.A3-2经制备液相分离(色谱柱ES Epic C18;流动相30%乙腈,流速4.5 mL·min-1)得到化合物1(2 mg)。Fr.B经Sephadex LH-20(甲醇)柱色谱分离,得组分Fr.B1和Fr.B2;Fr.B2经ODS柱色谱分离,依次用5%,10%,20%,30%,40%,50%,60%,80%甲醇梯度洗脱,洗脱液经薄层色谱检测,合并相同组分,得组分Fr.B2-1~Fr.B2-6,其中Fr.B2-3再经Sephadex LH-20(甲醇)柱色谱分离,得8个组分(Fr.B2-3-1~Fr.B2-3-8);Fr.B2-3-2经制备液相分离(色谱柱ES Sonoma C18;流动相33%甲醇;流速5.0 mL·min-1)得到化合物2(5 mg)。
3 结构鉴定
化合物1 淡黄色粉末。[α] 25D+20.33 (c 0.03,MeOH)。HR-ESI-MS m/z 499.178 7 [M+Na]+ (计算值为499.178 6),结合1H和13C-NMR谱确定分子式为C21H32O12,不饱和度为6。IR显示该化合物含有羟基(3 381 cm-1)和羰基(1 734 cm-1)等结构片段。
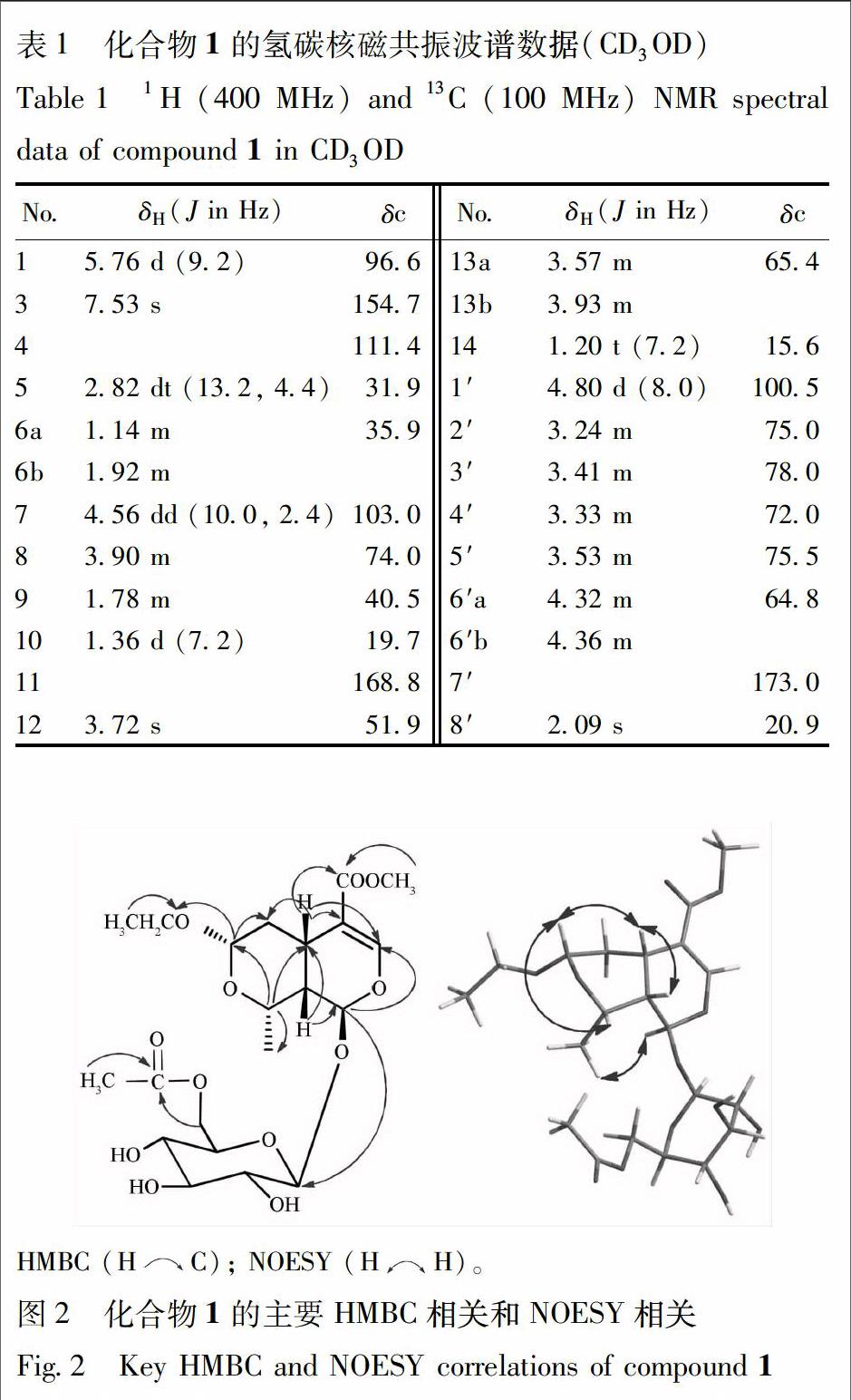
1H-NMR (CD3OD,400 MHz)谱(表1)高场区显示3个甲基质子信号δH1.20 (3H,t,J=7.2 Hz,H-14),1.36 (3H,d,J=7.2 Hz,H-10),δH2.09 (3H,s,H-8′ );1个甲氧基质子信号δH3.72 (3H,s,-OCH3);低场区显示3个缩醛质子信号δH4.56 (1H,dd,J=10.0,2.4 Hz,H-7),4.80 (1H,d,J=8.0 Hz,H-1′ ),5.76 (1H,d,J=9.2 Hz,H-1);1个连氧烯氢质子信号δH7.53 (1H,s,H-3);此外,δH3.24~4.36为1组葡萄糖特征质子信号,葡萄糖端基氢(δH4.80)的偶合常数为8.0 Hz,提示为β型葡萄糖。13C-NMR (CD3OD,100 MHz)谱(表1)共显示21个碳信号,结合DEPT谱分别为3个季碳,11个次甲基,3个亚甲基,4个甲基。结合HSQC谱进一步确定该化合物在高场区含有3个甲基碳信号δC15.6,19.7,20.9;1个亚甲基碳信号δC35.9;2个次甲基碳信号δC31.9,40.5;1个甲氧基碳信号δC51.9;1个连氧亚甲基碳信号δC65.4;1个连氧次甲基碳信号δC74.0;1组葡萄糖碳信号δC75.0 (C-2′),78.0 (C-3′),72.0 (C-4′),75.5 (C-5′),64.8 (C-6′);在中低场区显示3个缩醛碳信号δC96.6,100.5,103.0,其中δC100.5为葡萄糖的端基碳信号;1个烯碳信号δC111.4;1个连氧烯碳信号δC154.7;在低场区显示1个羰基碳信号δC168.8和1个乙酰基碳信号δC173.0;结合以上波谱数据,该化合物的NMR数据与7α-乙氧基莫诺苷[10]十分相似,不同之处在于该化合物的1H-NMR谱在δH2.09 (3H,s)处多出3个氢信号,13C-NMR谱在δC173.0和20.9处多出一组乙酰基信号。在HMBC谱(图2)中H-8′ (δH2.09)和H-6′ (δH4.32和4.36) 與C-7′ (δC173.0)远程相关,证明化合物的乙酰基结构片段和葡萄糖结构片段的6′位相连接。在NOESY 谱(图2)中,H-1与CH3-10α相关,H-5β与H-7,H-8,H-9相关,确定H-1,H-10为α构型,H-5,H-7,H-8,H-9为β构型。
化合物1 按照文献[11]方法进行酸水解和衍生化处理,HPLC分析结果显示化合物1的糖基部分衍生物与D-葡萄糖标准品的衍生物保留时间一致(t=18.513 min),故确定化合物1的结构中含有D-葡萄糖。
综合上述分析,化合物1的结构鉴定为6′-O-乙酰基-7α-O-乙基莫诺苷(图1)。经SciFinder系统文献检索,发现该化合物为未经报道的新化合物。
化合物 2 白色粉末。1H-NMR (CD3OD,400 MHz) δ: 6.75 (1H,d,J=8.0 Hz,H-5′),6.70 (1H,d,J=1.9 Hz,H-2′),6.66 (1H,s,H-8),6.65 (1H,d,J=2.0 Hz,H-6′),6.19 (1H,s,H-5),4.05 (1H,d,J=7.8 Hz,H-1″),3.85~3.64 (m),3.81 (3H,s,-OCH3),3.80(3H,s,-OCH3),3.36-3.23 (m),3.17(1H,m),3.06 (1H,m),2.89 (1H,m,H-1a),2.76 (1H,dd,J=4.0,15.4 Hz,H-1b),1.96 (2H,m,H-2,H-3);13C-NMR (CD3OD,100 MHz)δ: 149.1 (C-3′),147.4 (C-7),146.2 (C-6),145.4 (C-4′),138.9 (C-1′),133.9 (C-10),129.4 (C-9),123.6 (C-6′),117.5 (C-5),116.1 (C-5′),114.1 (C-2′),112.5 (C-8),104.0 (C-1″),78.4 (C-5″),78.0 (C-3″),75.2 (C-2″),71.5 (C-4″),70.9 (C-3a),65.6 (C-2a),62.6 (C-6″),56.6 (3′-OCH3),56.5 (7-OCH3),45.5 (C-3),41.3 (C-2),33.8 (C-1)。以上數据与文献[12]对比,故鉴定该化合物为(-)-isolariciresinol 3α-O-β-D-glucopyranoside。
化合物3 黄色针晶(甲醇)。1H-NMR (DMSO-d6,400 MHz) δ: 12.95 (1H,s,5-OH),7.91 (2H,d,J=8.8Hz,H-2′,6′),6.92 (2H,d,J=8.8 Hz,H-3′,5′),6.76 (1H,s,H-3),6.46 (1H,s,H-8),6.19 (1H,s,H-6);13C-NMR (DMSO-d6,100 MHz) δ: 181.7 (C-4),164.7 (C-7),163.7(C-2),161.4 (C-4′),161.3 (C-5),157.3 (C-8a),128.4 (C-2′),128.4 (C-6′),121.1 (C-1′),116.0 (C-3′),116.0 (C-5′),103.5 (C-4a),102.8 (C-3),99.0 (C-6),94.0 (C-8)。以上数据与文献[13] 对比,故鉴定该化合物为芹菜素(apigenin)。
化合物4 淡黄色粉末。1H-NMR (DMSO-d6,400 MHz) δ: 9.59 (2H,s,-CHO×2),7.50 (2H,d,J=3.6 Hz,H-3,3′),6.76 (2H,d,J=3.6 Hz,H-4,4′),4.63 (4H,s,H-6,6′);13C-NMR (DMSO-d6,100 MHz) δ: 178.4 (-CHO×2),157.3 (C-5,5′),152.3 (C-2,2′),123.7 (C-3,3′),112.3 (C-4,4′),63.7 (C-6,6′)。以上数据与文献[14] 对比,故鉴定该化合物为cirsiumaldehyde。
化合物5 淡黄色粉末。1H-NMR (DMSO-d6,400 MHz) δ: 7.50 (1H,d,J=8.0 Hz,H-7),7.47 (2H,d,J=15.6 Hz,H-3,5),6.78 (2H,d,J=8.0 Hz,H-2,6),6.28 (1H,d,J=15.6 Hz,H-8);13C-NMR (DMSO-d6,100 MHz) δ: 168.2 (C-9),159.5 (C-4),143.8 (C-7),130.0 (C-2,6),125.3 (C-1),115.7 (C-3,5),114.8 (C-8)。以上数据与文献[15] 对比,故鉴定该化合物为对香豆酸(p-coumaric acid)。
化合物6 淡黄色粉末。1H-NMR (DMSO-d6,400 MHz) δ: 7.41 (1H,d,J=16.0 Hz,H-7),7.02 (1H,d,J=2.0Hz,H-2),6.95 (1H,dd,J=2.0,8.4 Hz,H-6),6.75 (1H,d,J=8.4 Hz,H-5),6.17 (1H,d,J=16.0 Hz,H-8); 13C-NMR (DMSO-d6,100 MHz) δ: 167.6 (-COOH),147.8 (C-4),145.2 (C-7),144.2 (C-3),125.4 (C-1),120.8 (C-8),115.4 (C-6),114.9 (C-5),114.3 (C-2)。以上数据与文献[16] 对比,故鉴定该化合物为咖啡酸(caffeic acid)。
4 化合物对PC12细胞缺氧缺糖损伤的保护作用
大鼠嗜铬瘤PC12细胞用含10%FBS的High-DMEM培养基培养于37 ℃,5%CO2的培养箱中,隔天换培养液。待细胞铺满培养瓶底部的80%以上时,以0.25%胰蛋白酶消化 2 min后,加入10%新生牛血清的DMEM培养液终止消化,以弯头滴管轻轻吹下贴壁生长细胞,吹打均匀后分至新细胞培养瓶,加培养液,放入37 ℃,5% CO2的培养箱中培养。待培养瓶中PC12细胞的融合度达到80%以上时,经行传代操作并按照6万个/mL的密度铺满96孔板,100 μL/孔,并分为空白对照组,模型组,阳性药组,以及化合物组;24 h后依次加入1.0 μmol·L-1的化合物2~5,阳性药组加入终浓度为5.0 μmol·L-1的尼莫地平,空白组与模型组换液处理,放置于细胞培养箱中孵育,作用24 h后,对模型组,阳性药组,以及各浓度加化合物组加入终浓度为8.0 mmol·L-1无糖Earles稀释的Na2S2O4缺氧缺糖损伤45 min,然后各组均加入完全培养基复氧复糖4 h;与超净工作台中以10 μL/孔加入MTT,细胞培养箱中孵育4 h,用多功能酶标仪450 nm下测定各组的A。
实验结果显示,与空白组(100%)相比,模型组细胞存活率(54.1%)明显降低;与模型组相比,化合物4组细胞存活率从54.1%升高至69.2%,表明化合物4对缺糖缺氧损伤的PC12细胞有一定的保护作用,其他化合物对PC12细胞均无保护作用。
[参考文献]
[1] 中国科学院中国植物志编辑委员会. 中国植物志 [M]. 北京: 科学出版社,1990.
[2] 中国药典. 一部 [S]. 2015: 27.
[3] Cao G,Zhang Y,Cong X D,et al. Research progress on the chemical constituents and pharmacological activities of Fructus Corni[J]. J Chin Pharm Sci,2009,18: 208.
[4] Ma W,Wang K J,Cheng C S,et al. Bioactive compounds from Cornus officinalis fruits and their effects on diabetic nephropathy [J]. J Ethnopharmacol,2014,153: 840.
[5] Lin M H,Liu H K,Huang W J,et al. Evaluation of the potential hypoglycemic and beta-cell protective constituents isolated from Corni Fructus to tackle insulin-dependent diabetes mellitus [J]. J Agric Food Chem,2011,59: 7743.
[6] Park C H,Tanaka T,Yokozawa,et al. Anti-diabetic action of 7-O-galloyl-d-sedoheptulose,a polyphenol from Corni Fructus,through ameliorating inflammation and inflammation related oxidative stress in the pancreas of type 2 diabetics[J]. Biol Pharm Bull,2013,36(5): 723.
[7] Park C H,Noh J S,Kim J H,et al. Evaluation of morroniside,iridoid glycoside from Corni Fructus,on diabetes-induced alterations such as oxidative stress,inflammation,and apoptosis in the liver of type 2 diabetic db/db Mices[J]. Biol Pharm Bull,2011,34(10): 1559.
[8] Zhao L H,Ding Y X,Zhang L,et al. Cornel iridoid glycoside improves memory ability and promotes neuronal survival in fimbria-fornix transected rats[J]. Eur J Pharmacol,2010,647: 68.
[9] Zhang Q C,Zhao Y,Bian H M. Anti-thrombotic effect of a novel formula from Corni Fructus with malic acid,succinic acid and citric acid[J]. Phytother Res,2014,28: 722.
[10] 王曉燕,孙磊,乔善义,等. 六味地黄苷糖中糖苷部位的化学成分研究[J]. 中国中药杂志,2012,37(17): 2576.
[11] Tanaka T,Nakashima T,Ueda T,et al. Facile discrimination of aldose enantiomers by reversed-phase HPLC[J]. Chem Pharm Bull,2007,55: 899.
[12] Wen Q W,Lin X,Liu Y Q,et al. Phenolic and lignan glycosides from the butanol extract of Averrhoa carambola L. root [J]. Molecules,2012,17 (10): 12330.
[13] 任福才,王丽霞,王飞,等. 绵枣儿化学成分研究 [J]. 中草药,2014,45 (14):1984.
[14] 沈杰,杨峻山. 云南山竹子果实的化学成分研究 [J]. 中国药学杂志,2006,41 (9): 660.
[15] Fan W Q,Xiong M X,Ma Z,et al. Chemical constituents of Altemanthera philoxeroides[J]. Chin J Nat Med,2008,6 (2): 112.
[16] 姚士,徐乃玉,褚纯隽,等. 蓝萼香茶菜的抗补体活性成分研究[J]. 中国中药杂志,2013,38 (2):199.
[责任编辑 丁广治]

