独活肠吸收液对大鼠离体胸主动脉张力的影响❋
黄 颖,吴宏伟,王燕平
(1.中国中医科学院医学实验中心,北京 100700;2.中国中医科学院中药研究所,北京 100700; 3.中国中医科学院中医临床基础医学研究所,北京 100700)
独活肠吸收液对大鼠离体胸主动脉张力的影响❋
黄 颖1,吴宏伟2,王燕平3△
(1.中国中医科学院医学实验中心,北京 100700;2.中国中医科学院中药研究所,北京 100700; 3.中国中医科学院中医临床基础医学研究所,北京 100700)
目的:观察独活肠吸收液对大鼠离体胸主动脉环的舒张作用及其舒张机制。方法:应用外翻肠囊法制备独活含药肠吸收液,采用离体血管环技术制备大鼠胸主动脉环,使用累积加药法分别检测独活肠吸收液对PE、KCl刺激的内皮完整与去内皮胸主动脉环张力的影响,并探讨其Ca2+调节机制。结果:独活肠吸收液能够浓度依赖性地舒张PE、KCl引起的内皮完整与去内皮血管环收缩,内皮完整组与去内皮组最大舒张率比较差异无统计学意义。对PE或KCL预收缩的血管,独活肠吸收液均能抑制CaCl2所致最大收缩效应。结论:独活肠吸收液对PE、KCl引起的血管收缩均具有较好的舒张作用并呈剂量依赖性,其作用机制与抑制细胞外Ca2+内流密切相关。
独活;肠吸收液;血管舒张;机制
中药独活为伞形科植物当归属重齿毛当归(Angelica pubescens Maxim.f.shanet Yucm)的干燥根,始载于《神农本草经》,被列为上品,其味辛、苦、微温,归肾、膀胱经,具有祛风除湿、通痹止痛的功效,是传统临床治疗风湿痹痛的要药。现代药理研究表明,独活具有抗肿瘤、抗炎、镇痛、镇静催眠的作用,能治疗胃溃疡、抗血管生成、抑菌、抗氧化[1-4]。在心脑血管方面有降压和抗心律抗心律失常作用,能抗血小板聚集和抑制血栓形成[5-6]。
本课题组在以往对伞形科辛味中药研究中发现,独活主要活性成分蛇床子素、欧前胡素等均对离体血管具有舒张作用[7]。因此本研究采用“外翻肠囊-体外活性”的方法制作独活肠吸收液,考察独活被生物体吸收的有效成分对离体血管作用,明确独活的药理作用,为进一步扩大独活的临床应用范围提供实验依据。
1 材料
1.1 实验动物
清洁级雄性SD大鼠,体质量(250±20)g,购自北京维通利华实验动物技术有限公司(合格证号SCXK(京)2012-0001)。
1.2 试剂
Krebs-Henseleit(K-H)液配方:NaCl 118.96 mmol/L,KCl 4.73 mmol/L,KH2P041.17 mmol/L,MgSO41.17 mmol/L,NaHCO325.0 mmol/L,CaCl22.54 mmol/L;葡萄糖11.1 mmol/L,以上试剂为分析纯,均购自Alfa Aesar公司。苯肾上腺素、乙酰胆碱购自梯希爱(上海)化成工业发展有限公司。
1.3 仪器
Biopac MP150多导生理记录仪,美国BIOPAC公司生产;Radnoti离体组织灌流系统,美国Radnoti公司生产。
1.4 药物
独活药材购自北京同仁堂药店,经中国中医科学院中药研究所何希荣主管药师鉴定为伞形科当归属植物重齿毛当归的干燥根。
2 方法
2.1 独活肠吸收液的制备
将独活用清水洗净置于70℃烘箱中烘干。将烘干的独活打成粗粉,称取粉末100 g,加5倍量95%乙醇500 ml浸泡1 h回流2次,每次提取1 h,趁热过滤,合并滤液,40℃减压旋转蒸发回收乙醇,减压干燥得独活提取物。使用前用台氏液将独活提取物超声溶解、过滤,制成质量浓度为1.28 g生药· mL-1的供试液。
将实验前禁食12 h的大鼠称重后,断颈椎处死,沿腹中线和腹白线分别剪开皮肤与肌肉,迅速取出小肠,自胃幽门以下10 cm开始向下量取14 cm为肠段一,间隔10 cm量取14 cm为肠段二,再间隔10 cm量取14 cm为肠段三,从回盲瓣以上5 cm开始向上取14 cm为肠段四。将剪下的肠管放入0℃台氏液中冲洗至无肠内容物为止。将自制硅胶套管软端插入肠管用丝线结扎,小心将肠道翻转。用0℃台氏液冲洗内表面,将另一端用丝线结扎成囊状。麦氏浴管中预先加入上述独活供试液25 mL,通入混合气体(95%O2,5%CO2),保持37℃恒温。在肠管中注入台氏液2 mL放入麦氏浴管中,于60 min取样400 μL,同时补充等体积的37℃台氏液。样品放入干净的离心管中,合并后于-80℃密封直立保存。
2.2 大鼠胸主动脉环制备
2.2.1 内皮完整胸主动脉环制备方法 大鼠颈部脱臼,剪开胸腔迅速取出胸主动脉条,放置于4℃ K-H液中,小心剥去附在胸主动脉上的脂肪及结缔组织,横切成2~3 mm长的血管环。将血管环悬挂于预置5 mlK-H液的浴槽中,温度(37.0± 0.2)℃恒定,持续通入95%O2和5%CO2的混合气体。标本的一端固定,另一端经张力换能器连接Radnoti离体组织灌流系统,记录实验过程中张力的变化。稳定过程先以0 g张力开始,维持30 min后调节其基础张力至1 g,平衡1 h,期间每隔15 min更换1次K-H液。主动脉环稳定后用KCl(60 mM)刺激,以激发最大收缩,待收缩幅度稳定后用K-H液洗脱。
2.2.2 去内皮胸主动脉环制备方法 采用机械去内皮方法去除血管内皮,并检测内皮完整性。用终浓度1 μM的苯肾上腺素(PE)收缩血管环达到峰值,加入依浓度梯度10-9~10-5乙酰胆碱,给药时间间隔为3 min。至加入10-5乙酰胆碱后,血管舒张达到70%以上为内皮完整。舒张率<10%的认定为内皮去除。
2.3 独活肠吸收液对大鼠离体胸主动脉环张力的测定
2.3.1 对PE引起的内皮完整和去内皮血管环张力的影响 血管环用K-H液清洗数次,使其保持基础张力。以PE(1 μM)诱发最大收缩幅度为100%,主动脉环稳定后,采用累积加样法在浴槽中加入肠吸收液,累计依次加样至 25 μl、50 μl、100 μl、200 μl,每10 min加入1次。以加入受试药物后的血管张力变化幅度与KCl诱发最大收缩幅度之间的比率作血管舒张反应的量-效曲线;药物引起的收缩幅度均以第2次KCl(60 mM)引起的最大收缩幅度为相对标准值,用百分比表示。
2.3.2 对KCl引起的内皮完整和去内皮血管环张力的影响 实验方法同上,以KCl(60mM)诱发最大收缩幅度。
2.4 独活肠吸收液舒张血管作用的Ca2+介导机制
2.4.1 抑制PE引起的内皮完整和去内皮血管环收缩的Ca2+介导机制 将内皮完整或去内皮的血管环置于无Ca2+的K-H液中平衡1 h,其间每隔20 min换液1次。以独活肠吸收液孵育血管环10 min,再以1 μM的PE使收缩达最大峰值后,每隔5 min依浓度梯度加入CaCl2(1×10-7~1×10-4mol·L-1),观察血管收缩反应。对照组为同一大鼠未经独活肠吸收液孵育的主动脉环。
2.4.2 抑制KCl引起的内皮完整和去内皮血管环收缩的 Ca2+介导机制 实验方法同上,以60mM的KCL使收缩达最大峰值。
2.5 统计学方法
采用SPSS 13.0统计软件进行统计分析,数据以均数 ±标准差(±s)表示,各组数据采用Student’st test进行统计,P<0.05为差异有统计学意义。
3 结果
3.1 对PE引起的内皮完整与去内皮血管环张力的影响
表1图1、2显示,独活肠吸收液能够浓度依赖性舒张PE引起的内皮完整与去内皮血管环收缩,内皮完整组与去内皮组最大舒张率比较差异无统计学意义(P>0.05)。

表1 对PE引起内皮完整与去内皮血管环的舒张作用
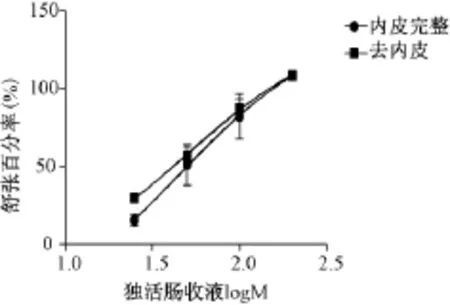
图1 独活肠吸收液对PE引起的内皮完整与去内皮血管环的舒张作用

图2 独活肠吸收液对PE引起的内皮完整与去内皮血管环的舒张实验过程图
3.2 对KCl引起的内皮完整与去内皮血管环张力的影响
表2图3、4显示,独活肠吸收液能够浓度依赖性舒张KCl引起的内皮完整与去内皮血管环收缩,内皮完整组与去内皮组最大舒张率比较差异无统计学意义(P>0.05)。

表2 对KCl引起的内皮完整与去内皮血管环的舒张作用
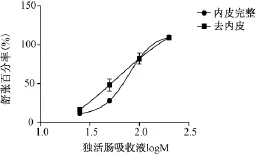
图3 独活肠吸收液对KCl引起的内皮完整与去内皮血管环的舒张作用
3.3 抑制PE引起的内皮完整和去内皮血管环收缩的Ca2+介导机制
表3图5、6显示,在无Ca2+的K-H液中,预先以60mM的KCL或1μM的PE收缩血管产生微弱持续的收缩,由 CaCl2(1×10-7~1×10-4mo1· L-1)刺激后收缩力显著升高,呈剂量依赖性。经独活肠吸收液孵育后,CaCl2所致最大收缩效应显著减弱(P<0.01)。

图4 独活肠吸收液对KCl引起的内皮完整与去内皮血管环舒张实验过程图
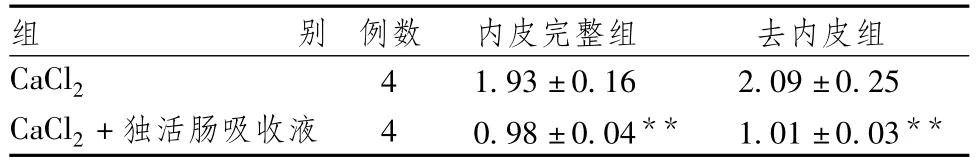
表3 对PE引起的内皮完整和去内皮血管环最大收缩力影响
3.4 抑制KCl引起的内皮完整和去内皮血管环收缩的Ca2+介导机制
表4图7、8显示,在无Ca2+的K-H液中,预先以60mM的KCL或1μM的PE收缩血管产生微弱持续的收缩,由 CaCl2(1×10-7~1×10-4mo1· L-1)刺激后收缩力显著升高,呈剂量依赖性。经独活肠吸收液孵育后,CaCl2所致最大收缩效应显著减弱(P<0.01)。

表4 对KCl引起的内皮完整和去内皮血管环最大收缩力影响
4 讨论
口服给药是最常用的临床给药途径之一。小肠是药物吸收的主要部位,药物口服吸收的程度与速度主要取决于肠内酶及其细胞对药物的代谢和屏障作用。外翻肠囊法又称肠外翻法,它是由Wilson和Wiseman于1954年创建,最早用于研究葡萄糖和氨基酸在肠道的代谢和转运[8]。这种模型已成功地应用于药物在肠道的吸收、转运、代谢等方面,是一种能够快速反应药物吸收行为的体外方法。本研究采用独活肠吸收液方法与临床用药吸收途径更为相符,能够反映独活被生物体吸收的有效成分的作用及机制。
血管平滑肌舒张主要有两种方式,一种是内皮依赖性舒张反应(endothelium-dependent dilatation,EDD),指血管内皮细胞(VEC)在药物或生理性刺激的作用下释放内皮舒张因子,诱导血管产生舒张作用,它依赖于结构完整和功能正常的血管内皮,VEC主要分泌的血管舒张因子是由前列环素(PGI2)、一氧化氮(NO)及内皮依赖性超极化因子(DEHF)共同作用完成;另一种非内皮依赖性舒张反应(endothelium-independent dilatation,EID),是不依赖于血管内皮而直接作用于血管平滑肌导致血管舒张。血管平滑肌上的电压依赖性钙通道和受体操纵性钙通道均对平滑肌活动起重要影响[9]。

图5 对PE引起的内皮完整(左)和去内皮(右)血管环最大收缩力影响

图6 独活肠吸收液对CaCl2收缩内皮完整(左)和去内皮(右)血管环的实验过程图
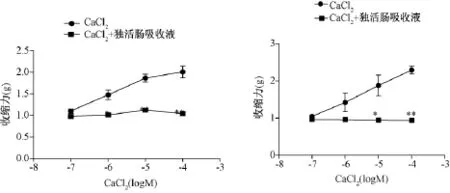
图7 对KCl引起的内皮完整(左)和去内皮(右)血管环最大收缩力影响

图8 独活肠吸收液对CaCl2收缩内皮完整(左)和去内皮(右)血管环的实验过程图
本研究结果显示,独活肠吸收液对kcl、PE引起的血管收缩具有较好的舒张作用并呈剂量依赖性,提示独活肠吸收液对血管舒张作用主要通过非内皮依赖性舒张反应实现,其直接作用于血管平滑肌而导致血管舒张。
血管是由内皮细胞、平滑肌细胞和成纤维细胞组成,细胞内钙离子浓度是血管收缩过程中的重要因素。当细胞内Ca2+浓度升高至一定水平,Ca2+与钙调蛋白(CaM)结合,激活肌球蛋白轻链激酶(MLCK),肌球蛋白轻链磷酸化,肌球蛋白与肌动蛋白结合,使血管收缩。当细胞内Ca2+浓度降低至一定水平,Ca2+与CaM分离,MLCK失活,血管松弛。而血管平滑肌细胞外Ca2+内流是引起细胞内Ca2+浓度升高的主要原因之一。细胞外高kcl可以激活电压依赖性钙通道,导致细胞外Ca2+内流而引起动脉环收缩。PE诱导的血管收缩,一方面通过作用于α1肾上腺素受体,激活磷脂酶C,产生三磷酸肌醇,刺激平滑肌细胞内贮钙的释放;另一方面,通过激活细胞膜上的受体操纵性钙通道和磷酸化电压依赖性钙通道使细胞外钙内流,因此PE通过细胞内游离钙浓度的增加而使血管收缩[10]。
本实验研究发现,内皮完整及去内皮的血管环经独活肠吸收液孵育后,都能明显抑制CaCl2引起的收缩,提示独活肠吸收液能通过抑制细胞外Ca2+内流,产生舒张血管效应。
[1]但飞君,蔡正军,朱烈彬,等.中药白根独活抗胃溃疡有效部位研究[J].三峡大学学报:自然科学版,2008,30(3):87-93.
[2]邹玺,王瑞平,戴虹,等.独活抗血管生成作用的实验研究[J].南京中医药大学学报,2008,24(3):194-196.
[3]张知侠.短毛独活精油提取及抑菌作用的研究[J].咸阳师范学院学报,2007,22(2):33-34.
[4]卢永昌,张雪梅.独活抗氧化作用的研究[J].青海师专学报:教育科学,2004(5):74-76.
[5]李荣芷,孟娟知,何云庆,等.中药独活抗心律失常活性成分γ氨基丁酸的研究[J].北京医科大学学报,1989,21(5): 376.
[6]李荣芷,何云庆,孟娟如,等.中药独活杭血小板聚集及抑制实验性血栓形成的活性成分研究[J].北京医科大学学报,1988(1):22.
[7]李振坤,刘玫琦,杨洪军,等.伞形科辛味中药主要化学成分对离体血管作用研究[J].中药药理与临床,2009,25(1): 38-40.
[8]WILSONT H,WISEMAN G.The use of sacs of evened small intestine for the study of the transference of substances from the mucosal to the serosal surface[J].Physiology,1954,123(1): 116.
[9] MANCINI GB,HENRY GC,MACAYA L,et al.Angiotensin converting enzyme inhibition,with quinapril, improves endothelial vasomotor dysfunction in patients with coronary artery disease:The TREND study(trial on reversing endothelial dysfunction)[J].Journalofthe American College of Cardiology,1996,27(2):258-265.
[10]姜建芳,沈晓兰,张宁.山楂总黄酮对大鼠离体血管功能的影响及其机制[J].中国现代应用药学,2011,28(7):614-617.
Effect of Intestinal Absorption Solution of Angelica Pubescens on the Tension of Rat Thoracic Aortic
HUANG ying1,WU hong-wei2,WANG yan-ping3△
(1.Experimental Research center,China Academy of Chinese Medical Sciences,Beijing 100700,China; 2.Institute of Chinese Materia Medica,China Academy of Chinese Medical Sciences,Beijing 100700,China;
3.Institute of Basic Research in Clinical Medicine,China Academy of Chinese Medical Sciences,Beijing 100700,China)
Objective:To observe the vasodilatation effect of intestinal absorption solution of Angelica Pubescens on thoracic aorta and its related mechanism.Methods:Intestinal absorption solution of Angelica Pubescens was prepared by everted gut sac method in vitro.To investigate the influence and the calcium-related mechanisms of intestinal absorption solution of Angelica Pubescens on endothelium intact or endothelium denuded with PE and KCl.Results:Intestinal absorption solution of Angelica Pubescens could produce relaxation of thoracic aortic rings pre-contracted by PE and KCl with endothelium intact or denuded in a dose dependent manner.There was no significant difference between the endothelium intact group and the endothelium denuded group.Intestinal absorption solution of Angelica Pubescens inhibit CaCl2-induced maximum contraction effect.Conclusion:Intestinal absorption solution of Angelica Pubescens shows vasodilator effects on a dose-dependent manner.The vasodilatation effect is mediated by inhibition of extracellular Ca2+influx.
Angelica Pubescens;Intestinal Absorption Solution;Vasodilation;Mechanism
R285.5
B
1006-3250(2017)02-0187-04
2016-07-13
国家自然科学基金资助项目(81273901)-伞形科常用辛味中药的成分组合与活血功效关联性研究
黄 颖(1978-),女,甘肃人,副研究员,医学博士,从事中药及复方作用机理研究。
△通讯作者:王燕平(1963-),男,研究员,医学本科,从事中医管理与科学研究、中医养生保健理论与方法及传染病中医药防治研究。

