穴位埋线对去卵巢大鼠骨密度及相关细胞因子的影响
王卫强
(山西大医院中医科,山西 太原 030032)
穴位埋线对去卵巢大鼠骨密度及相关细胞因子的影响
王卫强
(山西大医院中医科,山西 太原 030032)
目的:观察穴位埋线对去卵巢骨质疏松大鼠血清IGF-1及TNF-α含量的影响。方法:40只雌性大鼠分为伪手术组10只,去卵巢组30只(空白模型组10只、穴位埋线组、雌二醇组各10只)行相应治疗,12周后取血清测E2、IGF-1、TNF-α的含量,单侧股骨测骨密度。结果:空白模型组骨密度较伪手术组明显降低,治疗组显著高于空白模型组(P<0.05)。血清E2、IGF-1空白模型组含量低于伪手术组,治疗组显著高于空白模型组(P<0.05)。血清TNF-α空白模型组含量显著高于伪手术组,治疗组显著低于空白模型组(P<0.05)。结论:穴位埋线对去卵巢骨质疏松大鼠有一定的预防及延缓骨质疏松进展的作用。
穴位埋线;大鼠;骨密度;E2;IGF-1;TNF-α
本研究采用去卵巢复制大鼠绝经后骨质疏松症(postmenopausal osteoporosis,PMOP)模型,比较穴位埋线,雌激素对PMOP模型骨密度、血清E2、IGF-1、TNF-α含量的影响,为穴位埋线防治绝经后骨质疏松提供实验依据。
1 实验动物
6月龄未生育SD雌性大鼠40只,体质量240~280g,由贵阳医学院实验动物中心提供。
2 主要试剂与仪器
E2放免试剂盒、IGF-1放免试剂盒,TNF-α放免试剂盒(天津九鼎医学生物工程有限公司)。皮内针(麦粒型,江苏华佗医疗器械厂生产)。苯甲酸雌二醇(上海通用药业集团有限公司,批号050101)2mg/mL。双能X线骨密度测量仪(法国CHALLENGER公司)。多头放射免疫检测仪(GC-2010,中国科大中佳公司)。
3 动物饲养
各组动物在相同环境中分组分笼喂养,每笼5只,环境温度(20±3)℃,每天12h光照,12h黑暗,相对湿度40%左右,自由摄食和饮水。饲料成分为面粉20%、玉米粉20%、麦麸粉15%、鱼粉5%、豆饼20%、骨粉2%、食盐1%、植物油2%、奶粉15%,由贵阳医学院动物中心提供。
4 动物分组
40只雌性大鼠随机分为伪手术组10只与去卵巢模型30只。将30只去卵巢大鼠随机分为空白模型组10只和治疗组20只,分别为穴位埋线组和雌激素组,各组10只。
5 造 模
去卵巢大鼠模型用10%水合氯醛0.3mL/100g腹腔注射麻醉后,仰卧位固定,在剑突下2cm处腹正中线上行1.5cm纵向切口,完整摘除双侧卵巢,缝合腹腔。伪手术组(Sham)同样麻醉后在无菌条件下打开腹腔,不摘除卵巢,仅摘除卵巢周围的脂肪组织,大小与卵巢相同,分两层缝合。手术后给予常规青霉素肌注3天。
6 实验方法
穴位埋线组:选大鼠脾俞、肾俞,用7号埋线针,长约5~8mm,3个0的羊肠线进行埋线,2周1次。
雌激素组:以苯甲酸雌二醇后肢肌内注射,按人鼠剂量换算,每只鼠每次肌内注射0.1mg/kg,每周1次。在造膜1周后进行治疗,为期12周。
空白模型组及伪手术组:雌激素组治疗时,同样空白模型组及伪手术组两组大鼠相应抓取按压刺激,以保证条件的均衡性。
7 取材与测量
大鼠治疗12周后,股动脉取血,收集血清,应用放免法检测血清E2、IGF-1 及TNF-α(由贵阳医学院附院中心实验室十三协助完成)。无菌条件下完整取出右侧后肢股骨,剔净软组织。用双能X线骨密度仪测量,以“Small Animal Scout Scan”分析,扫描宽度为15cm,扫描速度60mm/s,对股骨整体、股骨近端、股骨远端进行骨密度及骨矿含量检测。
8 统计学处理
9 结 果
各组股骨骨矿含量与骨密度见表1。
表1 各组股骨骨矿含量与骨密度比较 (±s)
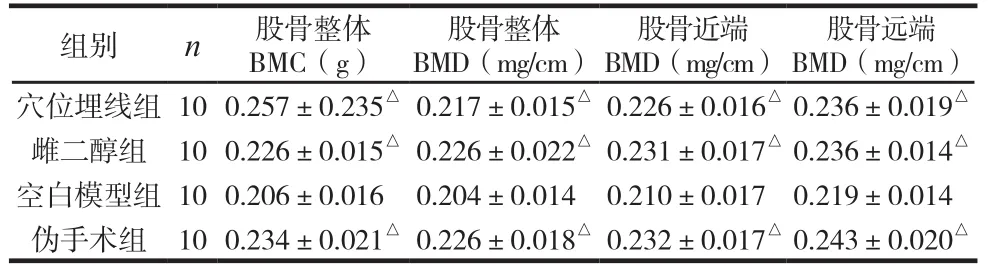
表1 各组股骨骨矿含量与骨密度比较 (±s)
注:与空白模型组比较,△P<0.05。
组别 n 股骨整体BMC(g)股骨整体BMD(mg/cm)股骨近端BMD(mg/cm)
各组血清E2、IGF-1、TNF-α含量见表2。
表2 各组血清E2、IGF-1、TNF-α比较 (±s)

表2 各组血清E2、IGF-1、TNF-α比较 (±s)
注:与空白模型组比较,*P<0.05;与伪手术组比较,#P<0.05;与雌二醇组比较,△P<0.05。
?
10 讨 论
雌激素是维持骨吸收和骨形成平衡的重要因素,雌激素水平降低导致骨形成抑制、骨吸收亢进已得到多数学者的公认。通过穴位埋线的治疗,去卵巢大鼠的骨密度及骨矿含量较模型组显著提升,且与雌激素及伪手术组无差异。穴位埋线组血清E2水平低于伪手术组且有显著性差异,而穴位埋线组的骨密度与骨矿含量与伪手术组无明显差异,可见穴位埋线对去卵巢大鼠作用不单纯是通过提高雌激素水平来介导的,还可能通过其它激素及包括IGF-1、TNF-α在内的一些相关细胞因子的相互作用来达到减缓骨质疏松进展。研究发现IGF-I是包括成骨细胞在内的多种细胞的促有丝分裂剂,IGF-1促进成骨细胞增殖、分化和募集,抑制细胞凋亡,刺激骨胶原的转录和DNA合成,抑制胶原的降解,增加骨基质沉积。IGF-1也可通过不依赖促有丝分裂的途径促进骨基质的合成和矿化,它以自分泌和旁分泌的形式调节骨骼细胞的功能,影响骨代谢[1]。Ostrowska等[2]采用去卵巢大鼠做骨质疏松模型,动态观察血清IGF-1水平,结果发现血清IGF-I浓度呈减低趋势,术后2-28周显著低于假手术对照组,在本实验中也得到证实。随着妇女更年期雌激素水平的下降,诱导骨吸收的细胞因子产生过多,使骨吸收活动增强。TNF-α是目前发现的强有力的骨吸收诱导剂,TNF-α引起骨吸收主要是通过刺激前祖细胞产生新的破骨细胞以增加破骨细胞数量,间接激活成熟的破骨细胞增强其吸收功能,并抑制破骨细胞的凋亡,呈现出对骨的快速分解效果[3]。TNF-α同时还可抑制成骨细胞的功能,降低成骨细胞碱性磷酸酶的活性,以减少骨基质钙化。研究发现[4],绝经后骨质疏松病人外周血中单个核细胞释放的TNF-α明显高于非绝经妇女或雌激素替代治疗绝经妇女,且与腰椎骨密度负相关,动物实验得出了类似结果。
骨质疏松症属中医“骨痿”、“骨痹”范畴,《素问·痿论》曰:“肾气热,则腰背不举,骨枯而髓减,发为骨痿。”华佗在《中藏经·五痹》中曰:“骨痹者,乃嗜欲不节,伤于肾也。肾气内消则不能关禁,不能关禁则中上俱乱,中上俱乱则三焦之气痞而不通。三焦痞,则饮食不糟粕,饮食不糟粕,则精气日衰,精气日衰,则邪气妄入。邪气妄入……下流腰膝,则为不遂,旁攻四肢,则为不仁,寒在中则脉迟……”认为骨质疏松发病的根本原因在于肾虚,由肾虚导致三焦之气机不畅,脾失健运,水谷精微不化,外邪乘虚而入所致。可见骨质疏松与脾肾虚衰的关系最为密切。因此,防治骨质疏松症必须以纠正脾肾虚亏为主。本实验选取脾俞、肾俞以健脾补肾、强筋壮骨,调节内分泌。通过背俞穴肌肉、神经、血管、淋巴等组织的刺激作用于全身,使大鼠下丘脑-垂体-多个靶腺轴及植物神经系统和免疫功能的紊乱恢复。显示穴位埋线可使模型大鼠骨密度与骨矿含量显著增加且与雌激素组无差异。可能机制是通过脏腑经络的调理,提高模型动物雌激素水平,提高机体的代谢,增加肠道对Ca的吸收利用,提高IGF-I的表达,降低TNF-α表达及调节相关的细胞因子和激素,促进成骨细胞增殖分化,使成骨活动增强,抑制破骨细胞增殖分化,使破骨活动减弱,从而预防及治疗骨质疏松。
雌激素替代疗法(Estrogen Replacement therapy,ERT)是预防和治疗PMOP以及预防骨折的首选方法,但大量研究表明长期使用雌激素类药物有导致乳腺癌、子宫内膜癌的潜在危险[5]。实验可知,穴位埋线预防及治疗骨质疏松能起到ERT的相同作用。且穴位埋线无副作用,故穴位埋线防治骨质疏松症具有较大的潜力与优势,值得进一步的深入研究。
[1] CELIKER R,ARSLAN S.comparison of serum insulin-like growth factor-1 and growth hormone levels in osteoporotic and non-osteoporotic post-menopausal women[J].Rheumatology International,2000,19(6):205-208.
[2] OSTROWSKA Z,KOS-KUDLA B,MAREK B,et al.Dynamic pattern of IGF-1 and chosen biochemical markers of bone metabolism in a rat model of postmenopausal osteoporosis[J].Endocrine Regulations,2002,36(1):9-17.
[3] KOBAYASHI K,TAKAHASHI N,JIMI E,et al.Tumor necrosis factor a1pha stimu1ates osteoblast differentiation by a mechanism independent of the ODF/RANKL-RANK interaction[J].J Exp Med,2000;191(2):275-286.
[4] NANES MS.Tumor necrosis factora:molecular and cellular mechanisms in skeletal pathology[J].Gene,2003,321(56):1-15.
[5] 田李军.中医药治疗绝经后骨质疏松症的研究概况[J].四川中医,2002,20(2):22.
Objective:To observe the effect of catgut implantation at acupoint on content of serum IGF-1 and TNF-α in ovariectomized osteoporosis(OVX-OP) rats. Method:Forty rats were divided into four groups,ten rats in each group.The first group were sham-operated(Sham-G) while the remaining groups,established by excising both sides ovary,were catgut implantation at acupoint group(EAG),estradiol group(EG) and model group(MG).There wasn’t any therapy in sham-operated group and model group.After 12 week corresponding therapy,all groups were sacrificed to procure blood serum for testing the contents of E2,IGF-1,TNF-α and right retral thighbone for testing bone mineral density(BMD).Result:The BMD of thighbone, IGF-1 of serum in EAG and EG was compared with Sham-G,there was no significant difference,but which was higher than MG(P<0.05),at same time which of MG was lower than Sham-G. TNF-α of serum in MG was higher than Sham-G,EAG and EG(P<0.05),but no significant difference was found among Sham-G,EAG and EG. Conclusion:Catgut implantation at acupoint could promote BMD in ovariectomized osteoporosis rats,so they can probably be usesed to prevent and treat PMOP.
Catgut implantation at acupoint;rat; bone mineral density;E2 ;IGF-1;TNF-α
R245.919.144
B
1004-2814(2017)02-0112-02
2016-09-26

