分子印迹固相萃取-化学发光法测定贝母素甲
韩鸿萍, 马天一, 向 辉, 谭 力, 郑 红,3*
(1. 青海师范大学 化学系, 西宁 810008; 2. 重庆师范大学 化学学院, 重庆 410331;3. 中国科学院 青海盐湖研究所, 西宁 810008; 4. 重庆大学 光电工程学院, 重庆 400044;5. 陕西师范大学 化学化工学院, 西安 710062)
分子印迹固相萃取-化学发光法测定贝母素甲
韩鸿萍1,5, 马天一4, 向 辉2, 谭 力2, 郑 红2,3*
(1. 青海师范大学 化学系, 西宁 810008; 2. 重庆师范大学 化学学院, 重庆 410331;3. 中国科学院 青海盐湖研究所, 西宁 810008; 4. 重庆大学 光电工程学院, 重庆 400044;5. 陕西师范大学 化学化工学院, 西安 710062)
将制备的粒径为70~100 μm贝母素甲分子印迹聚合物作为填料制作了分子印迹固相萃取(MIP-SPE)柱。将含有贝母素甲的样品溶液经过MIP-SPE后,在盐酸-高锰酸钾-甲醛的体系下,进行化学发光检测,建立了测定贝母属类样品中贝母素甲含量的分子印迹-化学发光法。贝母素甲的浓度在5.0×10-7~5.0×10-5mol·L-1内与化学发光强度呈线性关系,检出限(3s)为2.0×10-7mol·L-1。加标回收率在97.2%~102%之间,测定值的相对标准偏差在1.7%~2.2%之间。
贝母素甲; 分子印迹聚合物; 固相萃取; 化学发光法
贝母为百合科属植物,具有镇咳、祛痰、平喘、抗菌等功效,主要用于哮喘、支气管炎、淋巴结核、干咳少痰等疾病的治疗[1-2]。贝母素甲生物碱是贝母属植物的主要活性成分之一。目前测定贝母素甲的方法有酸性染料比色法[3]、重量法[4]、近红外光谱法[5]、薄层扫描法[6]、高速逆流色谱法[7]和高效液相色谱法[8-15]等。
化学发光法[16]具有很多优点,在食品检测、药物分析和大气污染检测等方面得到了广泛的应用。但其选择性存在一定的劣势,若其与具有特异识别性和选择性的分离手段联用,便能提高选择性,而近年来发展较为迅速的分子印迹聚合物技术便是一个较好的选择。
分子印迹聚合物(MIP)最早用于生物酶催化领域,后来逐步拓展到分离分析[17-18]领域。它是把模板分子、功能单体、制孔剂、交联剂一起聚合,得到高交联的刚性聚合物,再通过采用一定的物理或化学手段将模板分子洗脱出来,留下了具有特殊空间结构的空穴,其空穴对模板分子具有高度的选择吸附和特异识别性能。
本工作利用分子印迹聚合物技术,通过逐步聚合反应,分别以贝母素甲、环氧树脂、聚乙二醇1000和二乙烯三胺作为模板分子、功能单体、致孔剂和交联剂,制备出了贝母素甲分子印迹聚合物,选取粒径70~100 μm的贝母素甲分子印迹粉末,制作固相萃取柱(SPE),将其连入流动注射化学发光仪中,使用贝母素甲-酸性高锰酸钾-甲醛化学发光体系进行检测,建立测定贝母素甲的分子印迹固相萃取-化学发光分析法。
1 试验部分
1.1 仪器与试剂
IFFL-DD型流动注射化学发光仪;UV 2550型紫外-可见分光光度计;KQ-5200DB型数控超声波清洗器;AB 2042N型电子天平。
贝母素乙和(源叶生物);川贝母、浙贝母和青海暗紫贝母;环氧树脂。
高锰酸钾储备溶液:1.0×10-2mol·L-1,称取高锰酸钾3.16 g溶于2 L沸水中,过滤,室温下放置一周后使用。
二乙烯三胺和聚乙二醇1000为分析纯;试验用水为重蒸馏水。
1.2 贝母素甲MIP的制备
称取聚乙二醇1000(PEG) 4.0 g于500 mL烧杯中,在60 ℃水中溶解,加入贝母素甲1.0 mmol,搅拌混匀;然后加入二乙烯三胺1 g,继续混匀,随后加入环氧树脂4 g,强烈搅拌10 min后,超声振荡脱气,得到聚合物溶液,将其移入已封口的5.0 mL一次性注射器中,密封后,置于恒温烘箱内,保持在60 ℃下加热聚合反应24 h,得到白色棒状贝母素甲MIP。取出后冷却至柱体硬化,使用锉刀等工具将柱体变为粉末状。将粉末放入烧杯中,用60 ℃的水反复多次冲洗后,置于60 ℃烘箱中,研磨过筛,收集70~200 μm的粒径粉末备用。
非印迹聚合物(NIP)的制备,除不加贝母素甲外,其余步骤与上述相同。
1.3 贝母素甲MIP-SPE柱的制备
取一截直型塑料管(3 mm×15 mm),一端先用少许玻璃棉塞填充,然后从另一端填充贝母素MIP 10.0 mg后用玻璃棉封口,即成贝母素甲MIP-SPE柱。同样方法制备NIP-SPE柱。
进行数据分析前,先让酸性高锰酸钾-甲醛体系流过MIP-SPE柱,去除MIP-SPE柱上的贝母素甲。当体系溶液流过MIP-SPE柱时,与MIP-SPE柱的贝母素甲发生反应,产生化学发光信号。随着MIP-SPE柱中的贝母素甲被消耗,化学发光信号开始降低。当信号降至与NIP-SPE柱的信号相同且稳定时,表明MIP-SPE柱中的贝母素甲完全脱附。用水将MIP-SPE柱洗净,备用。
1.4 测定方法
按照图1流程,对贝母素甲进行测定。

P1,P2-蠕动泵;D-检测器;F-MIP-SPE柱;PC-计算机;W-废液;V-六通进样阀;M-混合块a-高锰酸钾溶液;b-盐酸溶液;c-甲醛溶液;d-样品或标准溶液;e-水图1 分子印迹固相萃取-化学发光法流程示意图Fig. 1 Schematic diagram of MIP-SPE chemiluminescence process
步骤1:贝母素甲的吸附。静止P2,六通进样阀(V)在d位置,转动P1,贝母素甲溶液流过MIP-SPE柱50 s并被吸附在MIP-SPE柱的空穴内。
步骤2:洗涤除去其他杂质。P2静止,V在c位置,P1输送甲醛溶液过MIP-SPE柱90 s,MIP-SPE柱上的干扰物被去除。
步骤3:贝母素甲化学发光检测。V在c位置,同时转动P1和P2,高锰酸钾、盐酸和甲醛合并溶液过MIP-SPE柱30 s,与吸附在MIP-SPE柱上的贝母素甲发生化学发光反应产生信号。
步骤4:清洗MIP-SPE柱。停止P1,V在e位置,P2转动,让水流过MIP-SPE柱70 s,洗去MIP-SPE柱上的残留物,备用。
2 结果与讨论
2.1 贝母素甲MIP的结合特性
使用振荡吸附法考察贝母素甲在MIP上的结合性能。在12个25 mL比色管内加入不同浓度(0~10.0 mmol·L-1)贝母素甲甲醇溶液5.0 mL,然后加入去除贝母素甲的MIP粉末50.0 mg,在室温下,置于恒温水浴中结合12 h。取离心分离后的适量溶液稀释至一定体积,在波长270 nm处,用紫外分光光度法测定贝母素甲的浓度,根据3次平行测定的平均值,计算贝母素甲在MIP上的结合量,采用Scatchard分析所测数据。以Q/C对Q作图,得图2。

图2 贝母素甲印迹聚合物的Scatchard曲线Fig. 2 Scatchard plot of methyl Peimine-imprinted polymer
图2中,Q/C对Q呈非线性关系,表明MIP对贝母素甲的吸附作用不是完全等价的,说明贝母素甲与MIP的结合存在高亲和力和低亲和力两种位点。拟合图中的两条直线,由此可以计算高亲和力结合位点的Kd1为6.92×10-4mol·L-1,最大表观结合量Qmax1为221.5 μmol·g-1,低亲和力结合位点的Kd2为4.31×10-3mol·L-1,最大表观结合量Qmax2为232.19 μmol·g-1。
2.2 贝母素甲MIP-SPE柱的填料粒径及稳定性
分别称取粒径70~100 μm和粒径100~200 μm的MIP粉末,制作MIP-SPE柱并连接在流通池中进行试验。结果表明:填充70~100 μm的MIP粉末的MIP-SPE,其化学发光信号强度大且重现性好。试验选择MIP粉末的粒径为70~100 μm。
对制作好的贝母素甲MIP-SPE柱重复使用百次以上,发现性能没有明显的变化,说明贝母素甲MIP-SPE柱性能稳定。
2.3 固相萃取条件的优化
2.3.1 吸附时间
当样品溶液通过贝母素甲MIP-SPE柱时,根据吸附剂量、溶液流量、浓度和吸附时间的不同,信号值会不同。固定贝母素甲的MIP量为20 mg,流量为2.0 mL·min-1,在10~120 s内考察吸附时间对化学发光强度的影响,结果见图3。
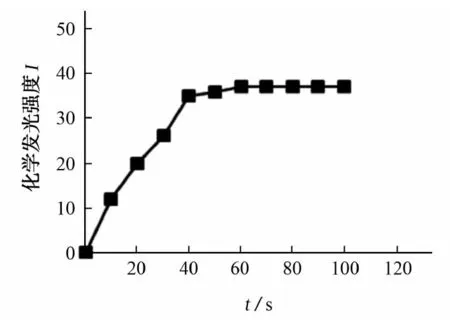
图3 吸附曲线Fig. 3 Adsorption curve
由图3可知:对于5.0×10-4mol·L-1贝母素甲溶液,随着吸附时间的增加,化学发光强度增大,吸附时间增加到50 s后,化学发光强度基本不再发生变化。所以试验选择50 s作为吸附时间。
2.3.2 洗涤时间
为了确定洗涤时间,试验选择与贝母素甲结构相近且同样能和体系发生化学反应的贝母素乙作为干扰物质。将浓度为5.0×10-4mol·L-1贝母素乙溶液加入到样品溶液中,然后考察10~200 s内洗涤时间对化学发光强度的影响。结果表明:当洗涤时间在90 s时,加入贝母素乙的样品溶液的化学发光强度趋于稳定,且基本与未加入贝母素乙的溶液的化学发光强度一致。试验确定洗涤时间为90 s。
2.3.3 化学发光反应时间
当体系的化学发光试剂流入MIP-SPE柱时,与富集在MIP-SPE柱上的贝母素甲发生反应,出现强烈的化学发光信号。当化学发光信号回到基线时,表明MIP-SPE柱上的贝母素甲已完全反应。试验表明完成此过程需要30 s。
2.3.4 清洗时间
当完成化学发光反应后,在10~120 s内,用水清洗MIP-SPE柱,清洗70 s即可将反应残留物洗净。因此,试验选择清洗时间为70 s。
2.4 化学发光反应条件的优化
2.4.1 保护剂
考察Na2S2O3、Na2SO3和甲醛等3种保护剂对体系化学发光强度的影响,结果表明:在盐酸介质中,甲醛和高锰酸钾体系产生最强的化学发光信号。所以,选择该体系的保护剂为甲醛。考察甲醛的质量比在10~60 g·kg-1内对MIP-SPE柱的保护作用,结果见图4。

图4 甲醛质量比对化学发光强度的影响Fig. 4 Effect of mass ratio of formaldehyde on chemiluminescence intensity
由图4可知:当甲醛的质量比为30 g·kg-1时,MIP-SPE柱对贝母素甲的选择性识别能力强且化学发光强度最大。
2.4.2 高锰酸钾浓度
考察高锰酸钾浓度在5.0×10-7~1.0×10-3mol·L-1内对体系化学发光强度的影响,结果见图5。

图5 高锰酸钾浓度对化学发光强度的影响Fig. 5 Effect of KMnO4 concentraction on chemiluminescence intensity
由图5可知:体系的化学发光强度在高锰酸钾浓度达到3.0×10-4mol·L-1时达到最大且基本保持稳定。所以,试验选择高锰酸钾的浓度是3.0×10-4mol·L-1。
2.4.3 酸介质
选择H2SO4、HNO3、HCl和H3PO4等不同介质,考察其对体系化学发光强度的影响。结果表明:体系在HCl介质中的化学发光强度最大 ,所以试验选择HCl介质。考察HCl浓度在0.5~8 mol·L-1内对体系化学发光强度的影响,结果见图6。

图6 HCl浓度对化学发光强度的影响Fig. 6 Effect of HCl concentraction on chemiluminescence intensity
由图6可知:HCl浓度在1.5 mol·L-1时体系的化学发光强度达到最大。所以,试验选择1.5 mol·L-1HCl溶液为酸介质。
2.5 干扰试验
在优化的试验条件下,分别使用MIP-SPE柱和未使用MIP-SPE柱测定3.0×10-5mol·L-1贝母素甲溶液,考察常见物质的干扰情况。结果表明:当相对误差在±5%之内时,各干扰物质的最大允许倍数见表1。
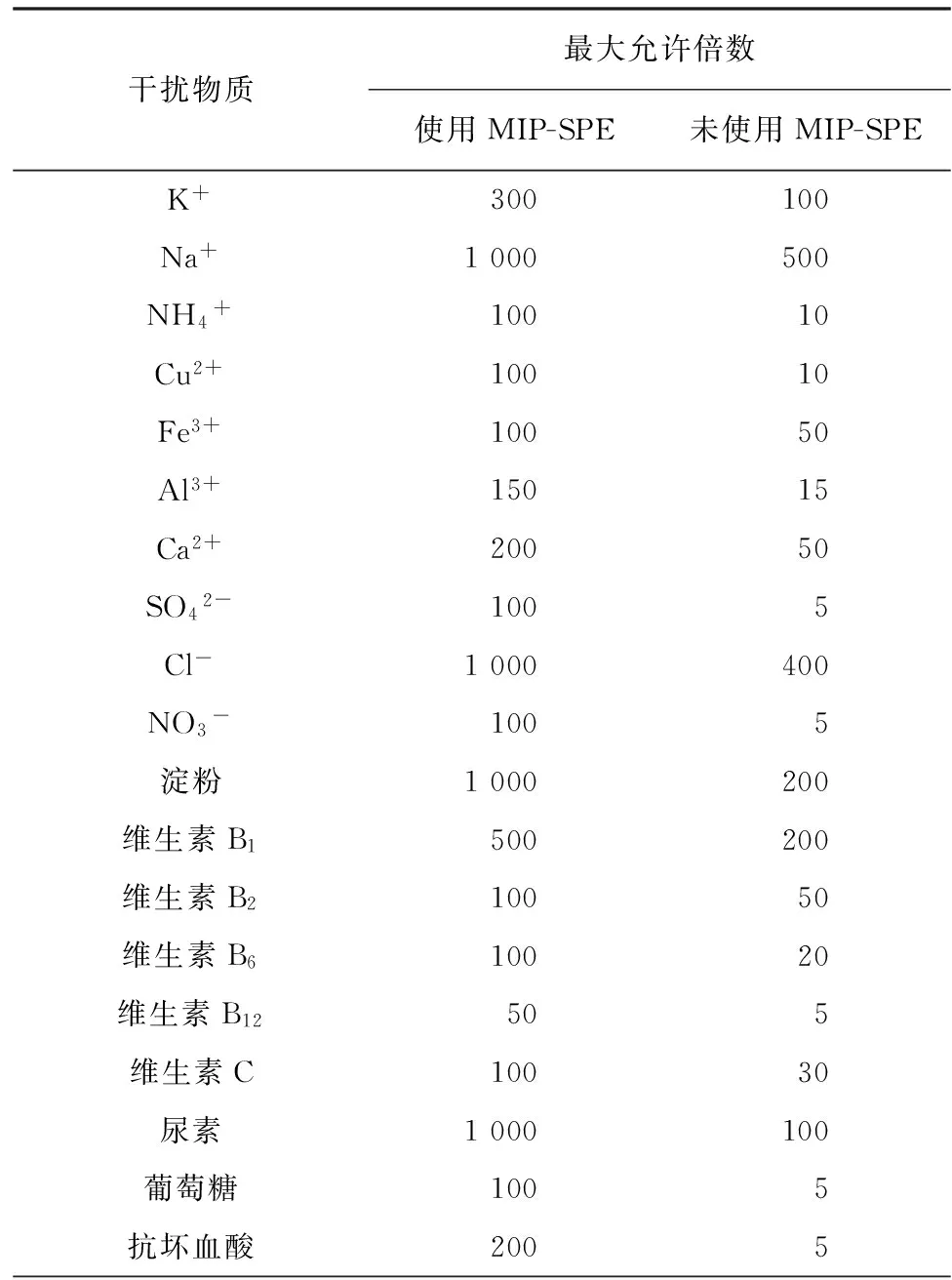
表1 干扰试验结果Tab. 1 Results of interference test

表1(续)
由表1可知:使用贝母素甲分子印迹聚合物固相萃取柱,有效地提高了化学发光法的选择性。
2.6 标准曲线与检出限
在优化的试验条件下,在5.0×10-7~5.0×10-5mol·L-1内,化学发光强度(I)与贝母素甲溶液浓度(c)呈线性关系,线性回归方程为I=7.893c+27.19,相关系数为0.998 4。对3.0×10-6mol·L-1贝母素甲溶液平行测定11次,测定值的相对标准偏差为3.6%。以11次空白溶液测定值的3倍标准偏差计算方法的检出限(3s)为2.0×10-7mol·L-1。
2.7 回收试验
在优化的试验条件下,将贝母素甲标准品加入空白样品溶液中,选择3个不同的加标量,按试验方法进行测定,结果见表2,加标回收率在97.2%~102%之间,说明该方法准确度较高。

表2 回收试验结果Tab. 2 Results of test for recovery
2.8 样品分析
分别称取1.000 g川贝母、浙贝母和暗紫贝母,研磨成粉末状,转移至100 mL容量瓶中,用水定容,浸泡5 h。取上层清液10 mL,加入80 g·L-1聚乙二醇溶液10 mL充分混合,再放置5 h。然后将样品溶液稀释到线性范围内按试验方法进行检测,平行测定3次,结果见表3。
本工作通过逐步聚合法合成了贝母素甲分子印迹聚合物,并将其制成固相萃取印迹柱,将此固相萃取柱与流动注射化学发光仪联用,作为分子识别原件,使用酸性高锰酸钾-甲醛发光体系,建立了高选择性的测定贝母素甲的分子印迹固相萃取-化学发光法。该方法具有较宽的线性范围和较低的检出限,可用于贝母属类样品中的贝母素甲的测定,并得到了满意的结果。

表3 样品分析结果(n=3)Tab. 3 Analytical results of samples
[1] 谢志民,吕润霞.贝母类中药功效订正[J].中药材, 2001,24(8):600-602.
[2] 于晓琳,季晖,王长礼,等.贝母的药理作用研究概况[J].中草药, 2000,31(4):313-314.
[3] 彭仕梅,高明远.酸性染料比色法测定川贝母中贝母素甲的含量[J].中国药事, 2006,20(1):687-688.
[4] 沙世炎.中草药有效成分分析法(上册)[M].北京:人民卫生出版社, 1982:59.
[5] 赵耀东,杜伟锋,王胜波,等.基于近红外光谱的浙贝母中贝母素甲和贝母素乙含量快速检测方法的建立[J].中华中医药学刊, 2013,31(4):756-758.
[6] 李成网,李清华.薄层扫描法测定皖贝精胶囊贝母素甲的含量[J].中国实验方剂学杂志, 2001,7(3):21-22.
[7] 金艳,沈平孃,张继全,等.高速逆流色谱法分离纯化浙贝母中贝母素甲、贝母素乙[J].中药研究与信息, 2005,7(12):13-15.
[8] 钱春花,何建华,孙志明.HPLC-ELSD测定乌贝益胃胶囊中贝母素甲和贝母素乙含量[J].中国中医药信息杂志, 2013,20(30):57-59.
[9] 唐云,刘汉清.HPLC-ELSD测定散结镇痛片中贝母素甲、贝母素乙[J].中成药, 2012,34(7):1295-1298.
[10] 杜伟锋,贾永强,张焱新,等.HPLC-ELSD法同时测定浙贝母饮片硫熏前后3种有效成分的含量[J].药物分析杂志, 2015,35(4):675-678.
[11] 马双成,张树潘,鲁静,等.高效液相色谱一蒸发光散射检测法测定鹤蟾片中贝母素甲和贝母素乙的含量[J].药物分析杂志, 2008,28(1):118-120.
[12] 徐玲,彭文兵,冯颂桥.3种贝母类药材贝母素甲和贝母素乙含量测定方法的优化[J].中国药师, 2015,18(8):1299-1301.
[13] 朱雪妍.HPLC-ELSD法测定胃可宁片中贝母素甲和贝母素乙含量)[J].中国医院用药评价与分析, 2015,15(2):165-167.
[14] 苏健,王宝琹,林瑞超.十几种贝母及其制剂中贝母素甲、乙及西贝碱的检验方法和品质的研究与进展[J].中国药事, 2013,27(1):88-92.
[15] 张雯杰,陈波,姚守拙.贝母生物碱的高效液相色谱-质谱联用分析[J].药物分析杂志, 2008,28(8):1217-1221.
[16] SOLOMONIA R O, MCCABE B J. Molecular mechanisms of memory in imprinting[J]. Neuroscience & Biobehavioral Reviews, 2015,50(3):56-59.
[17] 郭海燕,郑红,张晶,等.磺胺的分子印迹流动注射化学发光方法研究[J].分析科学学报, 2013,29(2):196-200.
[18] 郑红,张晶,夏晓姗,等.表面铅(Ⅱ)印迹聚合物的制备及其分离富集性能研究[J].理化检验-化学分册, 2014,50(8):1008-1012.
Determination of Peimine by Chemiluminescence with MIP-SPE
HAN Hong-ping1,5, MA Tian-yi4, XIANG Hui2, TAN Li2, ZHENG Hong2,3*
(1.DepartmentofChemistry,QinghaiNormalUniversity,Qinghai810008,China;2.DepartmentofChemistry,ChongqingNormalUniversity,Chongqing410331,China;3.QinghaiInstituteofSaltLakes,ChineseAcademyofSciences,Xining810008,China;4.CollegeofOptoelectronicEngineering,ChongqingUniversity,Chongqing400044,China;5.CollegeofChemistryandChemicalEngineering,ShanxiNormalUniversity,Xi′an710062,China)
The molecular imprinted polymer solid-phase extraction (MIP-SPE) column was made of the synthesized peimine imprinted polymer with particle size of 70-100 μm as filler. After peimine in the sample solution was extracted with MIP-SPE, chemiluminescence reaction was found in the system of hydrochloric acid-potassium permanganate-formaldehyde. Base on this, the method of chemiluminescence combined with peimine-imprinted polymer solid-phase extraction was proposed to determine peimine in Fritillaria samples. Linear relationship was found between the chemiluminescence intensity with the concentration of peimine in the range of 5.0×10-7-5.0×10-5mol·L-1, with detection limit (3s) of 2.0×10-7mol·L-1. Recovery rates obtained by standard addition method were in the range of 97.2%-102% and RSDs were in the range of 1.7%-2.2%.
Peimine; Molecular imprinting polymer; Solid phase extraction; Chemiluminescence
10.11973/lhjy-hx201703006
2016-02-08
青海省科技厅项目(2013-Z-752);重庆市教委科技 项目(KJ130650);国家自然基金项目(21267018);中国科学院“百 人计划”基金资助项目(Y410021011)
韩鸿萍(1974-),女,青海乐都人,副教授,博士研究 生,主要从事药物分析研究工作。
* 通信联系人。E-mail:zhenghong670@163.com
O657.3
A
1001-4020(2017)03-0275-06

