全水相制备聚甲基丙烯酸纳米水凝胶及其磁性功能化研究
陆亚明,张幼维,赵炯心
(东华大学材料科学与工程学院,上海 201600)
研究论文
全水相制备聚甲基丙烯酸纳米水凝胶及其磁性功能化研究
陆亚明,张幼维*,赵炯心
(东华大学材料科学与工程学院,上海 201600)
采用改进乳液聚合方法,实现了聚甲基丙烯酸(PMAA)纳米水凝胶的水相“绿色”制备。再以PMAA纳米水凝胶为前躯体,采用原位氧化法制备磁性PMAA纳米水凝胶。利用动态光散射,振动样品磁强计,热重分析等对PMAA纳米水凝胶及磁性PMAA微球的尺寸、磁含量等进行表征。结果表明,磁性PMAA纳米水凝胶具有超顺磁性,磁含量高达61.4%,在生物医用、废水处理等方面具有广阔的应用前景。
聚甲基丙烯酸 纳米水凝胶 磁性功能化
智能纳米水凝胶是指那些能够对外界特定的刺激源(如温度、pH、压力、磁场等)产生相应的物理结构或化学性质变化的一类高分子水凝胶。当其粒径小于1 μm时,则被称作智能纳米水凝胶。在药物控释载体、化学分离、催化反应和生物传感器等领域具有广泛应用[1-4],已成为智能材料和纳米材料的重要研究内容。随着科学研究发展,为进一步增强智能纳米水凝胶应用范围,人们尝试将各种功能性纳米粒子,如荧光量子点、磁性纳米粒子等,与智能纳米水凝胶复合,制备智能杂化纳米水凝胶[5-8],从而赋予其更优良的应用性能,其中研究较多的是磁性纳米水凝胶[9-12]。目前含高浓度功能基团(如羧基)的磁性纳米水凝胶主要采用反相乳液聚合、反相微乳液聚合、反相细乳液聚合和蒸馏(回流)沉淀等方法制备[13-17]。但上述合成方法均需使用大量的有机溶剂,易造成环境污染。
笔者首先在水相中制备了聚甲基丙烯酸(PMAA)纳米水凝胶,再以其为前躯体采用原位氧化沉淀的方法,在水相中成功制备了磁性纳米水凝胶。这种磁性纳米水凝胶是一种典型的pH敏感型纳米水凝胶,带有大量羧酸功能基团,具有良好生物相容性,可连结多肽、蛋白质和生物酶,也可经修饰连接其他的官能团,是理想的磁性功能化载体。
1 试 验
1.1 原料
聚氧乙烯失水山梨醇单月桂酸酯(吐温-20),分析纯;甲基丙烯酸(MAA)、十二烷基硫酸钠(SDS)均为化学纯;氢氧化钠、四水合氯化亚铁、亚硝酸钠、氨水均为优级纯,国药集团化学试剂有限公司制;偶氮二异丁腈(AIBN),N,N-亚甲基双(丙烯酰胺)(MBA),均为优级纯, Adamas制;盐酸、硝酸,均为分析纯,浙江平湖化工试剂厂;去离子水,自制。
1.2 主要仪器设备
连续注射泵,上海奥尔特生物科技有限公司,ALC-IP-80型;pH计,梅特勒-托利多S40型;纳米粒径电位仪,上海中晨数字技术设备有限公司,Malvern DTS1060型;傅里叶红外光谱仪,赛默飞世尔科技(中国)有限公司,Nicolet 6700型;热重分析仪,德国耐驰TG-209-F1型;振动样品磁强计,美国LAkeshore7407型。
1.3 实验过程
1.3.1 PMAA纳米水凝胶的制备
在100 mL四口烧瓶中加入pH=1.8的HNO3水溶液(55 mL) 、SDS(100 mg)和AIBN(80 mg),充分溶解后,通氮除氧1 h,升温至67 ℃。再加入吐温20(100 mg,0.24 mL),共同推加MAA(2 mL)和 MBA(100 mg),再反应4 h,反应过程中保持氮气气氛。反应结束后,将反应产物对水充分透析,以除去各种杂质。
1.3.2 PMAA纳米水凝胶的磁性功能化及提纯
取PMAA纳米水凝胶(200 mg)溶于去离子水中(100 mL),调节pH值至6,转移至三口瓶中,加入 FeCl2·4H2O(513 mg),搅拌4.5 h后,再加入NaNO2(71 mg)、 NH3·H2O(1 mL),继续反应2.5 h,反应过程中保持氮气氛围。微球中羧酸基团与Fe2+的投料摩尔比为n-COOH∶nFe2+=1∶1.5。
将磁性PMAA纳米水凝胶静置过夜,上层水凝胶在3 000 r/min下离心5 min,离心液调至一定pH值,磁析分离,用去离子水洗涤3次,得到纯化的磁性PMAA纳米水凝胶。
1.4 分析测试
1.4.1 流体力学性质测试
采用Malvern DTS1060光散射粒径仪测定PMAA纳米水凝胶的流体力学直径(
1.4.2 组成测试
采用KBr压片法,Nicolet 6700型傅里叶红外光谱仪测定磁性纳米水凝胶傅里叶红外光谱吸收谱。
1.4.3 热失重分析
采用德国耐弛TG-209-F1型热重分析仪测定PMAA磁性纳米水凝胶热失重曲线,气体氛围为氮气。
1.4.4 磁性能分析
采用D/mAx-2250 PC型X射线衍射仪测定其衍射图谱,将X射线衍射图谱上特征峰与标准图谱做对比,以确定晶体结构;采用lakeshore7407型振动样品磁强计测定磁性纳米水凝胶的磁滞回线(VSM)和饱和磁强度。
1.5 计算
(1) MAA转化率的计算
采用称重法测定MAA转化率,取10 mL PMAA纳米水凝胶分散液置于透析袋中(截留分子量14 000),充分透析后量取其体积(V1,mL)。另取一洗净称量瓶干燥后称重(m1,g),移取2 mL透析后分散液转移至称量瓶中,70 ℃烘干至恒重(m2,g)。假设透析已完全除去未反应的单体、表面活性剂SDS和吐温20,并假设AIBN和MBA 完全转化,按下式计算MAA转化率(CMAA,%):
(1)
V为反应体系总体积,mL;mMBA,mAIBN,mMAA分别为MBA,AIBN和MAA的质量,g。
(2) PMAA纳米水凝胶溶胀比的计算
定义PMAA基纳米水凝胶的溶胀比为纳米水凝胶在pH6和pH2的流体力学直径的比值,即:
(2)
(3) 磁性PMAA纳米水凝胶磁含量的计算
采用热失重法测定磁含量。由热失重法测定纳米水凝胶前驱体和磁性纳米水凝胶在700 ℃的残重W1和W2,按式3计算得到磁性纳米水凝胶的磁含量x:
(3)
2 结果与讨论
2.1 不同反应参数对PMAA纳米水凝胶的影响
采用乳液聚合法合成PMAA纳米水凝胶,并以其为前驱体采用氧化沉淀法制备磁性纳米水凝胶。对制备的PMAA磁性纳米水凝胶的组成、磁性能进行表征,研究了反应介质pH、MAA用量、交联剂用量、加料时间等参数对PMAA纳米水凝胶制备的影响。
2.1.1 反应介质pH对PMAA纳米水凝胶的影响
PMAA纳米水凝胶具有显著的pH响应性,在pH2介质中收缩,在pH6介质中溶胀。通过对比PMAA水凝胶在pH2和pH6中粒径变化来判断纳米水凝胶的pH敏感性能。表1为不同反应介质pH对PMAA纳米水凝胶流体力学直径和分布的数据。由表1可以看出,反应介质pH值对PMAA纳米水凝胶制备影响较大。在pH=1酸性反应介质中沉淀分层,在pH=1.8反应介质中可以得到多分散系数较小、单峰分布的PMAA纳米水凝胶。随着介质pH值继续增大,PMAA纳米水凝胶粒径不断减小,溶胀比减小,单体转化率降低。
MAA与非离子表面活性剂吐温20间存在氢键作用力,能够形成弱疏水的吐温20/MAA复合物,经聚合转变成强疏水的吐温20/PMAA复合物,从而形成PMAA纳米水凝胶。聚合过程中反应介质酸性越强,两者氢键作用力越强,形成吐温20/PMAA疏水复合物速度也越快,因此要维持反应体系稳定所需的SDS量也越大。当体系中SDS用量一定时,在pH=1强酸性介质中,MAA与吐温20氢键作用力较强,可在短时间内形成粒径较大PMAA纳米水凝胶,相互碰撞容易聚并,体系失稳产生宏观沉淀。随着pH值增加,MAA与游离吐温20间氢键作用逐渐减弱,形成吐温20/MAA复合物数目减少,纳米水凝胶粒径减小,溶胀比减小,体系中游离单体数目增加,单体转化率下降。
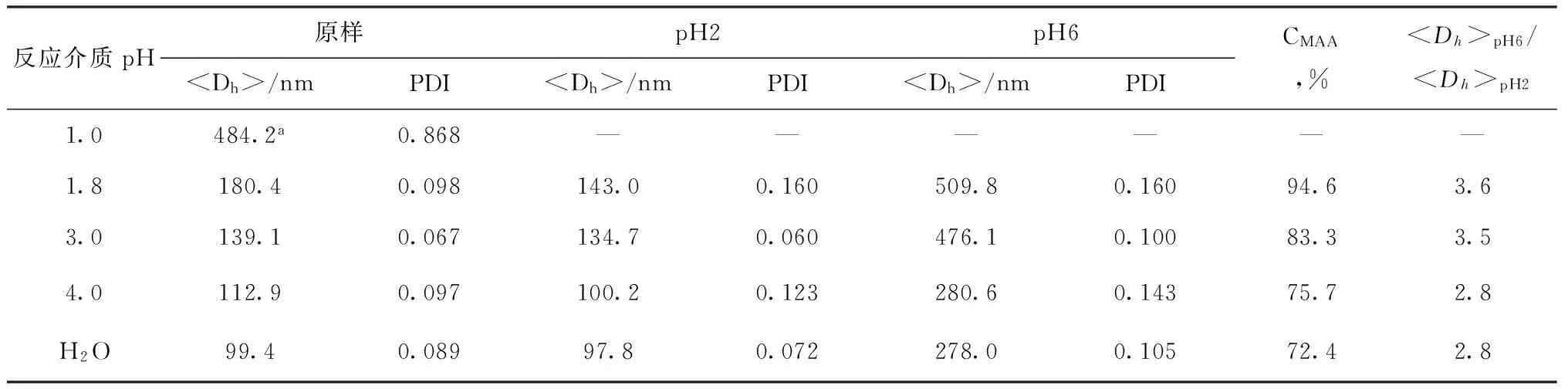
表1 反应介质对PMAA纳米水凝胶的流体力学直径和分布的数据
a流体力学直径分布曲线为多峰分布
2.1.2 MAA用量的影响
表2为不同MAA用量对PMAA纳米水凝胶流体力学直径及多分散系数的数据。

表2 MAA用量对PMAA纳米水凝胶流体力学直径及多分散系数的数据
a流体力学直径曲线呈多峰分布
从表中可以看出,MAA用量增加,PMAA纳米水凝胶的流体力学直径先增大后减小,转化率逐渐降低。当MAA用量增加至4 mL时,粒径减小,在pH6出现双峰分布。这可能是单体浓度过高时,粒径不易持续增长,更倾向于生成尺寸较小PMAA纳米水凝胶。
2.1.3 SDS用量对PMAA纳米水凝胶的影响
图1为表面活性剂SDS不同用量制备的PMAA纳米水凝胶流体力学直径分布曲线。当不添加SDS时,反应沉淀分层,随着SDS用量的增加,纳米水凝胶流体力学直径减小,且能稳定保存。说明SDS存在是制备稳定的PMAA纳米水凝胶分散液的必要条件。
当体系中没有SDS时,生成吐温20/PMAA疏水复合物容易聚并而无法稳定;当SDS用量增加至80 mg时,流体力学直径分布较宽,PMAA纳米水凝胶多分散系数较大,乳液不稳定,放置一段时间容易发生沉淀。当SDS继续增加至100 mg时,纳米水凝胶的粒径较小,且分布较窄,这说明,在MAA聚合过程中补加足够的SDS,可以使纳米水凝胶表面捕获足量的SDS,从而避免乳胶粒子间聚并,得到粒径较小且均一的PMAA纳米水凝胶。若继续增加SDS用量,则制备的PMAA纳米水凝胶流体力学直径增加。这可能是因为过量的SDS与吐温20发生疏水相互作用,裹挟在PMAA纳米水凝胶中或者吸附在其表面,使得粒径增加。
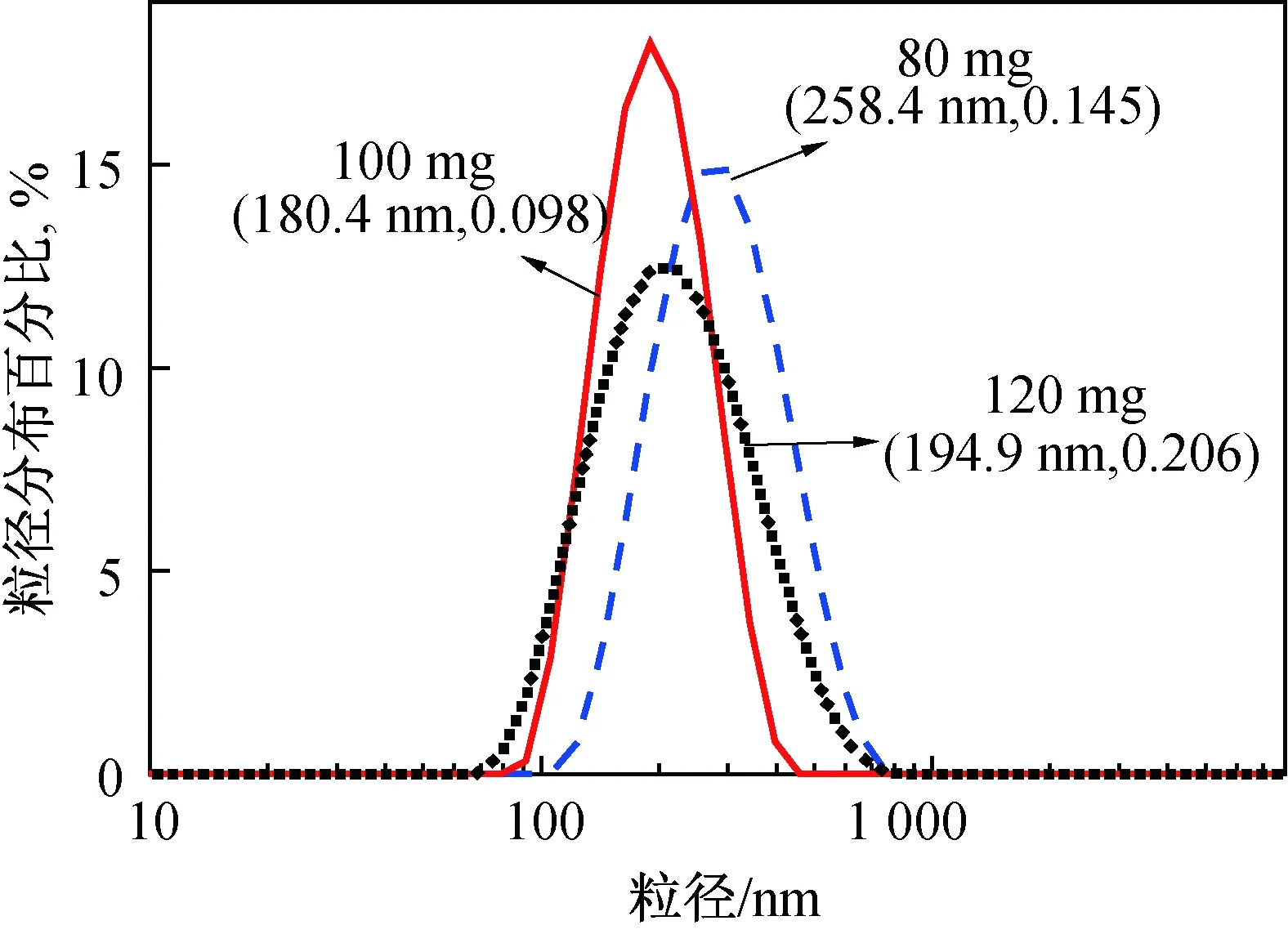
图1 不同SDS用量的PMAA纳米水凝胶流体力学直径分布曲线
2.1.4 MAA/MBA共同加料时间的影响
图2为不同MAA/MBA共同加料时间的PMAA纳米水凝胶流体力学直径分布曲线。
从图中可以看出,当共同加料时间为10 min时,PMAA纳米水凝胶在33.69 nm出现小峰,流体力学直径呈双峰分布。这可能是推加时间短,反应体系中瞬时MAA浓度较大,容易生成粒径较小的纳米乳胶粒。而继续延长推加时间,上述现象消失。随着共同加料时间增加,PMAA纳米水凝胶的粒径逐渐增大、分布变窄。这可能是由于延长MAA和MBA加料时间,单体浓度相对降低,聚合反应速率变慢,保证了吐温20与MAA(PMAA)和MBA充分作用,因此生成的PMAA纳米水凝胶粒径就愈均一,多分散系数愈小,交联结构愈均匀。
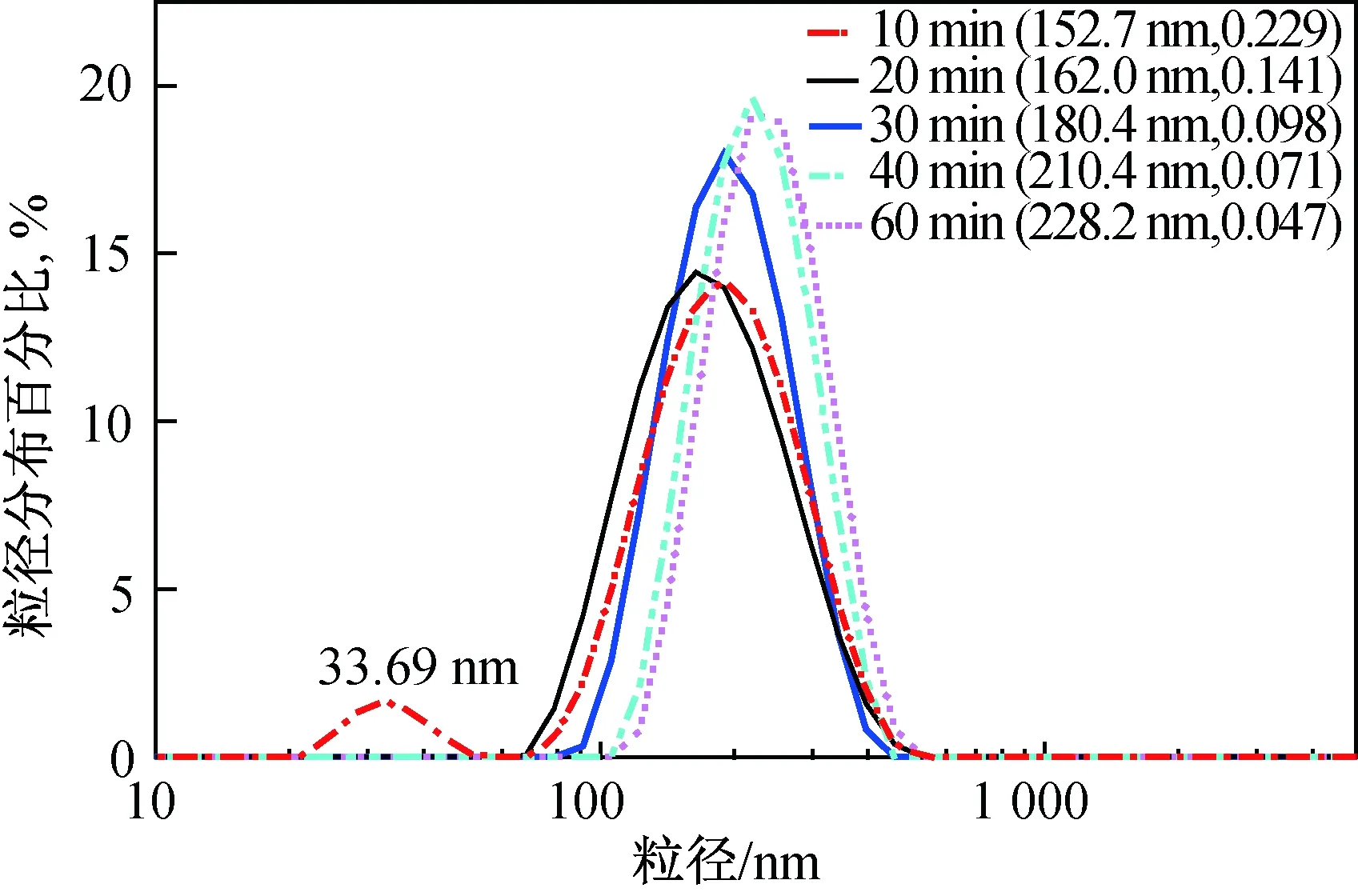
图2 不同MAA/MBA共同加料时间PMAA纳米水凝胶流体力学直径分布曲线
2.1.5 交联剂(MBA)用量的影响
图3为不同交联剂用量制备的PMAA纳米水凝
胶的流体力学直径分布曲线。
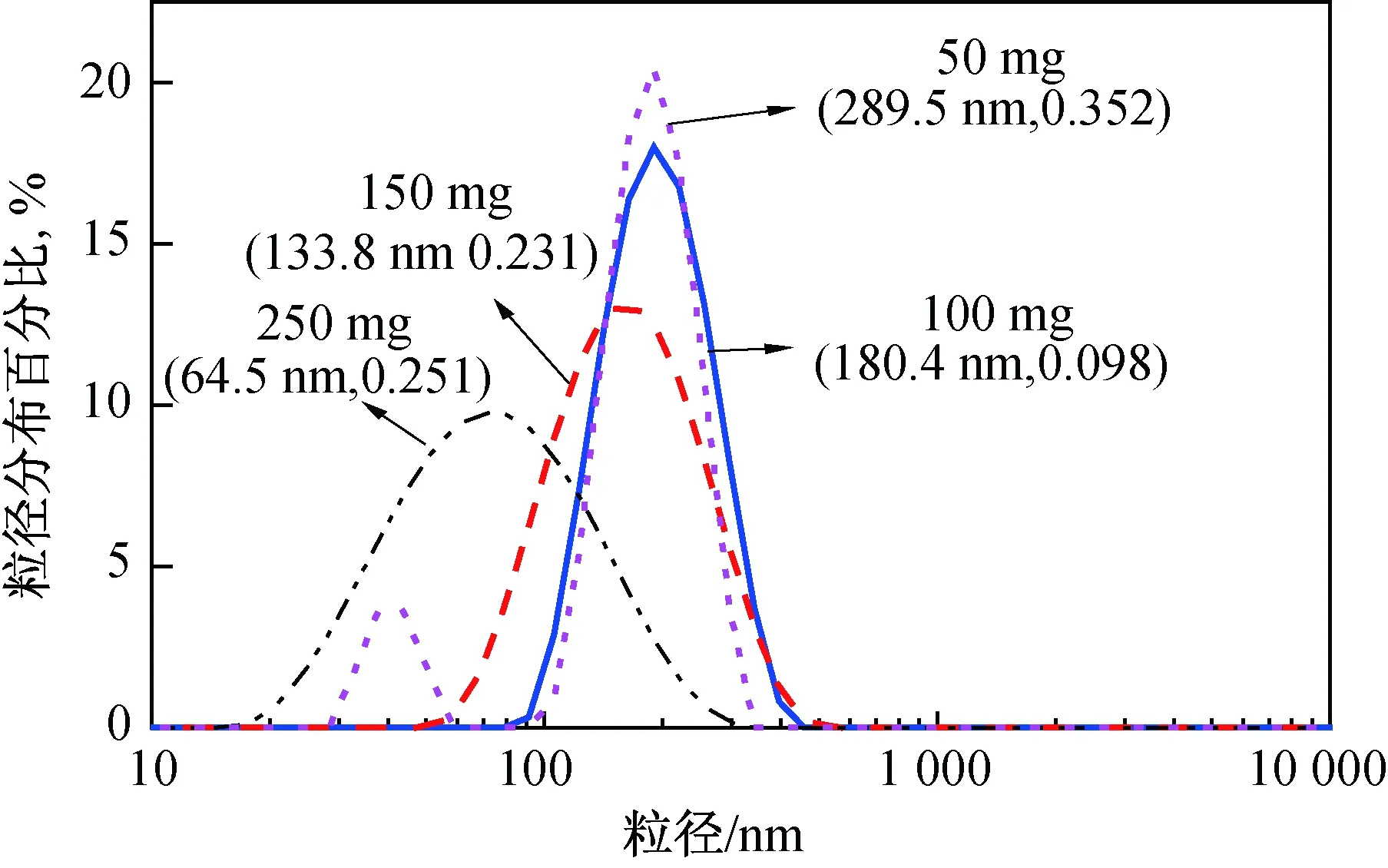
图3 不同交联剂用量的PMAA纳米水凝胶流体力学直径分布曲线
从图中可以看出,当MBA含量增加,PMAA纳米水凝胶的粒径减小。交联剂用量为50 mg时,由于交联剂用量较少,部分未交联MAA聚合形成粒径较小聚合物微球,因此流体力学曲线出现小峰;随着交联剂用量的增加,交联点密度升高,PMAA纳米水凝胶的粒径减小,流体力学直径分布曲线向左移动。
2.1.6 非离子表面活性剂吐温20用量的影响
表3为吐温20不同用量对PMAA纳米水凝胶流体力学直径分布的数据。
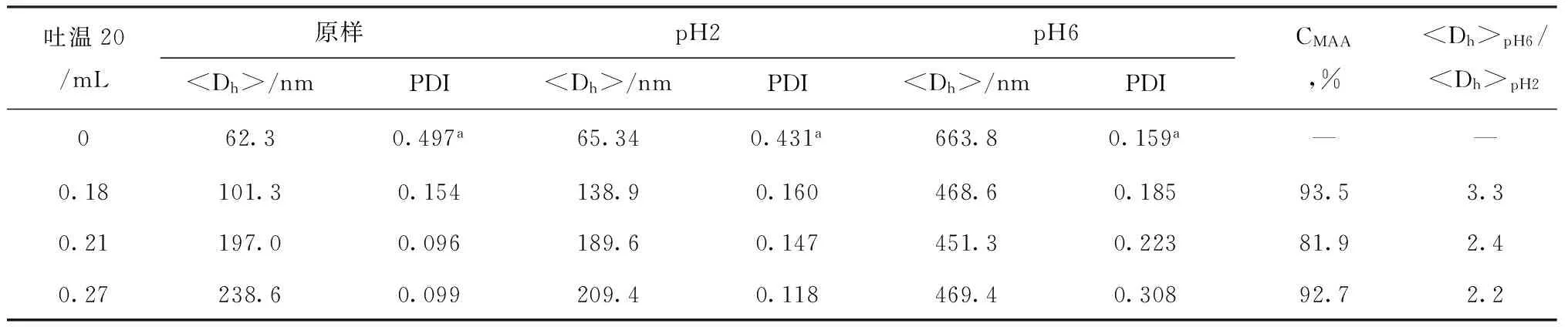
表3 吐温20的用量对PMAA纳米水凝胶流体力学直径和多分散系数的数据
a流体力学直径分布曲线为多峰分布
从表3中可以看到,无吐温20时,得到的纳米水凝胶的粒径为多峰分布。当吐温20用量较少时,纳米水凝胶的尺寸较小,分布宽。当吐温20用量达到0.18 mL时,可以制备流体力学直径为单峰分布的PMAA纳米水凝胶。这说明适量添加吐温20是制备单峰分布PMAA纳米凝胶的必要条件。当吐温20用量增加至0.27 mL以上,反应体系中出现少量沉淀物。这是因为吐温20用量增加,吐温20与MAA或PMAA间的作用力增强,生成疏水复合物的速度加快,SDS补加速度保持不变,部分乳胶粒子可能相互聚并,生成大尺寸的PMAA纳米水凝胶,引发沉淀。
2.2 PMAA纳米水凝胶磁性功能化的表征
2.2.1 磁性纳米水凝胶的X射线衍射分析
图4是以PMAA纳米水凝胶为前驱体,利用原位氧化沉淀法制备得到的磁性纳米水凝胶的XRD图谱。
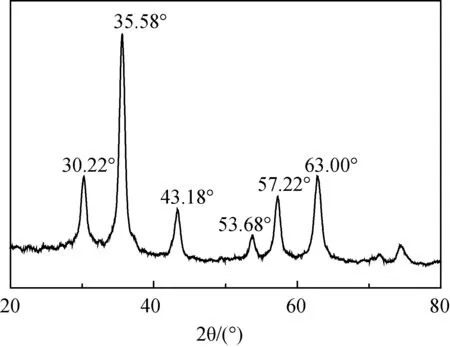
图4 原位氧化沉淀法制备得到的磁性纳米水凝胶的XRD图谱
原位氧化沉淀法制备磁性纳米水凝胶中,我们采用氧化剂NaNO2,将纳米水凝胶吸附的Fe2+原位转变为Fe3O4纳米粒子,其反应式为:
磁性纳米水凝胶衍射谱图中,30.22°、35.58°、43.18°、53.68°、57.22°和63.00°处的衍射峰,分别对应于四氧化三铁的(220)、(311)、(400)、(422)、(511)和(400)晶面。根据Debye-Scherrer公式4,由2θ=35.58°处的衍射峰半宽高可以计算得到磁性纳米水凝胶中Fe3O4的晶粒尺寸为14.0 nm。
(4)
其中D为垂直于晶面方向的晶粒直径;K为Scherrer常数,通常取0.89;λ是入射X射线波长,0.154 nm;β是校正后的衍射峰的半高峰宽;θ是布拉格衍射角。
2.2.2 PMAA磁性微球的红外图谱分析
图5为采用KBr压片法,将透析后PMAA纳米水凝胶和冷冻干燥后磁性PMAA纳米水凝胶粉末进行红外表征得到的红外谱图。

图5 PMAA与磁性PMAA纳米水凝胶的红外图谱
从纳米水凝胶前驱体PMAA和采用原位氧化沉淀法制备的磁性纳米水凝胶的红外谱图可以看出。图中586 cm-1左右的强吸收峰是Fe-O的特征吸收峰,3 436 cm-1左右是羟基吸收峰,2 994 cm-1左右处为亚甲基的反对称伸缩振动峰,2 932 cm-1是亚甲基的对称伸缩振动吸收峰,1 711 cm-1是羧基特征吸收峰,说明磁性纳米水凝胶样品中同时含有PMAA和Fe3O4。
2.2.3 PMAA磁性微球的热重分析
图6为PMAA磁性纳米水凝胶与其前躯体热失重曲线。
热失重测试结果表明,PMAA纳米水凝胶和磁性PMAA纳米水凝胶在700 ℃时的残余质量分别为13.1%和66.5%。由此估算得到磁性PMAA纳米水凝胶的磁含量可达61.4%。

图6 PMAA与磁性PMAA纳米水凝胶的热失重曲线
2.2.4 磁性PMAA纳米水凝胶的磁性能分析
图7中为PMAA纳米水凝胶的磁滞回线图。
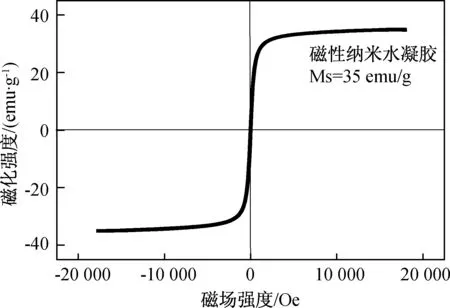
图7 PMAA磁性纳米水凝胶的磁滞回线图
利用振动样品磁强计分析氧化沉淀法制备磁性纳米水凝胶的磁性质。磁性PMAA纳米水凝胶的磁化曲线呈典型的S型:当外加磁场的强度增加,样品的磁化强度增加,当增加到一定值时达到饱和磁化强度(Ms),此时样品的磁化强度随着外加磁场强度的增加而不再变化;当磁场降低时,样品的磁化强度也随之降低,当磁场强度为零时,样品的磁化强度也几乎为零,说明样品具有超顺磁性。磁性PMAA纳米水凝胶的饱和磁化强度为35 emu/g。
3 结 论
a) 本研究采用改进乳液聚合方法,成功实现了聚甲基丙烯酸纳米水凝胶的水相“绿色”制备,研究反应参数对PMAA纳米水凝胶水相合成的影响。
b) 以PMAA纳米水凝胶为前驱体,通过原位氧化沉淀法制得了磁含量为61.4%,分散性良好、尺寸均一可控且含有大量羧基基团的磁性微球,在室温下,磁性PMAA纳米水凝胶具有超顺磁性,其饱和磁化强度为35 emu/g。
[1] 王秀琴, 查刘生. 智能纳米水凝胶的应用研究进展[J]. 化工新型材料, 2012, 40(11): 110-113.
[2] Liu T, Liu H, Wu Z, et al. The use of poly (methacrylic acid) nanogel to control the release of amoxycillin with lower cytotoxicity[J]. Materials Science and Engineering: C, 2014, 43: 622-629.
[3] Chertok B, Moffat B A, David A E, et al. Iron oxide nanoparticles asa drug delivery vehicle for MRI monitored magnetic targeting of brain tumors[J].Biomaterials, 2008, 29(4): 487-496.
[4] Ichikawa H, Fukumori Y. A novel positively thermosensitive controlled-release microcapsule with membrane of nano-sized poly (N-isopropylacrylamide) gel dispersed in ethylcellulose matrix[J]. Journal of Controlled Release, 2000, 63(1): 107-119.
[5] Leung K C F, Xuan S, Zhu X, et al. Gold and iron oxide hybrid nanocomposite materials[J]. Chemical Society Reviews, 2012, 41(5): 1911-1928.
[6] 龚子珊, 丁国生, 唐安娜. 磁性纳米粒子的制备及其在重金属离子处理中的应用[J]. 分析测试学报, 2014, 33(2): 231-238.
[7] Ge J, Huynh T, Hu Y, et al. Hierarchical magnetite/silica nanoassemblies as magnetically recoverable catalyst-supports[J]. Nano letters, 2008, 8(3): 931-934.
[8] Khng H P, Cunliffe D, Davies S, et al. The synthesis of sub-micron magnet-ic particles and their use for preparative purification of proteins[J]. Biotechnology and Bioengineering, 1998, 60(4): 419-424.
[9] Gaponik N, Radtchenko I L, Sukhorukov G B, et al. Luminescent polymer microcapsulesaddressable by a magnetic field[J]. Langmuir, 2004, 20(4): 1449-1452.
[10] Liu H, Wang C, Gao Q, et al. Magnetic hydrogels with supracolloidal structures prepared by suspension polymerization stabilized by Fe2O3nanoparticles[J]. Acta biomaterialia, 2010, 6(1): 275-281.
[11] Ilg P. Stimuli-responsive hydrogels cross-linked by magnetic nanoparticles[J]. Soft Matter, 2013, 9(13): 3465-3468.
[12] Zhu Z, Wu C, Liu H, et al. An Aptamer Cross-Linked Hydrogel as a Colorimetric Platform for Visual Detection[J]. Angewandte Chemie International Edition, 2010, 122(6): 1070-1074.
[13] 顾文娟, 陆亚明, 张幼维, 等. 聚甲基丙烯酸纳米水凝胶的水相合成及其磁性功能化[J]. 高分子学报, 2016,60(8): 1072-1078.
[14] 邓勇辉, 王雷, 杨武利, 等. 反相微乳液合成30~100 nm磁性聚合物纳米水凝胶[J]. 高等学校化学学报, 2003, 24(5): 920-923.
[15] Liu H, Wang C, Gao Q, et al. Magnetic hydrogels with supracolloidal structures prepared by suspension polymerization stabilized by Fe2O3nanoparticles[J]. Acta biomaterialia, 2010, 6(1): 275-281.
[16] Wang D, Silbaugh T, Pfeffer R, et al. Removal of emulsified oil from water by inverse fluidization of hydrophobic aerogels[J]. Powder Technology, 2010, 203(2): 298-309.
[17] Hu J, Lo I M C, Chen G. Comparative study of various magnetic nanoparticles for Cr (VI) removal[J]. Separation and Purification Technology, 2007, 56(3): 249-256.
Preparation and research on magnetic functionalization of poly (methacrylic acid) nano-hydrogels by aqueous phase
Lu Yaming,Zhang Youwei*,Zhao Jiongxin
(CollegeofMaterialsScienceandEngineering,DonghuaUniversity,Shanghai201620,China)
A novel modified emulsion polymerization for the “green” synthesis of poly (methacrylic acid) (PMAA) nano-hydrogel in aqueous solution was developed. The magnetic PMAA nano-hydrogels were prepared by in-situ oxidation precipitation method using the PMAA nano-hydrogels as the precursor. The size and size distribution, magneticcontent of the prepared magnetic nano-hydrogels were characterize by dynamic lightscattering, vibrating samplemagnetometer(VSM) and thermogravimetric analysis(TG). The result showed that the magnetic PMAA nano-hydrogels were superparamagnetic and with a high magnetic content of 61.4%. It has been widely employed in biomedical engineering, wastewater treatmen tand so on.
polymethacrylic acid;nano-hydrogel;magnetic functionalized
2017-01-16
陆亚明(1989-),河南洛阳人,在读研究生,研究方向为智能纳米水凝胶。
上海市自然科学基金项目15ZR1401300。
O632.52
A
1006-334X(2017)01-0001-06
*通讯作者: 张幼维,zhyw@dhu.edu.cn。

