Cu/MIL-101(Cr)吸附剂的制备及其CO吸附性能
徐言言,段 龙
(1.广东粤电新会发电有限公司,广东 江门 529100,2.南京工业大学材料化学工程国家重点实验室,江苏 南京 210009)
Cu/MIL-101(Cr)吸附剂的制备及其CO吸附性能
徐言言1,段 龙2
(1.广东粤电新会发电有限公司,广东 江门 529100,2.南京工业大学材料化学工程国家重点实验室,江苏 南京 210009)
采用浸渍法将甲酸铜与氯化铜前驱体负载到金属有机骨架材料MIL-101载体上,通过改变活化温度和铜盐负载量,制备Cu/MIL-101吸附剂。用XRD、FT-IR、TG、N2吸附和脱附等表征手段考察材料的结构和性能,测试Cu/MIL-101吸附剂在101.3kPa、25℃的CO、N2吸附量。结果表明,制备该吸附剂的最佳活化温度为220℃,最佳铜盐负载量为4mmol·(g MIL-101)-1。铜基改性后的吸附剂CO的吸附量由23.93cm3·g-1提高到53.55cm3·g-1,N2的吸附量由5.81cm3·g-1下降到3.29cm3·g-1,用理想吸附溶液理论IAST模型预测CO/N2吸附选择性由26提高到2194。吸附剂可在200℃、真空下再生。
金属有机骨架;一氧化碳;氯化亚铜;浸渍;吸附选择性
一氧化碳是重要的工业气体原料,可用于生产甲醇、醋酸、聚氨基甲酸乙酯、聚碳酸酯等[1],以及作为炼钢厂转炉底部进气、电子工业、磁性铁粉的还原性气体。一氧化碳的来源主要有以煤、石油及天然气通过部分氧化法或水煤气反应获得的合成气以及工业废气[2]。CO常与N2、H2、CH4及CO2气体同时存在,需要对一氧化碳进行分离纯化才能加以利用[3]。另外,CO若直接排放到大气中会造成环境污染问题,同时人体吸入后会中毒。随着经济的发展,工业生产中的节能减排和日益严峻的环境问题、污染物排放要求,以及在工业生产中一氧化碳的重要性,研究节能高效的一氧化碳分离、提纯技术具有重要的经济意义和社会意义。
从混合气体中分离CO的常用方法有深冷分离法、COSORB法和变压吸附法(PSA)[4]。深冷法工艺设备复杂、投资大,适用于大规模装置,但是当体系中存在氮气时,不能用此方法分离。COSORB法需要复杂的预处理系统和增设后处理工序,投资大,费用高,而且会对环境造成污染。PSA法工艺简单,技术先进,节能效果显著,已广泛应用于各种气体分离领域。用PSA法分离CO的主要难点是现有吸附剂对CO/N2的分离系数小。常用吸附剂是负载铜盐的沸石分子筛、活性炭或者氧化铝,由于这些载体的比表面积和孔容都很低,限制了铜盐负载量,导致CO吸附量不高。
因此,开发高效的新型吸附剂是PSA法分离CO的关键。金属有机骨架材料MIL-101具有高比表面积,孔隙率高,稳定性好,是理想的吸附剂载体[5]。本文利用π络合吸附原理,用铜基改性MIL-101,并对其CO/N2吸附分离性能进行研究。
1 实验
1.1 试剂
九水硝酸铬(分析纯),对苯二甲酸(≥99%),无水醋酸钠(分析纯),氟化氨(分析纯),醋酸(分析纯),四水甲酸铜(≥98.0%),二水合氯化铜(≥99.0%),无水乙醇(分析纯),去离子水(自制)。
1.2 主要仪器
Bruker D8 Advance X射 线 粉 末 衍 射 仪,BELSORP-max比表面积孔径分析仪,Micromeritics ASAP 2020自动物理吸附仪,AVATAR-360傅立叶红外光谱分析仪,Netzsch STA-449F3同步热分析仪。
1.3 样品的合成
MIL-101载体的合成与纯化参照本课题组的方法[6],Cu/MIL-101的制备按照专利[7]和文献[8]中的方法。首先将甲酸铜和氯化铜以摩尔比1∶1制成混合铜盐溶液,按Cu与MIL-101比为3mmol·g-1、4mmol·g-1、5mmol·g-1、6mmol·g-1、7mmol·g-1、8mmol·g-1,将载体MIL-101加入到混合铜盐溶液中,搅拌2h后用旋转蒸发仪蒸干溶剂,复合物烘箱过夜干燥。复合物在H2气氛,180℃下加热3.5h制成Cu/MIL-101吸附剂。然后固定铜盐负载量,将复合物分别在H2气氛,150℃、200℃、210℃、220℃、230℃、260℃下加热3.5h制得Cu/MIL-101吸附剂。
1.4 CO/N2吸附-脱附测试
采用Micromeritics ASAP 2020自动物理吸附仪,测量吸附剂对CO、N2的吸附-脱附实验。样品预处理条件为:200℃,真空脱气处理2h,测量温度25℃,测量压力P/P0范围:0~1。
2 结果与讨论
2.1 铜盐负载量对吸附剂性能的影响
图1为甲酸铜与氯化铜摩尔比为1∶1时,负载量不同的载体MIL-101在180℃、H2气氛下,反应3.5h所合成的Cu/MIL-101吸附剂对CO吸附性能的比较。由图1可知,随着甲酸铜与氯化铜负载量的增加,吸附剂对CO的吸附量不断提高。铜盐的分散量存在一个阈值,超过这个阈值,铜盐分子间会发生堆叠,使吸附位减少,而且会堵塞载体孔道,减小吸附剂比表面积,从而降低了吸附剂对CO的吸附量。当铜盐负载量为4mmol· (g MIL-101)-1时,吸附量达到最大为45cm3·g-1。甲酸铜与氯化铜在MIL-101上达到最佳分散量,反应生成的CuCl量最大且分散性好。
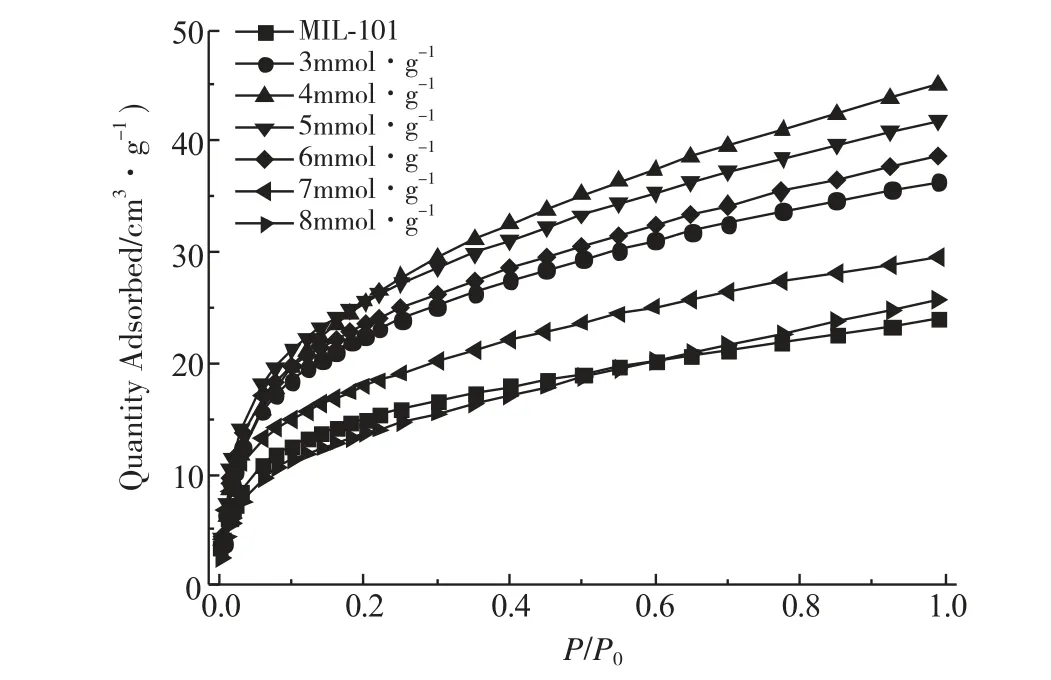
图1 Cu的负载量对样品CO吸附量的影响
2.2 活化温度对吸附剂性能的影响
图2为铜盐负载量为4mmol·(g MIL-101)-1的吸附剂在不同活化温度下,所得Cu/MIL-101吸附剂于298K、100kPa下的CO吸附量。由图2可知,随着活化温度的增加,CO吸附量不断上升,这是因为活化温度升高,氧化还原反应进行得更彻底,生成的CuCl也更多,在220℃达到最大吸附量55.42cm3·g-1。之后随着活化温度的增加,CO吸附量逐渐降低,并且样品颜色逐渐加深呈铁灰色。这是由于温度过高,CuCl被过度还原成了对CO没有π络合作用的铜单质。因此,温度220℃是最佳活化温度,此时反应生成的CuCl最多,Cu/MIL-101吸附剂的CO吸附量最好。
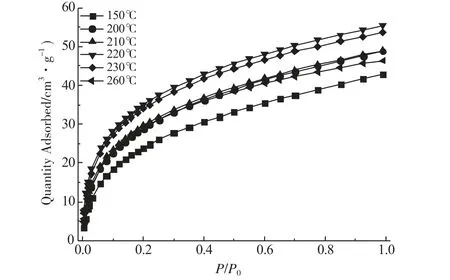
图2 活化温度对样品CO吸附量的影响
2.3 样品表征
2.3.1 粉末XRD衍射分析
图3是活化前不同铜盐负载量样品的XRD谱图,由图3可知,负载铜盐后,MIL-101的特征峰依然存在,只是随着铜盐负载量的增加有所减弱,骨架仍然保持完整。当铜盐负载量为4mmol·(g吸附剂)-1时,没有前驱体的特征峰,说明氯化铜与甲酸铜成功进入了载体MIL-101的孔道中并且分散均匀,当铜盐负载量增加到超过分散阈值时,铜盐开始聚集,所以氯化铜与甲酸铜的特征峰不断增强。
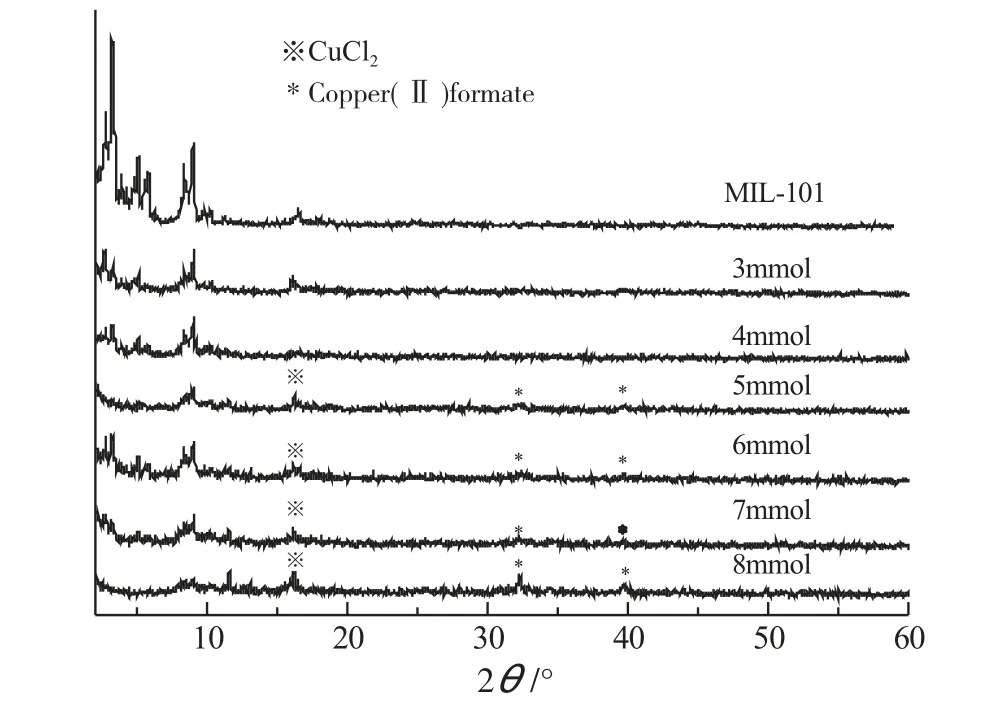
图3 活化前不同铜盐负载量样品的XRD谱图
图4为活化后不同铜盐负载量吸附剂的XRD谱图。由图4可知,氯化铜与甲酸铜前驱体的特征峰消失,出现了CuCl的特征峰,说明在H2氛围、180℃下,前驱体成功转化成了目标产物CuCl。随着铜盐负载量的增加,MIL-101特征峰不断减弱,CuCl产量不断增加且特征峰逐渐加强。
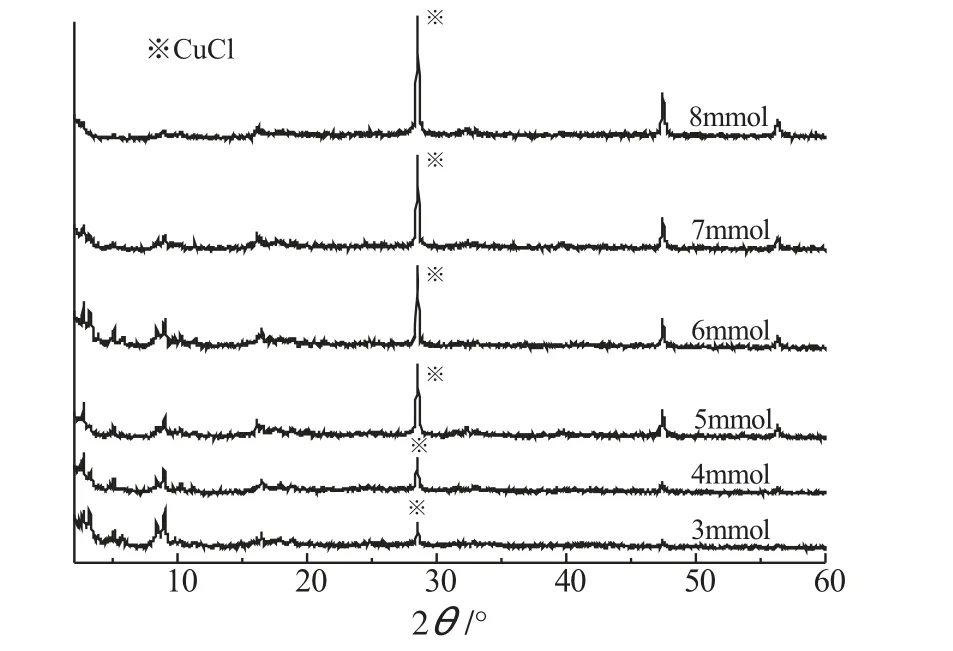
图4 活化后不同铜盐负载量样品的XRD谱图
图5为铜盐负载量为4mmol·(g MIL-101)-1时,前驱体与载体MIL-101在H2氛围、不同活化温度下反应3.5h制备的吸附剂的XRD谱图。由图5可知,在150~200℃时,产物CuCl的特征峰不断增强,说明温度越高越有利于反应的进行。在最佳活化温度220℃时,CuCl的晶相峰减弱消失,说明氯化亚铜在高温下发生了原子水平的分散[9]。当温度达到230℃时,已经出现了铜单质的特征峰,说明在H2气氛下,过高的反应温度使生成的CuCl再次被还原,CuCl还原为对CO没有π络合吸附作用的Cu单质。
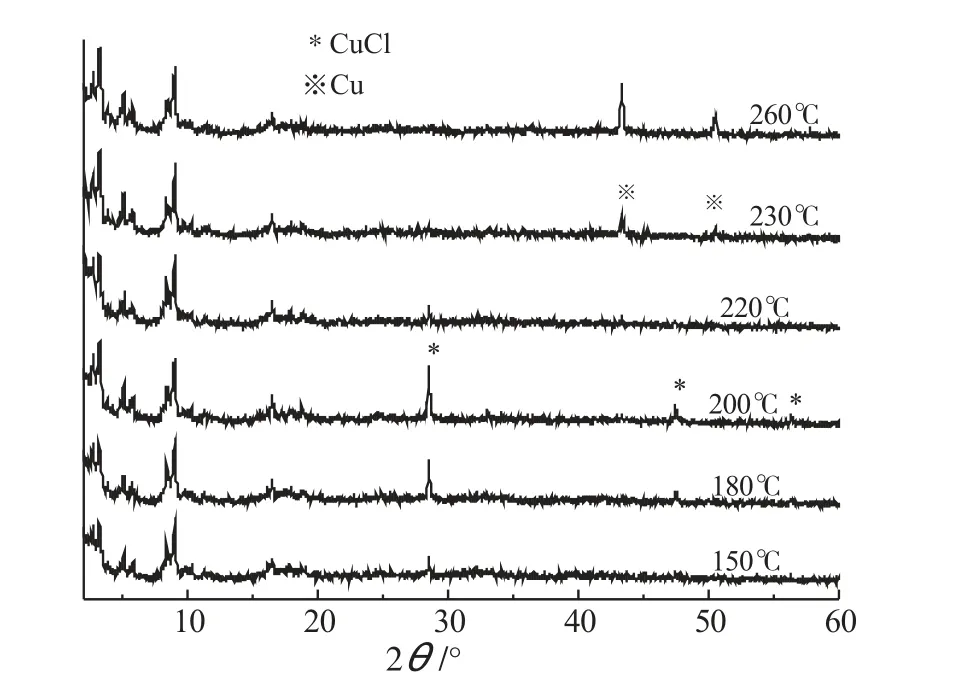
图5 不同活化温度下样品的XRD谱图
2.3.2 FT-IR
图6是铜盐负载量为4mmol·(g MIL-101)-1、反应温度220℃、H2气氛下反应3.5h,样品活化前后的红外谱图。由图6可知,载体MIL-101的红外谱图与铜基改性的MIL-101谱图相比,基本形状相同,说明铜盐的加入没有破坏MIL-101中存在的基团。未经活化的铜基吸附剂Cu/MIL-101-before在3448cm-1、3362cm-1、1618cm-1、1577cm-1出现了羧酸盐中的-COO-吸收峰[10],这是前驱体甲酸铜的加入引起的。经过活化,Cu/MIL-101-after在相同位置没有明显出峰,说明经过活化,前驱体甲酸铜发生了转化。
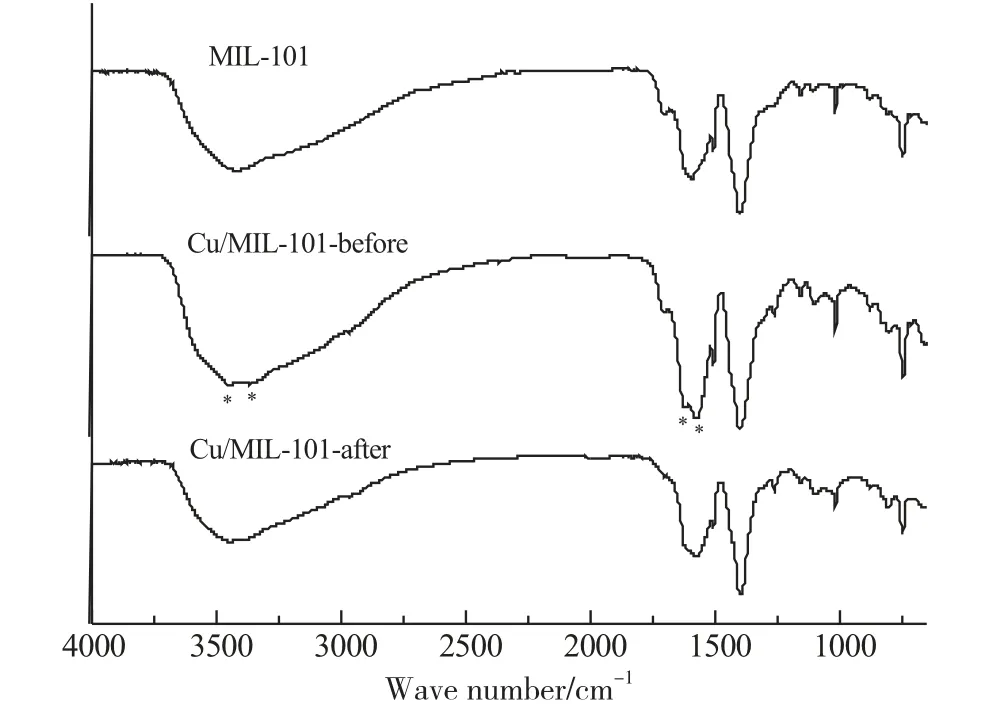
图6 活化前后样品的FT-IR谱图
2.3.3 TGA
图7为载体MIL-101、铜基吸附剂活化前后的热重曲线图。MIL-101有两个失重阶段,第一个失重阶段发生在30~275℃之间,主要是客体水分子的脱除;第二个失重阶段发生在300~500℃之间,主要是MIL-101骨架中羟基或氟离子的脱除以及骨架的坍塌。未活化的铜基吸附剂Cu/MIL-101-before有3个失重阶段,第一失重阶段发生在30~100℃之间,主要是水分子的脱除;第二个失重阶段发生在150~250℃之间,主要是铜盐前躯体发生了氧化还原反应,生成了CO、H2O、CO2等气体产物;第三个失重阶段发生在300~500℃,主要是MIL-101骨架中羟基或氟离子的脱除以及骨架的坍塌。活化后的铜基吸附剂Cu/MIL-101-after有两个失重阶段,与载体MIL-101的失重情况相同,不过由于铜盐的引入,热稳定性有一定提高,Cu/MIL-101-after 吸附剂在150~250℃没有发生失重,也说明经过活化,前驱体完成了氧化还原反应,已完全转化为CuCl。
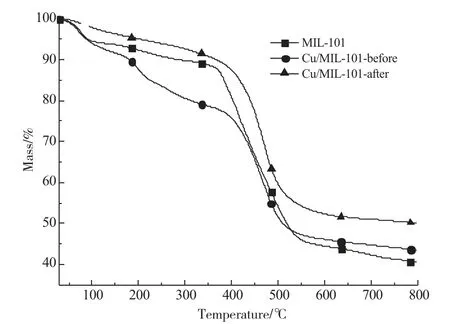
图7 活化前后样品热重曲线图
2.3.4 比表面积及孔结构
图8为MIL-101和活化前后的Cu/MIL-101吸附剂在77K下氮气吸脱附等温线对比图。由图8可知,3条吸附等温线形状基本一致,只是吸附量的差异,说明经过铜盐负载和加热处理,载体MIL-101的孔道结构没有发生大的变化,骨架结构没有遭到破坏,依然保持完好。负载铜盐后未活化处理的Cu/MIL-101-before吸附剂,其氮气吸附量明显下降,说明载体MIL-101孔道被前驱体混合铜盐氯化铜与甲酸铜所占据,孔容和比表面积都有所减小。而经过活化处理后的Cu/MIL-101-after吸附剂相比Cu/MIL-101-before,其氮气吸附量有所上升,这是因为经过活化处理,混合铜盐氯化铜与甲酸铜发生了氧化还原反应,生成了CuCl、H2O、CO2和CO,反应前后甲酸的缺失引起了空洞表面积增加[11]。表1是根据样品在77K下的氮气吸附等温线计算出的比表面积和孔容。可以明显看出,铜盐负载后,比表面积和孔容大为减少,Cu/MIL-101吸附剂在经过加热处理后,比表面积和孔容有所增加。
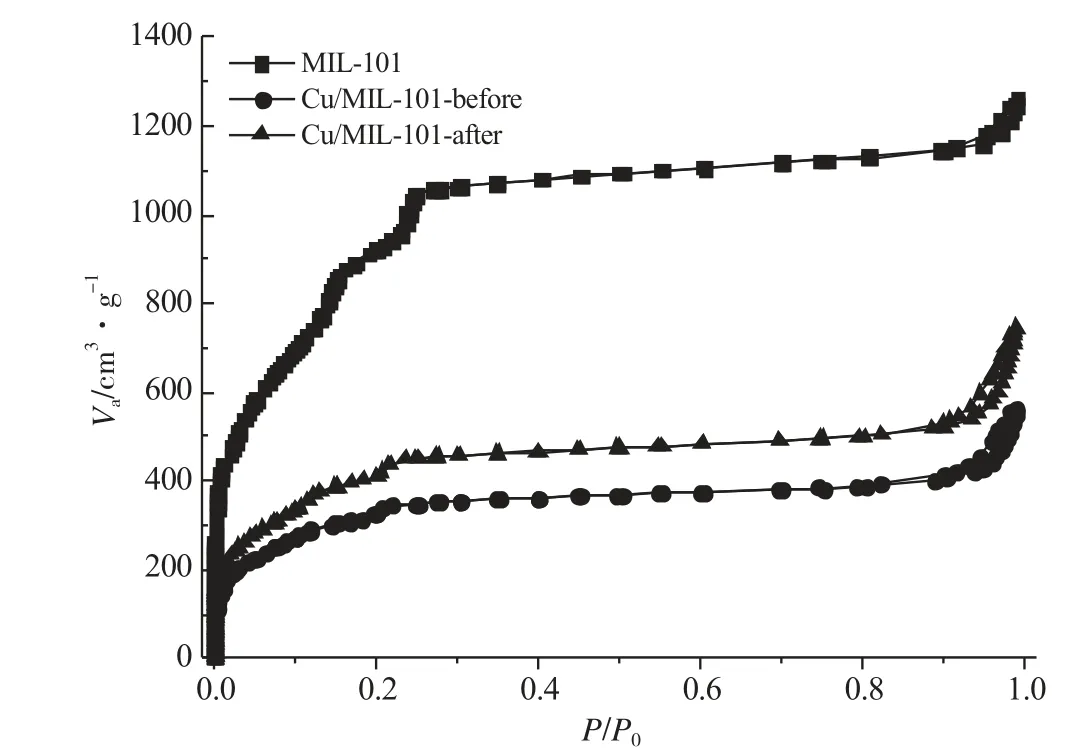
图8 样品在77K下的N2吸附等温线

表1 样品的比表面积及孔容
使用非定域密度泛函法(NLDFT)计算了载体MIL-101、活化前后的Cu/MIL-101的孔径分布。由图9可以看出,MIL-101拥有0.96nm的微孔和2.53nm、3.41nm的介孔,与文献报道一致[12]。铜盐负载后,未经活化的Cu/MIL-101-before的孔径发生了很大的变化,其中0.96nm的微孔被铜盐所占据,2.53nm的介孔缩小为2.08nm,而3.41nm的介孔则被铜盐多层覆盖缩小为1.51nm的微孔。活化后的Cu/MIL-101-after的孔径分布与Cu/MIL-101-before类似,但是由于活化处理后甲酸的缺失引起了空洞表面积增加,1.51nm的微孔、2.21nm的介孔的个数有所增加。
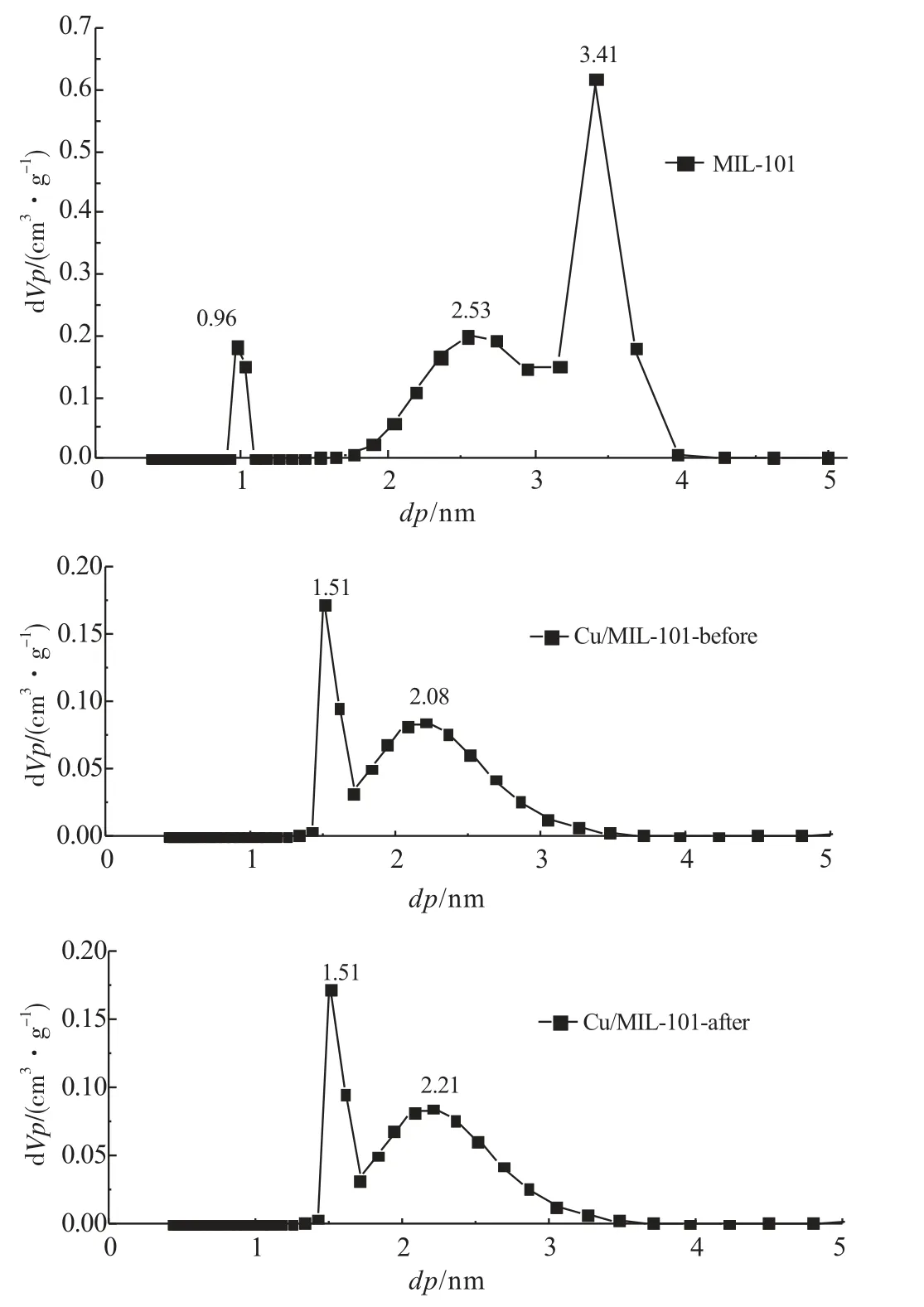
图9 样品的孔径分布
2.3.5 CO/N2的吸附选择性
图10为载体MIL-101及在最佳条件下制备的Cu/MIL-101吸附剂,在298K下的单组分吸附等温线。载体MIL-101在298K、100kPa下对N2、CO的吸附量分别为5.81cm3·g-1、23.93cm3·g-1;负载铜盐后Cu/MIL-101在同样条件下对N2、CO的吸附量分别为3.29cm3·g-1、53.55cm3·g-1。Cu/MIL-101吸附剂对CO的吸附量明显提升,N2的吸附量有所下降,这是因为铜盐的负载反应生成的CuCl对CO有络合吸附作用,加大了吸附剂对CO的吸附量,而铜盐的负载给载体带来比表面积的减少、孔道的堵塞及孔容的减少,造成了N2吸附量的下降。下面将通过DL-IAST模型[13-14],预测摩尔比n(CO)/n(N2)=1的CO/ N2混合组分在不同压力下吸附剂的吸附选择性。
在0~100kPa,拟合方程的回归系数R2>0.999,说明双Langmuir方程很好地描述了吸附剂CO和N2的吸附等温线。
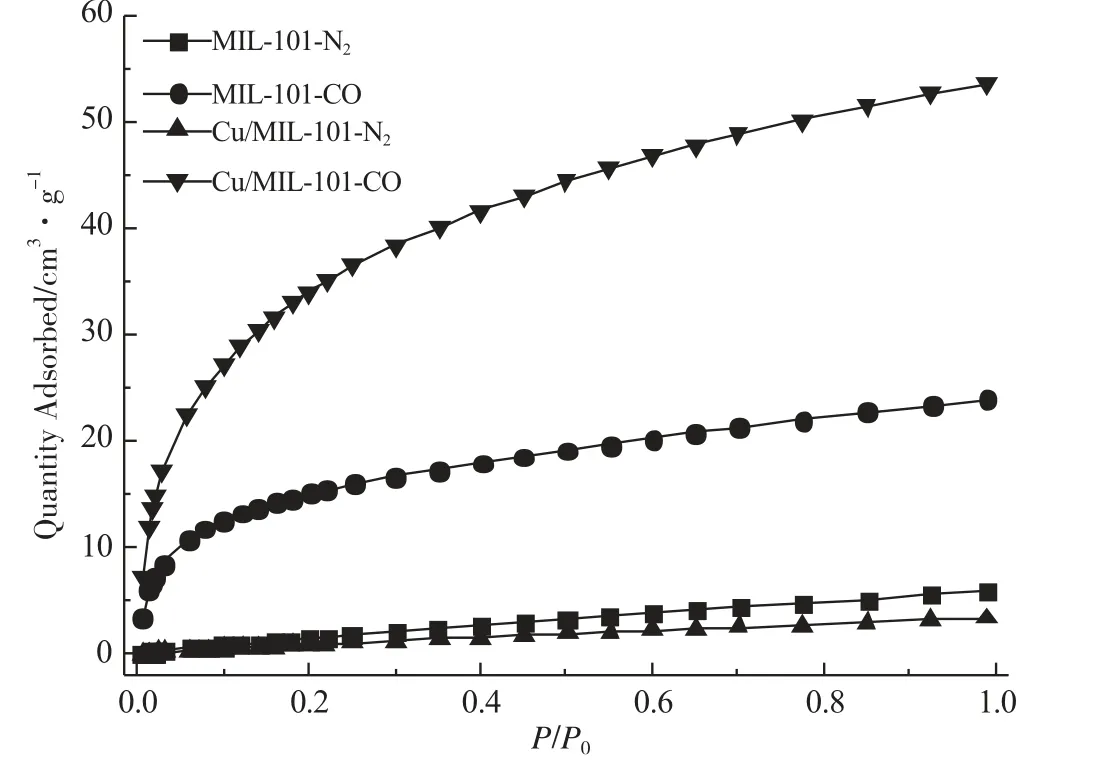
图10 298 K下的CO和N2的吸附等温线
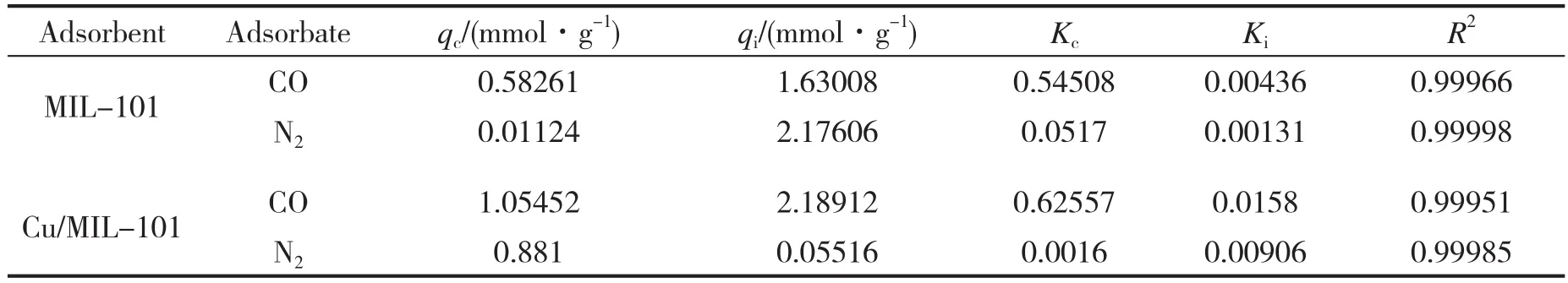
表2 CO和N2的DL模型拟合参数
图11给出了IAST模型计算得到的MIL-101、Cu/MIL-101吸附剂对CO/N2的吸附选择性。结果表明,在0~100kPa压力范围,MIL-101对CO/N2的吸附选择性逐渐降低,在100kPa时下降到26,说明虽然MIL-101对CO有大的吸附量,但是吸附选择性有限;在0~100kPa压力范围,Cu/MIL-101对CO/N2的吸附选择性逐渐升高,在100kPa时升高到2194,说明负载铜盐后,Cu(Ⅰ)对CO产生了π络合作用,加大了吸附剂对CO的吸附能力,随着CO分压的增高,CO吸附容量大幅增加。而Cu(Ⅰ)对N2没有π络合作用,随着压力的增高,只是略微上升。所以Cu/MIL-101对CO/N2有更好的吸附选择性。
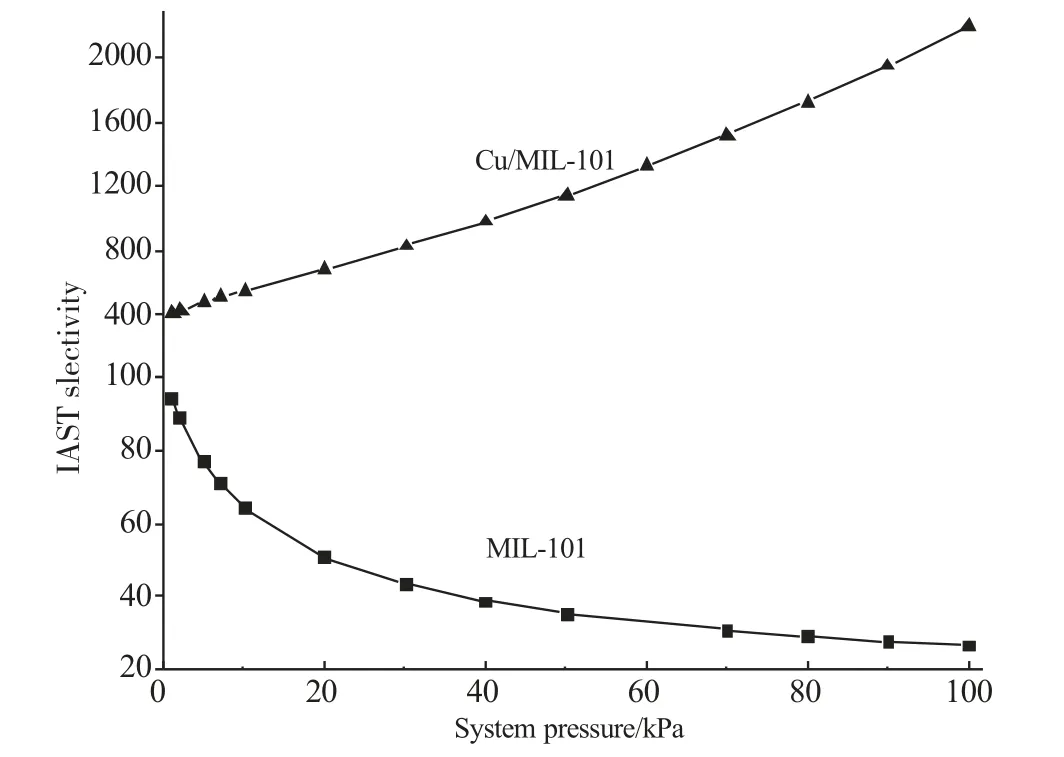
图11 298K下摩尔分数相等的CO/N2混合器的吸附选择性
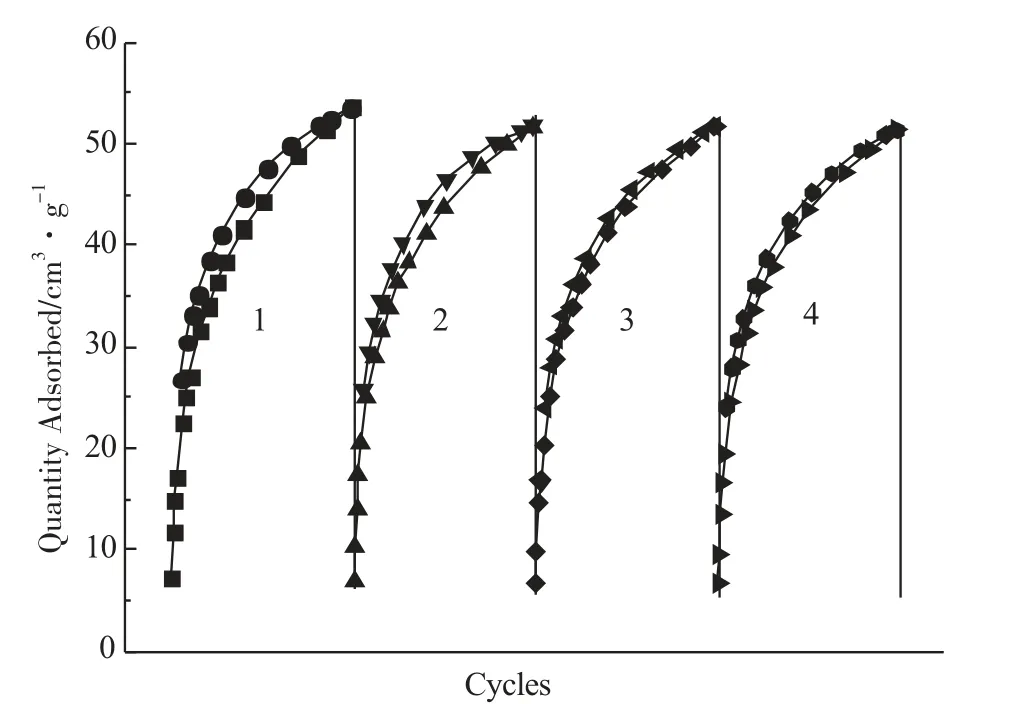
图12 Cu/MIL-101吸附剂的4次吸脱附曲线
2.3.6 吸附剂的再生性
图12为吸附剂经200℃抽真空预处理2h后,在ASAP2020分析仪上测定吸附-脱附循环4次的结果。从图12中可以看到,经4次吸附-脱附实验后,吸附剂对CO的吸附量没有明显减少,表明每次都脱附完全,说明利用混合铜盐法制得的CO吸附剂具有良好的再生性能。Cu/MIL-101吸附剂在空气中暴露数小时后,其CO吸附量会大幅下降,这是由于吸附剂中的Cu(Ⅰ)在空气中极易被氧化为Cu(Ⅱ),而Cu(Ⅱ)与CO没有络合吸附作用。但是我们发现,将被氧化的Cu/MIL-101吸附剂重新经200℃抽真空30min后,吸附剂对CO的吸附量又能回到50cm3·g-1以上。
3 结论
制备Cu/MIL-101吸附剂的最佳活化温度为220℃,最佳铜盐负载量为4mmol·(g MIL-101)-1。在298K、100kPa下,Cu/MIL-101吸附剂对CO的吸附量由23.93cm3·g-1提高到53.55cm3·g-1,对N2的吸附量由5.81cm3·g-1下降到3.29cm3·g-1,CO/ N2的吸附选择性由26提高到2194。同时Cu/MIL-101吸附剂在200℃、真空条件下可再生。因此,采用二价铜前驱体改性提高MIL-101对CO的吸附量及CO/N2的分离效率是可行的,具有应用前景。
[1] Zarca G, Ortiz I, Urtiaga A. Copper (Ⅰ) -containing supported ionic liquid membranes for carbon monoxide/nitrogen separation[J]. Journal of Membrane Science, 2013, 438(7): 38-45.
[2] Xie Y, Zhang J, Qiu J, et al. Zeolites modified by CuCl for separating CO from gas mixtures containing CO2[J]. Adsorption-journal of the International Adsorption Society, 1997(1): 27-32.
[3] N. Heymans, B. Alban, S. Moreau, et al. Experimental and theoretical study of the adsorption of pure molecules and binary systems containing methane, carbon monoxide, carbon dioxide and nitrogen. Application to the syngas generation[J]. Japanese Journal of Health & Human Ecology, 2011, 66(17): 3850-3858.
[4] Kohl A L, Nielsen R. Gas Purification[M]. Gulf Professional Publishing, 1997.
[5] Férey G, Mellotdraznieks C, Serre C, et al. A chromium terephthalate-based solid with unusually large pore volumes and surface area[J]. Science, 2005, 309(5743): 2040-2042.
[6] 郭金涛,陈勇,荆钰,等. 以醋酸盐为矿化剂合成金属有机骨架MIL-101[J]. 高等学校化学学报,2012,33(4):668-672.
[7] Shimada T, Ochi K. Ingredient and process for producing copper (Ⅰ) chloride, adsorbent and adsorbing method for reductive gas each with the use of copper (Ⅰ) chloride, and recovering method of carbon monoxide gas: US, 20050217483[P]. 2005.
[8] 李丽. CuCl负载型吸附剂的制备及其CO吸附性能研究[D]. 太原:太原理工大学,2010.
[9] 赵振国. 吸附作用应用原理[M].北京:化学工业出版社,2005.
[10] 翁诗甫. 傅里叶变换红外光谱仪[M].北京:化学工业出版社,2005.
[11] 岛田孝,越智幸史. 氯化铜(Ⅰ)的制造原料和方法及还原性气体吸附剂、吸附方法和一氧化碳气体的回收方法:CN,1683249[P]. 2005.
[12] Hong D, Kyu H Y, Christian S, et al. Porous Chromium Terephthalate MIL-101 with Coordinatively Unsaturated Sites: Surface Functionalization, Encapsulation, Sorption and Catalysis[J]. Advanced Functional Materials, 2009: 1537-1552.
[13] Zhu W, Graaf J M V D, Broeke L J P V D, et al. TEOM: A Unique Technique for Measuring Adsorption Properties. Light Alkanes in Silicalitel[J]. Industrial & Engineering Chemistry Research, 1998, 37(5): 1934-1942.
[14] Myers A L, Prausnitz J M. Thermodynamics of Mixed-Gas Adsorption[J]. International Review of Education, 1965, 11(1): 121-127.
Preparation and CO Adsorption Performance of Cu/MIL-101 Adsorbents
XU Yanyan1, DUAN Long2
(1. Guangdong Yuedian Xinhui Generation Co. Ltd., Jiangmen 529149,China, 2.Nanjing Tech University State Key Laboratory of Materials-Oriented Chemical Engineering, Nanjing 210009, China )
Copper(Ⅱ) formate and cupric chloride precursor were loaded to metal organic framework MIL-101 by impregnation method. Cu/MIL-101 adsorbents were prepared by change of the activation temperature and different copper loadings. Their crystal structure and properties were characterized by XRD, N2adsorption and desorption, FT-IR and TG. The adsorption capacities of CO and N2on Cu/MIL-101 adsorbents were measured under 298K and 101.3kPa. The results showed that optimum activation temperature and copper loadings of the adsorbents was 493K and 4mmol/g MIL-101. Copper base-functionalized MIL-101 adsorbent, the adsorption capacity of CO was improved from 23.93cm3/g to 53.55cm3/g, while the adsorption capacity of N2was decreased from 5.81cm3/g to 3.29cm3/g, the ideal adsorbed solution theory (IAST) model was used to predict the adsorption separation of CO over N2, the adsorption selectivity increased from 26 of MIL-101 to 2194 of Cu/MIL-101. The adsorbents could be regenerated under conditions of 200℃ and vacuum.
metal organic framework; carbon monoxide; cuprous chloride; impregnation; adsorption selectivity
TQ 424.2
A
1671-9905(2017)03-0012-06
2017-01-19

