抗骨增生片的质量标准提高研究
陈 希,万林春,张文婷(江西省药品检验检测研究院/江西省药品与医疗器械质量工程技术研究中心,南昌330029)
抗骨增生片的质量标准提高研究
陈 希*,万林春,张文婷#(江西省药品检验检测研究院/江西省药品与医疗器械质量工程技术研究中心,南昌330029)
目的:完善和提高抗骨增生片的质量标准。方法:采用薄层色谱法(TLC)对制剂中骨碎补、淫羊藿、鸡血藤进行定性鉴别;采用高效液相色谱法测定制剂中毛蕊花糖苷和淫羊藿苷的含量:色谱柱为Diamonsil C18,流动相为乙腈-0.1%甲酸溶液(梯度洗脱),流速为1.0 mL/min,检测波长为270 nm(淫羊藿苷)、334 nm(毛蕊花糖苷),柱温为25℃,进样量为10µL。结果:骨碎补、淫羊藿、鸡血藤的TLC图斑点清晰,分离度好,阴性对照无干扰。毛蕊花糖苷、淫羊藿苷检测进样量线性范围分别为0.018 8~1.88 μg(r=0.999 9)、0.107~2.14 μg(r=0.999 9);精密度、稳定性、重复性试验的RSD<2.0%;加样回收率分别为100.2%~105.0%(RSD=1.6%,n=9)、96.2%~99.5%(RSD=1.4%,n=9)。结论:该标准能更加有效地控制抗骨增生片的质量。
抗骨增生片;柚皮苷;淫羊藿苷;毛蕊花糖苷;鸡血藤;薄层色谱法;高效液相色谱法
抗骨增生片具有活血、止痛和补肾的功效[1-3],适用于肥大性脊椎炎、跟骨刺、颈椎病、大骨节病、增生性关节炎的治疗。该制剂由熟地黄、骨碎补、鸡血藤、淫羊藿和肉苁蓉等7味中药组成,其糖衣片和薄膜衣片分别收载于《卫生部药品标准·中药成方制剂》[4]和《国家药品标准》[5],内容均只有鸡血藤的薄层色谱(TLC)鉴别和片剂的常规检查,标准较简单,不利于产品的质量控制。笔者采用TLC对骨碎补、淫羊藿和鸡血藤进行定性鉴别;采用高效液相色谱法(HPLC)同时测定制剂中毛蕊花糖苷、淫羊藿苷的含量,以期为提高抗骨增生片的质量标准提供参考。
1 材料
1.1 仪器
LC-2010C型HPLC仪,包括紫外检测器(日本Shimadzu公司);BT125D型电子分析天平(德国Sartorius公司);BUG25-06型超声波清洗仪(上海必能信超声有限公司,功率:250 W,频率:25 kHz)。
1.2 药品与试剂
抗骨增生片(陕西济康药业有限公司,批号:100301、090701;陕西白云制药有限公司,批号:091101、090901;江门名盛制药有限公司,批号:20080801,规格均为0.26 g/片);淫羊藿苷对照品(批号:110737-200415,纯度:100%)、柚皮苷对照品(批号:110722-200610,纯度:100%)、毛蕊花糖苷对照品(批号:111530-200303,纯度:96.8%)均购自中国食品药品检定研究院;鸡血藤对照药材(笔者购自江西樟树中药材市场,经本单位万林春副主任中药师鉴定为真品);羟甲基纤维素钠、硅胶G(青岛海洋化工厂分厂);乙腈为色谱纯,其余试剂均为分析纯,水为超纯水。
2 方法与结果
2.1 定性鉴别
2.1.1 骨碎补、淫羊藿 取样品20片,除去包衣,研细,加石油醚(60~90℃)30 mL,加热回流1 h,放冷,滤过,滤液备用;残渣加乙酸乙酯70 mL,加热回流1 h,放冷,滤过,滤液蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液。另取淫羊藿苷、柚皮苷对照品各适量,分别加甲醇制成质量浓度均为0.5 mg/mL的单一对照品溶液。按抗骨增生片处方和工艺分别制备缺骨碎补、淫羊藿的单一阴性样品,并按供试品溶液制备方法制成单一阴性对照溶液。按TLC法[2015年版《中国药典》(四部)][6]试验,吸取上述5种溶液各5 μL,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以乙酸乙酯-丁酮-甲醇-水(10∶1∶1∶1,V/V/V/V)为展开剂,展开,取出,晾干,喷以三氯化铝试液,加热至紫外光灯(365 nm)下可见。结果,供试品色谱中,在与对照品色谱相应位置上显相同颜色的斑点,阴性对照无干扰,详见图1。

图1 骨碎补、淫羊藿的薄层色谱图1.缺骨碎补的阴性对照;2.缺淫羊藿的阴性对照;3~5.供试品;6.淫羊藿苷对照品;7.柚皮苷对照品Fig 1 TLC chromatograms of Drynaria fortunei and Epimedii Folium1.negative control without D.fortunei;2.negative control without Epimedii Folium;3-5.test samples;6.reference substance of icariin;7.reference substance of naringin
2.1.2 鸡血藤 取“2.1.1”项下石油醚提取液,挥干,残渣加三氯甲烷1 mL使溶解,作为供试品溶液。另取鸡血藤对照药材1 g,按供试品溶液制备方法制成对照药材溶液。按抗骨增生片处方和工艺制备缺鸡血藤的阴性样品,并按供试品溶液制备方法制成阴性对照溶液。按TLC法[2015年版《中国药典》(四部)][6]试验,吸取上述3种溶液各20 μL,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以石油醚(30~60℃)-乙酸乙酯(19∶5,V/V)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,105℃下加热至斑点显色清晰,置日光下检视。结果,供试品色谱中,在与对照药材色谱相应位置上显相同颜色的斑点,阴性对照无干扰,详见图2。
2.2 含量测定
2.2.1 色谱条件与系统适用性试验 色谱柱:Diamonsil C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%甲酸溶液(B),洗脱程序(0~12 min,20%A;12~30 min,30%A;30~40 min,20%A);流速:1.0 mL/min;检测波长:270 nm(淫羊藿苷)、334 nm(毛蕊花糖苷);柱温:25℃;进样量:10µL。在上述色谱条件下,理论板数以毛蕊花糖苷和淫羊霍苷峰计>3 000;各成分基线分离良好,分离度>1.5,详见图3、图4。
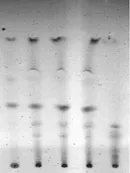
图2 鸡血藤的薄层色谱图Fig 2 TLC chromatogram of spatholobus suberectus
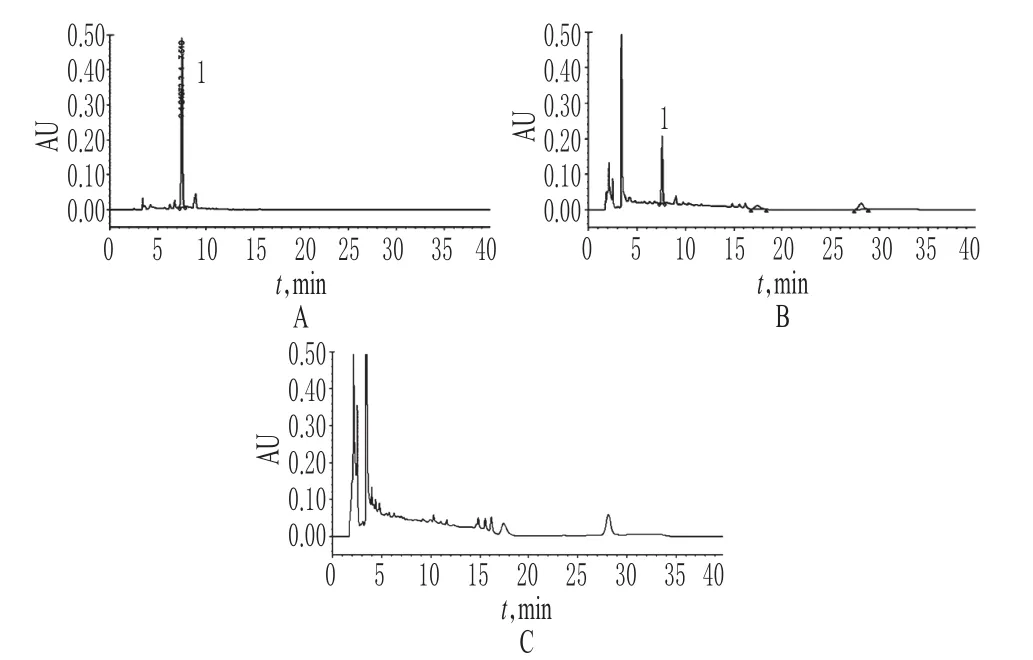
图3 高效液相色谱图(334 nm)Fig 3 HPLC chromatograms(334 nm)
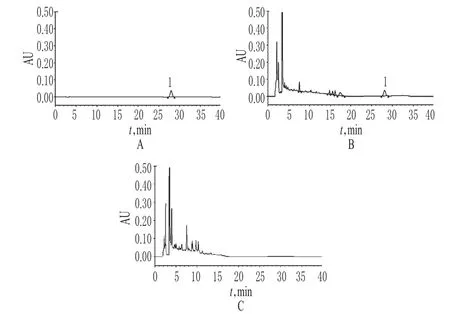
图4 高效液相色谱图(270 nm)Fig 4 HPLC chromatograms(270 nm)
2.2.2 混合对照品溶液的制备 取待测成分对照品适量,精密称定,加甲醇制成毛蕊花糖苷、淫羊藿苷质量浓度分别为10、60µg/mL的混合对照品溶液。
2.2.3 供试品溶液的制备 取样品20片,除去包衣,精密称定,研细,取约1.0 g,精密称定,置于具塞锥形瓶中,精密加50%甲醇25 mL,称定质量,超声处理60 min,放冷,再次称定质量,加50%甲醇补足减失的质量,摇匀,滤过,即得。
2.2.4 线性关系考察 取待测成分对照品适量,加甲醇制成毛蕊花糖苷、淫羊藿苷质量浓度分别为9.09、10.70 μg/mL的单一对照品溶液,分别精密量取上述毛蕊花糖苷对照品溶液2、5、10、20、50、100、200 μL,淫羊藿苷对照品溶液1、2、5、10、20 μL,按“2.2.1”项下色谱条件进样测定,记录峰面积。以待测成分进样量(x,μg)为横坐标、峰面积(y)为纵坐标进行线性回归,得毛蕊花糖苷、淫羊藿苷的回归方程分别为y=3 201 368x-31 313(r=0.999 9)、y=412 757x-17 158(r=0.999 9)。结果表明,毛蕊花糖苷、淫羊藿苷检测进样量线性范围分别为0.018 8~1.88、0.107~2.14 μg。
2.2.5 精密度试验 取“2.2.2”项下混合对照品溶液适量,按“2.2.1”项下色谱条件连续进样测定6次,记录峰面积。结果,毛蕊花糖苷、淫羊藿苷峰面积的RSD分别为1.5%、0.2%(n=6),表明仪器精密度良好。
2.2.6 稳定性试验 取“2.2.3”项下供试品溶液(批号:20080801)适量,分别于室温下放置0、1、2、4、8、12 h时按“2.2.1”项下色谱条件进样测定,记录峰面积。结果,毛蕊花糖苷、淫羊藿苷峰面积的RSD分别为0.60%、1.90%(n=6),表明供试品溶液在室温放置12 h内基本稳定。
2.2.7 重复性试验 精密称取同一批样品(批号:20080801)适量,按“2.2.3”项下方法制备供试品溶液,共6份,再按“2.2.1”项下色谱条件进样测定,记录峰面积。结果,毛蕊花糖苷、淫羊藿苷峰面积的RSD分别为1.9%、0.9%(n=5),表明本方法重复性良好。
2.2.8 加样回收率试验 取已知含量样品(批号:20080801)适量,共9份,分别加入低、中、高质量的待测成分对照品,按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表1。
2.2.9 样品含量测定 取5批样品各适量,分别按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并计算样品含量,结果见表2。
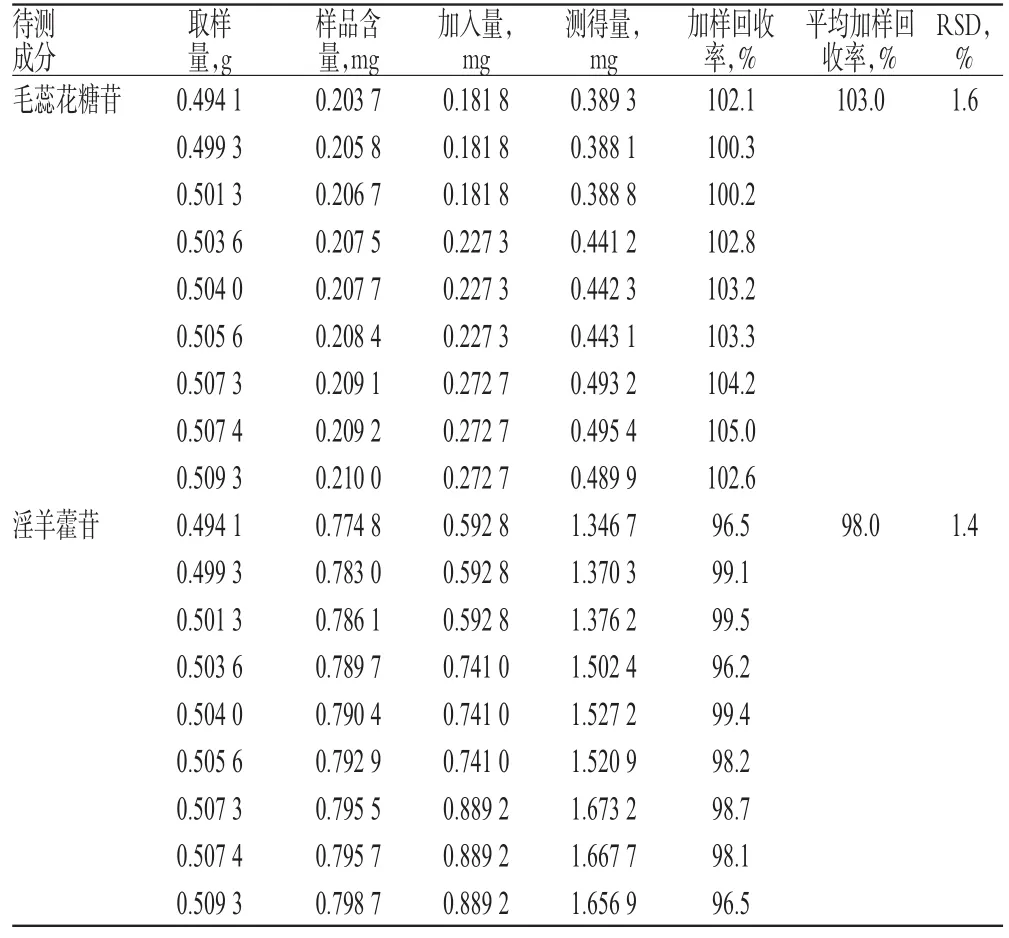
表1 加样回收率试验结果(n=9)Tab 1 Results of recovery tests(n=9)

表2 样品含量测定结果(n=3,μg/片)Tab 2 Results of contents determination of samples(n=3,μg/tablet)
3 讨论
3.1 定性指标的选择
骨碎补和淫羊藿中的鉴别大多都是单独鉴别,鉴于提取方法和极性近似[7],笔者考虑在同一TLC中同时鉴别,原设计还打算同时鉴别毛蕊花糖苷,但因阴性干扰,未加入。处方中含有鸡血藤原粉,笔者考虑采用鸡血藤对照药材进行鉴别。前两者先采用石油醚除去杂质,后采用乙酸乙酯提取后进行鉴别,而鸡血藤的鉴别又正好利用了上述石油醚提取液作为供试液,这样不但操作简便,并且节省了分析成品量和时间,同时阴性均无干扰,专属性好。
3.2 含量测定条件的选择
已有文献大多是针对抗骨增生片(丸)中淫羊藿苷进行含量测定研究,很少有毛蕊花糖苷含量的研究报道,更未见两者同时测定的研究[7-10]。因甲醇提取样品中的毛蕊花糖苷和淫羊藿苷效果良好,所以选择双波长同时测定这两个成分,而流动相中加入0.1%甲酸溶液可以改善峰形[11-15],但两者出峰时间相隔较远,所以采用梯度洗脱的方法,使出峰时间大大缩短。本试验含量测定方法简便快捷、结果准确、重复性好,可用于该制剂的质量控制。
[1] 周军,刘晓海,宋亚玲,等.抗骨增生胶囊对大鼠骨性关节炎的实验研究[J].中国实验方剂学杂志,2012,18(10):145-147.
[2] 陈履平,李龙.抗骨增生胶囊治疗膝骨关节炎的临床[J].实用临床医药杂志,2010,14(15):98-100.
[3] 邹文孝,田维君,张春,等.抗骨增生片联合骨肽片治疗骨质增生症60例[J].中国药业,2012,21(8):93-94.
[4] 国家卫生部.卫生部药品标准:中药成方制剂:第7册[S].北京:化学工业出版社,1993:74-75.
[5] 国家食品药品监督管理总局.国家药品标准[S].WS3-B-1338-93-1.
[6] 刘湘豫,彭词艳,胡焰,等.抗骨增生片制备工艺及质量标准研究[J].中南药学,2013,11(8):572-574.
[7] 国家药典委员会.中华人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2015:57-57.
[8] 杨立芳,宋文耆.高效液相色谱法测定抗骨增生丸中淫羊藿苷的含量[J].中国药房,2006,17(18):1420-1422.
[9] 杨小妹,朱俊彦.高效液相色谱法测定抗骨增生片中淫羊藿苷含量[J].中国现代应用药学杂志,2005,22(4):314-315.
[10] 刘淑妦,张妮瑜,辛秀,等.抗骨增生片定性定量方法研究[J].中南药学,2014,12(6):574-575.
[11] 顾利红,张莹.HPLC测定护心胶囊中淫羊藿苷的含量[J].中成药,2008,30(7):1092-1094.
[12] 杨增明.HPLC法测定淫羊藿苷含量研究[J].中国药品标准,2008,9(1):143-144.
[13] 蒋桂平.高效液相色谱法测定抗骨增生丸中淫羊藿苷的含量[J].中南药学,2008,6(3):322-323.
[14] 张贵财,朱旭江,杜兴,等.HPLC法测定兰州肉苁蓉中毛蕊花糖苷的含量[J].中国药事,2010,24(8):801-803.
[15] 柴茂,董诚明,江道会,等.不同品种怀地黄中梓醇和毛蕊花糖苷的高效液相色谱法测定[J].中医学报,2013,28(5):690-692.
(编辑:张 静)
Study on Improving the Quality Standards of Kanggu Zengsheng Tablet
CHEN Xi,WAN Linchun,ZHANG Wenting(Jiangxi Institute for Drug Control/Jiangxi Provincial Engineering Research Center for Drug and Medical Device Quality,Nanchang 330029,China)
OBJECTIVE:To develop and improve the quality standard for Kanggu zengsheng tablet.METHODS:TLC was used for the qualitative identification of Drynaria fortunei,Epimedii Folium and Spatholobus suberectus;HPLC was used for the contents determination of icariin and acteoside:the column was Diamonsil C18with mobile phase of acetonitrile-0.1%formic acid solution(gradient elution)at a flow rate of 1.0 mL/min;detection wavelength was 270 nm for icariin and 334 nm for acteoside,Cdumn temperature was 25℃,and the injection volume was 10µL.RESULTS:The TLC spots of D.fortunei,Epimedii Folium and S.suberectus were clear and well separated,negative control without interference.The linear range was 0.018 8-1.88 μg for acteoside(r=0.999 9)and 0.107-2.14 μg for icariin(r=0.999 9);RSDs of precision,stability and reproducibility tests were lower than 2.0%;recoveries were 100.2%-105.0%(RSD=1.6%,n=9)and 96.2%-99.5%(RSD=1.4%,n=9).CONCLUSIONS:The improved standard can more effectively control the quality of Kanggu zengsheng tablet.
Kanggu zengsheng tablet;Naringin;Icariin;Acteoside;Spatholobus suberectus;TLC;HPLC
R284.1;R917
A
1001-0408(2017)06-0838-04DOI10.6039/j.issn.1001-0408.2017.06.32
2016-02-06
2016-02-26)
*主管检验师,硕士。研究方向:药物分析和食品分析。电话:0791-88158796。E-mail:89276794@qq.com
#通信作者:副主任药师,硕士。研究方向:药物分析。电话:0791-88158630。E-mail:2819176959@qq.com

