铝取代微/纳米结构氢氧化镍的制备及电化学性能
孙海峰,蒋文全
(北京有色金属研究总院,北京 100088)
1 前言
近年来,随着人们对镍电极放电原理的深入了解以及纳米材料在化学能源领域内的扩展,纳米级氢氧化镍得到了广泛的关注[1,2]。我国是继日、美进入产业化研究最早的发展中国家,镍氢电池的发展已取得了很大进步,但在高比能量、高比功率、循环寿命以及高低温性能方面仍落后国际水平,因此提高正极活性材料电荷转移数,研究高比功率、高比能量的镍电极活性材料将是提高镍氢电池性能及应用的发展方向和研究重点[3,4]。为了制备稳定的α-Ni(OH)2,已经进行了大量的研究工作。国内外学者尝试掺杂其它金属元素如Al,Zn,Fe,Co,Mn等形成结构稳定的α-Ni(OH)2,其中Al取代α-Ni(OH)2既具有较高的结构稳定性又具有优异的电化学性能。掺杂Mn元素可以提高α-Ni(OH)2电极的循环稳定性。Kamath等人[5]采用化学沉淀法制备了Al稳定的α-Ni(OH)2,Demourgues等[6-7]研究了锰掺杂的α-Ni(OH)2的物理、化学和电化学性能。Dai等[8]报导了具有纳米结构的Al掺杂α-Ni(OH)2稳定结构、形貌和电化学性。尽管这些工作都取得了一定进展,其产品有较高的质量比容量,但其振实密度较低,用作镍氢电池正极活性材料的体积比容量和活性物质含量都相对较低。
为进一步提高Ni(OH)2的结构和电化学稳定性,拟采用水热法,利用尿素均相沉淀制备Al掺杂的α-Ni(OH)2,深入研究了Al取代含量对α-Ni(OH)2结构、电化学性能以及在强碱中陈化影响,并对添加剂作用机理进行了初步探讨。
2 制备方法
以硫酸镍、硫酸铝和尿素为原料,配成一定比例的混合溶液并放入聚四氟乙烯内衬的压力容器中,密封,恒温反应数小时冷却至室温。洗涤干燥。
表1为铝掺杂样品实验参数。从表中可看出,掺杂铝后,反应溶液的pH值明显降低,这是因为溶液中铝离子消耗了大量氢氧根离子。
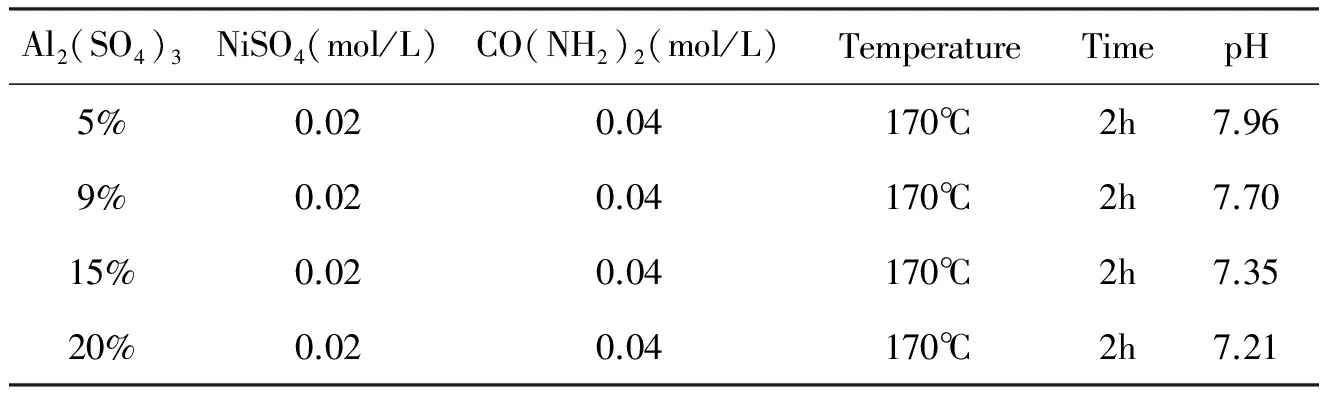
表1 制备铝掺杂样品的实验参数
3 物理性能表征
3.1 X射线衍射分析
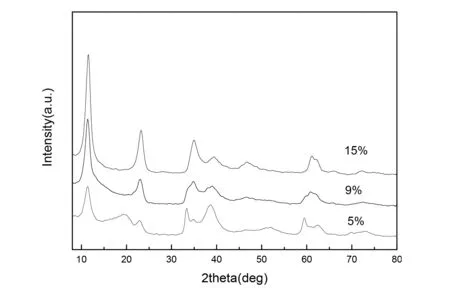
图1 不同铝掺杂量制备样品的XRD图
如图1所示为不同铝掺杂量制备样品的XRD图,从图中可以看出,随着铝掺杂量的增加,样品由混合相结构转变成典型的α-Ni(OH)2结构,铝掺杂量5%样品在19°附近出现β相在(001)晶面的特征衍射峰,而2θ=11°、23°和38°附近则出现了α-Ni(OH)2涡旋结构特征峰。整个XRD衍射峰发生了一定程度偏移,这可能与生成的氢氧化镍层与层之间发生扭曲和平移所形成的湍层结构以及两相分布不均有关。与标准谱峰对比,不同铝含量的样品在每一个晶面所对应的衍射峰都发生了明显的宽化,衍射强度也明显下降。其中掺杂量为15%的衍射峰型比较尖锐,这说明制备样品的结晶度较好。
不同样品晶格常数和层间距d如表2所示,从表中可以看出随着Al掺杂量的增加晶格常数a和c都逐渐减小,同时d值也有所降低。这一结果和Wang C Y[9]等报道的结果是一致的。这说明A13+通过共沉积进入了Ni(OH)2晶格中,而且随着反应溶液中铝含量的增加,插入层间的A13+增多。造成晶格常数和d值变化的原因可能是Al3+的离子半径(0.54)比Ni2+(0.69)的离子半径小,同时Al3+插入晶格中会降低层间的排斥力。

表2 不同铝含量样品的晶格常数和d值
3.2 不同铝含量掺杂α-Ni(OH)2的结构稳定性研究
如图2所示为室温下,不同铝含量样品在6mol/L KOH溶液中陈化6天的X 射线衍射谱图。从图中可以看出,在强碱性溶液中陈化三天后,未掺杂的氢氧化镍在19°、33°、39°、52°、59°出现β相衍射峰,α相完全消失,这说明样品已经完全转化成 β-Ni(OH)2。铝含量为5%的样品经过6天陈化后,未转变成β相,仍然保持混合相结构的特征峰,但与陈化前相比,α相特征衍射峰发生了宽化。9%和15%铝含量的样品仍保持纯的α相结构,衍射峰未发生明显变化。

图2 不同铝掺杂量样品在电解液中陈化6天后XRD图
3.3 扫描电镜分析
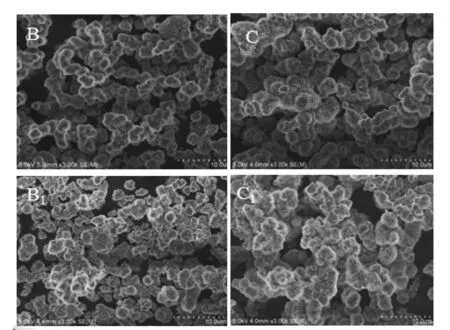
图3 不同铝含量样品陈化前后SEM图(B和C为陈化前含5%Al和15%Al样品,B1和C1为陈化后含5%Al和15%Al样品)
如图3所示为室温下不同铝含量样品在6M KOH溶液中陈化前后的扫面电镜照片,从图中可以看出,陈化前不同铝含量样品都表现为典型的花瓣球形颗粒,且大小均匀,颗粒之间有一定团聚。陈化后颗粒仍为花瓣微球,但其团聚情况更加明显,颗粒整体尺寸有所增加。陈化过程中,小颗粒之间通过连接聚集而团聚,并且小颗粒不断溶解,并在大颗粒上沉淀析出促使大颗粒不断生长如图3(B1、C1)。Wang C Y也报道了陈化中微晶通过溶解-重结晶的过程长大,陈化过程中结晶度所有提高,层状无序性降低。文献[10]中报道Al取代α-Ni(OH)2都没有确定的形状,界面模糊。与不规则的氢氧化镍相比,球状结构具有颗粒状形态,流动性好,纳米片层组装体也有利地提高了材料的比表面积,增大了与电解液的接触面积和在泡沫镍中的填充量。
3.4 电化学性能测试
3.4.1 充放电性能测试
图 4为不同铝含量样品在0.2C倍率下第十个循环的充放电曲线。由图可见,样品的放电容量随着Al含量的增加先增大后减小。铝含量为9%的样品具有最高的放电比容量,达262mAh/g。而且所有样品都有一个较为平坦的放电平台,均高于未掺杂样品的放电电位,放电电位随着铝含量的增加而升高。但放电电位增加的同时充电电位也有所增加,这与通常的充放电规律并不相符,也需要进一步的研究和解释。

图4 不同铝含量样品0.2C充放电曲线
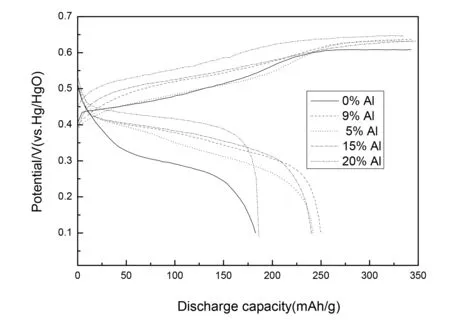
图5 不同铝含量样品在1.0C充放电曲线
不同样品在小电流0.2C充放倍率下活化10个循环后,再进行大电流1.0C倍率的充放电性能测试。图5为不同Al含量的Ni(OH)2样品在1.0C倍率下第5个循环的充放电曲线。从图中可以看出,掺杂Al后,样品的质量比容量有了一定提高,其中掺Al 9%时质量比容量达到249.8mAh/g比未掺杂纳米Ni(OH)2(182.8mAh/g)增加了36.6%,但是铝掺杂量并不是越多越高,随着铝含量的增加样品的放电比容量呈现先增加后减小的趋势,掺杂Al 20%时放电容量仅186.3mAh/g跟未掺杂纳米Ni(OH)2基本相同。这是因为掺杂Al以后改变了各样品晶格参数和层间距, Ni(OH)2层间夹杂了大量的阴离子,导致电化学阻力增大,另外Al的掺杂量增多导致了电极放电活性物质的减少,氧化电位和析氧电位差值降低,活性物质利用率降低。由图还可以看出,制备的所有样品都具有较平坦的放电平台,样品的放电电位随着铝含量的增加而升高,这与小电流充放电时的情况相似。这说明掺杂Al以后电池的极化变小了。
3.4.2 循环稳定性测试
图6-7分别给出了不同Al含量的氢氧化镍在25℃下1.0C和3.0C倍率的充放电循环曲线图。从图中可以看出,总体上掺杂Al之后的氢氧化镍放电性能比未掺杂的氢氧化镍好,不同Al含量的氢氧化镍电极均具有较为稳定的循环寿命,而未掺杂样品在开始的十周内随着循环次数的增加而迅速衰减,不同倍率放电循环图中还可以看出,铝含量为9%的样品放电比容量最大,而无掺杂样品的放电比容量最低。而研究表明传统液相沉淀法制备的α-Ni(OH)2中铝含量达到20%以上才具有稳定的结构。由此可见,水热法可制备出电化学性能良好且结构稳定的铝掺杂α-Ni(OH)2。

图6 不同铝含量样品1.0C放电循环曲线
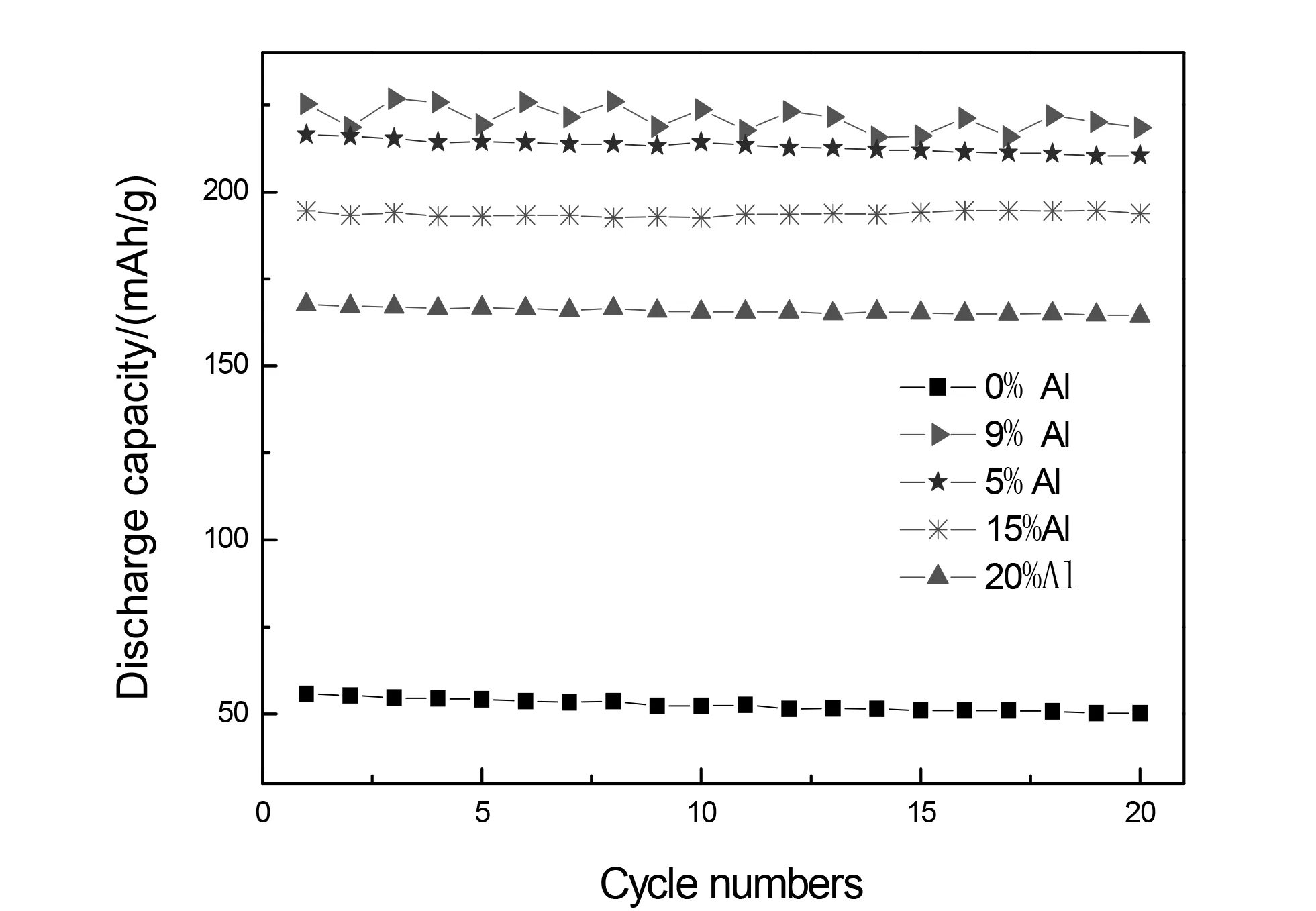
图7 不同铝含量样品3.0C放电循环曲线
4 结论
采用水热法,以尿素为沉淀剂制备得到了铝掺杂纳米花瓣状Ni(OH)2,XRD分析表明随着Al掺杂量的增加晶格常数a和c都逐渐减小,同时d值也有所降低。不同铝含量的样品都表现为典型的纳米片层组装的微米级球形颗粒,且大小均匀。电化学充放电性能测试结果表明,铝的掺入提高了α-Ni(OH)2的充放电电位,铝的掺入可以降低电极的电化学极化,铝掺杂样品也表现优异的循环寿命,1.0C和3.0C倍率循环20周后,铝摩尔分数为9%的样品放电比容量分别衰减了0.5mAh/g和6mAh/g。
[1] 邹建梅,邹全忠.泡沫镍正极添加剂的研究[J].电源技术,1998,22(4):144-147.
[2] 冷拥军,马紫峰,张存根,等.铁取代氢氧化镍制备、结构与电化学性能-I 电化学性能[J].电源技术,1999,23(6):322-324.
[3] 吴敏银.改性氢氧化镍的制备结构和电化学性能[D].杭州:浙江大学,2006.
[4] Sugimoto A,Ishida S,Hanawa K.Preparation and characterization of Ni/Al-layered double hydroxide[J].Journal of the Electrochemical Society,1999,146(4):1251-1255.
[5] Dixit M,Jayashree R S,Kamath P V,et al.Electrochemically imprenated aluminum- stabiliz α-Nickel hydroxide electrodes[J].Electrochemical and Solid-State Letters,1999,2(4):170-171.
[6] Demourgues G L,Denage C,Delmas C.New manganese-substituted nickel hydroxides: Part 1.Crystal chemistry and physical characterization[J].Journal of Power Sources,1994,52(2):269-274.
[7] Guerlou-Demourgues L,Delmas C.Electrochemical behavior of the manganese-substituted nickel hydroxides[J].Journal of The Electrochemical Society,1996,143(2):561-566.
[8] Dai J X,Li S F Y,Xiao T D,et al.Structural stability of aluminum stabilized alpha nickel hydroxide as a positive electrode material for alkaline secondary batteries[J].Journal of Power Sources,2000,89(1):40-45.
[9] Wang C Y, Zhong S, Konstantinov K,et al.Structural study of Al-substituted nickel hydroxide[J].Solid state ionics,2002,148:503-508.
[10] Johnston C,Graves P R.In situ Raman spectroscopy study of the nickel oxyhydroxide electrode (NOE) system[J].Applied Spectroscopy,1990,44(1):105-115.