数学思想方法在化学中的应用
江苏 印志林
(作者单位:江苏省常州市横山桥高级中学)
数学思想方法在化学中的应用

作为一门工具学科,数学在化学的各个领域中都有着广泛的应用。在化学复习中重视数学思想方法的运用,有意识地将化学问题抽象为数学问题,可提高自己的思维能力和复习效率。下面具体举例,就数学思想方法在化学中的应用进行分析。
一、基础数学知识的运用
数学知识在化学中的运用几乎是无处不在的。例如,用数轴表示溶液的pH或化学反应的产物,用几何知识判断有机物分子中原子的位置关系,用集合图表示化学概念之间的逻辑关系,用数学归纳法归纳核外电子的排布规律或某类有机物的分子通式,用排列组合知识判断同分异构体的数目,用不等式求数值范围,等等。学习时要有数学意识,自觉地建立数学模型,借用数学知识分析解决化学问题。
例1 研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是
( )
A.密闭容器中CuO和C高温反应的气体产物:


B.Fe在Cl2中的燃烧产物:

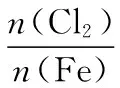
C.AlCl3溶液中滴加NaOH后铝的存在形式:
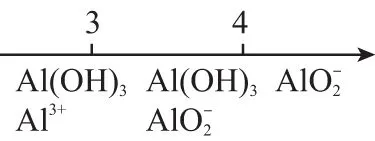

D.氨水与SO2反应后溶液中的铵盐:
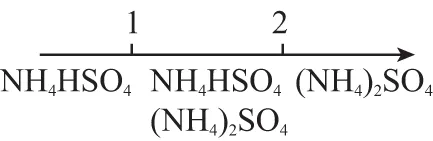

解析:A、C、D项中反应的产物与反应物的物质的量之比有关;Fe在Cl2中燃烧的产物只有FeCl3,与Fe和Cl2的用量无关。
答案:B
( )
A.5___________ B.7___________ C.8___________ D.10
答案:D
二、基本数学思想的运用
数学思想是对数学事实与理论经过概括后产生的本质认识,掌握数学思想,就是掌握数学的精髓。将数学思想应用于化学学科,是化学学科趋于成熟的一大表现。
1.数形结合思想
化学中形式多样的图象问题,就是数形结合的具体体现。不管是哪类图象题,解题的关键都是要看懂图象,分析曲线的坐标、起点、转折点、平台、终点及变化趋势所表示的含义,联系有关知识规律解决问题。
例3 25℃时,取浓度均为0.1 mol·L-1的醋酸溶液和氨水各20 mL,分别用0.1 mol·L-1NaOH溶液、0.1 mol·L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示。下列说法正确的是
( )

A.曲线Ⅰ:滴加溶液到10 mL时,
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B.曲线Ⅰ:滴加溶液到20 mL时,
C.曲线Ⅱ:滴加溶液在10 mL~20 mL之间,
D.曲线Ⅱ:滴加溶液到10 mL时,
c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)]

答案:D
2.方程函数思想
方程函数思想在化学计算中的使用非常普遍。有关混合物的计算是高中化学中常见的题型,其解题过程大体可分为两个阶段,第一阶段利用化学知识找出题目中各物质或量的关系,第二阶段利用关系列出方程计算得出结果。
例4 1.52 g铜镁合金完全溶解于50 mL密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1 120 mL (标况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到 2.54 g 沉淀,下列说法不正确的是
( )
A.该合金中铜与镁的物质的量之比是2∶1
B.该浓硝酸中HNO3的物质的量浓度是14.0 mol/L
C.NO2和N2O4的混合气体中,NO2的体积分数是80%
D.得到2.54沉淀时,加入NaOH溶液的体积是600 mL

答案:D
另外,分类讨论、等价转化、分类与整合、化归与转化、特殊与一般等数学思想在化学中也都有重要应用,同学们可以在做题过程中自己去体会。
三、重要数学方法的运用
在化学计算中,有几种常用的特殊数学方法,运用这些方法解题,往往可以出奇制胜。
1.差量法
差量法是指根据化学反应前后物质的量发生的变化,找出“理论差量”。这种差量可以是质量、物质的量、气态物质的体积和压强、反应过程中的热量等。用差量法解题时,应先把化学方程式中的对应差量(理论差量)跟差量(实际差量)列成比例,然后求解。
例5 为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1g样品加热,其质量变为w2g,则该样品的纯度(质量分数)是
( )
解析:样品受热时NaHCO3分解,根据固体质量变化可列质量差比例求解。

168___________ 106___________62
m(NaHCO3)___________(w1-w2) g

答案:A
2.平均值法
若混合物只有A、B两种成分,且已知M1>M2,则必有M1>M>M2[M代表平均相对原子(分子)质量、平均浓度、平均含量、平均生成量、平均消耗量等]。若已知M,则M1和M2必有一个比M大,另一个比M小。也就是说我们只要知道M就可推知M1、M2的取值范围,而不需要进行复杂的计算就可以迅速得出正确的答案。
例6 将15 g由两种金属组成的混合物投入足量盐酸中,充分反应后得到11.2 L H2(标准状况),则原混合物的组成肯定不可能为
( )
A.Mg和Ag________________B.Zn和Cu
C.Al和Zn___________D.Al和Cu
解析:本题可用平均摩尔电子质量(即提供1 mol电子所需的质量)法求解。反应中H+被还原生成H2,产生0.5 mol H2需得到1 mol e-,即15 g 金属混合物可提供1 mol e-,其平均摩尔电子质量为15 g·mol-1。各选项中,金属Mg、Zn、Al的摩尔电子质量分别为12 g·mol-1、32.5 g·mol-1、9 g·mol-1,其中不能与盐酸反应的Ag和Cu的摩尔电子质量可看作无穷大。根据平均值原理可知,原混合物中一种金属的摩尔电子质量大于15 g·mol-1,另一金属的摩尔电子质量小于15 g·mol-1,据此可得答案。
答案:B
3.极值法
极值法是采用极限思维方式解决一些模糊问题的解题技巧。它是将题设构造为问题的两个极端,然后依据有关化学知识确定所需反应物或生成物的量值,进行判断分析,求得结果。
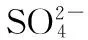
( )
A.9.0 L___________B.13.5 L
C.15.7 L___________D.16.8 L
解析:12.0 g CuO 的物质的量为0.15 mol。混合气体中,NO2和NO的体积比为1∶1,则其组成相当于NO1.5,N的平均化合价为+3价。
①若混合物中只有CuS,则CuS的物质的量为0.15 mol。

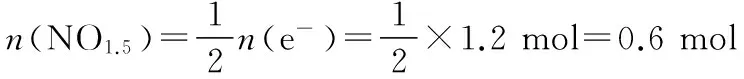
②若混合物中只有Cu2S,则Cu2S的物质的量为0.075 mol。


因此,V的取值范围为8.4 答案:A (作者单位:江苏省常州市横山桥高级中学) 趣味阅读 诺贝尔化学奖趣闻(一) 获奖人数——自1901年设立以来至2013年,诺贝尔化学奖一共颁发了105次。在112年的历史上,共有166人次获颁诺贝尔化学奖。不过,由于英国生物化学家弗雷德里克·桑格曾在1958年及1980年两度问鼎,实际获奖人数应该是165。从1901年到2013年,独享诺贝尔化学奖荣耀的科学家共有63位;由两位获奖者平分秋色的情况出现过23次;另有19次为三个人分享大奖,今年便是如此。 最年轻的获奖者——1935年,35岁的法国科学家弗雷德里克·约里奥捧得诺贝尔化学奖桂冠,成为该奖项最年轻的获奖者,与他携手走上领奖台的还有他的妻子伊雷娜·约里奥·居里(居里夫人的长女)。 8次空缺——诺贝尔化学奖的颁发出现过8次空缺:1916年、1917年、1919年、1924年、1933年、1940年、1941年和1942。原因不外乎两点:没有能够达到评奖标准的候选者,以及众所周知的不可抗力——一战和二战。

