三维打印双相磁性纳米复合支架材料的性能测定*
黄江鸿王大平熊建义*丁文斌王大明刘威尤微朱伟民段莉陈洁琳刘启颂贾兆锋
三维打印双相磁性纳米复合支架材料的性能测定*
黄江鸿1,2,3王大平1,2,3熊建义1,2,3*丁文斌4王大明1,2,3刘威1,2,3尤微1,2,3朱伟民1,2,3段莉1,2,3陈洁琳1,2,3刘启颂1,2,3贾兆锋1,2,3
目的研究制备出一种新型双相磁性纳米复合支架材料(PLGA/Col-I-PLGA/n-HA/Fe2O3),通过各项生物学性能检测,评价并探讨其作为骨组织工程支架的可行性。方法通过低温快速成型方法制备双相磁性纳米复合支架材料(PLGA/Col-I-PLGA/n-HA/Fe2O3),采用电子试验机检测支架材料的抗弯,抗压,弹性模量评价其力学性能,通过电镜观察支架材料超微结构;以介质(乙醇)浸泡法测定支架材料的孔隙率,将支架材料与骨髓间充质干细胞复合共培养,检测其生物相容性。结果双相磁性纳米复合支架材料力学检测结果显示其具有良好的力学性能,电镜观察结果显示上下两层孔径均匀分布,上层软骨相孔径较小,中间连续相良好融合,孔径及孔隙率检测结果显示软骨层支架的孔径为189um,孔隙率86.5%。骨层支架的孔径为364um,孔隙率77.1%,符合双层支架材料的设计要求。双相磁性纳米复合支架材料与骨髓间充质干细胞共培养,结果显示骨髓间充质干细胞的增殖效果很好,能更好的促进分化为目的细胞,说明双相磁性纳米复合支架材料具有良好的生物相容性。结论双相磁性纳米复合支架材料(PLGA/Col-I-PLGA/n-HA/Fe2O3)有很好的力学性能和生物相容性,孔径及孔隙率达到细胞粘附生长的要求,与正常的关节软骨及软骨下骨生理结构更加接近,有望可以更好的修复骨关节炎或者外伤等疾病带来的软骨和软骨下骨损伤。
低温快速成型;3D打印;双相磁性纳米
临床上各种疾病,如关节炎或者外伤等疾病造成等关节软骨损伤,多伴有软骨下骨一并损伤,因此,软骨及软骨下骨共同修复比仅修复软骨的效果要好。骨组织工程中的支架主要为三维立体的多孔形态,并需要满足细胞粘附、细胞间的调节及相互作用,具有一定的力学性能和释放生物活性分子等特点,并可促进种子细胞的诱惑分化和增殖,如形成骨髓间充质干细胞向软骨细胞和成骨细胞分化的微环境,促进骨或软骨生组织形成[1]。双相骨组织工程支架主要原理是由两层不同的支架空三维空间结合,将不同或相同的种子细胞接种于两层不同的支架,病理检查其形成不同骨组织类型。因此,这样的双相骨组织工程支架可以更好的模拟正常骨组织中不同层次的理化性质和生物活性,良好的与软骨下骨契合,以达到良好的固定和修复缺损病灶[2]。
快速成型技术为制造三维支架材料的主要方法,包括熔融沉积、选择性激光烧结、三维打印等,具有制备迅速,数字化可调控材料生产,具有支架商品化潜质及三维打印可调控等优势,目前研究广泛[3]。低温快速成型技术基于结合相分离法,快速成型,操作简便,具有支架成型可控性。低温环境下各材料的生物学活性保持良好,并在打印过程中可三维控制支架材料的行走及空间孔隙率,目前已被广泛应用于骨组织工程支架的制备[4]。本实验中通过低温成型技术制备出一种新型的双相磁性纳米复合支架材料(PLGA/Col-IPLGA/n-HA/Fe2O3),并检测复合材料的各项生物学指标。
1 材料与方法
1.1 主要实验材料、试剂及仪器
聚乳酸-聚羟基乙酸(PLGA),I型胶原(Col-I),纳米羟基磷灰石(n-HA),磁性三氧化二铁(Fe2O3)(深圳欣城生物科技有限公司);低温快速成型仪(中国科学院深圳先进技术研究院),力学试验机CTM4000,(深圳清华大学研究院),电子显微镜(MIRA3TESCAN,深圳清华大学研究院)。1.2PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料的制备方法
1.2.1 软骨相支架溶液配制
向PLGA加入有机溶剂(1,4-二氧六环),混匀,加入Col-I粉末,配成质量比为20%的溶液。震荡15分钟,电磁搅拌12小时,混匀。
1.2.2 骨相支架溶液配制
向PLGA加入有机溶剂(1,4-二氧六环),混匀,按质量比加入n-HA,Fe2O3,配成20%的溶液。震荡15分钟,电磁搅拌12小时,混匀。
1.2.3 PLGA-Col-I/PLGA-n-HA-Fe2O3制备
在低温快速成型仪上,先打印出软骨相PLGA-Col-I,再打印骨相PLGA-n-HA-Fe2O3,-4℃条件下打印,先将配置的溶液转入低温快速成型仪中打印,打印出具有一定间隔的空间平行排列的三维材料初产品,此时具有一定的孔隙,向三维材料的孔隙中加入配制好的生物复合材料溶液,填充,材料表面磨平整理,使加入的复合材料均匀分布,重复以上步骤。
成形后藏室,复合材料中冰融化的空余空间即为磁性纳米多孔人工骨支架材料的初步空间孔隙,真空冷冻干燥,以此去除有机溶剂;风干2天,代有机溶剂升华后,三维复合支架材料的空间孔隙将进一步增大,即得所需的到PLGACol-I/PLGA-n-HA-Fe2O3复合材料(见图1,彩图见插页)。

图1 PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料
1.3 PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料的生物学性能检测
力学性能测试:PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料的拉伸强度、弯曲强度、弯曲模量测试均在抗弯拉伸实验室的三思电子万能试验机CTM4000,用三点弯曲法予以表征,测试指点的跨距为20mm,加载速率为5.00mm/min。
显微结构观察:制备PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料的新鲜断口,喷金处理后,进行断口扫描分析,用捷克泰思肯的场发射扫描电镜,图像为二次电子图像和背散射电子图像,观察分析试样横断面的形态和显微特征。
孔隙率的测定:采用介质(乙醇)浸泡法测定。先测得PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料总体积(V)及质量m1,浸入乙醇,充分填满孔隙,吸去表面乙醇,测出此时支架总质量m2,计算孔隙率:=(m2-m1)/乙醇V。
主要观察指标:PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料的生物力学性能(拉伸强度、弯曲强度、弯曲模量),横断面微观结构,孔隙率。
1.4 PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料的生物相容性研究
取3月龄新西兰大白兔,常规麻醉、消毒备皮,左侧股骨大转子处骨穿,用含有2mL肝素注射器抽取约3mL骨髓。置于10mL离心管,加入PBS液至5mL,1200r/min离心10分钟,弃上清,再加PBS液1000r/min洗涤2次。将沉淀的细胞悬液加入5mL高糖DMEM培养液中(含有10%FBS、1%双抗(青霉素/链霉素)),5%CO2和37℃条件下培养。48小时后换液,每2~3天换液1次,待贴壁生长的细胞集落80%融合时传代(图2,彩图见插页)。取第3代的BMSCs与复合材料复合共培养,观察复合材料的生物相容性。

图2 BMSCs显微镜下形态呈椭圆形、梭形、三角形或不规则多边形(100×),A:P0,B:P1,C:P3
1.4.1 细胞增殖活性检测
采用CCK-8法。A、B两组,每组5个复孔,在细胞培养第1、3、5、7、9天,于每孔中加入CCK-8液50 L,在37℃孵箱中孵育4小时,将各孔液体转移到96孔板中,使各孔内液体量相等,用酶标仪在490nm波长下测其光吸收值(A值),绘制细胞增殖曲线。
1.4.2 立体光学显微镜观察
分A、B两组,A组:PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料与BMSCs复合,B组:单纯的PLGA支架与BMSCs复合,共培养1周后的培养板去盖直接放在立体光学显微镜下放大100倍观察细胞生长情况。
1.4.3 扫描电子显微镜观察
分为A、B两组,A组:PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料与BMSCs复合,B组:单纯的PLGA支架与BMSCs复合,共培养1周后,将两组的材料用PBS清洗2次,2.5%戊二醛4℃固定2小时,乙醇逐级脱水,CO2临界点干燥,喷金,扫描电镜观察细胞在支架上的黏附情况。
1.4.4 PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料与BMSCs复合后成骨及成软骨分化研究
将PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料与BMSCs复合后一周,骨层支架PLGA/n-HA/Fe2O3用成骨诱导培养基继续培养21天,而软骨层支架PLGA/Col-I则用成软骨诱导培养基继续培养21天,检测相关指标。
1.4.4.1 诱导成骨细胞Von Kossa染色
将细胞/支架的复合体的诱导的成骨细胞用4%多聚甲醛固定30分钟,蒸馏水冲洗3次,加入1%硝酸银放置紫外线孵育1小时。蒸馏水漂洗3次,流水冲洗10分钟,加入5%硫代硫酸钠孵育2分钟,蒸馏水漂洗后显微镜下观察。
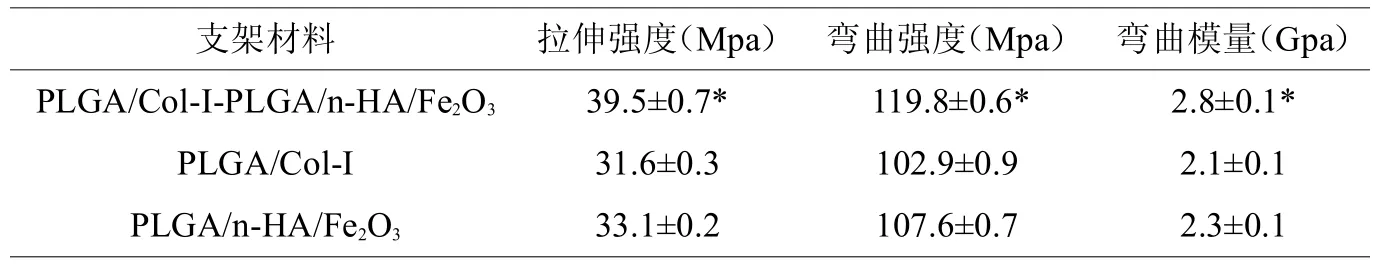
表1 PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料力学性能(±s,n=10)
1.4.4.2 诱导成软骨细胞甲苯胺蓝染色
将细胞/支架的复合体的诱导的成软骨细胞用4%多聚甲醛4℃固定1小时。用蒸馏水漂洗,配置好1%的甲苯胺蓝染液,加入染液染1小时。去除多余染液,用PBS漂洗多余的染液,在显微镜下观察。
1.5 统计学方法
统计学分析:采用SPSS13.0统计软件对实验数据进行统计学分析,数据以(±s)表示,进行方差分析,<0.05为差异有统计学意义。
2 结果
2.1 PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料力学性能(见表1)
通过三点抗弯实验检测材料的力学性能,结果显示双相磁性纳米复合支架材料与单层的支架材料相比具有更好的力学性能。
2.2 PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料的结构性能
复合支架的分上下两层,均为多孔网状结构,上层为软骨相,相对下层骨相孔径较小、稀疏,骨相与软骨相结合紧密,孔径大小差别逐渐过度,分布均匀。电镜观察见上下两层孔径均匀分布,上层软骨相孔径较小,中间连续相良好融合(见图3)。

图3 A:PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料软骨相扫描电镜观(2000×);B:PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料骨相扫描电镜观(2000×);C:PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料骨与软骨相连接处的扫描电镜观(2000×)
2.3 PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料的孔径及孔隙率
双相磁性纳米复合支架材料的孔径及孔隙率检测结果显示软骨层支架的孔径为189um,孔隙率86.5%。骨层支架的孔径为364um,孔隙率77.1%,符合双层支架材料的设计要求。
表2 PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料的孔径及孔隙率(±s,n=10)

表2 PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料的孔径及孔隙率(±s,n=10)
支架材料孔径(um)孔隙率(%)PLGA/Col-I-PLGA/n-HA/Fe2O324382.3±0.6 PLGA/Col-I18986.5±0.2 PLGA/n-HA/Fe2O336477.1±0.9
2.4 PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料的生物相容性
2.4.1 细胞增殖活性检测
CCK-8法检测BMSCs在PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料上面的增殖情况(见图4,彩图见插页)。在实验组和对照组中,细胞增殖无明显差异(>0.05)。
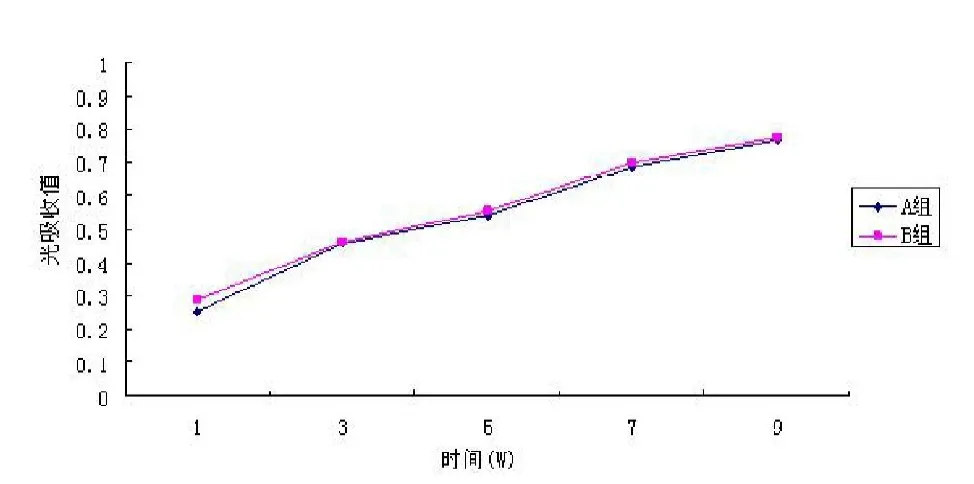
图4 BMSCs在PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料表面的增殖率(A组)与组织培养塑料平板上的细胞增殖率(B组)无明显差别(>0.05)
2.4.2 立体光学显微镜观察
培养1周后观察到A组与双层支架材料复合的BMSCs呈多角形外观,细胞间通过突起相互间接触,随着时间增殖分化良好,并出现规则叠层生长(见图5-A),而B组与单纯的PLGA支架复合的BMSCs呈多角形外观,增殖良好,但是细胞的数量相对较少(见图5-B)。可见双层支架材料具有更好的生物相容性。(图5彩图见插页)

图5 材料与BMSCs共培养1周的光学立体显微镜观(100×),A组:细胞规则排列生长,无杂乱变异生长,细胞增殖良好,数量较多;B组:细胞规则排列生长,无杂乱变异生长,细胞的增殖数量相对较少
2.4.3 扫描电镜观察
扫描电镜结果可见A组:PLGA/Col-I-PLGA/n-HA/Fe2O3复合材料表面孔隙内有大量梭形或多角形细胞贴附、聚集,而B组的PLGA材料表面粘附的细胞数量较少,证实双层支架材料与BMSCs的生物相容性良好(见图6)。

图6 材料与BMSCs共培养一周的扫描电镜观(2000×)。A组:材料表面孔隙内有大量梭形或多角形细胞贴附、聚集;B组:材料表面表面粘附的细胞数量较少
2.4.4 双层支架材料与BMSCs复合后成骨及成软骨分化研究
2.4.4.1 诱导成骨细胞Von Kossa染色
骨层支架与BMSCs复合后诱导BMSCs向成骨细胞转化形成矿化结节,经Von-Kossa染色呈黑色结节(图7,彩图见插页),可见BMSCs与双层支架复合后能向成骨细胞转化。

图7 Von Kossa染色显微镜下观察(100×)A:BMSCs;B:BMSCs诱导成骨细胞形成矿化结节
2.4.4.2 诱导成软骨细胞甲苯胺蓝染色
软骨层支架与BMSCs复合后诱导BMSCs向成软骨细胞转化,诱导的软骨细胞经甲苯胺蓝染色后细胞被染成蓝色(图8,彩图见插页),可见BMSCs与双层支架复合后能向成软骨细胞转化。

图8 甲苯胺蓝染色显微镜下观察(100×)A:BMSCs;B:BMSCs诱导成软骨细胞被染成蓝色
3 讨论
骨与软骨组织工程目前主要包括三个重要组成部分:种子细胞、细胞因子及支架材料,支架材料为细胞载体,为最基本的元素,并要求其各项生物学特性可促进骨与软骨组织的修复。理想的支架材料应包括以下几点:①生物相容性良好,对细胞毒性低;②可控的降解性;③合适的孔隙结构;④力学性能良好,可载荷骨缺损部位的力学负荷;⑤能够备承并协同生长因子发挥促进细胞活性、分化及分泌细胞外基质等特点;⑥与周围组织粘合延续良好,无明显组织排斥反应;但目前尚未研究出满足上述要求的较为满意的支架材料。
PLGA是由聚乳酸(PLA)和聚羟基乙酸(PGA)按照一定比例形成的高分子共聚物,降解性能及生物力学性能良好,体外细胞培养表明其细胞粘附能力良好,且无明显细胞毒性,已被美国FDA批准的可用于人体植入的生物材料,因此本研究我们采用PLGA作为双相复合支架的主体原材料[5-7]。I型胶原(Col-I)在生物体内主要以结缔组织的成分存在。从动物的结缔组织中提取胶原蛋白,并通过合适的方法去除其抗原性物质,来制备成具有合适良好的生物相容性的材料,这种材料具有一定的促进细胞粘附、增殖、降解产物毒性低以及引起的过敏及发热反应小等优点。本研究中,在软骨相的材料中加入Col-I,目的是利用其良好的软骨特性,复合BMSCs诱导成软骨修复软骨缺损部位。纳米羟基磷灰石(n-HA)为典型的生物陶瓷,其理化性质接近人骨组织,为体内骨和齿的主要无机成分,在纳米分子水平,作为生物组织材料,保留了独特的纳米生物活性,目前骨组织工程领域里作为原材料研究广泛。已经证实其骨修复能力良好,并被广泛应用[8,9],在本实验过程中,在骨相的材料中加入n-HA,目的是利用其良好的成骨特性,复合BMSCs填充并诱导缺损部位的成骨诱导分化。磁性纳米铁粒子(Fe2O3),不仅保留作为纳米材料的生物活性,同时可以在恒定磁场下定向聚集和定位,即磁响应性和超顺磁性。在恒定磁场条件下,nFe2O3可通过偶联方式与细胞表面结合,使得通过恒定的磁场进行调控细胞功能具有一定的可行性[10]。Kazunorl[11]认为nFe2O3在恒定的外加磁场条件下具有诱导h-BMSCs分化为成骨细胞、脂肪细胞、软骨细胞的能力,可作为一个可调控的物理因子及方法应用于骨及软骨的修复实验过程中。
孔径和孔隙率是骨与软骨组织工程支架材料的一个重要参数,直接影响到支架材料的力学性能,并与细胞生物相容性有关,与细胞的粘附和增殖有关[12]。生物支架材料不仅要求材料具有100~500um的大孔直径,同时也应包含10~50um的微孔,而对于其孔隙率并无明确的定量标准,目前研究认为一般将材料的孔隙率控制在40%以上,且要求生物支架材料在三维层面上具有良好的贯通性。本实验研究通过综合考虑骨和软骨的力学性能和组织结构的差异,将双相复合支架材料中的软骨层孔隙率设定为83%~87%,孔径150~200um左右;而成骨相中的孔隙率设定在75%~78%,孔径300~400um左右。将制备好的双相生物材料通过电镜观察并验证是否满足参数设定的要求,包括孔径及孔隙率,是否分布均匀,双相复合材料结合处是否逐渐延伸,保证结合处为均一逐渐过渡的过渡层,及是否紧密结合,有无明显界限。以满足与正常组织中的关节软骨和软骨下骨的结构层次相适应。
本实验研究中双相复合磁性纳米支架材料通过低温快速成型技术制备,此方法为3D制造,可以通过计算机控制成型材料的孔径及孔隙率,力学测试表明制备的双层复合材料的生物力学性能可满足骨与软骨组织工程支架材料的要求,且双层复合支架材料的过渡延伸层面在电镜下观察到紧密结合,不易再次裂开。双层复合支架材料与BMSCs共培养的生物相容性研究中,CCK-8法检测发现BMSCs可大量增殖,长势良好,证实此种双相的复合纳米材料生物相容性良好,无明显细胞毒性,对BMSCs的增殖分化有一定的正性作用,光镜和电镜下均观察到BMSCs粘附在双层复合支架上,增殖分化良好,细胞/支架复合21天后通过Von Kossa染色和甲苯胺蓝染色发现BMSCs可以在双层支架材料上向软骨和成骨细胞双向分化。本研究显示双层支架材料可满足正常体内关节软骨和软骨下骨组织的生理结构的差异,后期将进一步进行动物体内实验研究,通过影像学、病理学等方式来动态分析其修复关节软骨和软骨下骨损伤的能力,并对修复的标本进行生物力学、降解性能等方面的检测,探讨其作为骨与软骨组织工程修复骨和软骨缺损支架材料的可能性。
[1]刘明,项舟,裴福兴,等.BMSCs种植双相复合支架修复兔关节软骨及软骨下骨缺损[J].中国修复重建外科杂志,2010,24(1):87-92.
[2]O`Shea TM,Miao X.Bilayered scaffolds for osteochondral tissue engineering[J].Tissue Eng B Rev,2008,14(4):447-464.
[3]张建明,张西正,李瑞欣,等.快速成型方法制备组织工程支架的研究和应用[J].中国组织工程研究,2013,17(8):1435-1440.
[4]Liu YY,Fang SH,HanZZ,et al.Studyon low-temperature deposition manufacturing process parameters of three-dimensional Chitosan scaffold[J].Key Eng Mater,2012,522:97-102.
[5]Yoon SJ,Park KS,Kim MS.Repair of diaphyseal bone defects with calcitriol-loaded PLGA Scaffolds and marrow stromal cells[J].Tissue Eng,2007,13(5):1125-1133.
[6]Kim SS,Park MS,Gwak SJ.Accelerated bonelike apatite growth on Porous Polymer/ceramic composite scaffolds in vitro[J].Tissue Eng,2006,12(10):2997-3006.
[7]Hayakawa T,Mochizuki C,Hara H,et al.In vivo evaluation of composites of PLGA and apatite with two different levels of crystallinity [J].J Mater Sei Mater Med,2010,21(l):251-258.
[8]Zhao J,Lu X,Duan K,et al.Improving mechanical and biological properties of macroporous HA scaffolds through composite coatings[J].Colloids Surf B Biointerfaces,2009,74(l):159-166.
[9]Fabbri P,Bondioli F,Messori M,et al.Porous scaffolds of Polycaprolaetone reinforced with in situ generated hydroxyapatite for bone tissue engineering[J].J Mater sci Mater Med,2010,21(l): 343-351.
[10]Wu Y,Jiang W,Wen X,et al.A novel calcium phosphate ceramicmagnetic nanoparticle composite as potential bone substitute[J]. Biomedical materials(Bristol,England),2010,5(1):1500-1501.
[11]Shimizu K,Ito A,Yoshida T.Bone tissue engineering with human mesenchymal stem cell sheets constructed using magnetite nanoparticles and magnetic force[J].Tissue Engineering,2004,11(9-10):1553-1561.
[12]Ikeda R,Fujioka H,Nagura I,et al.The effect of porosity and mechanical property of a synthetic polymer scaffold on repair of oesteochondral defects[J].Int Orthop,2009,33(3):821-828.
Determination of the three-dimensional magnetic properties of duplex printing nanocomposite scaffold
HuangJianghong 1,2,3,Wang Daping 1,2,3,XiongJianyi 1,2,3,et al.1 NationalKeyOrthopedicDepartment,Shenzhen SecondPeople'sHospital;2ShenzhenTissueEngineeringKey Laboratory;3 ShenzhenDigitalOrthopaedic Engineering Laboratory,Shenzhen GuangDong,518035;4 Department of Orthopedic,Huangshan People's Hospital,Huangshan AnHui,242700,China
Objective Study prepared a novel two-phase magnetic nanocomposite scaffolds(PLGA/Col-I-PLGA/n-HA/ Fe2O3),through various biological performancetesting,evaluationandtoexplorethefeasibility of bonetissue engineering scaffolds.Methods Preparation of two-phase magnetic nanocomposite scaffolds(PLGA/Col-I-PLGA/n-HA/Fe2O3)by cryogenic rapidprototypingmethod,usingelectronic detectionmachinescaffoldflexural,compressive strength,elastic modulus to evaluate the mechanical properties by electron microscopy ultrastructure scaffold;in the medium(ethanol)immersion assay scaffold porosity between the scaffold and bone marrow mesenchymal stem cells co-cultured detect its biocompatibility.Results Duplex magnetic nanocomposite scaffold mechanical test results show it has good mechanical properties,electron microscopy showed uniform pore size distribution of the upper and lower layers,the upper layer of cartilage with smaller pore size,good fusion between successive phase,pore size and porosity of the test results showed cartilage aperture layer scaffold to 189um,a porosity of 86.5%.Aperture bone scaffold layer is 364um,a porosity of 77.1%,in line with the double scaffold design requirements.Duplex between magnetic nano composite scaffold co-cultured with bone marrow mesenchymal stem cells,showed that bone marrow mesenchymal stem cell proliferation effect isverygood,betterable topromote the differentiationofcells for the purposedescribedbiphasic magneticnanocomposite scaffolds have good biocompatibility.Conclusion Duplex magnetic nanocomposite scaffolds(PLGA/Col-I-PLGA/n-HA/Fe2O3)has good mechanical properties and biocompatibility,pore size and pore growth rate of cell adhesion requirements,and normal joint subchondral bone and cartilage physiological structure closer,is expected to be able to better repair osteoarthritis and other diseases caused by trauma or cartilage and subchondral bone damage under.
Lowtemperaturerapid prototyping;3D printing;Duplex magnetic nano
R318
A
10.3969/j.issn.1672-5972.2017.01.003
swgk2016-09-00220
黄江鸿(1982-)男,硕士,副主任技师。研究方向:骨科生物材料。
*[通讯作者]熊建义(1963-)男,硕士,主任医师。研究方向:骨科。
深圳市科技研发资金项目(编号:CXZZ20140813160132596)
1深圳市第二人民医院国家重点骨科;2深圳市组织工程重点实验室;3深圳市数字骨科技术工程实验室,广东深圳518035;4黄山市人民医院骨科,安徽黄山242700

