间溴异丙苯的合成及产率优化
胡 壮,阎 峰,张寒冰,王 政,毕 寒,卓桢成,关 瑾
间溴异丙苯的合成及产率优化
胡 壮,阎 峰,张寒冰,王 政,毕 寒,卓桢成,关 瑾
(沈阳化工大学 应用化学学院,辽宁 沈阳 110142)
以4-异丙基苯胺为原料,与醋酸酐发生氨基的酰化反应,所得产物与液溴进行邻位取代,再经酸性条件下的水解后进行重氮化-去氨基还原反应合成间溴异丙苯,并且通过正交试验探究了氧化溴化法和次磷酸还原法的反应条件,找到最合适反应温度和最佳投料比,总收率为77.8%。产物结构用IR,1HNMR进行了表征。
间溴异丙苯;溴化反应;重氮化-去氨基反应
间溴异丙苯是有机合成中的重要中间体,在香料、医药等领域都有着十分广泛的应用,尤其在金属有机合成中具有重要地位。可通过异丙苯直接溴化[1]获得,但由于异丙基的供电子效应,该方法副产物太多导致产率极低;也可通过间氨基异丙苯或间溴苯乙酮法[2]制备,由于反应条件较为苛刻,污染严重等缺陷,未能实现大批量生产;Sylvie Concalves-Contal等[3]曾以4-异丙基苯胺为原料,经酰胺化[4]、溴化、重氮化-去氨基反应后[5-7]获得目标产物间溴异丙苯,但两步反应的收率分别为75%和77%,总收率仅有57%,本文在此基础上加以改进,以氧化溴化法和次磷酸还原重氮盐来提高间溴异丙苯的产率,反应条件温和,操作简单,并通过正交试验找到最佳反应温度和投料比。具体合成路线如图1。
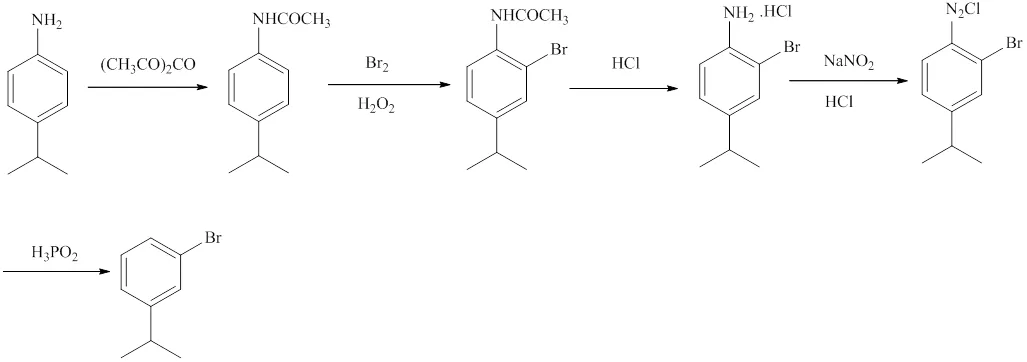
图1 间溴异丙苯的合成路线
为避免4-异丙基苯胺的多溴取代,需进行N-酰基化反应获得4-异丙基乙酰苯胺,常用的乙酰化试剂有乙酰氯、乙酸酐、冰乙酸等。乙酰氯反应较剧烈且产生的氯化氢需用缚酸剂吸收,冰乙酸法转化率较低,所以最终选用乙酸酐做酰化试剂。溴化反应中溴分子充当溴化剂和氧化剂双重角色,自身被还原为溴化氢[8],所以在反应中滴加H2O2能有效提高Br2的原子利用率[9-11]。重氮化反应一般是在低温且用酸过量的亚硝酸盐的条件下进行[12,13],还原过程常选用乙醇或次磷酸进行,后者产率相对较高。
1 实验部分
1.1 试剂和仪器
4-异丙基苯胺,萨恩化学技术(上海)有限公司;次磷酸,山东西亚化学有限公司;乙酸酐,天津市凯信化学工业有限公司;乙醇、乙酸、盐酸等试剂均为天津博迪化工有限公司提供。
傅立叶变换红外光谱仪(美国Niaelet公司);Bruker300型核磁共振仪,DMSO作溶剂;X4型数字熔点测定仪。
1.2 合成方法
1.2.1 对异丙基乙酰苯胺的合成
量取6.8 mL对异丙基苯胺加入到三口瓶中,用30 mL冰乙酸溶解。在冷水浴下滴加5.7 mL乙酸酐,保持搅拌,并保持温度不超过30 ℃。滴完后继续搅拌30 min。然后倒入200 mL水中,析出固体。抽滤,得到白色固体,干燥。
1.2.2 4-异丙基-2-Br-乙酰苯胺的合成
称取8.86 g对异丙基乙酰苯胺加入到三口瓶中,用30 mL冰乙酸溶解。滴加12 g (40%)液溴的冰乙酸溶液,保持搅拌,控制温度在40~50 ℃。滴完后继续搅拌30 min,升温至60 ℃。滴加12 g (30%)H2O2溶液,继续搅拌30 min,冷却后倒入200 mL水中,析出固体。用20% NaHSO3溶液洗去过量的溴,直至使KI淀粉试纸不变色为止。抽滤,经乙醇重结晶,干燥后得白色晶体。
1.2.3 水解反应
称取12.81 g 4-异丙基-2-溴乙酰苯胺加入到三口瓶中,并加入30 mL乙醇。升温至回流,加入7.4 g(6.3 mL)37%盐酸。 继续回流反应3 h。冷却至室温,抽滤,固体用乙酸乙酯洗涤,干燥,得白色细小晶体。
1.2.4 间溴异丙苯的合成
称取12.53 g 4-异丙基-2-溴苯胺盐酸盐加入到三口瓶中,并加入50 mL水和10 g(8.4 mL)37%盐酸。5 ℃以下加入3.6 g亚硝酸钠溶于10 mL水的溶液,保持温度不超过10 ℃。一次性加入33 g 50%次磷酸溶液,升温至50 ℃,继续反应1 h。冷却至室温,分出油层,无水硫酸镁干燥。减压蒸馏收集88 ℃/1.25 kPa的馏分。经柱层析后取样进行IR、1HNMR表征。
2 结果与讨论
2.1 红外光谱分析
从图2中看出:1 594.6 cm-1、1 568.2 cm-1、1 478.4 cm-1、1 459.8 cm-1为苯环碳骨架振动吸收峰;3 061.3 cm-1为苯环的C-H伸缩振动;781.6 cm-1、694.6 cm-1为1,3-二取代苯环的C-H弯曲振动吸收峰;2 962.5 cm-1和2 870.9 cm-1的峰为甲基的C-H伸缩振动;1 384.3 cm-1、1 364.2 cm-1为异丙基的C-H弯曲振动;663.2 cm-1为C-Br伸缩振动,说明红外光谱呈现的官能团符合间溴异丙苯的结构。

图2 间溴异丙苯的红外光谱图
2.2 核磁共振氢谱分析
1HNMR (500 MHz, DMSO): δ 7.42(1H, s, Ar -H), δ7.36 (1H, t, Ar-H), δ7.25 (2H, t, Ar-H); δ 2.89 (1H,m, C-H),1.1 (6H, d, , 2CH3)。得每组氢的位置与计算所得的位置接近(2.5 ppm的峰为溶剂氘代DMSO残余质子峰)。

图3 间溴异丙苯的核磁共振氢谱图
2.3 氧化溴化反应条件的探究
以原料和溴的摩尔比、原料和过氧化氢的摩尔比、加溴时的温度(1)、加过氧化氢时的温度(2)为影响因素,每个因素选择三个水平,设计正交试验,如表2.1所示。

表2.1 氧化溴化正交试验表
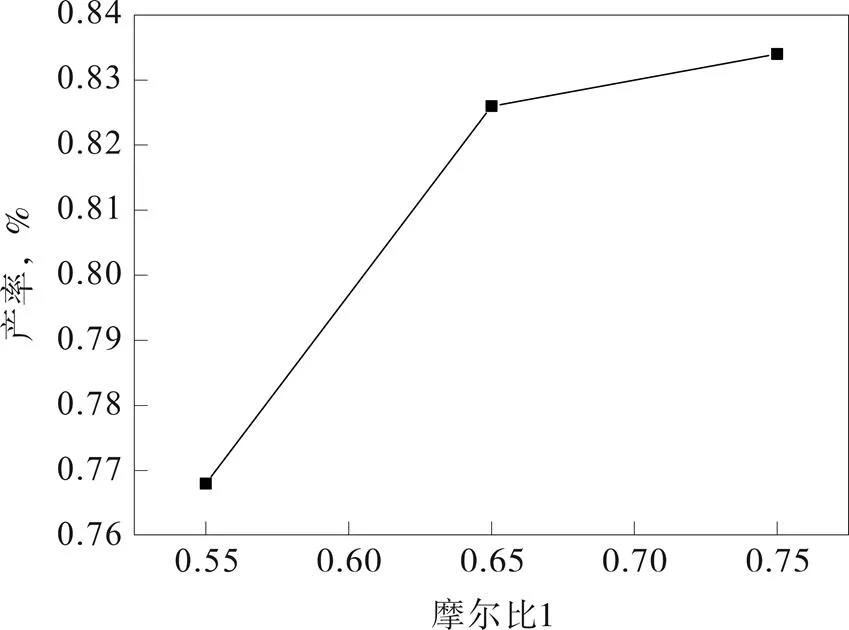
图4 n溴/n原料对收率的影响
由图4可知,当溴与原料的摩尔比的增大,产物的收率不断增加,当摩尔比大于0.65之后,产物收率上升的趋势降低;由图5可知,随着H2O2与原料的摩尔比的增大,产物的产率也不断增加,同样当摩尔比大于2之后,产物收率上升趋势也降低。说明过多的增加投入量并不能使反应收率成比例增加,而且某种反应物的投入量过大也会增加副反应发生,所以为了避免原料浪费,采用图像中拐点处比例为最佳投料比。
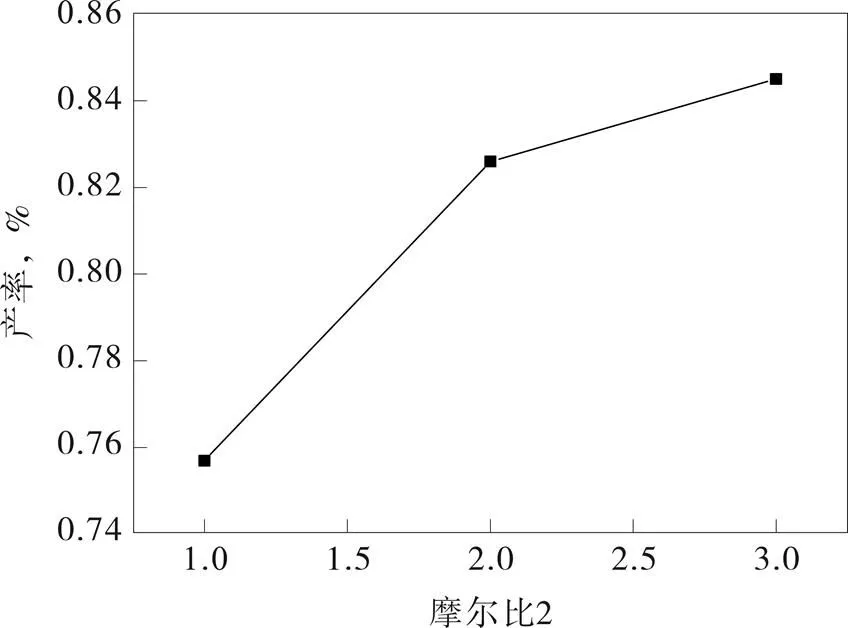
图5 nH2O2 /n原料对收率的影响
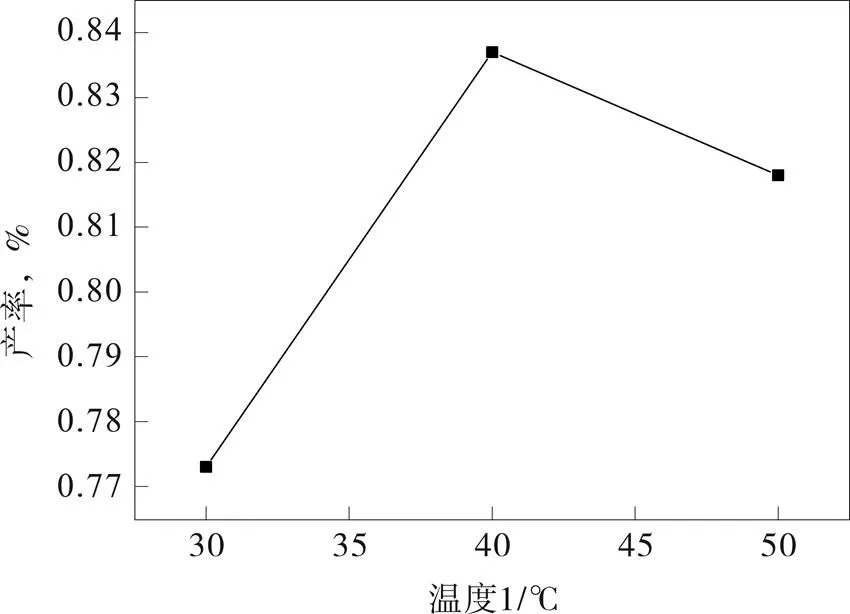
图6 T1温度对收率的影响
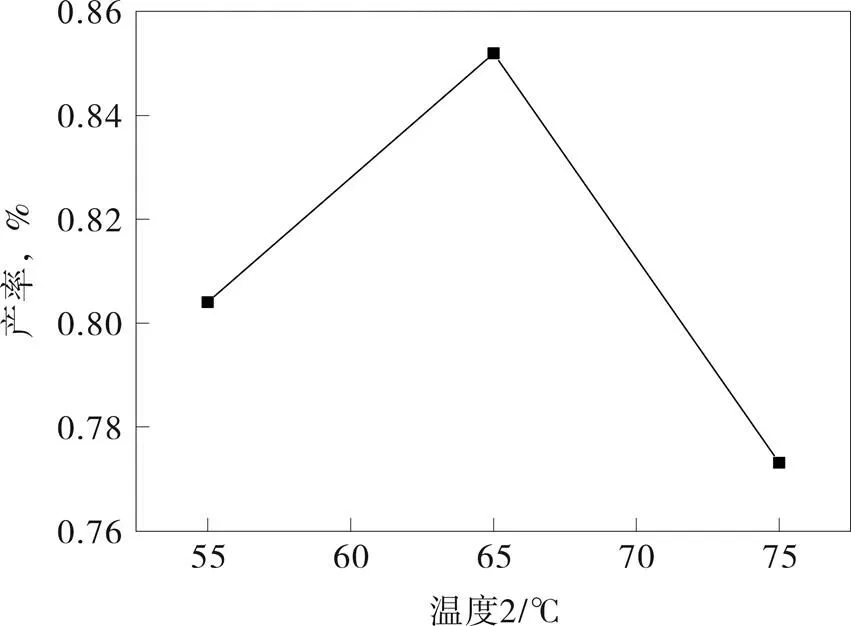
图7 T2温度对收率的影响
由图6可知,反应温度1为40 ℃时,产物收率达到最大值,随着温度升高,分子运动性加强,温度过高会加快溴的挥发导致收率降低;由图7可知,当反应温度2为65 ℃时,产品的收率有最大值,因为过高的温度会导致过氧化氢分解,造成氧化效率降低。
为了验证正交试验的准确性,以溴/原料为0.65:1;H2O2/原料为2:1;控制滴加液溴温度在40 ℃,滴加过氧化氢时温度为65 ℃为条件做了三组验证实验,结果如表2.2所示。

表2.2 氧化溴化验证实验表
理论产量为12.81 g,平均收率为91.7%。
2.4 次磷酸还原反应条件的探究
以原料和盐酸的摩尔比、原料和次磷酸的摩尔比、重氮化反应的温度(1)、去氨基还原反应的温度(2)为影响因素,设计正交试验如表2.3,探究4个因素对间溴异丙苯产率的影响。
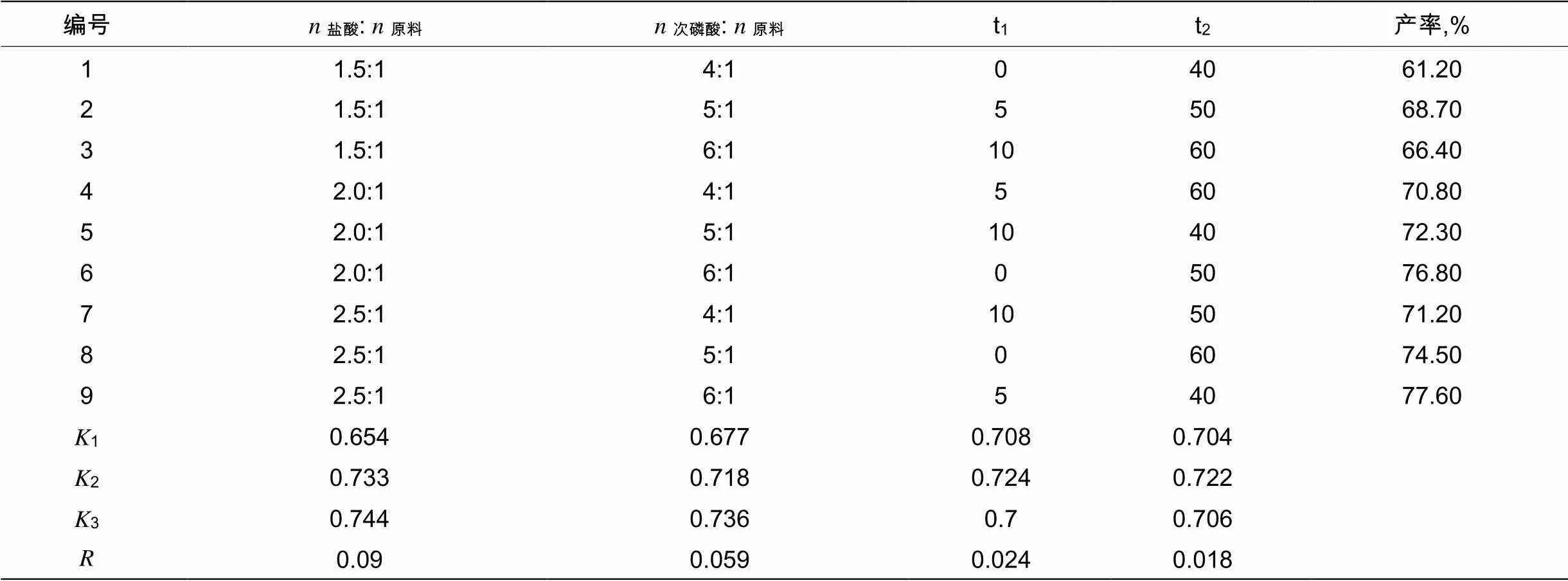
表2.3 次磷酸还原法正交试验表

图8 n盐酸/ n原料对产率的影响
由图8可知,当盐酸与原料的摩尔比增加时,产物的产率不断增加,当摩尔比大于2时,产物收率上升趋势降低;由图9可知,当次磷酸与原料的摩尔比增加时,产物的产率也不断增加,当摩尔比大于5时,产物收率上升趋势也降低;说明过多加入盐酸和次磷酸并不能使反应收率成正比增加,为了避免原料浪费,采用图像中拐点处比例为最佳投料比。
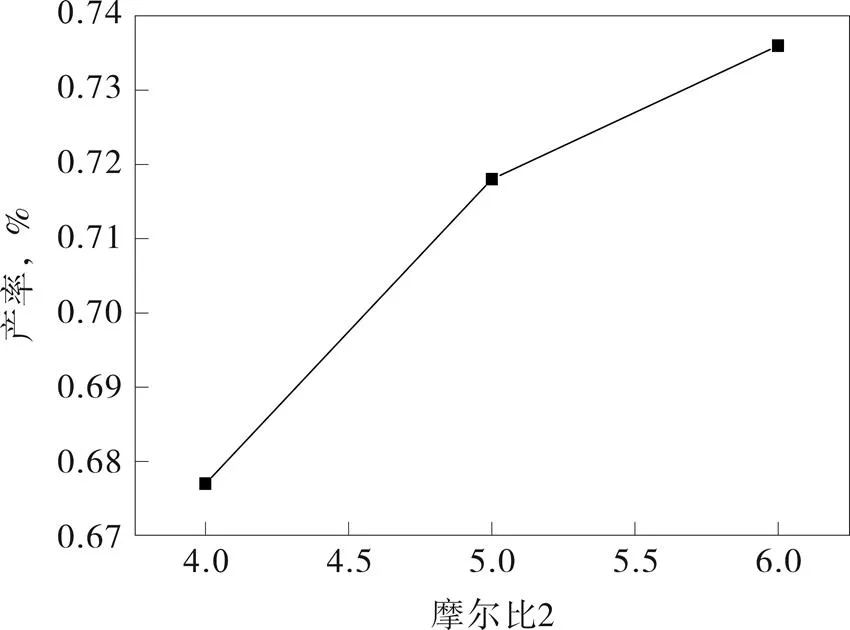
图9 n次氯酸/n原料对产率的影响
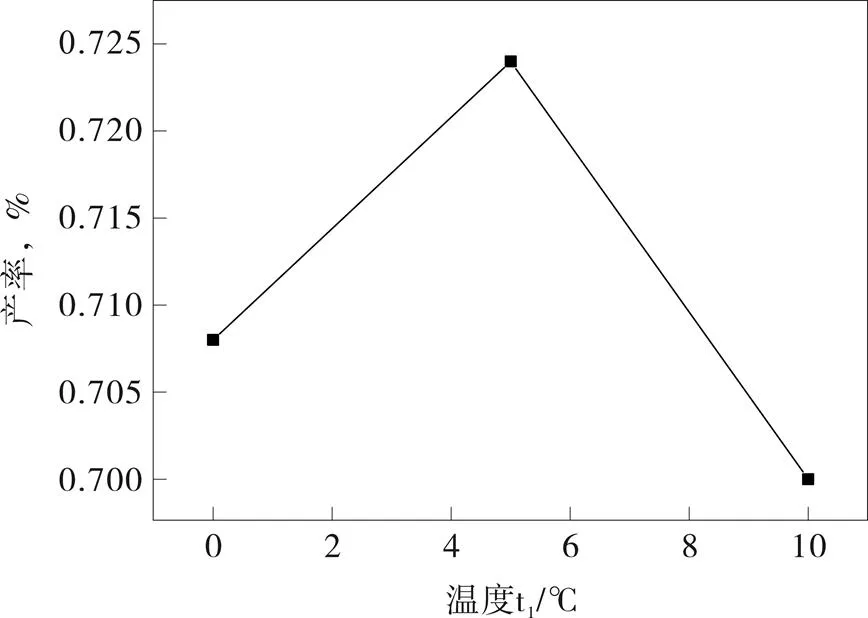
图10 t1温度对产率的影响
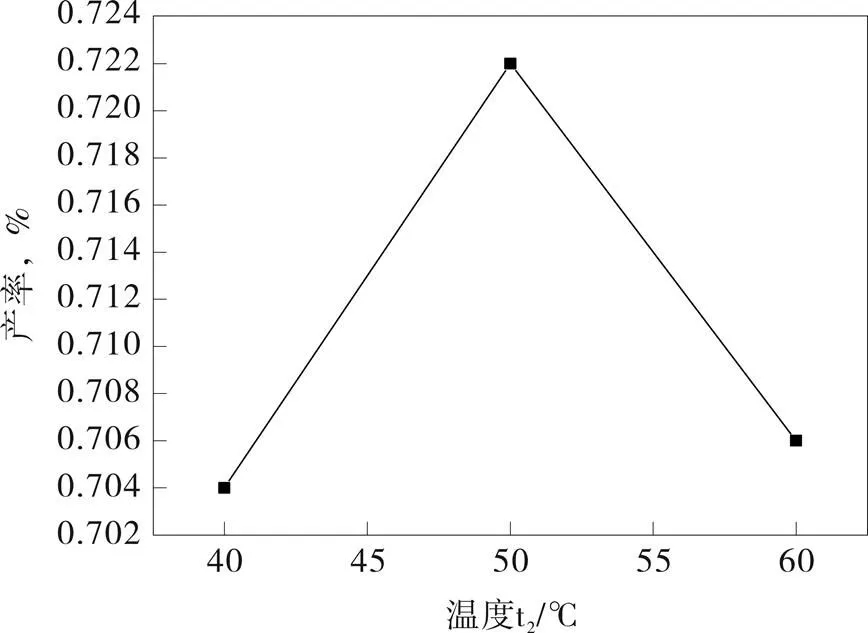
图11 t2温度对产率的影响
由于重氮盐的稳定性较差,温度过高会导致产物分解,由图7可知,反应温度1为5 ℃时,产物收率达到最大值;次磷酸的还原反应中,温度低时反应活性不够导致收率不高,温度过高有可能导致导致副反应增加,由图8可知,当反应温度2为50 ℃时,产物的收率有最大值。
为了验证正交试验的准确性,以盐酸/原料为2:1;次磷酸/原料为5:1;控制重氮化反应温度5 ℃,设定加入次磷酸时的温度为50 ℃为条件进行了3组验证实验,结果如表2.4所示:
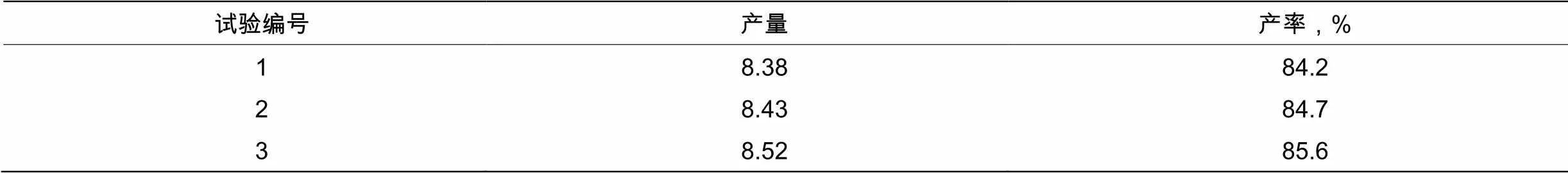
表2.4 次磷酸还原验证实验表
理论产量为9.95 g,平均收率为84.8%。
3 结 论
以4-异丙基苯胺为原料,经乙酰化、溴化、重氮化和次磷酸还原反应所得生成物经IR、1HNMR谱图鉴定,再结合颜色、气味、沸点等物理特征,确定产品为间溴异丙苯。氧化溴化正交试验结果:原料与溴的最佳摩尔比为1:0.65;原料与过氧化氢的最佳摩尔比为1:2;加溴时的最佳温度为40 ℃;加过氧化氢时的最佳温度为65 ℃。次磷酸还原重氮盐正交试验结果:原料与盐酸的最佳摩尔比为1:2;原料与次磷酸的最佳摩尔比为1:5;重氮化反应的最佳温度为5 ℃;去氨基还原反应的最佳温度为50 ℃。反应总收率达到77.8%。
[1]Gruzdev M S, Virzum L V, Krylov E N. Bromination of alkylbenzenes in 1-butyl-3-methylimidazolium bromide and its dibromide complex[J]. Russian Journal of General Chemistry, 2010, 80(2):263-267.
[2]Reetz M T, Kyung S H. Direct Geminal Dimethylation of Aromatic Aldehydes with Dichlorodimethyltitanium[J]. European Journal of Inorganic Chemistry, 1987, 120(1):123-123.
[3]Goncalves-Contal S, Gremaud L, Palais L, et al. Copper-Catalyzed Enantioselective Conjugate Addition to α,β-Unsaturated Aldehydes with Various Organometallic Reagents[J]. Synthesis, 2016, 48(19): 3301-3308.
[4]王雅珍, 祁秀春, 郭晓振. 2—甲基乙酰苯胺合成工艺的优化[J]. 江苏理工学院学报, 2011, 17(8):24-27.
[5]李光明, 刘有智, 张巧玲,等. 重氮盐水解制备愈创木酚的实验工艺研究[J]. 化工中间体, 2010(3):46-50.
[6]李淑辉, 刘传玉, 张智,等. 重氮化法合成9,9-二苯基芴[J]. 化学与粘合, 2013, 35(4):43-45.
[7]张清玉. 重氮化-水解法制备间甲酚的合成工艺研究[J]. 杭州化工, 2015, 45(2):23-26.
[8]居洁, 高建荣, 李郁锦. 有机化合物的氧化溴化研究进展[J]. 应用化学, 2010, 27(6):621-625.
[9]Khan A T, Goswami P, Choudhury L H. A Mild and Environmentally Acceptable Synthetic Protocol for Chemoselective α-Bromination of β-Keto Esters and 1,3-Diketones.[J]. ChemInform, 2006, 47(30): 2751-2754.
[10]Narender N, Srinivasu P, Kulkarni S J, et al. ChemInform Abstract: Liquid Phase Regioselective Bromination of Aromatic Compounds over HZSM-5 Catalyst.[J]. Synthetic Communications, 2000, 31(20): 3669- 3675.
[11]张国富, 王涌, 丁成荣,等. 芳香化合物氧化溴化研究进展[J]. 有机化学, 2011, 31(6):804-813.
[12]李淑辉, 刘传玉, 张智,等. 重氮化法合成9,9-二苯基芴[J]. 化学与粘合, 2013, 35(4):43-45.
[13]李怀刚. 芳香伯胺重氮化的特殊反应条件[J]. 淮海工学院学报:自然科学版, 2000(S1):4-5.
Synthesis and Characterization of Meta-Br-Cumene
(College of Applied Chemistry, Shengyang University of Chemical Technology, Liaoning Shengyang 110142, China)
The product whichprepared from 4-isopropylaniline and acetic anhydride by the acylation,reacted with liquid bromine by ortho substitution to synthesize meta-Br-cumene via hydrolysis under acid condition,diazotization and deamination reaction. Orthogonal experiment was usedto explore the best reaction conditions of oxidation bromination and reduction reaction by hypophosphorous acid. Andsuitable reaction temperature and the best feed ratio were determined. Under the best conditions, the overall yield can reach to 77.8%.At last, the product wascharacterized by IR and1HNMR spectrum.
meta-Br-cumene; bromide reaction; diazotization and deamination reaction
辽宁省精细化工协同创新中心协同创新团队资助项目,项目号:00005
2016-11-28
胡壮(1991-),男,硕士研究生,辽宁锦州人,2017年毕业于沈阳化工大学化学专业,研究方向:精细化学品的合成。
O 625.21
A
1004-0935(20167)01-0011-05

