栀子、连翘等中药配方颗粒体外肝细胞毒性研究*
任艳青 李葆林 田宇柔 牛丽颖 甄亚钦 王鑫国(石家庄 050091)
河北中医学院 河北省中药配方颗粒工程技术研究中心
栀子、连翘等中药配方颗粒体外肝细胞毒性研究*
任艳青 李葆林 田宇柔 牛丽颖 甄亚钦 王鑫国(石家庄 050091)
河北中医学院 河北省中药配方颗粒工程技术研究中心
目的:对栀子、连翘、大黄、续断、首乌藤、麻黄、淫羊藿、丹参、地黄、陈皮10种中药配方颗粒的体外肝细胞毒性进行研究评价。方法:以人正常肝细胞LO2为研究对象,设定一系列浓度梯度,MTT法观察不同浓度配方颗粒对LO2细胞的细胞毒作用;Hoechst33258荧光染色法观察细胞核形态。结果:100、1 000mg/L栀子配方颗粒对LO2细胞呈现明显毒性作用(P<0.05或P<0.01),荧光染色可见明显的核荧光强度增强、固缩等凋亡表现;连翘等其他9种配方颗粒在0.001~1 000mg/L范围内,对LO2细胞无明显毒性作用(P>0.05),也未观察到明显的细胞核形态学改变。结论:本研究以中药配方颗粒作为体外实验的载体,对栀子、连翘等10种常用中药配方颗粒的早期肝毒性进行了评价,提示栀子配方颗粒若在较大剂量下使用,可能会存在明显的肝脏毒性,其他9种中药配方颗粒对人正常肝细胞LO2无明显毒性,为上述中药配方颗粒的临床应用提供了参考。
中药配方颗粒;栀子;连翘;大黄;续断;首乌藤;麻黄;肝细胞毒性;安全性评价;LO2细胞
中药配方颗粒是在中医理论指导下,采用现代科技手段将传统中药饮片按一定的生产工艺制成的提取物与适当的辅料或药材细粉制成的供临床调剂使用的粉状或颗粒状产品。[1]目前关于中药配方颗粒的研究多集中在化学成分分析、临床应用、工艺和药效学等方面,研究最少的是毒性和临床安全性,[2]对中药配方颗粒的安全性进行评价是配方颗粒研究中亟待解决的问题,中药配方颗粒体外肝细胞毒性相关研究尚未见报道,本研究以中药配方颗粒为载体,利用MTT、荧光染色技术,观察了栀子、连翘、大黄、首乌藤、续断、麻黄、淫羊藿、丹参、地黄、陈皮10种常用中药配方颗粒对体外培养的人正常肝细胞LO2细胞毒性的影响,为上述药物的临床安全应用提供指导。
1 材料与方法
1.1 试验药物 栀子10g饮片/g配方颗粒,栀子苷含量126.9mg/g(每1g配方颗粒相当于临床10g中药饮片使用量,经高效液相检测,每1g配方颗粒中栀子苷含量为126.9mg),产品批号14081811;连翘14.3g饮片/g配方颗粒,连翘苷含量15.5mg/g,产品批号14090711;大黄2.4g饮片/g配方颗粒,芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚含量之和为8.9mg/g,产品批号14121811;续断9.1g饮片/g配方颗粒,川续断皂苷VI含量67.1mg/g,产品批号15010411;首乌藤18.8g饮片/g配方颗粒,1,2,3,5,4'-四羟基二苯乙烯-2-O-β-D-葡萄糖苷含量40.3mg/g,产品批号15012811;麻黄10g饮片/g配方颗粒,盐酸麻黄碱含量24.9mg/g,产品批号14082811;淫羊藿20g饮片/g配方颗粒,淫羊藿苷含量42.9mg/g,产品批号14100921;丹参5.6g饮片/g配方颗粒,丹酚酸B含量24.5mg/g,产品批号14081411;地黄5g饮片/g配方颗粒,梓醇含量18.8mg/g,产品批号14060911;陈皮6g饮片/g配方颗粒,橙皮苷含量6.7mg/g,产品批号14122121,以上配方颗粒均由石家庄神威药业集团有限公司提供。
1.2 细胞 人正常肝细胞株LO2,购于中国医学科学院肿瘤细胞库。
1.3 试剂 高糖DMEM、胎牛血清(均购自美国Gibco公司);四甲基偶氮唑蓝(MTT)、二甲基亚砜(DMSO)(均购自美国Amresco公司);Hoechst33258(美国ThermoFisherScientific公司)。
1.4 仪器MCO-15ACCO2培养箱(日本SANYO);超净工作台(力康生物医疗科技控股有限公司);TGL-16台式高速冷冻离心机(长沙湘仪离心机仪器有限公司);DMI3000B倒置荧光显微镜(德国Leica);MultiskanFC酶标仪(美国ThermoFisherScientific公司)。
1.5 方法
1.5.1 细胞培养:快速将冻存的LO2细胞置于 37 ℃水浴复苏,复苏后800r/min离心5min,吸去上清加入5mL含 15%胎牛血清的高糖DMEM培养基,转入培养瓶中培养。待细胞生长融合至80%汇合时即可进行传代:弃旧培养基,1×PBS清洗细胞3次,0.25%胰酶消化,轻轻吹打细胞,待细胞分散后加入完全高糖DMEM培养基终止消化,1︰3传代,细胞在37℃,5%CO2培养箱中培养。
1.5.2 药物配制:将连翘、大黄等10种中药配方颗粒直接溶解于无血清高糖DMEM中,溶解性均良好,0.22μm微孔滤膜过滤除菌,依次稀释至工作浓度1 000、100、10、1、0.1、0.01、0.001mg/L。
1.5.3 细胞毒性检测:生长状态良好的LO2细胞消化后制备单细胞悬液,调整细胞密度为1×105个/mL,接种到96孔板,每孔100μL,细胞培养24h后换用无血清高糖DMEM培养基继续培养24h使细胞饥饿,分裂活动停止,吸弃无血清培养基,每孔加入相应的药物孵育24h,药物作用时间结束后吸弃含有药物的培养基,每孔加入新鲜无血清高糖DMEM培养基100μL、MTT20μL,置于培养箱中继续培养4h,小心吸除上清,每孔加入100μLDMSO将结晶溶解,微量振荡仪振荡10min,使结晶充分溶解,酶标分析仪检测各孔于492nm处的OD值。
1.5.4 细胞形态学染色观察:参照文献[3]方法,LO2细胞接种于96 孔培养板,每孔5 000个细胞,同步化24h,每种配方颗粒选定1、1 000mg/L两个作用浓度,孵育细胞24h后弃掉含药培养基,PBS冲洗2次,4%多聚甲醛固定细胞10min,吸弃多聚甲醛,PBS再次漂洗3次,每孔加入终浓度为5μg/mL的Hoechst33258 染液100μL,室温避光孵育10min,PBS轻轻漂洗2次,倒置荧光显微镜下观察荧光并拍照。
2 结果
2.1 栀子、连翘等10种中药配方颗粒的LO2细胞毒作用 与空白对照组相比,0.01、0.1mg/L栀子配方颗粒可明显促进LO2细胞增殖(P<0.05或P<0.01),但100、1 000mg/L栀子配方颗粒孵育细胞,OD值明显下降,呈现出明显的毒性作用(P<0.05或P<0.01);连翘、大黄、续断、首乌藤、麻黄、淫羊藿、丹参、地黄、陈皮9种配方颗粒在0.001~1 000mg/L范围内对培养的LO2细胞均无明显毒性作用(P>0.05),1、10、100mg/L大黄配方颗粒、100、1 000mg/L续断配方颗粒,1 000mg/L淫羊藿配方颗粒,10、100、1 000mg/L丹参配方颗粒孵育细胞,OD值显著上升,体现出了明显的促LO2细胞增殖作用(P<0.05)。详见表1。
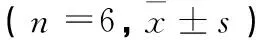
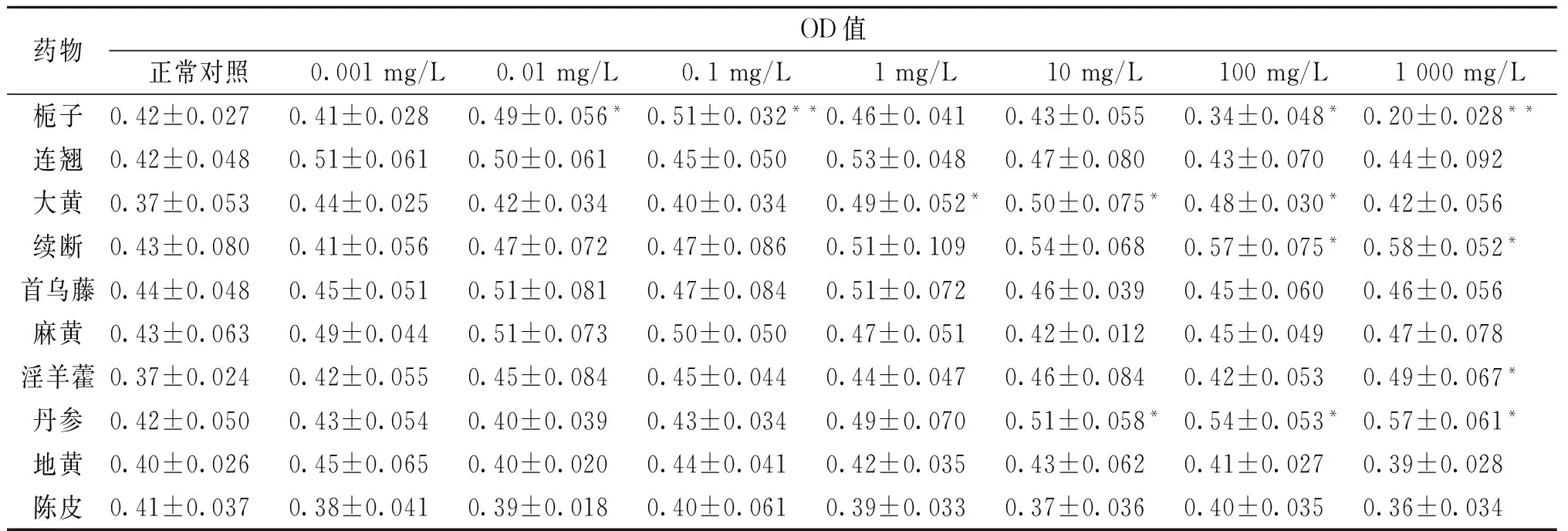
药物OD值正常对照0.001mg/L0.01mg/L0.1mg/L1mg/L10mg/L100mg/L1000mg/L栀子0.42±0.0270.41±0.0280.49±0.056*0.51±0.032**0.46±0.0410.43±0.0550.34±0.048*0.20±0.028**连翘0.42±0.0480.51±0.0610.50±0.0610.45±0.0500.53±0.0480.47±0.0800.43±0.0700.44±0.092大黄0.37±0.0530.44±0.0250.42±0.0340.40±0.0340.49±0.052*0.50±0.075*0.48±0.030*0.42±0.056续断0.43±0.0800.41±0.0560.47±0.0720.47±0.0860.51±0.1090.54±0.0680.57±0.075*0.58±0.052*首乌藤0.44±0.0480.45±0.0510.51±0.0810.47±0.0840.51±0.0720.46±0.0390.45±0.0600.46±0.056麻黄0.43±0.0630.49±0.0440.51±0.0730.50±0.0500.47±0.0510.42±0.0120.45±0.0490.47±0.078淫羊藿0.37±0.0240.42±0.0550.45±0.0840.45±0.0440.44±0.0470.46±0.0840.42±0.0530.49±0.067*丹参0.42±0.0500.43±0.0540.40±0.0390.43±0.0340.49±0.0700.51±0.058*0.54±0.053*0.57±0.061*地黄0.40±0.0260.45±0.0650.40±0.0200.44±0.0410.42±0.0350.43±0.0620.41±0.0270.39±0.028陈皮0.41±0.0370.38±0.0410.39±0.0180.40±0.0610.39±0.0330.37±0.0360.40±0.0350.36±0.034
注:与正常对照组比较,*P< 0.05,**P< 0.01
2.2 连翘、大黄等10种中药配方颗粒对细胞核形态的影响 显微镜下观察可见1 000mg/L栀子配方颗粒组细胞核浓染,并呈现出明显的核固缩;其余各给药组细胞与正常对照组细胞相比,细胞核形态无明显差异,均未观察到明显的凋亡特征,细胞呈均匀淡染的蓝色荧光,核形态完好,详见图1。
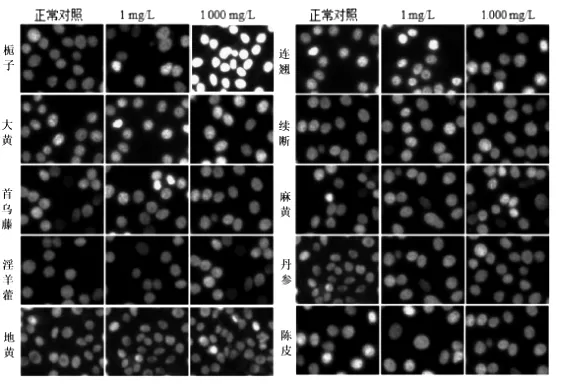
图1 10种配方颗粒Hoechst 33258染色观察(×200)
3 讨论
肝脏是药物产生毒性的重要靶器官,随着中药临床的广泛应用以及近年来中药毒理学研究的不断深入,中药导致肝损伤的报道逐渐增多,越来越引起人们的重视,[4-5]中药致肝毒性损伤已成为令人关注的热点问题,[6]药物的肝细胞毒性评价在早期毒理学评价中起着至关重要的作用。[7]中药配方颗粒是利用先进的生产技术和现代分析测试方法对中医传统用药方式所进行的一次变革,是对传统中药饮片的继承和创新,它将推动我国中药研究和生产的发展。建立中药配方颗粒质量控制标准,解决中药配方颗粒最基本的真伪鉴别、质量优劣及安全性评价等问题是中药配方颗粒行业发展和国际化的当务之急,[8-9]中药配方颗粒安全性的研究目前尚缺乏系统的研究资料,中药配方颗粒体外肝细胞毒性相关研究尚未见报道,对中药配方颗粒进行早期肝细胞毒性评价,是中药配方颗粒研究中急需解决的问题。
近年来体外肝细胞在药物的早期安全性评价中逐渐成为通用的肝毒性评价体外试验工具,并广泛应用于药物细胞毒性的早期研究。[7]药物对细胞毒性的评价可以从细胞生长和增殖活性、细胞形态学、细胞结构的损伤、细胞凋亡、细胞周期、细胞代谢功能和细胞的转运功能等多个方面进行,[10-11]人正常肝细胞LO2目前已成为研究药物肝毒性的重要细胞模型,[12]细胞水平的毒性筛选可快捷迅速的发现有潜在毒性的药物,所以在中药配方颗粒肝细胞毒性研究中,笔者采用体外实验方法进行筛选,以MTT、细胞核荧光染色为手段,为药物安全性评价提供先期的实验依据。在MTT筛选中,为充分暴露其毒性反应,实验中每种受试物的浓度涵盖从较低的药理学剂量到毒理学剂量,研究发现,连翘、大黄、续断、首乌藤、麻黄、淫羊藿、丹参、地黄、陈皮9种常用中药配方颗粒在0.001~1 000 mg/L范围内对培养的LO2细胞均无明显毒性作用,荧光染色也未观察到细胞核受损后所发生的核固缩等典型的凋亡形态特征。实验中笔者还发现,栀子配方颗粒0.01、0.1 mg/L,大黄配方颗粒1、10、100 mg/L,续断配方颗粒100、1 000 mg/L,淫羊藿配方颗粒1 000 mg/L,丹参配方颗粒10、100、1 000 mg/L可促进LO2细胞增殖,提示上述中药配方颗粒可能对肝细胞具有一定的保护作用,但还有待进一步的研究,另外,实验中还发现100、1 000 mg/L栀子配方颗粒孵育细胞,细胞毒性作用明显,荧光染色也观察到了核荧光强度增强、固缩等凋亡的典型特征,提示栀子配方颗粒若在较大剂量下使用,可能会存在明显的肝脏毒性,其导致肝毒性的直接物质基础及毒作用机制课题组目前正在进行深入的研究。综上所述,本研究从体外细胞水平,采用细胞毒理学方法,探讨了多种配方颗粒的体外肝细胞毒性,本研究为中药配方颗粒的安全性评价提供了参考资料,并可为临床安全应用提供参考。
[1]李松林,宋景政,徐宏喜.中药配方颗粒研究浅析[J].中草药,2009,40(增刊):1-7
[2]崔景朝,赵自明.中药配方颗粒研究进展(Ⅰ)—文献综合分析[J].中国实验方剂学杂志,2011,17(3): 235-238
[3]张丹,王玉霞,王威,等.Ghrelin对棕榈酸诱导的大鼠主动脉内皮细胞凋亡的影响[J].中国动脉硬化杂志,2011,19(9):747-750
[4]陈莹蓉,杨水新.中药肝毒性及配伍减毒研究进展[J].浙江中医杂志,2012,47(7):536-538
[5]谢丽华,樊星,李泽君,等.转录组学技术在中药肝毒性研究中的应用[J].中草药,2015,46(10):1 536-1 541
[6]孙蓉,杨倩,黄伟,等.肝功能相关指标在中药肝毒性损伤中作用与毒性相关程度分析[J].中药药理与临床,2008, 24(6):82-84
[7]刘利波,陈伟,龙隆,等.基于高内涵分析技术的新型PPARα/γ双重激动剂C333H和P633H的肝细胞毒性初步研究[J].军事医学,2011,35(12):928-932
[8]陈培胜,朱月信.中药配方颗粒行业标准研究思路[J].中医杂志,2012,53(6):469-472
[9]涂瑶生,毕晓黎,罗文汇.中药配方颗粒的质量控制研究[J].世界科学技术(中医药现代化),2011,13(1):41-46
[10]ZhangL,MuX,FuJ,etal.Invitrocytotoxicityassaywithselectedchemicalsusinghumancellstopredicttarget-organtoxicityofliverandkidney[J].ToxicolInVitro,2007, 21(4):734-740
[11]LiW,ChoyDF,LamMS,etal.Useofculturedcellsofkidneyorigintoassessspecificcytotoxiceffectsofnephrotoxins[J].ToxicolinVitro,2003,17:107-113
[12]周倩,姚广涛,金若敏.中药体外肝肾细胞毒性评价的研究进展[J].时珍国医国药, 2013,24(3): 718-720
(2016-11-07 收稿)
*河北省自然科学基金资助项目:No.H2014206302;河北省高等学校科学技术研究项目:No.ZD2015001;河北省中医药 管理局科研计划项目:No.2014007;河北中医学院青年教师科研基金项目:No.QNZ2014007
王鑫国,男,教授,硕士研究生导师。
R
A
1007-5615(2017)01-0043-04

