HTPE与CL-20和HMX混合体系的热分解
王国强,杨立波,陆洪林,张正中,张昊越,屈 蓓
(西安近代化学研究所,西安 710065)
HTPE与CL-20和HMX混合体系的热分解
王国强,杨立波,陆洪林,张正中,张昊越,屈 蓓
(西安近代化学研究所,西安 710065)
利用差示扫描量热(DSC)法,得到端羟基聚醚(HTPE)/六硝基六氮杂异伍兹烷(CL-20)和HTPE/奥克托今(HMX)混合体系在不同升温速率(2.5、5.0、10.0、20.0 ℃/min)下的热分解曲线;用Kissinger公式和Ozawa公式,计算了HTPE/CL-20和HTPE/HMX体系热分解的表观活化能。结果表明,HTPE/CL-20混合体系表观活化能分别为132.11、130.60 kJ/mol;HTPE/HMX混合体系表观活化能分别为193.80、198.57 kJ/mol。对于同一体系,2种公式计算的结果基本一致。与单组分(CL-20或HMX)相比,HTPE/CL-20和HTPE/HMX体系的表观活化能分别降低了28.3~29.8 kJ/mol和80.2~85.0 kJ/mol。HTPE均降低了2种高能组分(CL-20和HMX)的分解放热峰温度,CL-20和HMX的分解放热峰峰温降低了36.0 ℃和17.3 ℃。HTPE/CL-20体系分解放热量减少了354.5 J/g,而HTPE/HMX体系分解放热量不变。
物理化学;端羟基聚醚(HTPE)/六硝基六氮杂异伍兹烷(CL-20)混合体系;端羟基聚醚(HTPE)HTPE/奥克托今(HMX)混合体系;热分解
0 引言
新型粘合剂端羟基聚醚HTPE是低易损性推进剂的关键组分之一。尽管HTPE粘合剂与目前常用的无规共聚醚PET粘合剂均是环氧乙烷/四氢呋喃共聚醚,但两者分子结构有较明显的区别[1-3]。有关HTPE粘合剂和HTPE固体推进剂的报道较多,汪存东等[4]研究了HTPE及其弹性体的性能,Comfort等[2,5]介绍了HTPE推进剂的研究进展,赵孝彬等[6]研究了HTPE推进剂慢速烤燃特性的影响因素。
CL-20(六硝基六氮杂异伍兹烷)和HMX(奥克托今)均属于硝胺类含能材料,可显著提高固体推进剂的能量。徐劲祥[7]研究了CL-20的催化热分解行为及非等温分解动力学。王阳等[8]研究了HMX热分解行为。刘子如[9]研究了CL-20和HMX的热分解和热分解动力学。丁黎等[10]研究了CL-20/HMX混合体系在不同压强下的热分解行为。但有关新型粘合剂HTPE与CL-20和HMX混合体系热分解的报道较少。
由于推进剂配方包含多种组分,因此推进剂的热分解过程非常复杂,组分间相互作用更复杂[9]。为了避繁就简,本研究利用差示扫描量热(DSC)法,得到HTPE/CL-20和HTPE/HMX二元混合体系在不同升温速率下热分解曲线,用Kissinger公式和Ozawa公式,计算了HTPE/CL-20和HTPE/HMX体系热分解的动力学参数,以期研究这种新型粘合剂对二元混合体系热分解的影响,为HTPE在低易损性推进剂配方的应用提供理论依据。
1 实验
1.1 原材料及样品制备
新型粘合剂HTPE:Mn=4 081,羟值为4.847×10-4mol/g,平均官能度fn=1.98,水分含量为0.045%,黎明化工研究设计院责任有限公司提供。CL-20和HMX:均为西安近代化学研究所提供。
将HTPE分别与CL-20和 HMX各称量5 g在50 ml的烧杯中,加入30 ml丙酮(分析纯),搅拌均匀,加热抽真空除去丙酮后,得到混合体系样品。单一体系直接取样称量即可。
1.2 仪器和实验条件
DSC 204型差示扫描量热仪(德国NETZSCH公司),样品质量约0.500~1.000 mg,升温区间为50~350 ℃(对于单一体系,升温区间为50~500 ℃),升温速率分别为2.5、5.0、10.0、20.0 ℃/min,N2气氛,流速为50 ml/min。
2 结果与讨论
2.1 HTPE/CL-20和HTPE/HMX混合体系的热分解特征
HTPE/CL-20和HTPE/HMX混合体系在10.0 ℃/min升温速率下的DSC曲线见图1。表1是2种混合体系的DSC分解热测试结果。
从图1和表1可看出,对于单组分,CL-20在230 ℃以前是稳定的,最大分解热峰温为250.1 ℃,分解气体产物主要是NO2[9];DSC曲线上没有熔融吸热过程,CL-20的分解属于固相分解[9]。HTPE/CL-20混合体系的DSC最大分解放热峰温为214.1 ℃,与单组分CL-20相比,DSC曲线上也没有熔融吸热过程,混合物中CL-20的分解仍属于固相分解。由此可见,在HTPE/CL-20混合体系中,HTPE并没有影响CL-20的分解方式,但使得CL-20的放热峰温降低了36.0 ℃;峰形变小许多,峰宽变小不多。

体系ΔHd/(J/g)CL20单组分3101[9]HTPE/CL20混合体系1196HMX单组分1987[9]HTPE/HMX混合体系994.4
从图1和表1还可看到,单组分CL-20分解放热量为3 101 J/g,而HTPE/CL-20混合体系分解放热仅为1 196 J/g。由于单组分HTPE的分解放热非常小,可忽略不计。因此,按比例折算,实际相对于单组分CL-20,混合体系的放热量减少了354.5 J/g(1 196~3 101/2),即HTPE/CL-20混合体系分解放热量减少了354.5 J/g。
对于单组分,HMX在195 ℃有1个晶型转变吸热峰,在280 ℃有1个熔融吸热峰,紧接着是最大分解放热峰,峰温为285.3 ℃;可发现HMX是一种典型的“分解熔融”或“熔融分解”型物质,在常压下,HMX的分解是固液反应同时进行的非均相过程[9];HTPE/HMX混合体系的DSC分解放热峰温为268.0 ℃,与单组分HMX相比,该混合体系中HMX仍有1个晶型转变吸热峰(178.0 ℃)和1个熔融吸热峰(266.0 ℃),峰形似乎没有变小。可看出,在HTPE/HMX混合体系中,HTPE并没有影响HMX的分解方式,但使得HMX放热峰温降低了17.3 ℃。同样,由单组分HMX和混合体系放热量按比例折算,HTPE/HMX混合体系放热量没有增加或减少。
2.2 不同升温速率下2种混合体系的热分解特征和动力学参数
2.2.1 不同升温速率下2种混合体系的热分解特征
不同升温速率下,HTPE/CL-20和HTPE/HMX混合体系的DSC曲线见图2。从图2可看出,2种混合体系在升温速率增大时,热分解峰温逐渐向高温推移,放热量也逐渐增大,与含能组分在不同升温速率下热分解的现象一致[9]。
2.2.2 Kissinger公式计算2种混合体系的热分解动力学参数
根据Kissinger的特定反应机理模式[11],在不同升温速率下,最大热分解反应处的转化率α基本相同,利用特征温度Tm的直观性来判断反应速率的变化情况。从DSC曲线测得不同升温速率时最大热分解速率对应的峰温Tm,由Kissinger公式计算表观活化能和指前因子等,如表2所示。
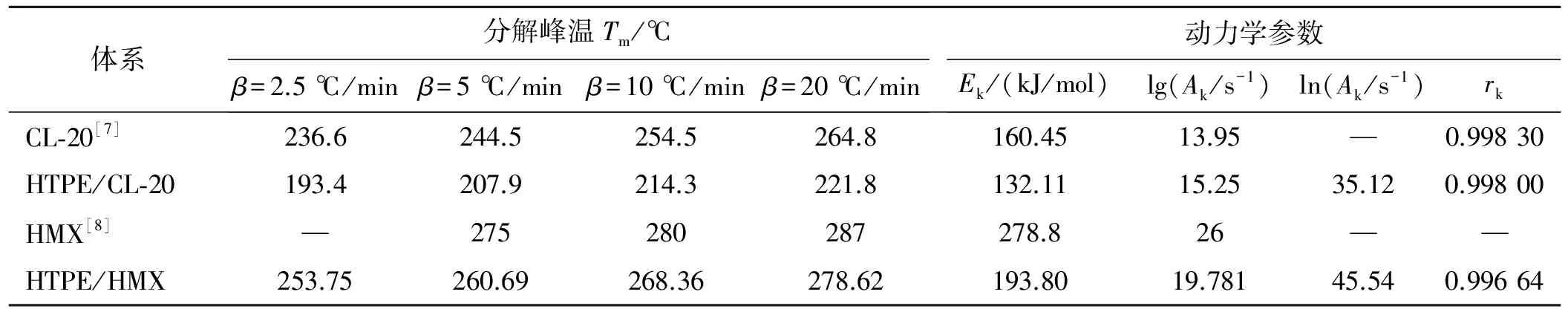
体系分解峰温Tm/℃β=2.5℃/minβ=5℃/minβ=10℃/minβ=20℃/min动力学参数Ek/(kJ/mol)lg(Ak/s-1)ln(Ak/s-1)rkCL20[7]236.6244.5254.5264.8160.4513.95—0.99830HTPE/CL20193.4207.9214.3221.8132.1115.2535.120.99800HMX[8]—275280287278.826——HTPE/HMX253.75260.69268.36278.62193.8019.78145.540.99664
从表2可看到,在不同升温速率(2.5、5.0、10.0、20.0 ℃/min)下,HTPE/CL-20混合体系高温分解反应的表观活化能Ek=132.11 kJ/mol、指前因子Ak=1.778 3×1015s-1,相关系数大于0.99。与CL-20单组分[7]比较,HTPE/CL-20混合体系中CL-20的分解反应的表观活化能降低了28.34 kJ/mol,而指前因子却增大了约20倍。由阿仑尼乌斯方程可知:
CL-20的方程式为
kCL-20=8.912 5×1013exp(-19.299/T)
HTPE/CL-20混合体系的方程式为
kHTPE-CL-20=1.778 3×1015exp(-15.890/T)
由此可知,kHTPE-CL-20>kCL-20,说明HTPE的确加速了CL-20的热分解。
还可以看到,与HMX[8]单组分比较,HTPE/HMX混合体系的表观活化能Ek为193.80 kJ/mol,降低了85.0 kJ/mol,指前因子Ak由1.000 0×1026s-1减小到6.039 5×1019s-1,减小了1.66×106倍。由HMX的分解反应速率常数式kHMX=1.000 0×1026exp(-33.534/T)和HTPE/HMX混合体系的分解反应速率常数式kHTPE-HMX=6.039 5×1019exp(-23.310/T)可知,kHMX﹥﹥kHTPE-HMX,说明尽管HTPE降低了HMX热分解反应的表观活化能,却大大降低了HTPE/HMX混合体系的分解反应速率常数,抑制了HMX的分解反应。由此可得出,HTPE对CL-20和HMX热分解反应的作用不尽相同。
2.2.3 Ozawa公式计算2种混合体系的热分解动力学参数
对不同升温速率下DSC曲线上HTPE/CL-20的分解峰积分,获得HTPE/CL-20混合体系反应转化率与温度(α-T)关系曲线(图3),通过对曲线上CL-20的分解峰积分,获得HTPE/CL-20混合体系反应深度(转化率)与温度(即α-T)关系曲线(见图3),从而获得了混合体系中CL-20分解在等反应深度α=0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8和0.9时所对应的温度,见表3。
通过Ozawa公式[11]及表2中的数据作lgβ-1/T曲线,线性回归得到了混合体系中CL-20在α为上述9种情况时的表观活化能E0,并假定是Ozawa公式[11]中G(α)=-ln(1-α),求得lnA0,结果列于表3。
由表3可看出,在不同升温速率(2.5、5.0、10.0、20.0 ℃/min)和反应深度分别为0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8和0.9的条件下,分解温度在增加;HTPE/CL-20混合体系的平均表观活化能E0=130.60 kJ/mol、指前因子A0=1.82×1015s-1。与Kissinger方程计算动力学参数一致。

数据点反应深度分解温度T/℃β=2.5℃/minβ=5℃/minβ=10℃/minβ=20℃/min动力学参数E0/(kJ/mol)lg(A0/s-1)ln(A0/s-1)r010.1178.15188.13196.69210.81109.2412.4828.740.9999020.2184.74195.46203.66215.92118.9413.7531.650.9987530.3188.31199.28207.60218.32125.9914.6333.680.9983540.4190.78201.87210.44219.74143.6116.6538.350.9999050.5192.63203.66212.41221.16133.0615.5835.870.9971060.6194.23205.01214.20222.15151.0717.6240.580.9986570.7196.20206.62215.97223.38127.0615.0334.620.9990580.8198.42208.40217.77224.80131.0415.5435.790.9995590.9201.79211.42220.78227.20135.3716.0837.020.99980平均值—————130.6015.2635.14—
同样,依据图3所示的HTPE/HMX混合体系的热分解温度,采用Ozawa公式计算出HTPE/HMX混合体系的动力学参数(表4)。
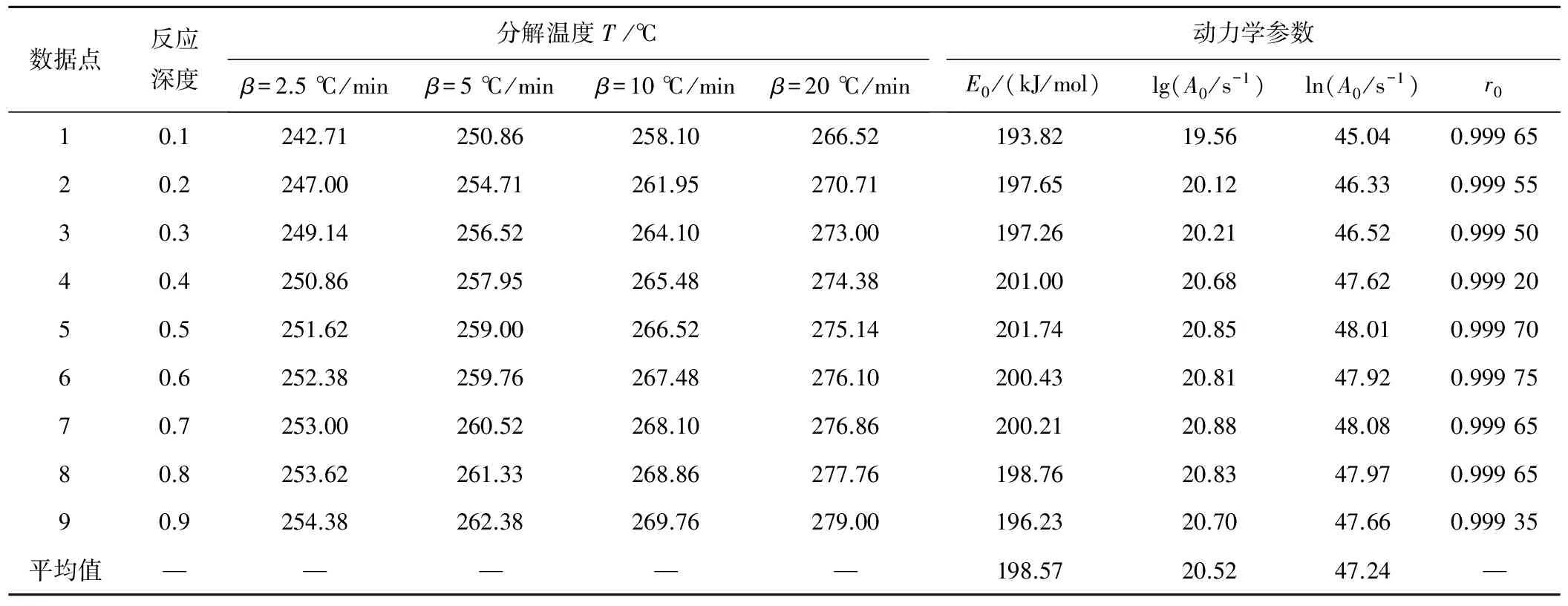
表4 HTPE/HMX混合体系的热分解温度和Ozawa公式计算动力学参数
由表4可看出,在不同升温速率(2.5、5.0、10.0、20.0 ℃/min)和反应深度分别为0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8和0.9的条件下,分解温度在增加;HTPE/HMX混合体系的平均表观活化能E0=198.57 kJ/mol、指前因子A0=3.31×1020s-1,与Kissinger方程计算动力学参数一致。
2.3 HTPE/CL-20和HTPE/HMX混合体系热分解特征不同的原因分析
从2.1节结果看,加入HTPE均导致HTPE/CL-20和HTPE/HMX混合体系分解放热峰温向低温方向偏移,但混合体系放热量变化却不同,以下分别进行分析说明。
(1)从热分解的特征来看,与惰性的HTPE高分子粘合剂相比,含能组分CL-20和HMX的热分解有以下特点:1)分解温度较低;2)放热量大;3)放热过程比较集中;4)放热峰较尖锐。当HTPE分别与CL-20和HMX形成混合体系时,在含能组分颗粒的表面均匀包覆了一层粘合剂薄膜。这种薄膜隔离了原本相邻的含能组分颗粒,使得其在受热达到其起始分解温度时各自分解放热,放热过程相互影响减弱,热量不能集中释放。由于HTPE的分解温度较高,因此含能组分分解放出热量被HTPE薄膜吸收,通常情况下,混合体系内(组分之间或组分与产物之间或产物之间)没有发生物理变化或化学反应作用时,其放热量将会减少约为含能组分放热量的一半,放热峰温通常也会降低。
(2)与CL-20或HMX相比,惰性的HTPE分子结构中没有含能基团,在整个热分解过程中,HTPE放热量非常小,分解温度较高,加入混合体系后,对混合体系低温阶段的分解放热几乎没有贡献。
(3)对于HTPE/CL-20混合体系,分解峰温大幅降低,放热量显著减少,减少了354.5 J/g。原因可能有以下几个:一个原因是HTPE加速了CL-20的分解反应。在2.2节中可发现,与单组分CL-20的相比,混合体系的表观活化能降低了,且指前因子和分解反应速率常数均增大了,从而加速了CL-20的分解反应。大多数情况下,活化能降低或升高时,指前因子也会发生降低或升高的变化[7,12]。由此分析认为,在高温下,CL-20固相分解的产物(如NO2等[9])可能与HTPE中的羟基发生了反应,使得CL-20分解产物种类发生变化,破坏了CL-20分解反应的某种平衡,使CL-20分解反应加速。而且还有,由于混合体系在CL-20分解时的温度很低(214 ℃),而提升混合体系的温度,达到HTPE的分解温度(381 ℃)[13]需要大量的热量;HTPE包覆的含能组分颗粒在混合体系中分解放热时,CL-20释放的热量完全被HTPE所吸收用于提升体系温度;由于HTPE的包覆作用,CL-20颗粒分解产生的热量难以集中释放出来。因此,由于这几个原因的影响作用,混合体系放热量大幅减少;同时,CL-20分解峰温也大幅降低。
(4)HTPE对HMX热分解的影响与CL-20明显不同,即放热量没有变化。可做如下解释:由于HTPE的存在,使得HMX的分解可能受到一定程度地抑制,因此在2.2节的动力学参数计算中,才出现了(与单组分HMX的相比)混合体系表观活化能和指前因子均大幅降低的结果,从而导致HMX热分解反应速率常数大大减小。尽管这样,但由于HMX发生“分解熔融”或“熔融分解”及自加热和自催化[9]分解放热,才没有导致HTPE/HMX混合体系像HTPE/CL-20混合体系一样的分解温度大幅降低。其他还有,由于HMX分解时的温度较高,分解释放的热量能满足HTPE的需要。由于混合体系在HMX分解时的温度约为268 ℃,而提升混合体系的温度,达到HTPE的分解温度(381 ℃)[13]需要的热量,可能与HMX分解放出的热量相当;HTPE包覆的含能组分颗粒在混合体系中分解放热时,HMX释放的热量完全被HTPE所吸收用于提升体系温度;HMX分解的产物与极少量HTPE分解的产物[14]酯类,还有烯类、甲基和新的醇类几乎没有相互作用。也就是说,HTPE对HMX热分解的影响不大。因此,由于这几个因素的影响作用,混合体系放热量没有变化。
3 结论
(1)对于同一混合体系,Kissinger公式和Ozawa公式计算的HTPE/CL-20混合体系和HTPE/HMX混合体系热分解表观活化能、指前因子等结果基本一致。
(2)HTPE明显降低了HTPE/CL-20混合体系的表观活化能,并提高了指前因子和反应速率常数;HTPE使CL-20放热峰温降低了36.0 ℃,混合体系分解放热量减少了354.5 J/g;即HTPE加速了CL-20的分解反应。
(3)HTPE大幅降低了HTPE/HMX混合体系的表观活化能的同时,也更大幅降低了指前因子和反应速率常数;结果使混合体系中HMX放热峰温降低了17.3 ℃,混合体系分解放热量没有变化。
[1] 宋晓庆,周集义,王文浩,等.HTPE推进剂研究进展[J].含能材料,2008,16(3):349-352.
[2] Comfort T,Shanholtz C,Fletcher G.Progress in HTPE propellants[C]//NDIA 39th Annual Gun & Ammunition/Missiles & Rocket Conference,Baltimore,USA,2004.
[3] 闫大庆,徐丹丹,师经国.固体推进剂粘合剂HTPE研究及其分子设计思想概述[J].固体火箭技术,2009,32(6):644-653.
[4] 汪存东,罗运军,夏敏.HTPE的合成及弹性体的性能[J].含能材料,2011,19(5):518-522.
[5] Comfort T,Grow S.Update on HTPE propellant service life[C]//Insensitive Munitions and Energetic Materials Technology Symposium,Tucson,Arizona,USA,May 2009.
[6] 赵孝彬,李军,程立国,等.固体推进剂慢速烤燃特性的影响因素研究[J].含能材料,2011,19(6):669-672.
[7] 徐劲祥.CL-20的催化热分解行为及非等温分解动力学[J].火炸药学报,2007,30(5):36-41.
[8] 王阳,邱瑞,王琦,等.新型含能材料NOG2Tz对HMX热分解行为的影响[J].含能材料,2014,22(1):22-25.
[9] 刘子如.含能材料热分析[M].北京:国防工业出版社,2008: 73-89;92-95.
[10] 丁黎,赵凤起,刘子如.CL-20/HMX混合体系的热分解[J].固体火箭技术,2008,31(2):164-167.
[11] 高大元,董海山,李波涛,等.炸药热分解动力学研究及其应用[J].含能材料,2006,12(增刊): 307-310.
[12] 郭子如,王小红.AN和硝酸钠混合物热分解的动力学分析[J].含能材料,2004,12(6):361-363.
[13] 夏敏,罗运军,毛铸科.HTPE粘合剂的热分解机理及其对AP热分解特性的影响[C]//2014年(第六届)含能材料与钝感弹药技术学术研讨会论文集,成都,2014:347-350.
[14] 罗善国,谭惠民,张建国,等.环氧乙烷/四氢呋喃共聚醚的热降解机理[J].北京理工大学学报,1995,15(6):79-88.
(编辑:刘红利)
Thermal decomposition of HTPE/CL-20 and HTPE/HMX mixed systems
WANG Guo-qiang,YANG Li-bo,LU Hong-lin,ZHANG Zheng-zhong,ZHANG Hao-yue,QU Bei
(Xi'an Modern Chemistry Research Institute,Xi'an 710065,China)
The thermal decomposition behavior of hydroxyl-termined polyether(HTPE)/hexanitrohexaazaisowurtzitane(CL-20) and HTPE/octogen(HMX) mixed systems under different heating rates were investigated by DSC.The thermal decomposition apparent activation energy of HTPE/CL-20 and HTPE/HMX mixed system were calculated by Kissinger's and Ozawa's methods.Results show that two kinds of calculated apparent activation energy of HTPE/CL-20 mixed system are 132.11 kJ/mol and 130.60 kJ/mol,respectively.Two kinds of calculated apparent activation energy of HTPE/HMX mixed system are 193.80 kJ/mol and 198.57 kJ/mol,respectively.Both results are about the same for the same system calculated with different method.Compared with single component(such as CL-20 or HMX),the apparent activation energy of HTPE/CL-20 and HTPE/HMX mixed systems decreased by 28.3~29.8 kJ/mol and 80.2~85.0 kJ/mol,respectively.HTPE decreased the decomposition peak temperature of the two kinds of energetic components(CL-20 and HMX),the decomposition peak temperature of CL-20 in the HTPE/CL-20 mixed system reduces 36.0 ℃,and the decomposition peak temperature of HMX in the HTPE/HMX mixed system reduces 17.3 ℃.The decomposition of the heat release of HTPE/CL-20 mixed systems decreased 354.5 J/g,while the decomposition of the heat release of HTPE/HMX mixed systems remained unchanged.
physical chemistry;HTPE/CL-20 mixed system;HTPE/HMX mixed system;thermal decomposition
2015-10-08;
2016-10-26。
武器装备预先研究项目(51328040301)。
王国强(1963—),男,高级工程师,主要从事固体推进剂配方和工艺研究。E-mail:13571984349@163.com
V512
A
1006-2793(2017)01-0070-06
10.7673/j.issn.1006-2793.2017.01.012

