中药黄芩苷对鸡胚成纤维细胞的安全浓度和生长的影响
丁婵,褚秀玲,苏建青
(聊城大学农学院 山东聊城 252059)
中药黄芩苷对鸡胚成纤维细胞的安全浓度和生长的影响
丁婵,褚秀玲*,苏建青
(聊城大学农学院 山东聊城 252059)
为了研究中药黄芩中有效成分黄芩苷对鸡胚成纤维细胞(CEF)生长的影响,应用细胞病变观察法(CPE)观察黄芩苷对CEF细胞生长的影响,并采用四甲基偶氮唑蓝(MTT)比色法测定黄芩苷对鸡胚成纤维细胞的最大安全浓度。黄芩苷浓度在312.5 μg/mL时为最大安全浓度,低于此浓度时黄芩苷能促进CEF的贴壁及生长,细胞生长良好,呈梭形,折光性强。结果表明,黄芩苷在中、低浓度能促进CEF细胞的贴壁和生长且对CEF细胞的作用都具有时效性,应用细胞病变观察法与MTT法,最终得出黄芩苷对CEF的最大安全浓度为312.5 μg/mL。
黄芩苷;CEF细胞;安全浓度
中药具有多功能、多靶向和药食同源的作用,是保障畜禽健康养殖,替代抗生素的重要途径之一[1-2]。黄芩(Radix Scutellariae)是唇形科植物黄芩属多年生草本植物,其根可入药,性寒味苦,具有清热燥湿、泻火解毒的功效,是临床畜禽呼吸道疾病常用的一种清热类中药[3]。黄芩药材中主要含有黄芩苷、黄芩素和汉黄芩素等有效成分,其中黄芩苷的含量较高,是黄芩发挥药效的主要成分之一[4]。药理学研究证实,黄芩苷具有抗微生物、抗病毒、利胆、保肝和解痉等作用[5-7]。
近几年,通过对黄芩苷的相关生物学活性进行的初步研究发现黄芩苷对鸡MDV无论在细胞上还是在鸡体内都有较强的抑制作用,对鸡体内由MDV引起的淋巴组织增生性肿瘤的形成具有抑制作用,并显著提高了机体的免疫力。为了深入探讨黄芩苷的生物学活性,拟以鸡马立克氏病为模型,系统研究黄芩苷的抗病毒活性,并进一步阐明其作用机理,为临床获取能有效控制病毒所致肿瘤性疾病的黄酮类化合物提供依据,并为进一步实施人工合成提供研究思路与方法。
本试验选用体外试验中药黄芩苷对鸡胚成纤维细胞的安全浓度和生长的影响,为下一步体外抗病毒试验做准备。
1 材料与方法
1.1 材料
1.1.1 鸡胚 SPF鸡胚,山东育凤农业科技有限公司提供。
1.1.2 药品 黄芩苷,黄芩购于聊城利民中药有限公司,采用煎煮法提取黄芩中的黄芩苷,运用紫外分光光度法在278 nm处对黄芩苷的含量进行测定,分析提取次数、料液比和提取时间等因素的影响,并在此基础上进行正交试验,优化提取工艺参数。得出结果,当提取次数为2次,料液比为1∶25,每次煎煮50 min时,黄芩苷的提取效果最好,提取率为20.36%。1.1.3 试剂和耗材 胎牛血清、青霉素、链霉素、Dulbecco’s Modified Eagle’s Medium(DMEM)培养粉、胰蛋白酶、细胞冻存液。MTT溶液、二甲基亚砜(DMSO),其他试剂为分析纯试剂。100 mL培养瓶、96孔板、微孔滤膜、细胞冻存管,泰安联星公司。
1.1.4 主要仪器 水浴锅、倒置显微镜、高压灭菌锅、离心机、天平、CO2培养箱、鼓风式电热干燥箱、超净台、4 ℃冰箱、-20 ℃冰箱、超声波清洗器、酶标仪。
1.2 鸡胚成纤维细胞(chick embryo fibroblast,CEF)的制备、培养和保存 鸡胚成纤维细胞的制备按文献进行[8-10],简述如下:选择9~11日龄照蛋观察血管粗壮的鸡胚于蛋架上,先后消毒气室部外壳用无菌眼科镊子击破该部位的蛋壳和卵膜,轻轻夹住鸡胚颈部取出鸡胚,放入无菌平皿中[11-12]。用灭菌剪刀剪去鸡胚头部、腿部、翅膀和内脏,留下躯干组织。用Hanks液冲洗2~3次,除去血液后用灭菌剪刀尽量剪碎(1 mm3小块),再用Hanks液冲洗2次直至组织发白为止,然后将洗液上清吸弃。根据鸡胚组织块的多少加入大约4倍量的胰酶(5~6 mL),于37 ℃温箱内消化20~30 min,视其组织碎块变松散(聚合成一团、边缘毛样模糊)即可。用无菌纱布过滤后,2000 rpm 3~5 min离心,将胰蛋白酶去除干净。加适量DMEM营养液,用吸管反复吹吸数次,使细胞分散,制成细胞悬液。静置1 min,使未吹散的组织块沉淀,吸出细胞悬液分到培养瓶中,将培养瓶中的营养液添至适度。在细胞生长至80%~90%的单层时,将培养液倒掉,加入0.25%胰蛋白酶适量进行消化,用吸管进行吹打,将细胞从培养瓶上吹下来,计数后,2000 r/min离心5 min,弃掉上清培养液,再加入适量细胞冻存液将细胞浓度调整至2×107个细胞/mL,装入1.5 mL专用细胞冻存管中,依次从4 ℃放置2 h、-20 ℃放置2 h,-80 ℃过夜,-180 ℃液氮中保存[13]。
1.3 黄芩苷对鸡胚成纤维细胞最大安全浓度的测定1.3.1 药物的稀释 称取试验药物1 g溶于50 mL细胞维持液中,即为0.02 g/mL。吸取试验药物溶液100 μL至96孔细胞培养板第一孔中,然后从第1~10孔,每孔加入100 μL细胞维持液,再将第1孔内液体混匀,吸取100 μL至第2孔内,再混匀,吸取100 μL至第三孔内,如此反复至第10孔,则药物稀释倍数分别为21~210。其浓度分别为10 mg/mL、5 mg/mL、2.5 mg/mL、1.25 mg/mL、0.625 mg/mL、312.5 μg/mL、156.25 μg/mL、78.13 μg/mL、39.06 μg/mL、19.53 μg/mL[11]。
1.3.2 药物对CEF贴壁的影响 CEF原代细胞用0.25%胰蛋白酶消化制成细胞悬液,计数后以105个/孔浓度接种入96孔培养板上,每孔加入0.1 mL,然后各孔分别加入不同稀释度的黄芩苷和阳性对照利巴韦林各0.1 mL,每个稀释度4孔,并设置空白细胞作正常对照。然后至37 ℃ 5% CO2培养箱中继续培养,分别在24、48、72 h后观察细胞生长情况,判定药物对细胞贴壁的影响。
1.3.3 药物对CEF单层的影响 取细胞悬液加入96孔细胞培养板中,每孔100 μL,密封后,置二氧化碳培养箱中37 ℃培养24 h,待细胞长成均匀单层后取出,吸出生长液,加入Hanks液洗1遍,弃去,各孔分别加入各浓度药物100 μL或细胞维持液100 μL。每种药物浓度重复4孔,同时设不加药物的对照孔4孔。密封,置37 ℃恒温箱中继续培养,分别于24、48、72 h观察单层细胞生长情况。
1.3.4 观察结果
1.3.4.1 观察细胞融合、坏死、脱落、漂浮、死亡等细胞病变效应(CPE) “-”表示细胞生长极差,全部为未贴壁圆细胞,细胞破碎、不完整或轮廓不清;“+”表示细胞生长很差,基本为圆细胞,极少贴壁细胞;“++”表示细胞生长较差,未形成单层,有大量圆细胞和空隙;“+++”表示细胞生长一般,未形成单层,有较多空隙和极少圆细胞;“++++”表示细胞生长良好,全部或基本形成完整单层,无空隙,细胞折光性强。1.3.4.2 用MTT法观察黄芩苷不同浓度对CEF生长的影响 用PH7.4的Hanks液配制成0.5 mg/mL的溶液(需遮光处理),将在37 ℃、5% CO2培养箱中培养了72 h的96孔板取出,每孔加入20 μL MTT溶液,继续培养4 h,倒置显微镜下观察MTT结晶状况,然后弃去上清液,每孔内加入150 μL DMSO,低速振荡10 min后,在酶标仪A490 nm下测定光密度(OD)值,设置细胞对照孔和空白对照孔。选择加药孔的A490值显著大于或与细胞对照孔的A490平均值无显著差异的药物最大浓度作为其最大安全浓度[14-16]。
1.3.4.3 数据处理 计算4孔平均值和标准差, 数据以“x±s”表示,用SPSS统计分析软件进行方差分析和多重比较。
2 结果与分析
2.1 应用细胞病变观察法观察黄芩苷对细胞生长的影响
2.1.1 黄芩苷对CEF贴壁的影响 对结果进行观察,黄芩苷浓度高时,药物颜色较深,细胞生长极差,全部为未贴壁圆细胞,并且随着作用时间的延长,部分细胞开始死亡(图1A),能够说明黄芩苷对细胞有一定毒性。黄芩苷浓度低一些时,毒性也随之降低,药物颜色不影响观察,细胞表现为部分贴壁,但大部分还处于未贴壁状态(图1B、图1C)。当黄芩苷浓度降到无毒浓度时,细胞生长良好呈梭形,长成单层的整个细胞面只见到极少数圆细胞,折光性强(图1D)。
2.1.2 黄芩苷对CEF单层的影响 对结果进行观察,黄芩苷浓度高时,药物颜色较深,基本观察不到细胞,对细胞的影响很大(图2A)。黄芩苷浓度逐渐变低时,能够观察到细胞,并且有极少贴壁,大部分为圆形细胞,细胞间隙较大(图2B、图2C)。和黄芩苷对CEF贴壁的影响相同,它对细胞的毒性也具有剂量依赖特性,即毒性随着药物浓度的降低而降低,黄芩苷毒性降低很快,在细胞形态上可能表现为上一个浓度细胞状态很差,下一个浓度细胞就生长状态很好。在黄芩苷无毒浓度下,对细胞单层没有影响,细胞生长良好、折光性强(图2D)。
2.1.3 药物作用时间对细胞的毒性作用 对CEF细胞贴壁的影响 通过观察黄芩苷对CEF细胞24、48、72 h贴壁作用的影响,发现药物作用具有一定的时效性,药效要达到一定时间才能发挥出来。同一浓度下,48 h的细胞形态优于24 h的细胞形态。但72 h的细胞形态和48 h的细胞形态基本相同(表1)。
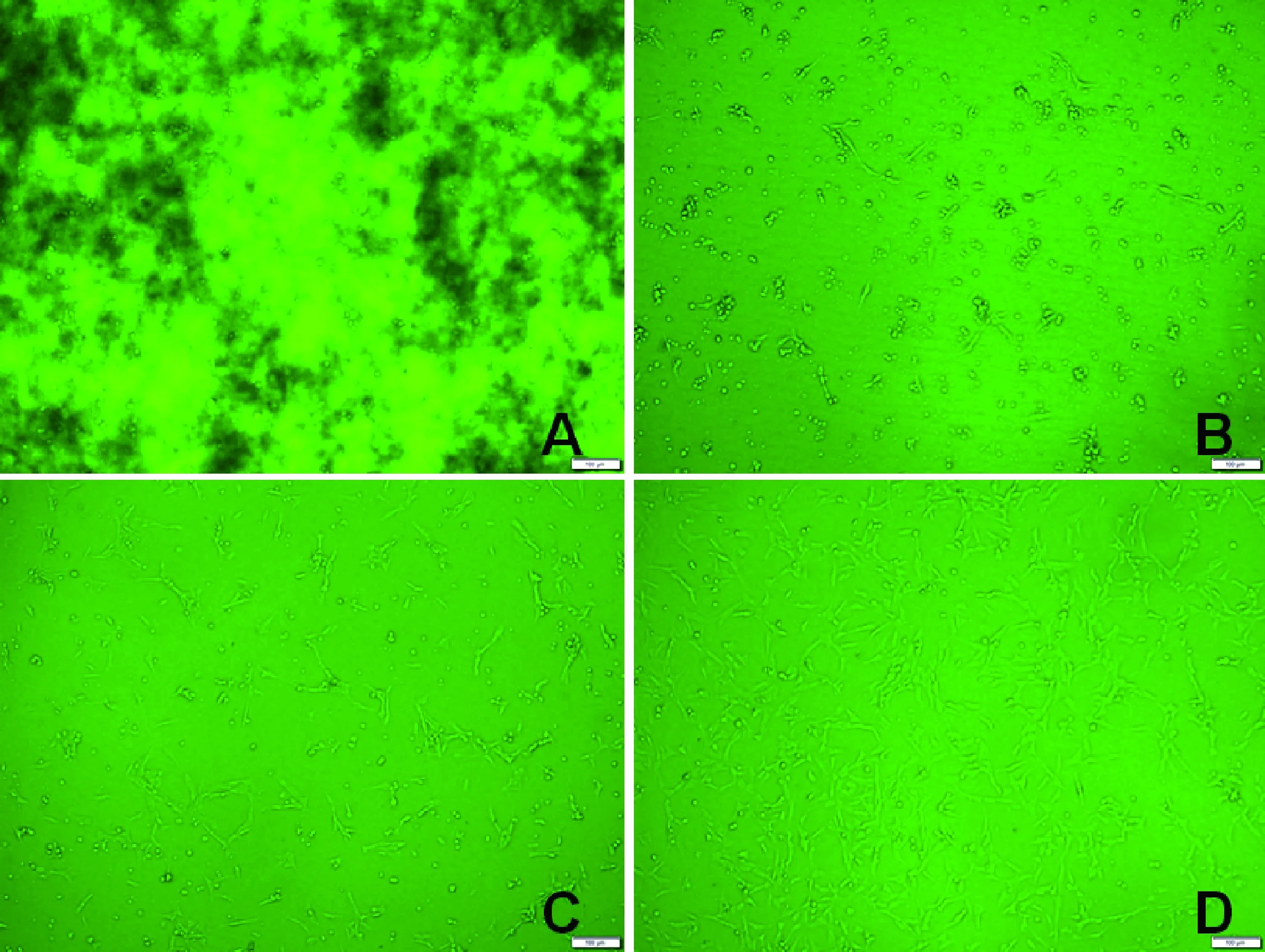
A:浓度为5000 μg/mL的药物对CEF的影响,药物浓度大且有颜色,细胞生长较差,破碎不完整或轮廓不清;B:浓度为156.25 μg/mL的药物对CEF的影响,细胞部分贴壁,大多数为圆细胞;C:浓度为78.13 μg/mL的药物对CEF的影响,细胞大量贴壁,有少量圆细胞和空隙;D:正常对照细胞,细胞生长良好,形成了较好的单层。图1 药物48 h时对CEF细胞贴壁的影响(100×)

A:浓度为5000 μg/mL的药物对单层CEF的影响,药物浓度大颜色深,对细胞观察有影响;B:浓度为625 μg/mL的药物对单层CEF的影响,极少贴壁,大部分为圆细胞;C:浓度为312 μg/mL的药物对单层CEF的影响,细胞生长较差,极少贴壁,大部分为圆细胞,空隙大,死亡细胞少;D:浓度为78.13 μg/mL的药物对单层CEF的影响,细胞生长良好、折光性强。图2 药物24 h时对单层CEF细胞的影响(100×)

药物时间浓度/(μg·mL-1)10000500025001250625312.5156.2578.1339.0619.530黄芩苷24-----++++++++++++++++++48---+++++++++++++++++++++++72---++++++++++++++++++++++++++
++++表示细胞生长良好,全部或基本形成完整单层;+++表示细胞生长一般,有大量圆形细胞和空隙;++表示细胞生长较差,未形成单层;+表示细胞基本为圆细胞,极少贴壁细胞;-表示细胞生长极差,全部为未贴壁圆细胞。
对CEF细胞单层的影响 通过观察药物对CEF细胞24、48、72 h影响单层作用的结果,发现药物对CEF单层的影响和贴壁的影响相同,也具有时效依赖性。同一浓度下,24 h的细胞形态优于48 h的细胞形态。但72 h的细胞形态和48 h的细胞形态基本相同(表2)。

表2 黄芩苷对CEF单层的影响
++++表示细胞生长良好,全部或基本形成完整单层;+++表示细胞生长一般,有大量圆形细胞和空隙;++表示细胞生长较差,未形成单层;+表示细胞基本为圆细胞,极少贴壁细胞;-表示细胞生长极差,全部为未贴壁圆细胞。
2.2 MTT法检测对CEF生长的影响 对CEF细胞贴壁的影响,从表3可知,中药黄芩苷质量浓度在625 μg/mL及其更大时,与细胞对照组有显著差异,质量浓度在312.5 μg/mL以及低于这个浓度时,与细胞对照组无显著差异。对CEF细胞单层的影响,中药黄芩苷质量浓度在1250 μg/mL及其浓度更高时,与细胞对照组有显著差异,质量浓度在625 μg/mL及其低于此浓度时,与细胞对照组无显著差异。
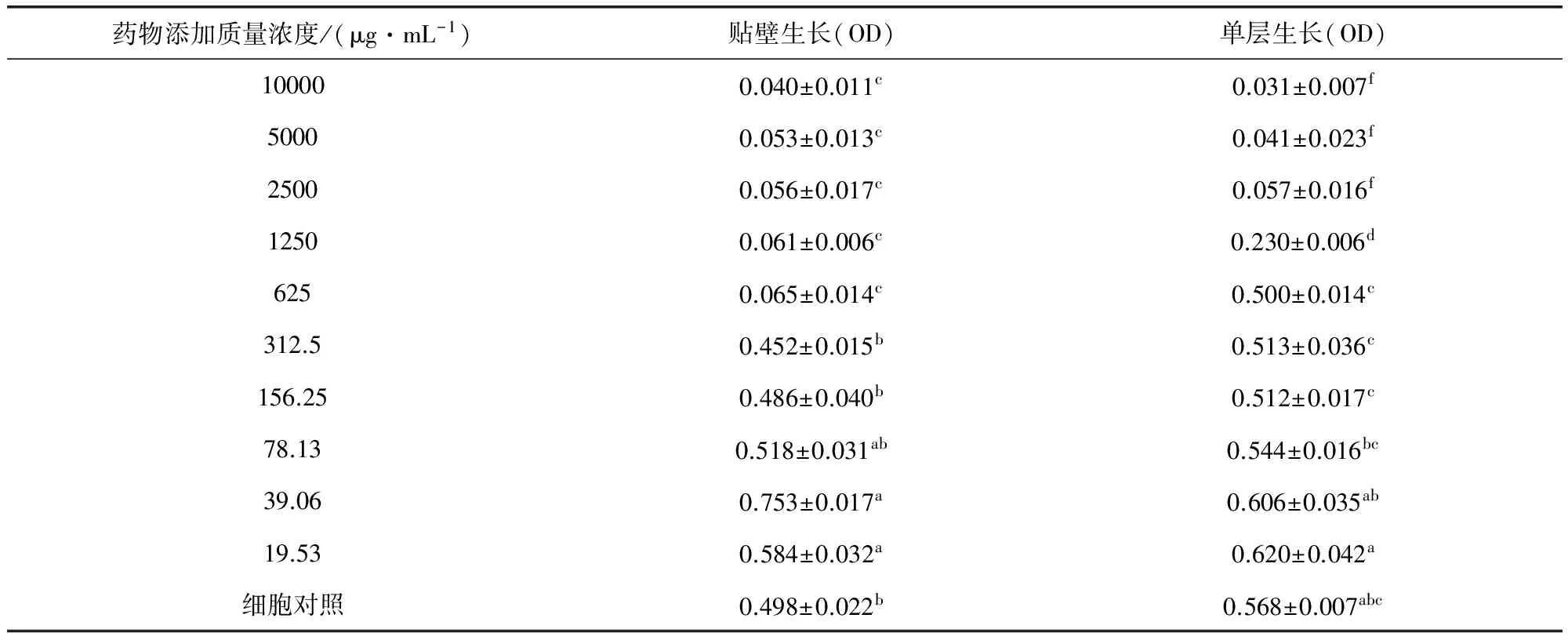
表3 中药黄芩苷对CEF贴壁单层生长(A490)的影响
同列数据肩标不同字母者表示在0.05水平差异显著。
3 讨论与小结
黄芩苷对细胞具有一定的毒性,无论是黄芩苷对CEF细胞的贴壁,还是单层生长,对CEF细胞的毒性均表现为剂量依赖性,高浓度抑制细胞生长,低浓度对细胞不表现毒性。试验中还发现,药物在中、低浓度能促进CEF细胞的贴壁和生长,与正常对照相比,细胞贴壁和生长更快,细胞形态更好。
无论是黄芩苷对CEF细胞的贴壁,还是单层生长,药物对CEF细胞的作用都具有时效性,药效要达到一定时间才发挥出来。同一浓度下,48 h的细胞形态优于24 h的细胞形态,但72 h的细胞形态和48 h的细胞形态基本相同。通过观察,发现黄芩苷对CEF细胞贴壁的影响大于对CEF细胞单层的影响,可能是由于CEF细胞长成单层后对外界的抵御能力要大于未贴壁的CEF细胞。
以药物对CEF细胞贴壁和单层均没有影响的最低稀释倍数,作为药物对CEF的最大安全浓度。应用MTT法,根据A490 nm测定结果判定中药对CEF的安全浓度,选择A490 nm与对照差异不显著的试验组的最高黄芩苷浓度作为安全浓度的上限,综合贴壁试验、单层试验结果,能够看出,黄芩苷的最大安全浓度,即最小稀释浓度为312.5 μg/mL。应用细胞病变观察法,综合贴壁试验、单层试验结果,可以看出,黄芩苷的最大安全浓度为625 μg/mL。综合两种测定结果,最终得出黄芩苷对CEF的最大安全浓度为312.5 μg/mL。
在进行黄芩苷对鸡胚成纤维细胞的最大安全浓度测定中,最常用的方法是观察细胞病变效应(CPE),但此种方法有一定的主观性,且不能进行精确的定量分析。MTT比色法简单直观,与CPE法相结合可准确测定黄芩苷对CEF的最大安全浓度。本试验结合两种方法,提高了试验的准确度,结果表明,黄芩苷对CEF的最大安全浓度为312.5 μg/mL,低于最大安全浓度时,黄芩苷能促进CEF的贴壁及生长。
[1] 孙良媛,刘涛,张乐.中国规模化畜禽养殖的现状及其对生态环境的影响[J].华南农业大学学报:社会科学版.2016,(02):23-30.
[2] 陈希,穆祥,许剑琴. 抗菌中药筛选思路的解析及实践[J]. 中国兽药杂志,2016,(02):1-6.
[3] 侯艳宁,朱秀媛,程桂芳.黄芩苷的抗炎机理[J].药学学报,2000,(03):161-164.
[4] 沙子健,付双,许凤.中药黄芩中黄芩苷的提取工艺研究[J].齐齐哈尔医学院学报.2010,(12):1928.
[5] 李玉山.黄芩的化学成分及黄芩苷的提取方法[J].西北药学杂志.2008,(06):410-411.
[6] 刘春憬.正交优化黄芩中黄芩苷的提取工艺[J].农产品加工,2015,(01):22-24.
[7] 顾正勤,孙颖浩,许传亮,等.黄芩苷诱导前列腺癌细胞株DU145凋亡的体外研究[J].中国中药杂志,2005,30(1):63.
[8] Ma X,Guo Z H,Wang D Y,etal.Effects of sulfated polysaccharides and their prescriptions on immune response of ND vaccine in chicken[J].Carbohydrate Polymers,2010,82(1):9-13.
[9] 司徒镇强,吴军正.细胞培养[M]. 世界图书出版公司,2007.
[10]斯佩克特DL,戈德曼RD,莱因万德L A.细胞实验指南:上册[M].黄培堂,译. 北京:科学出版社,2001.
[11]Resnitzky D,Gossen M, Bujard H,etal.Acceleration of the G1/S phase transition by expression of cyclin D1 and E with an inducible system[J].Molecular and Cellular Biology,1994,14 ( 3 ):1669-1679.
[12]Jiang W.Kahn S M, Zhou P,etal. Overer expression of cyclin D1 in rat fibroblasts causes abnormalities in growth control,cell cycle progression and gene expression[J]. Oncogene,1993,8 (12):3447-3457.
[13]辛华.细胞生物学实验[M].北京:科学出版社,2001.
[14]褚秀玲.分子修饰前后的人参皂苷抗马立克氏病毒的作用及其机制研究[D].吉林大学.
[15]徐玉凤,刘家国,王德云,等.芪蓝抗毒饮及其主要成分在鸡胚成纤维细胞上最大安全浓度的测定[J].畜牧与兽医,2009,41(11):52-54.
[16]邢玉娟,陈茜,陈玉库,等.4个中药复方对鸡胚成纤维细胞的安全浓度和生长的影响[J].江苏农业科学,2014,42(6)149-151.
(编辑:陈希)
Effect of Baicalin on Safety Concentrations and Growth of Chicken Embryo Fibroblast
DING Chan,CHU Xiu-ling*,SU Jian-qing
(AgriculturalCollegeofLiaochengUniversity,Shandong,Liaocheng252059,China)
The cell culture of Chinese herbs skullcap active ingredients baicalin on chick embryo growth of fibroblasts (CEF)invitro. Cytopathic observation (CPE) to investigate the effects of baicalin on CEF cell growth, and the use of tetrazolium blue (MTT) colorimetric assay of baicalin on chick embryo fibroblasts maximum safe concentration, the concentration of baicalin at 312.5 μg/mL is the maximum safe concentration, below which the concentration of baicalin can promote the growth of CEF and adherent cells grew well, fusiform, strong refraction. Baicalin in low concentration could promote CEF cell adherence and growth and the role of CEF cells for both time-sensitive applications cytopathic observation and MTT assay, the final results of baicalin maximum safe concentration of CEF for 312.5 μg/mL.
baicalin; CEF cells; safe concentration
山东省自然科学基金(ZR2013CL010)
丁婵,硕士研究生,从事动物疫病发生机理及防控方向研究。
褚秀玲。E-mail:chuxiul@163.com
2016-09-05
A
1002-1280 (2017) 01-0035-06
S853.74

