大豆磷脂酰聚乙二醇单甲醚2000的制备及性能
陈圳,卫延安
大豆磷脂酰聚乙二醇单甲醚2000的制备及性能
陈圳,卫延安
(南京理工大学化工学院,江苏南京 210094)
以大豆磷脂为原料,首先制备出大豆磷脂酸钠,再与聚乙二醇单甲醚2000对甲苯磺酸酯(mPEG2000-OTs)反应制备大豆磷脂酰聚乙二醇单甲醚2000(SP-mPEG2000)。实验结果为:以65mg NaH处理大豆磷脂得到大豆磷脂酸钠,(大豆磷脂酸钠)∶(mPEG2000-OTs)= 0.45∶1,反应时间为4h,反应温度为90℃,转化率为71.2%,产物为淡黄色固体。经1HNMR和IR表征,证明为SP-mPEG2000。该合成路线反应条件温和,大豆磷脂利用率高。SP-mPEG2000水溶液临界胶束浓度为0.5g/L,此时表面张力为42mN/m。通过SP-mPEG2000对正己烷和水形成的乳状液的稳定性表征,表明产物的动力学稳定性优于大豆粉末磷脂。
大豆磷脂;聚乙二醇单甲醚2000;改性;临界胶束浓度;性能
聚乙二醇(polyethylene glycol,PEG)在水及各类有机溶剂中均能较好的溶解,并且无毒无刺激性,是极少有的被 FDA列为可入药的合成高分子化合物[1],将其引入到其他分子中能够有效地改变其材料或生物特性[2-3],聚乙二醇两端均为有活性的羟基,为避免某些情况下用其修饰分子时产生交联,采用一端以甲基封闭的甲氧基聚乙二醇(methoxy polyethylene glycol,mPEG)[4],其端位为羟基时活性较低,通常将其进行官能团转换,如转化成—COOH[5]、—OTs[6]、—Cl[7]及—NH2[8]等。杨阳等[9]成功在大豆磷脂的烷基链上引入两个聚乙二醇链,得到双子表面活性剂,陈龙等[10]对大豆磷脂中脑磷脂的氨基进行修饰,乳化能力较好,具有较好的表面活性并且能够形成胶束。
本方法为首次尝试对大豆磷脂的磷酸羟基进行改性,得到磷酸三酯类产物。首先对脑磷脂的氨基进行乙酰化,同时乙酰基也是判断产物形成的一个特征。反应后利用NaOTs不溶于绝大多数有机溶剂而溶于乙醇的特征将其分离出,干燥称重用于计算产率,同时利用产物溶解于四氢呋喃而不溶于无水乙醚的特征能够将产物分离出。详细流程见图1。本方法的优点在于反应操作简单,条件较为温和,改性后的磷脂产物性能均优于大豆磷脂。
1 实验部分
1.1 试剂和仪器
聚乙二醇单甲醚(mPEG),工业级;工业大豆磷脂,工业级;NaH,60%;其他试剂均为国产分析纯,未经进一步纯化直接使用。Bruker AVANCE 500MHz核磁共振仪:德国Bruker;Nicolet iS10 FT-IR型红外光谱仪:美国赛默飞世尔科技公司;BZY-2 全自动表/界面张力仪,上海衡平仪器仪表厂;CT14DII High-speed Benchtop Centrifuge,天美(中国)科学仪器有限公司Techcomp (China).,Ltd。
1.2 大豆粉末磷脂的制备
采用丙酮萃取法[10]。
1.3 乙酰化大豆磷脂的制备
参照文献[11]制备乙酰化大豆磷脂。由于大豆磷脂组分及乙酰化脑磷脂均不溶于丙酮[12],而过量的乙酸酐及副产物乙酸均可溶,因此先旋蒸除去溶剂,而后加入大量丙酮,将沉淀过滤,以丙酮洗涤沉淀3次即得乙酰化大豆磷脂。
1.4 大豆磷脂酸钠的制备
称取乙酰化大豆磷脂1g置于100mL烧瓶中,加入20mL二氯甲烷,待全部溶解后,缓慢加入65mg NaH,30℃下反应20min,反应毕,旋蒸除去溶剂得到沉淀,以无水乙醇洗涤沉淀即得大豆磷脂酸钠产物,性状为黄色颗粒。
1.5 mPEG-OTs的制备
参照文献[6]制备mPEG-OTs,对甲苯磺酰氯用量减半。
1.6 SP-mPEG2000的制备
称取0.45g大豆磷脂酸钠和1g mPEG-OTs置于烧瓶中,加入30mL甲苯,室温搅拌溶解,升温至90℃,反应4h,反应毕,待溶液温度降至室温,离心,沉淀以二氯甲烷离心,得到沉淀和上清液,沉淀以无水乙醇离心,转移合并上清液旋蒸除去乙醇,干燥称重;合并上清液旋蒸除去溶剂,以四氢呋喃重复离心合并上清液,旋蒸除去四氢呋喃,加入无水乙醚沉淀出产物,离心,沉淀以无水乙醚多次离心,取出沉淀,真空干燥称重。mPEG2000-OTs的转化率通过反应结束产生的NaOTs的质量表述,方法如下。
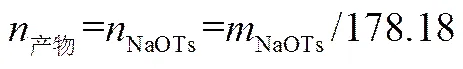
1.7 SP-mPEG2000临界胶束浓度(CMC)测定
分别配制浓度为10–7g/mL、5×10–7g/mL、10–6g/mL、5×10–6g/mL、10–5g/mL、5×10–5g/mL、10–4g/mL、5×10–4g/mL、10–3g/mL和10–2g/mL的SP-mPEG2000水溶液,采用威廉米吊片法测定25℃下各浓度SP-mPEG2000水溶液的表面张力。
1.8 SP-mPEG2000的动力学稳定性
取0.05g试样,加入蒸馏水于烧杯中充分溶解,加至具塞量筒中,加入去离子水至50mL,量取50mL 正己烷加入具塞量筒中,塞上盖子猛烈晃动至充分乳化,立即测定两相分开一定体积所消耗的时间。
1.9 SP-mPEG2000的泡沫性能
25℃下,分别以25mL容量瓶配制SP-mPEG2000质量分数为0.1%、0.5%、1%的水溶液,取20mL溶液加入100mL具塞量筒内,用力振荡15次,记录泡沫高度,静置5min后,记录泡沫高度[13]。
2 结果与讨论
2.1 结构分析
图2为最优条件下产物的核磁谱图,1H NMR(D2O)H:0.87(—CH3;a),1.17~1.5(脂肪链上的饱和C原子上H,—CH2—;b),1.56(酯基-C上H,—CH2—C—COOR;c),1.93~2.07(烯丙基饱和C原子上H,—C==C—CH2—;d),2.31(—C==C—CH2-C==C—;e),2.37(酯基-C上H,—CH2—COOR;f),2.73(磷酸酯亚甲基上H,—CH2—O—P==O;g),3.17(O—CH3;h),3.6~3.75(聚乙二醇重复单元,—CH2—CH2—O—;i),3.82,4.03(—COO—CH2—,—COO—CH—,j),4.19(修饰磷脂产物乙醇胺类结构中H;k),5.3(烯烃上H,—CH==CH—;l)
图3为红外谱图,a为乙酰化大豆磷脂,b为mPEG2000-OTs,c为产物,a和c中1737cm–1为乙酰化大豆磷脂结构中的峰,b中683cm–1、663cm–1为mPEG2000-OTs上OTs苯环上氢的面外变形振动,b和c中1100cm–1处为聚乙二醇C—O—C结构的伸缩振动峰,由c中出现C—O—C结构和脑磷脂上的羰基峰,同时OTs峰已十分微弱,说明两部分已经成功连接,可以判断产物的生成。
2.2 原料配比和NaH使用量对转化率的影响
原料配比对转化率的影响见图4。由图4可知,随着质量比的增加,mPEG2000-OTs的转化率逐渐升高,当其他条件相同,(大豆磷脂酸钠)∶(mPEG2000-OTs)=0.45∶1时,mPEG2000-OTs转化率达到71.9%,因此选择投料比(大豆磷脂酸钠)∶(mPEG2000-OTs)= 0.45∶1。
NaH用量对转化率的影响见图5。由图5可知100mg NaH/1g大豆磷脂制得的大豆磷脂酸钠中NaH的量明显过量,以65mg NaH/1g大豆磷脂制得的大豆磷脂酸钠已经足够得到较优的转化率,达到71.2%,产物为淡黄色固体。
2.3 SP-mPEG2000的临界胶束浓度
SP-mPEG2000水溶液的表面张力见图6。图6表明,25℃下曲线的拐点对应的SP-mPEG2000的 lg= –3.3,即= 0.5g/L,表明 SP-mPEG2000水溶液临界胶束浓度为0.5g/L,此时表面张力(CMC)为42 mN/m。
2.4 SP-mPEG2000的动力学稳定性
SP-mPEG2000动力学稳定性实验结果见表1。由表1可见,SP-mPEG2000分开10 mL 所用时间为309s,远大于乙酰化大豆磷脂所耗时间8s及mPEG2000-OTs所耗时间95s,当SP-mPEG2000的乳液分出40mL体积后油-水不再分离,低于mPEG2000-OTs的44mL,并且SP-mPEG2000的乳液在放置过夜后依然维持40mL,量筒上部形成稳定的乳状液,因此SP-mPEG2000的动力学稳定性优于乙酰化大豆磷脂及mPEG2000-OTs。
2.5 SP-mPEG2000的泡沫性能
SP-mPEG2000的泡沫性能见表2,由表2可见,SP-mPEG2000发泡力一般,稳泡性良好。
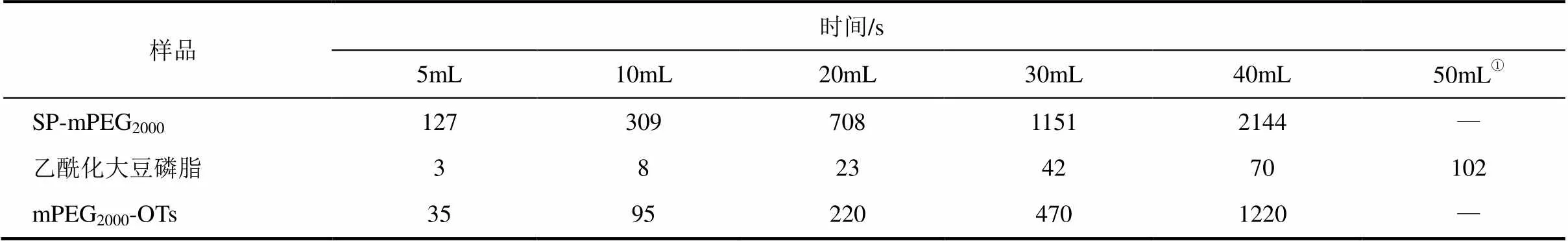
表1 不同物质的油-水两相分开体积与所用时间之间的关系
①SP-mPEG2000与mPEG2000-OTs在分出40mL后不再分离。
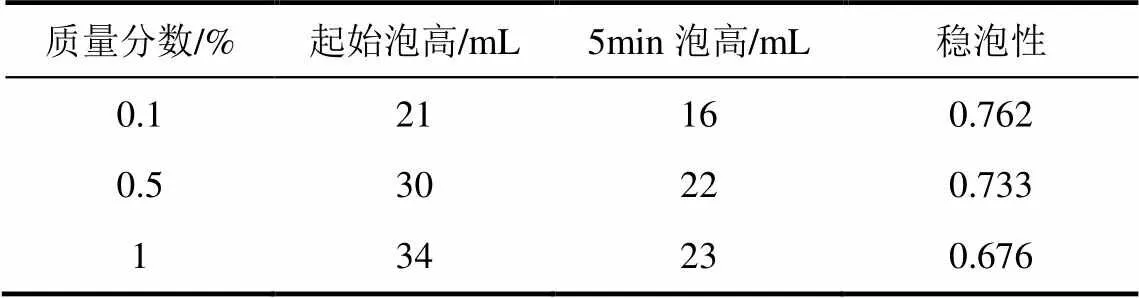
表2 SP-mPEG2000的泡沫性能
3 结论
(1)以乙酰化大豆磷脂和mPEG2000-OTs为原料成功制备SP-mPEG2000,产物为淡黄色固体,产物经1H-NMR和IR表征。得到最优条件:以65mgNaH处理大豆磷脂得到大豆磷脂酸钠,(大豆磷脂酸钠)∶(mPEG2000-Ots)= 0.45∶1,90℃下反应4 h,在最佳合成条件下转化率为71.2%。
(2)SP-mPEG2000的临界胶束浓度为0.5g/L,此时表面张力(CMC)为42 mN/m。对正己烷-水乳状液体系,充分乳化下分开10 mL所用时间为309 s,并且当分出40mL后不再分离,表明其动力学稳定性优于原料乙酰化大豆磷脂及mPEG2000-OTs。泡沫性能研究发现SP-mPEG2000发泡力一般,稳泡性良好。
[1] Greenwald R B. PEG drugs:an overview[J]. Journal of Controlled Release Official Journal of the Controlled Release Society,2001,74(1–3):159-171.
[2] 肖进新,暴艳霞,方磊. 正负离子表面活性剂与高聚物混合双水相体系的相行为及蛋白质的分配[J]. 高等学校化学学报,2001,22(1):112-114.
XIAO Jinxin,BAO Yanxia,FANG Lei. Phase behavior and protein partitioning in aqueous two-phase systems formed by mixtures of polymer and cationic-anionic surfactants[J]. Chemical Journal of Chinese Universities,2001,22(1):112-114.
[3] 王杰,索中军. PEG表面修饰硬脂酸脂质纳米粒的制备与体外细胞摄取[J]. 药学学报,2000,35(8):622-625.
WANG Jie,SUO Zhongjun. Stearic acid solid lipid nanoparticles surface-modified with poly(ethylene glycol):preparation and uptake by cells[J]. Acta Pharmaceutica Sinica,2000,35(8):622-625.
[4] FEENEY R E. Chemical modification of proteins: comments and perspectives[J]. International Journal of Peptide & Protein Research,1987,29(2):145-61.
[5] 陈龙,卫延安. 聚乙二醇单甲醚羧基衍生物的制备[J]. 精细化工,2013,30(10):1177-1180.
CHEN Long,WEI Yan’an. Preparation of carboxyl-monomethoxy poly(ethylene glycol)[J]. Fine Chemicals,2013,30(10):1177-1180..
[6] 赵静,李三喜,张文政. 聚乙二醇对甲苯磺酸酯的制备[J]. 辽宁化工,2011,40(6):547-548.
ZHAO Jing,LI Sanxi,ZHANG Wenzhen. Preparation of poly(ethylene glycol)tosylate[J]. Liaoning Chemical Industry,2011,40(6):547-548.
[7] ZALIPSKY S. Functionalized poly(ethylene glycols)for preparation of bio-logically relevant conjugates[J]. Bioconjugate Chemistry,1994,6(2):150-65.
[8] 魏海南,石亮亮,成昌梅,等. 聚乙二醇单甲醚衍生物的合成[J]. 化学试剂,2012,34(2):151-153.
WEI Hainan,SHI Liangliang,CHENG Changmei,et al. Synthesis of methoxy polyethylene glycol derivatives[J]. Chemical Reagents,2012,34(2):151-153.
[9] 杨阳,卫延安. 一种改性磷脂的合成工艺及性能[J]. 化工进展,2012,31(4):889-892.
YANG Yang,WEI Yan’an. Synthesis and properties of a new modified phospholipids[J]. Chemical Industry and Engineering Progress,2012,31(4):889-892.
[10] 陈龙,卫延安. 大豆磷脂酰乙醇胺-聚乙二醇单甲醚2000的制备及其性能研究[J]. 中国粮油学报,2015,30(5):111-115.
CHEN Long,WEI Yan’an. The study on preparation and performance research of soybean phosphatidyl ethanolamine-methoxy polyethylene gly-col 2000[J]. Journal of the Chinese Cereals and Oils Association,2015,30(5):111-115.
[11] 田志茗,初阳. 磷脂的乙酰化羟化改性工艺及其表面活性研究[J]. 精细石油化工,2004,2004(2):14-16.
TIAN Zhimin,CHU Yang. Study on synthesis of acetylated-hydroxylated phosphatide and its surface active properties[J]. Speciality Petrochemicals,2004(2):14-16.5.
[12] 安红,高树刚,杨烨. 大豆脑磷脂乙酰化改性及其乳化性能测定[J]. 食品与机械,2010,26(1):86-88.
AN Hong,GAO Shugang,YANG Ye. Acetylation of soya phosphatidylethanolamine and it’s emulsification[J]. Food & Machinery,2010,26(1):86-88.
[13] 黄良仙,肖波,杨军胜,等. 季铵化三硅氧烷的制备及其应用性能[J]. 印染,2013,39(3):1-4.
HUANG Liangxian,XIAO Bo,YANG Junsheng,et al. Preparation of quternary ammonium trisiloxane and its applied propeperties[J]. Dyeing and Finishing,2013,39(3):1-4.
Preparation and performance of soybean phosphatidyl methoxy polyethylene glycol 2000 ester
CHEN Zhen,WEI Yan’an
(School of Chemical and Engineering,Nanjing University of Science and Technology,Nanjing 210094,Jiangsu,China)
With soybean phospholipid as raw material,first it was converted into sodium soy phospholipids and then reacted with monomethoxypolyethylene glycol 2000 tosylate (mPEG2000-OTs) to prepare soybean phosphatidyl methoxy polyethylene glycol 2000 ester(SP-mPEG2000). The experimental results were as follows: soybean phospholipid was reacted with 65mg NaH to obtain sodium soy phospholipids,(sodium soy phospholipids)∶(mPEG2000-OTs) = 0.45∶1,reaction time was 4 hours,reaction temperature was 90℃,and the conversion rate was 71.2%. The solid product is pale yellow color. Analyzed by1HNMR and IR,the product was proved to be SP-mPEG2000. This method has the characteristics of mild reaction condition and high utilization of soybean phospholipid. The critical micelle concentration of SP-mPEG2000is 0.5g/L with surface tension of 42mN/m,The kinetic stability of SP-mPEG2000was confirmed by emulsifying power of-hexane and water,which indicated that kinetic stability of the product is superior to soybean phospholipid powder.
soybean phospholipids;methoxy polyethylene glycol 2000;modification; critical micelle concentration;properties
TQ645.9+6
A
1000–6613(2017)01–0350–05
10.16085/j.issn.1000-6613.2017.01.045
2016-05-19;修改稿日期:2016-06-12。
陈圳(1992—),男,硕士研究生。E-mail:1141030003 33@njust.edu.cn。联系人:卫延安,博士,副教授,研究方向为精细化工产品合成及含能材料安全技术。E-mail:weiya_69@163.com。

