月桂酸咪唑啉硫酸酯盐缓蚀剂在A3钢表面吸附成膜行为
郭睿,程敏,杨江月,李欢乐,刘爱玉
月桂酸咪唑啉硫酸酯盐缓蚀剂在A3钢表面吸附成膜行为
郭睿,程敏,杨江月,李欢乐,刘爱玉
(陕西科技大学,教育部轻化工助剂化学与技术重点实验室,陕西西安 710021)
采用失重法、接触角测试、原子力显微镜和X射线光电子能谱等分析方法研究了实验室自制月桂酸咪唑啉硫酸酯盐缓蚀剂(LIMS)在盐酸溶液中对A3钢的缓蚀吸附行为,同时探讨了LIMS在A3钢表面的成膜行为和作用机理。结果表明,月桂酸咪唑啉硫酸酯盐缓蚀剂LIMS分子可以明显抑制A3钢在盐酸溶液中的腐蚀,随着盐酸溶液中LIMS质量浓度的增加,缓蚀率增加。当LIMS质量浓度为800mg/L时,在298~318K温度范围内缓蚀效果良好,缓蚀率可达90%以上。LIMS可在金属表面形成一层吸附膜,这种吸附膜来源于长链烷基在金属表面形成的疏水薄膜和N、S、O与金属表面的强烈作用,成膜试片表面的接触角随着缓蚀剂质量浓度的增加而增大,接触角可达103.51°,接触角增大,吸附膜作用增强,致密性越好。
咪唑啉硫酸酯盐;表面;吸附;动力学;缓蚀机理
油田开采中采用酸化工艺可以提高采油率,但注入的大量酸液会对采油设备和金属管线造成严重腐蚀,给工业生产带来很大的经济损失和安全隐患[1-2]。在金属腐蚀的防护方法中,使用缓蚀剂是工艺简便、成本低廉的一种方法。将少量的缓蚀剂加入到腐蚀介质中,可以抑制金属的腐蚀过程和机械性能改变过程,从而延长金属设备的使用寿命。
咪唑啉是一种含氮五元杂环化合物,是一类应用广泛的缓蚀剂。1946年9月咪唑啉及其衍生物以其优良的缓蚀性能,作为缓蚀剂首次在美国获得专利[3]。咪唑啉具有独特的分子结构,咪唑啉环和它含有的杂原子,都具有多个孤对电子,能够和金属的空d轨道结合,吸附在金属表面。国内外有很多学者在咪唑啉的研究开发上已经做了大量工作,目前主要集中在咪唑啉缓蚀剂的作用机理方面。ZHAO等[4]研究了油酸基咪唑啉和苯甲酸钠的缓蚀协同效应和作用机理,研究结果表明两者在金属表面的吸附是分步进行的,先是油酸基咪唑啉(OIMA)分子通过物理吸附和化学吸附的方式吸附在金属表面,溶液中添加苯甲酸钠(SB)后,SB会发生水解反应,形成苯甲酸根离子(PhCOO–),由于静电引力吸附到Q235钢表面,从而对Q235钢起到更好的保护作用。ZHANG等[5]研究了一种溴代咪唑啉在盐酸溶液中对碳钢的缓蚀性能,通过热力学分析得到了温度和吸附膜厚度的关系,研究表明,该物质在金属表面的吸附符合Langmuir吸附等温式,表观活化能的增加是因为缓蚀剂分子在金属表面形成了吸附膜,吸附膜的厚度随着温度的增加而减小。
虽然目前人们对缓蚀剂在油田上的应用已有充分的了解,但在其缓蚀机理方面的研究还存在不足,尤其对其在碳钢表面形成的缓蚀吸附膜的研究和成膜机理还需要进一步研究探讨。作者在此基础上,以实验室合成的月桂酸咪唑啉硫酸酯盐(LIMS)为研究对象,采用失重法、接触角测试、原子力显微镜(AFM)和X射线光电子能谱(XPS)等分析手段对LIMS的缓蚀性能进行研究,并对缓蚀吸附膜的组成和致密性进行了探讨。
1 实验部分
1.1 实验材料
月桂酸咪唑啉硫酸酯盐LIMS,实验室自制,分子结构如图1所示。
A3钢片,主要化学成分为(质量分数,%):C 0.14~0.22,Mn 0.30~0.65,P≤0.045,S≤0.05,Si≤0.03,Fe余量。试片规格为:失重法,40mm×12mm×2mm;光谱法,5mm×5mm×2mm。实验前,先将钢片用砂纸打磨至表面光亮,用纯水清洗表面,丙酮除油后用乙醇浸泡1min后放入干燥器内干燥备用。
1.2 失重法
失重法参照石油天然气行业标准SY-T5405—1996《酸化用缓蚀剂性能试验方法及评价指标》[6]进行。在质量分数10%的HCl溶液中分别加入不同质量浓度的缓蚀剂LIMS,然后将钢片分别浸入不同溶液中,4h后将钢片取出,清洗干燥称重。缓蚀率计算如式(1)、式(2)。
=(0–)/(1)
=[(0–)/0]×100%。 (2)
式中,0和分别为腐蚀前后的钢片质量,g;为试片表面积,m2;为试片腐蚀时间,h;0和分别为空白酸液和添加缓蚀剂后的腐蚀速率,g/(m2·h)。
1.3 接触角测试
采用DSA100光学接触角测量仪(德国KRUSS公司)测定液滴在钢片表面的接触角。
298K时,将试片分别在10%空白盐酸溶液和加入缓蚀剂的盐酸溶液中浸泡24h,取出清洗干燥,在试片表面分别滴出5mm的纯水小液滴,通过所得的液滴形状,可得水滴与试片表面的接触角,观察水滴在金属表面的铺展程度。
同时为了研究酸液在钢片表面的铺展情况,用不同质量分数的盐酸小液滴,进行疏水性实验。根据所拍照片对盐酸液滴在金属表面的铺展程度与纯水的进行对比。
1.4 AFM测试
将A3钢片在298K下分别浸泡在10%空白盐酸溶液和800mg/L的LIMS溶液中24h,取出后用纯水清洗表面,充分干燥后备用。采用SPI3800N/SPA400原子力显微镜(日本精工)进行AFM测试,扫描速率2Hz,扫描方式为轻敲模式,使用Si探针,测量试片表面的形貌图。
1.5 XPS分析
将A3钢片在298K下浸泡在800mg/L的LIMS溶液中24h,取出后用纯水清洗表面,充分干燥。采用AXIS SUPAR X射线光电子能谱(英国Kratos公司)进行XPS测试。将单色化的AlKa阳极靶作为激发源,测试电压15kV,发射电流8mA,起飞角45º。
2 结果与讨论
2.1 失重法
缓蚀剂分子在试片表面成膜的过程中,影响成膜效果的因素较多,其中以LIMS质量浓度、温度、时间和盐酸质量分数对腐蚀过程的影响较为显著。因此,采用失重法讨论各影响因素对LIMS分子缓蚀性能的影响。
2.1.1 缓蚀剂质量浓度对缓蚀效率的影响
固定腐蚀时间为4h的条件下,考察了不同温度下LIMS质量浓度对A3钢缓蚀性能的影响,结果如图2所示。
如图2所示,随着缓蚀剂质量浓度的增加,缓蚀率逐渐增加,缓蚀剂质量浓度为50mg/L时,缓蚀效果不明显,当质量浓度增加到800mg/L时,缓蚀率达到93.1%,继续增加缓蚀剂质量浓度,对缓蚀率影响不大,这是因为当缓蚀剂质量浓度为800mg/L时,咪唑啉硫酸酯盐分子在钢片表面已经形成了一层致密的吸附膜,覆盖度已经达到了饱和,分子质量浓度增大时,咪唑啉硫酸酯盐分子不能有效地吸附在金属表面,从而使缓蚀率有所下 降[7]。同时由图2可知,当腐蚀温度低于318K时,缓蚀效率平稳,继续升高温度,缓蚀效率有明显降低趋势。因为咪唑啉季铵盐是一种吸附型缓蚀剂,随着温度的升高,缓蚀剂分子的溶解度逐渐增加,在金属表面的吸附能力减弱,原本吸附的分子发生脱落,覆盖率降低,而且温度升高后,H+活性增大,使金属的腐蚀速率增大,缓蚀率降低[8]。
2.1.2 腐蚀时间对缓蚀效率的影响
在298K,缓蚀剂质量浓度为800mg/L的条件下,考察了不同腐蚀时间下LIMS对A3钢缓蚀性能的影响,结果如图3所示。
由图3可知,在最初的20h内,缓蚀率随着时间的增加逐渐增加,腐蚀时间为24h时,缓蚀率达到最大,当腐蚀时间超过24h后,缓蚀率有较小范围的下降,这说明缓蚀剂需要一段缓慢的时间逐渐吸附在碳钢表面,当形成致密的吸附膜之后,缓蚀性能达到最佳,超过这个时间,缓蚀性能有所下降。所以需要定期添加缓蚀剂,才能保证最佳的缓蚀效果[9]。
2.1.3 酸度对缓蚀效率的影响
在298K,缓蚀剂质量浓度为800mg/L,腐蚀时间为24h,考察了盐酸质量分数对A3钢缓蚀性能的影响,结果如图4所示。
从图4可以看出,随着盐酸质量分数的增加,溶液的pH逐渐减小,对碳钢的腐蚀更为严重,腐蚀速率有所增加,当盐酸质量分数达到20%时,缓蚀效率显著减小,腐蚀速率增加较为明显,这可能是因为在盐酸质量分数较小时,缓蚀剂分子能够和H+有效结合,生成带正电的离子,形成有效的保护层,阻止金属被腐蚀,当盐酸质量分数增加时,腐蚀介质中的H+浓度增大,氢离子和缓蚀剂分子在碳钢表面形成竞争吸附,从而使缓蚀剂在金属表面的覆盖度降低,降低缓蚀效率。所以,缓蚀剂在盐酸质量分数为20%以下时,具有良好的缓蚀性能。
2.2 AFM测试
298K时,分别浸泡在盐酸溶液和800mg/L LIMS溶液中24h后A3钢表面的AFM形貌图如图5所示,相应的侧面高度图如图6所示。从图6(a)可以清晰地看出打磨试片时所留下的痕迹,未腐蚀钢片的最大表面粗糙度仅为44.46nm,而在空白盐酸中浸泡的6(b)试片表面严重受损,呈现出表面粗糙、凹凸不平的状况,明显受到了严重的腐蚀,最大表面粗糙度增加到800.48nm,表面粗糙度分布不均匀,起伏较大,在LIMS溶液中浸泡的试片6(c)与空白盐酸中浸泡的试片相比,表面明显平整,形成的缓蚀吸附膜分布致密[10],均匀地在试片表面覆盖,最大表面粗糙度降低为141.33nm,表面粗糙度变化平稳,进一步说明了缓蚀剂LIMS能够有效地抑制A3钢片的腐蚀。
2.3 接触角测试
图7中的(a)~(d)图分别为A3钢在空白盐酸和添加不同质量浓度缓蚀剂的溶液中浸泡后表面的疏水性示意图,液滴为纯水。e~h图为盐酸液滴所得的疏水性示意图,接触角测试结果列于表1。
从图7(a)~(d)可以看出,在缓蚀剂溶液中浸泡的钢片表面的疏水性比空白溶液显著增强,随着缓蚀剂质量浓度的增加,接触角逐渐增大。空白溶液中的接触角为27.50°,在800mg/L缓蚀剂溶液中浸泡的钢片表面的接触角为103.51°,这是由于咪唑啉分子极性基团中的长碳链吸附在碳钢表面,碳链部分伸向缓蚀剂溶液中,形成疏水界面,将碳钢和腐蚀介质隔开,缓蚀剂质量浓度越大,长碳链的疏水效果越好,则缓蚀效率越高。接触角越大,水滴在试片表面的铺展程度越小,则说明分子表面形成膜的致密性更好,腐蚀介质不易入侵,对金属的保护作用更明显。
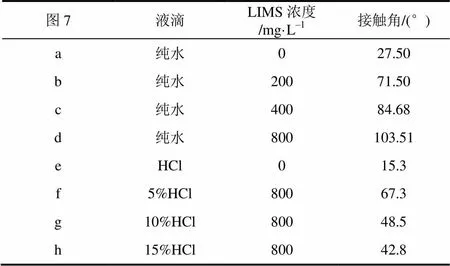
表1 A3钢片表面接触角
由图7(e)~(h)可以看出,当小液滴为盐酸溶液时,在缓蚀剂溶液中浸泡的A3钢表面的接触角仍然比空白溶液明显增大,随着酸液质量分数的增加,接触角有所减小。对比可知,该缓蚀剂分子在金属表面形成的疏水薄膜不但可以抑制纯水对金属的腐蚀,也可以很好的阻挡酸液的入侵,从而减缓金属的腐蚀。
2.4 盐酸介质中缓蚀剂LIMS的吸附动力学
腐蚀过程可以认为是一种Arrhenius反应过 程[11]。根据Arrhenius公式,A3钢片发生腐蚀的表观活化能a可通过式(3)得出。
=exp(–a/) (3)
式(3)中,为腐蚀速率,g/(m2·h);为指前因子,g/(m2·h)。根据失重法所得腐蚀速率作lnν与1/的线性拟合直线,所得结果如图8所示,通过其斜率可以求得腐蚀反应的表观活化能a和指前因子,结果如表2所示。
从表2可以看出,添加缓蚀剂LIMS后的表观活化能a和指前因子与空白盐酸溶液相比有所增加,随着添加缓蚀剂质量浓度的增大,表观活化能和指前因子也逐渐增加。未加缓蚀剂LIMS时A3钢在盐酸溶液中的腐蚀更容易进行。加入缓蚀剂后,缓蚀剂分子在金属表面形成吸附膜,覆盖了金属表面的活性位点,此时体系需要克服较高的能量障碍才能使腐蚀过程进行[12-13],咪唑啉环和长碳链能够在靠近金属表面形成很大的立体结构,防止腐蚀介质与碳钢表面的直接接触,同时可以提高腐蚀过程的活化能,抑制腐蚀过程的进行。而质量浓度增大也能够加剧分子间的碰撞,使得单位时间有更多的缓蚀剂分子吸附在金属表面。
图8 不同浓度LIMS的ln与1/的线性拟合直线
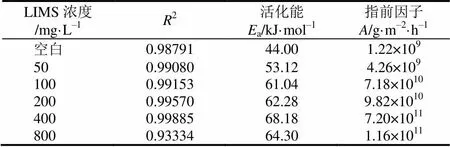
表2 A3钢的腐蚀动力学参数
TANG等[14]研究表明:当表观活化能a和指前因子数值呈现先增大后减小的趋势,有个“峰值”的情况下,一般表观活化能a对金属腐蚀过程的影响比指前因子大,但是当指前因子数值变化较大时,影响金属腐蚀的主要因素可能是指前因子。由Arrhenius方程可知,温度一定时,腐蚀速率随着指前因子的减小和表观活化能的增大而减小,在质量浓度为50~400mg/L之间时,两者数值均增大,此时认为表观活化能是影响腐蚀速率的主要因素,质量浓度为400~800mg/L之间时,两者均减小,此时认为指前因子是影响腐蚀速率的主要因素。
2.5 XPS测试
298K时,浸泡在800mg/L LIMS溶液中的A3钢表面的XPS图谱如图9所示。从图9(a)可以看出,在钢片表面检测到C、N、O、Fe的存在,其中C和O的含量较多,N和Fe的含量较少。C来自碳钢和缓蚀剂LIMS,在测试体系中只有LIMS分子含有N元素,所以N元素来自缓蚀剂分子,表明钢片表面存在的吸附膜是由于钢片表面吸附了LIMS分子所产生的。这两种元素是LIMS分子中的基本元素,而S元素含量较少,所以在298K下没有检测到S元素。C 1s 284.6eV的结合能作为结合能的荷电效应校正。从XPS图9(c)中可以看出531.0eV的峰是O 1s峰,由氧化铁中的氧和缓蚀剂分子中的氧共同组成。而在结合能为725.5eV和710.7eV处对应的峰分别为铁的Fe2p 1/2和Fe2p 3/2的光电子发射峰。它们对应铁的氧化态,表明铁的表面已经有一定程度的氧化[15]。缓蚀剂LIMS分子中含有两个N,其中一个为季铵正离子,将N1s峰进行了分峰拟合[16],拟合的结果如图9(e)所示。其中,结合能400.1eV处的峰为N 1s峰,399.1eV处的峰为缓蚀剂分子中C==N的峰,399.7eV处的峰属于缓蚀剂分子中的C—N,400.6eV和400.2eV处的峰分别为N、N+与Fe相互作用在试片表面形成的配位键所得的峰[17]。通常认为N和Fe相互作用后,N的电子云密度向铁转移一部分,N的电子云密度会降低,价态对内层电子产生微扰作用,导致N的1s电子不易激发,使结合能升高[18]。综上所述,证实缓蚀剂分子LIMS中的杂原子与钢片相互作用发生化学吸附,在钢片表面形成了一层致密的保护膜。
更进一步的是,随着腐蚀过程的进行,腐蚀形成的产物会形成一层膜,覆盖于A3钢片表面,而体系中存在的Fe2+不断向溶液中扩散,和腐蚀产物膜共同作用使碳钢表面的配位中心发生变化,腐蚀产物中的Fe2+和溶液中存在的Fe2+能够将缓蚀剂分子和金属表面连接起来,使吸附膜和腐蚀产物膜共同作用形成更加致密的膜[19]。
3 结论
(1)缓蚀剂LIMS在HCl溶液中对A3钢有明显的缓蚀作用,缓蚀效率随着LIMS质量浓度的增大而增大,温度低于318K时,受温度影响较小,呈现出良好的缓蚀性能。
(2)根据疏水性测试结果,LIMS分子中的烷基长链能够在A3钢表面形成一层疏水保护膜,提高腐蚀过程的活化能,纯水和盐酸液滴在成膜钢片表面的铺展程度小,接触角可达103.51°,膜的致密性良好。
(3)微观形貌和XPS测试结果表明LIMS中的杂原子与钢片相互作用发生化学吸附,在钢片表面形成了一层致密的保护膜,与疏水膜共同作用于钢片表面,使其具有良好的缓蚀性能。
[1] 刘洁,刘峥,陈世亮.石油生产中腐蚀的原因及缓蚀剂的应用[J].腐蚀与防护,2012,33(8):657-663.
LIU J,LIU Z,CHEN S L.Cause of corrosion and application of inhibitors in oil protection[J].Corrosion &Protection,2012,33(8):657-663.
[2] 李强,赵永峰,左禹.油气田缓蚀技术研究进展[J].石油化工腐蚀与防护,2010,27(8):1-6.
LI Q,ZHAO Y F,ZUO Y.Development of corrosion inhibition technology in oil-gas fields[J].Corrosion & Protection in Petrochemieal Industry,2010,27(8):1-6.
[3] BLAIR C M,GROVES W,GROSS W F,et al.Processes for preventing corrosion and corrosion inhibitors:US2466517[P]. 1949-04-05.
[4] ZHAO J M,CHEN G H.The synergistic inhibition effect of oleic-based imidazoline and sodium benzoate on mild steel corrosion in a CO2-saturated brine solution[J].Electrochimica Acta,2012,69:247-255.
[5] ZHANG K G,YANG W Z,XU B,et al.Corrosion inhibition of mild steel by bromide substituted imidazoline in hydrochloric acid[J].Journal of the Taiwan Institute of Chemical Engineers,2015,57:167-174.
[6] 石油工业标准化技术委员会.SY/T 5405—1996 酸化用缓蚀剂性能试验方法及评价指标[S].北京:中国石油天然气总公司,1996.
Standardization Technical Committee of Petroleum Industry.SY/T 5405—1996 Experiment instruction and standards for inhibitive performance of inhibitors in acidizing[S].Beijing:China National Petroleum Corporation,1996.
[7] 吴刚,郝宁眉,陈银娟,等.新型油酸咪唑啉缓蚀剂的合成及其性能评价[J].化工学报,2013,64(4):1485-1492.
WU G,HAO N M,CHEN Y J,et al.Synthesis of new oleic imidazoline corrosion inhibitors and evaluation of their performance[J].CIESC Journal,2013,64(4):1485-1492.
[8] 张可桂,杨文忠,徐斌,等.1-乙氨基-2-三氯甲基-咪唑啉的制备及其缓蚀性能[J].腐蚀与防护,2015,36(2):122-127.
ZHANG K G,YANG W Z,XU B,et al.Synthesis and inhibition efficiency of 2-(2-trichloromethyl-4.5-dihydro-imidazol-1-yl)-ethylamine[J].Corrosion & Protection,2015,36(2):122-127.
[9] 郭睿,张春生,包亮,等.新型咪唑啉缓蚀剂的合成与应用[J].应用化学,2008,25(4):494-498.
GUO R,ZHANG C S,BAO L,et al.Synthesis and application of a novel imidazoline inhibition[J].Chinese Journal of Applied Chemistry,2008,25(4):494-498.
[10] JEVREMOVIC I,SINGER M,NESIC S,et al.Inhibition properties of self assembled corrosion inhibitor talloil diethylenetriamine imidazoline for mild steel corrosion in chloride solution saturated with carbon dioxide[J].Corrosion Science,2013,77:265-272.
[11] LI X H,DENG S D,FU H,et al.Synergistic inhibition effect of rare earth cerium(Ⅳ) ion and sodium oleate on the corrosion of cold rolled steel in phosphoric acid solution[J].Corrosion Science,2010,52(4):1167-1178.
[12] BOUKLAH M,HAMMOUTI B,LAGRENEE M,et al.Thermodynamic properties of 2,5-bis(4-methoxyphenyl)- 1,3,4-
oxadiazole as a corrosion inhibitor for mild steel in normal sulfuric acid medium[J].Corrosion Science,2006,48:2831-2842.
[13] 胡松青,胡建春,高元军,等.月桂基咪唑啉对Q235钢的缓蚀吸附作用[J].化工学报,2011,62(1):147-155.
HU S Q,HU J C,GAO Y J,et al.Corrosion inhibition and adsorption of lauryl-imidazoline for Q235 steel[J].CIESC Journal,2011,62(1):147-155.
[14] TANG L,MU G,LIU G.The effect of neutral red on the corrosion inhibition of cold rolled steel in 1.0 M hydrochloric acid[J].Corrosion Science,2003,45:2251.
[15] 由庆,王业飞,魏勇舟,等.咪唑啉型缓蚀剂的合成及其缓蚀机理的研究[J].腐蚀与防护,2006,27(3):122-125.
YOU Q,WANG Y F,WEI Y Z,et al.Synthesis and inhibition mechanism of imidazoline corrosion inhibitor[J].Corrosion & Protection,2006,27(3):122-125.
[16] MOULDER F,STICKLE W F,SOBOL P E.Handbook of X-Ray photoelectron spectroscopy[M].Minnesot,USA:Perkin-Elmer Corp.,1992.
[17] WANG B,DU M,ZHANG J.Inhibition performance of an imidazoline derivative as a gas- liquid two phase inhibitor for Q235 steel against CO2corrosion[J].Acta Physico-Chimica Sinica,2011,27(1):120-126.
[18] OEHOA N,MORAN F,PEBERE N,et al.Influence of flow on the corrosion inhibition of carbon steel by fatty amines in association with phosphonocarboxylic acid salts[J].Corrosion Science,2005,47(3):593-604.
[19] 任呈强,刘道新,白真权,等.咪唑啉衍生物在含H2S/CO2油气井环境中的缓蚀行为研究[J].天然气工业,2004,24(8):53-55.
REN C Q,LIU D X,BAI Z Q,et al.Research on the inhibition behavior of imidazoline derivant in the oil/gas well containing H2S/CO2[J].Natural Gas Industry,2004,24(8):53-55.
Adsorption behavior oflauryl imidazoline sulfuric ester inhibitor on the surface of A3 steel
GUO Rui,CHENG Min,YANG Jiangyue,LI Huanle,LIU Aiyu
(Key Laboratory of Auxiliary Chemistry & Technology for Chemical Industry of the Ministry of Education,Shaanxi University of Science and Technology,Xi’an 710021,Shaanxi,China)
The inhibition performance and adsorption mechanism of lauryl imidazoline sulfuric ester on the A3 steel surface have been studied using weight loss method,contact angle test,atomic force microscope,and X-ray photoelectron spectroscopy. The film-forming mechanism on the A3 steel surface was also discussed. The results indicated that LIMS molecules adsorption film could inhibit the corrosion of A3 steel significantly. Inhibition efficiency increased with the increase of mass concentration. The inhibition efficiency was above 90% at a mass concentration of 800mg/L at the temperature range of 298—318K. LIMS could form adsorbed film on metal surface,it was from hydrophobic film oflong chain alkyl and strong effect between N,S,O and metal surface. Contact angle of film-forming steel surface increased with the mass concentration of LIMS. The contact angle was up to 103.51°. The higher the contact angle was,the higher the density of the adsorption film was.
imidazoline sulfuric ester;surface;adsorption;kinetics;corrosion inhibition mechanism
O626.23
A
1000–6613(2017)01–0336–07
10.16085/j.issn.1000-6613.2017.01.043
2016-06-07;修改稿日期:2016-08-10。
陕西省科技统筹创新工程计划项目(2014KTCL01-11)。
郭睿(1959—),男,硕士,教授,主要从事精细化学品及工业助剂合成与开发研究。E-mail:guor@sust.edu.cn。

