醚基功能化离子液体催化合成乙酸正丁酯
胡甜甜,赵地顺,武宇,张拴力,扈士海,翟建华
(1河北科技大学化学与制药工程学院,河北 石家庄 050018;2石家庄新宇三阳实业有限公司,河北 石家庄 051430)
醚基功能化离子液体催化合成乙酸正丁酯
胡甜甜1,赵地顺1,武宇1,张拴力2,扈士海2,翟建华1
(1河北科技大学化学与制药工程学院,河北 石家庄 050018;2石家庄新宇三阳实业有限公司,河北 石家庄 051430)
合成了5种醚基功能化酸性离子液体[Me(OEt)1-MOR-C3SO3H][MeSO3]、[Me(OEt)2-MOR-C3SO3H][MeSO3]、[Me(OEt)3-MOR-C3SO3H][MeSO3]、[2(C3SO3H-MOR)-(OEt)200][2MeSO3]、[2(C3SO3H-MOR)-(OEt)400][2MeSO3],使用红外光谱和核磁共振氢谱对合成的离子液体结构进行表征,考察离子液体的黏度、溶解性和腐蚀性。以正丁醇和乙酸的酯化反应考察了离子液体的催化活性,并使用响应面分析法优化反应工艺。结果表明,当酸醇摩尔比为1.2:1、催化剂[2(C3SO3H-MOR)-(OEt)400][2MeSO3]用量为醇质量的5%、带水剂用量为醇质量的16%时,在90℃下反应5 h,酯收率可达97.8%,离子液体经回收干燥重复使用8次催化活性没有明显的降低。
醚基功能化;吗啡啉;离子液体;催化;酯化;响应面
引 言
乙酸正丁酯是重要的有机化学产品,可作溶剂、萃取剂和脱水剂,广泛应用在涂料、药物中间体、人造香料和玻璃等制造中[1-2]。到目前为止,工业上生产乙酸正丁酯基本使用传统的浓硫酸催化酯化法,该工艺催化剂用量小、收率高、工艺条件成熟,但是该法存在设备腐蚀严重、副反应多、工艺复杂等问题,同时产生大量的废水、废渣,破坏环境[3]。近年来,酯化法合成酯类化合物的研究过程中相继出现了固体超强酸[4]、杂多酸[5]、强酸性阳离子交换树脂[6]、改性分子筛[7]、酶[8]等催化剂,但上述催化剂均出现催化活性低、产率低、易失活、回收及重复使用困难等问题。因此,寻找高催化活性和高选择性、重复使用性良好的环境友好型绿色催化剂成为当务之急。
离子液体是在环境温度或低温下呈液态并由阴阳离子组成的熔融盐[9]。离子液体因可以选择适当的阴阳离子或调整阳离子侧链,改善离子液体的物理和化学性质,被称为“绿色设计者溶剂”。离子液体的研究及应用已涉及催化[10-11]、分离[12-13]、电化学[14-15]等领域。2002年Cole等[16]首次报道了磺酸功能化咪唑类离子液体,酯化催化剂大多为此类离子液体。然而,咪唑类离子液体质子化后形成环共轭结构,质子不易给出,致使其酸性较弱[17],而且咪唑高昂的价格致使此类离子液体的成本较高。除此之外,离子液体的黏度与传统溶剂相比要高出1~3个数量级。成本和黏度成为限制离子液体应用的两大重要因素。因此,设计合成成本低、黏度低且催化活性高的离子液体成为离子液体研究的重要方向。黄宝华等[18-20]系统地研究了以氮杂环类物质作为阳离子主体制备的离子液体催化酯化反应,其中吗啡啉类离子液体不仅合成成本低,并且催化活性高,酯收率可达93.4%。Schrekker等[21]合成了不同侧链、不同阴离子的咪唑类离子液体,结果表明引入醚基功能化基团可以有效地降低离子液体的黏度。本研究以价格低、毒性小的吗啡啉作为阳离子主体,设计合成了一系列吗啡啉类离子液体,测定了其溶解性、黏度、腐蚀性等,通过催化合成乙酸正丁酯考察其催化活性,并对反应条件进行了优化。
1 实验材料和方法
1.1 材料
RE-2000B 型旋转蒸发器(上海亚荣生化仪器厂);DF-101S 型集热式恒温加热磁力搅拌器(长城科工贸有限公司); FTS-135 型傅里叶变换红外光谱仪(美国 BIO-RAD 公司); Bruker Avance 500MHz型核磁共振仪(瑞士BRUKER 公司); NDJ-1型旋转黏度计(上海昌吉地质仪器有限公司)。
吗啡啉(分析纯,山东西亚化学工业有限公司),乙二醇甲醚(分析纯,天津市永大化学试剂有限公司),二乙二醇甲醚(分析纯,天津市光复精细化工研究所),三乙二醇甲醚(分析纯,山东西亚化学工业有限公司),聚乙二醇-200(分析纯,天津市永大化学试剂有限公司),聚乙二醇-400(分析纯,天津市永大化学试剂有限公司),二氯甲烷,甲苯,三乙胺,甲磺酰氯(分析纯,山东西亚化学工业有限公司),1,3-丙烷磺酸内酯(分析纯,武汉吉和昌化工科技有限公司),正丁醇(分析纯,天津市红岩化学试剂厂),冰醋酸(分析纯,天津市永大化学试剂有限公司)。
1.2 醚基磺酸双功能化离子液体的合成
取0.06 mol聚乙二醇-400、150 ml二氯甲烷、0.12 mol三乙胺加到250 ml四口烧瓶中,氮气保护、搅拌、冰浴条件下30 min内滴加0.12 mol甲磺酰氯,滴加完毕后室温反应4 h,然后静置,溶液分层,抽滤,除去固体三乙胺盐酸盐,留上层清液,旋蒸除去溶剂二氯甲烷,剩余液体为甲磺酸酯。取上一步产品、0.12 mol 吗啡啉、150 ml甲苯加到250 ml四口烧瓶中,80℃下搅拌24 h,加入0.12 mol 1,3-丙烷磺酸内酯,反应24 h,产品与溶剂分层,分液,离子液体相用乙醚洗涤3次,除去溶剂得棕红色离子液体[2(C3SO3H-MOR)-(OEt)400][2MeSO3](5)。反应过程如图1所示。
按同样的方法,以乙二醇甲醚、二乙二醇甲醚、三乙二醇甲醚、聚乙二醇-200为原料制得离子液体[Me(OEt)1-MOR-C3SO3H][MeSO3](1)、[Me(OEt)2-MOR-C3SO3H][MeSO3](2)、[Me(OEt)3-MOR-C3SO3H][MeSO3](3)、[2(C3SO3H-MOR)-(OEt)200][2MeSO3](4)。
1.3 酯化反应
称取1 mol(74.12 g)正丁醇、1.2 mol(72.06 g)冰醋酸,3.7 g醚基功能化酸性离子液体和11.9 g环己烷,加到配有分水器、回流冷凝管、温度计和磁力搅拌的四口烧瓶中,并在分水器中加带水剂至分水器支管口,90℃下反应5 h,静置冷却至室温,分层,上层为酯层,下层为离子液体,减压蒸馏回收重复使用。
2 实验结果与讨论
2.1 产品结构表征
2.1.1 FT-IR 采用FT-IR法对合成的5种吗啡啉类离子液体进行了结构表征,红外谱图如图2所示。
2933 cm−1附近是—CH3和—CH2—上C—H的反对称伸缩振动峰,2871 cm−1附近是—CH3和—CH2—上C—H的对称伸缩振动峰,1455 cm−1和1348 cm−1附近是—CH3上 C—H的弯曲振动峰,1107 cm−1附近是—SO3H和MeSO3上S═O的伸缩振动峰,1037 cm−1附近是醚基的C—O—C的伸缩振动峰,920 cm−1附近是吗啡啉环上的C—O—C的伸缩振动峰,732 cm−1附近是—CH2—的面内摇摆振动峰。红外谱图与目标物质的官能团相对应,初步证明离子液体为目标产物。
2.1.21H NMR 以CDCl3为溶剂对所合成的醚基磺酸双功能化离子液体进行了核磁共振表征[22],1H NMR (500 MHz, CDCl3) δ结果如下。
[Me(OEt)1-MOR-C3SO3H][MeSO3]:2.060~2.072 (d, 2H, —CH2CH2CH2—),3.039(s, 3H, —SCH3),3.324~3.357(t, 2H, —SCH2CH2—),3.536(s,3H,—OCH3),3.627~3.639(m, 6H,3.929~3.948(m, 6H, —OCH2CH2—),9.073(s, 1H,—SOH)。
[Me(OEt)2-MOR-C3SO3H][MeSO3]:2.037~2.064 (d, 2H, —CH2CH2CH2—),2.821(s, 3H, —SCH3),3.048~3.079(d, 2H, —SCH2CH2—),3.259 (s, 2H,), 3.350~3.378(t, 2H, —OCH2CH2—), 3.530(s, 3H, —OCH3),3.537~3.546(m, 6H,),3.650~3.667(m, 6H, —OCH2CH2), 9.038(s, 1H, —SOH)。
[Me(OEt)3-MOR-C3SO3H][MeSO3]:2.261~2.274 (d, 2H, —CH2CH2CH2—),2.837(s, 3H, —SCH3),3.024~3. 065 (d, 2H, —SCH2CH2—),3.157~3.182 (m, 2H, —CH2CH2CH2—),3.249~3. 264 (m, 6H,),3.382 (s, 3H, —OCH3),3.615~3. 634 (m, 8H, —OCH2CH2—),3.856~3. 874 (m, 6H,—OCH2CH2—),9.043(s, 1H, —SOH)。
[2(C3SO3H-MOR)-(OEt)200][2MeSO3]:2.035~2.060(d, 4H, —CH2CH2CH2—),2.819(s, 6H, —SCH3),3.030~3.049(m, 8H, —SCH2CH2—),3.227~3.236(m, 4H,),3.472~3.486(m, 12H,—CH2CH2CH2—),3.623~3.662 (m, 20H,—OCH2CH2—),3.935~3.954(m, 12H, —OCH2CH2—),9.018(s, 2H, —SOH)。
[2(C3SO3H-MOR)-(OEt)400][2MeSO3]:2.049~2.057(d, 4H, —CH2CH2CH2—),2.799(s, 6H,—SCH3),2.995~3.089(m, 8H, —SCH2CH2—),3.307~3.312(m, 4H,),3.347~ 3.366(m, 12H, —CH2CH2CH2—),3.623~3.653(m, 36H, —OCH2CH2—),3.933~3.979(m, 12H,—OCH2CH2—),9.089(s, 2H, —SOH)。
综上所述,合成的离子液体[Me(OEt)1-MOR-C3SO3H][MeSO3]、 [Me(OEt)2-MOR-C3SO3H][MeSO3]、[Me(OEt)3-MOR-C3SO3H][MeSO3]、[2(C3SO3H-MOR)-(OEt)200][2MeSO3]、[2(C3SO3H-MOR)-(OEt)400][2MeSO3]为目标产物。
2.2 离子液体的黏度
黏度是流体的一项基本物性参数,是流体在实际应用中的一项重要考察指标。离子液体的黏度主要与范德华力、离子间的库仑作用力和氢键作用有关。黏度较大是限制离子液体应用的一个重要因素。表1是室温下离子液体的黏度测试结果。结果表明,在相同的温度下离子液体的黏度随醚基链长增加而降低。
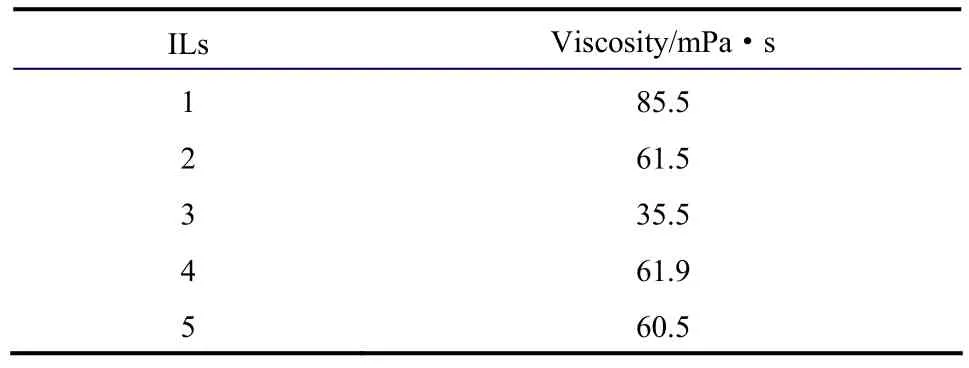
表1 离子液体黏度Table 1 Viscosity of ionic liquids
2.3 离子液体的溶解性
离子液体溶解范围广,亲油或亲水性能可调,因此可以根据离子液体的应用领域对其进行设计。在常温常压下,取一定量的离子液体与适量的有机溶剂,经振荡、剧烈搅拌,研究离子液体与有机溶剂的溶解情况,结果见表 2。醚基功能化离子液体与非极性溶剂不互溶,与极性溶剂相溶,如这类离子液体溶于水却不溶于酯,在酯化反应结束后催化剂和酯自动分层,简化了催化剂与产品的分离。
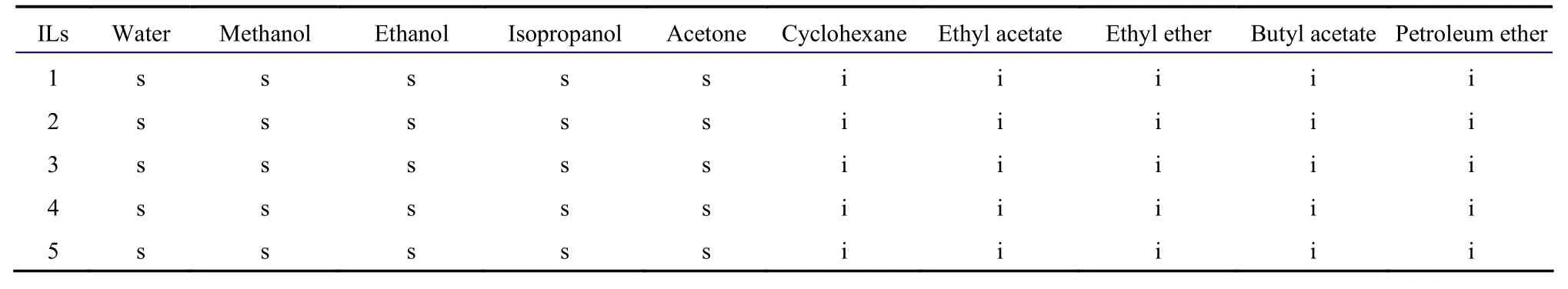
表2 离子液体的溶解性Table 2 Solubility of ionic liquids
2.4 离子液体的酸性
酯化反应催化剂以酸性催化剂为主,催化剂酸性的强弱在一定程度上也关系着催化剂的催化活性。表3为不同浓度下不同离子液体水溶液与浓硫酸水溶液pH的对比。由表3可以看出,在相同浓度的水溶液中离子液体的酸性强弱与浓硫酸相差不大。离子液体有可以与浓硫酸相比的酸性,但没有浓硫酸的脱水性、强氧化性,可有效地减少在催化反应过程中副反应的生成。
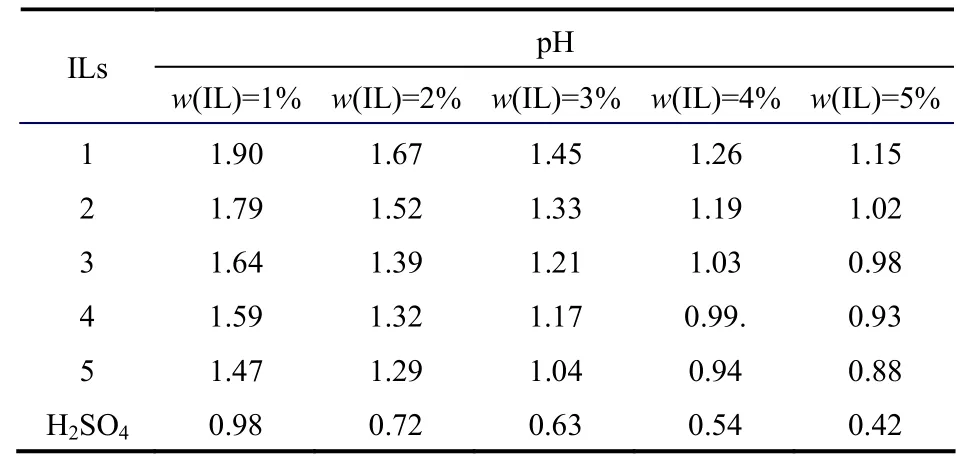
表3 不同离子液体的酸性Table 3 Acidity of various ionic liquids in water
2.5 离子液体的腐蚀性
目前,酯化反应常用催化剂浓硫酸的使用造成了严重的设备腐蚀,高昂的设备维修及更换费用使得腐蚀性成为衡量催化剂安全性和经济性的重要指标。在1 mol正丁醇、1.2 mol冰醋酸、11.9 g环己烷及3.7 g醚基功能化酸性离子液体或浓硫酸的相同酯化条件下,对比316 L不锈钢在醚基功能化离子液体和浓硫酸催化的酯化体系中的腐蚀率,结果见表4。由结果可知,相较于浓硫酸体系,离子液体体系中的钢板质量只有少量的损失,甚至只有浓硫酸腐蚀速度的 1/8以下,腐蚀性弱可以有效地减少设备腐蚀率,延长设备的使用时间,降低成本。
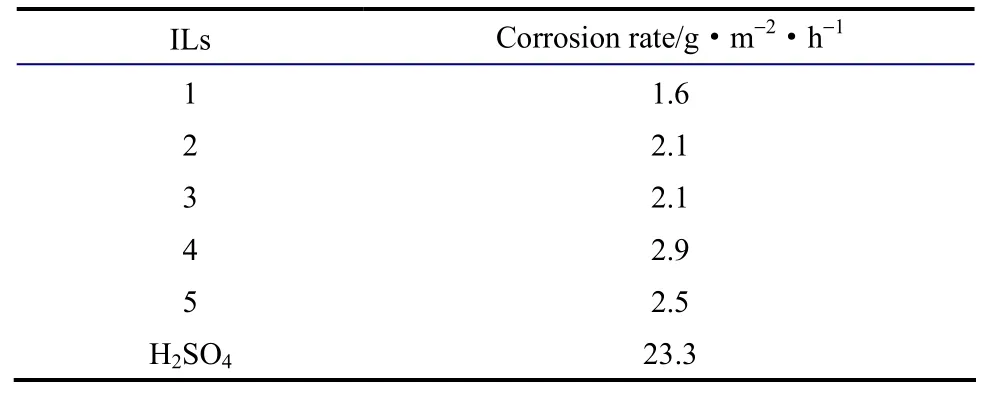
表4 离子液体的腐蚀性Table 4 Corrosion of ILs for Austenitic stainless steel 316 after immersion
2.6 离子液体的催化活性
酯化反应是可逆反应,加入催化剂可以降低反应活化能,加快反应速率。在酸醇摩尔比为1.2:1、带水剂环己烷用量为醇质量的20%、催化剂用量为醇质量的5%条件下,在90℃下反应5 h,催化合成乙酸正丁酯,考察不同离子液体的催化活性,结果见表5。

表5 离子液体的催化活性Table 5 Catalytic activity of ionic liquids
由表5中数据对比可知,离子液体的催化活性与浓硫酸的催化活性相当,而且离子液体的黏度越低,酯化反应收率越高,因为黏度降低可以增加体系的流动性,更有利于反应物间的接触。离子液体的催化活性也是基本随离子液体酸性增加逐渐增长。因此,对于均相的酯化反应,催化剂的黏度、酸性均对催化剂的催化活性有较大的影响。
2.7 响应曲面法优化酯化反应工艺
2.7.1 响应面试验方案设计及结果 采用Design-Expert软件中的Box-Behnken模型对酯化反应中主要工艺条件的相关数据进行分析,用于描述各个因素之间的相互作用对乙酸正丁酯收率的影响。选取酸醇摩尔比、催化剂用量、带水剂用量和反应时间为自变量,以乙酸正丁酯的收率为响应值,进行中心组合实验设计,试验因素和水平设计见表6。以A、B、C和D为自变量,以乙酸正丁酯的收率为响应值,试验方案及结果见表7,其中试验1~24是析因试验,试验25~29 是中心试验,中心试验重复5次,用于估计试验误差。
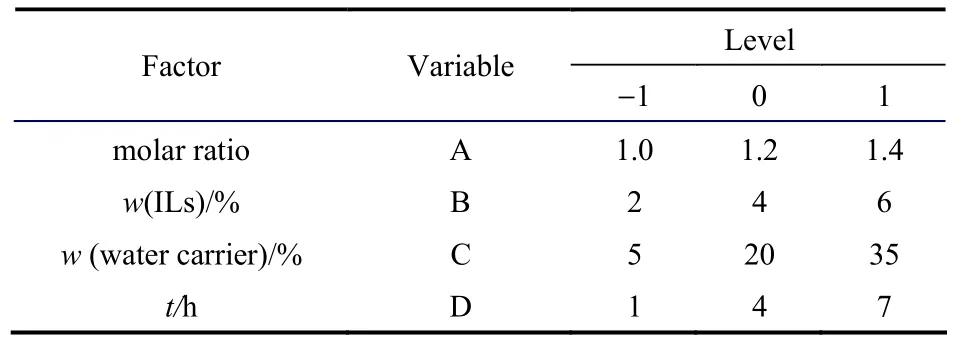
表6 试验设计中各因素的编码水平Table 6 Factors and levels of response surface method
2.7.2 模型的建立与显著性检验 以乙酸正丁酯的收率为响应值,对结果进行方差分析,分析结果见表8。由表8可得,模型的F=54.09,P<0.0001,表明二次回归模型高度显著。实测值与预测值的相关系数为0.9865,说明模型的实际值与预测值拟合较好,自变量与响应值之间的线性关系显著,而且该模型的回归项显著,失拟项不显著。综合多个参数说明该模型合理可靠,自变量与因变量之间关系设计合理,可用该回归模型预测乙酸正丁酯的收率。
由表8中的F值可知,各个因素对酯化反应收率影响的显著次序为催化剂用量>反应时间>带水剂用量>反应物摩尔比,而且反应物摩尔比、催化剂用量和带水剂用量3个因素间交互影响差异极显著。
为更加明确地表示各因素对响应值的影响,得到二次多项回归方程
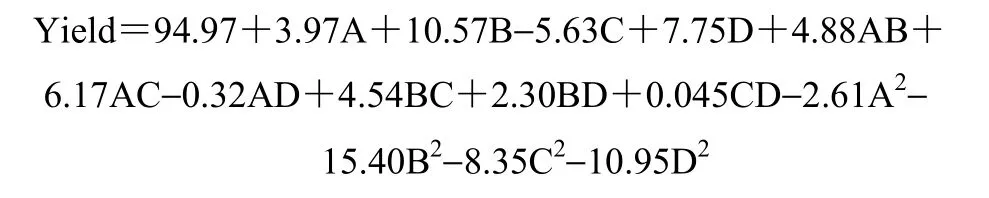

表7 响应面分析结果Table 7 Results of response surface analysis
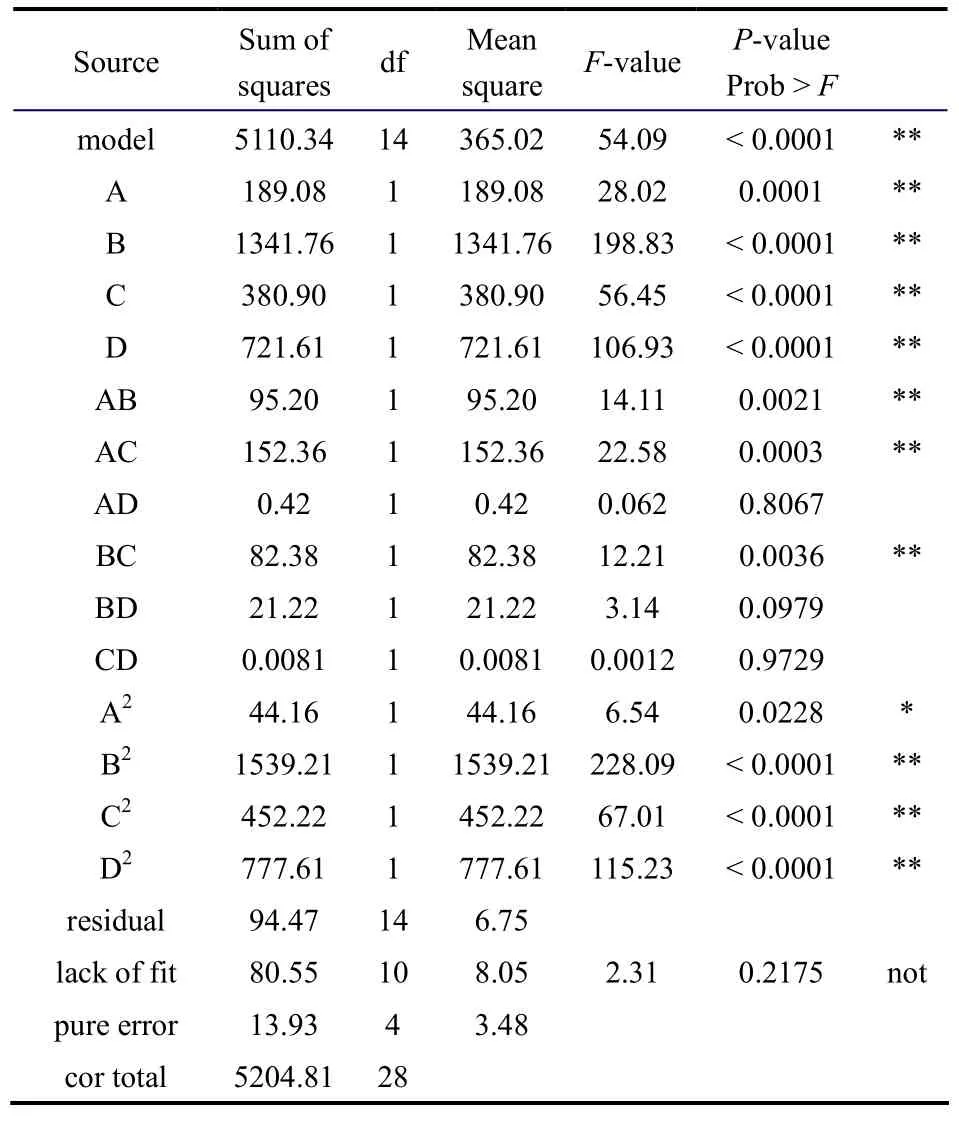
表8 方差分析Table 8 Variance analysis
2.7.3 因素间的交互影响 对 4个因素间的交互作用进行响应面分析,绘制出以酯收率为响应值的趋势图(图3~图8)。等高线图可以直观地反映出2个变量之间的交互作用显著程度,等高线越趋向于扁平的椭圆形说明两因素间的交互作用越大,等高线越趋于圆形说明两因素间的交互作用越小。
由图3可以看出,当酸醇摩尔比一定时,酯收率随催化剂用量增加先增加后趋于平缓;当催化剂用量一定时,酯收率变化并不明显。因此,在乙酸正丁酯的合成中,相较于酸醇摩尔比的改变,催化剂用量的增加对酯收率的影响更为显著,加入催化剂可以降低反应活化能,以加快反应进程。根据等高线图可以看出两因素的交互效应显著,这与方差分析结果相一致。
由图4可以看出,当带水剂用量一定时,改变反应物的摩尔比,乙酸正丁酯的收率先增大后减小,但变化较小;当酸醇摩尔比一定时,增加带水剂的用量,酯收率先增大后减小。两因素相比,带水剂用量对酯化反应收率的影响更大。带水剂可以与水形成共沸,使生成物迅速离开反应体系,不断打破反应平衡,促使反应正向移动。根据等高线图可以看出两因素的交互效应显著,这与方差分析结果相一致。
由图5可以看出,酸醇摩尔比一定时,随着反应时间的增长,乙酸正丁酯的收率逐渐增大,达到一定值后趋于稳定;当反应时间一定时,随着酸醇摩尔比的变化,酯化反应收率先增大后减小。酯收率对两因素的变化都比较明显,两因素的交互作用不显著,与方差分析结果相一致。
由图6可以看出,当带水剂用量一定时,随着催化剂用量的增加,酯收率先增大后趋于平缓;当催化剂用量不变时,增加带水剂用量,酯收率增长明显。催化剂用量和带水剂用量两因素间交互作用显著,这与方差分析结果相一致。
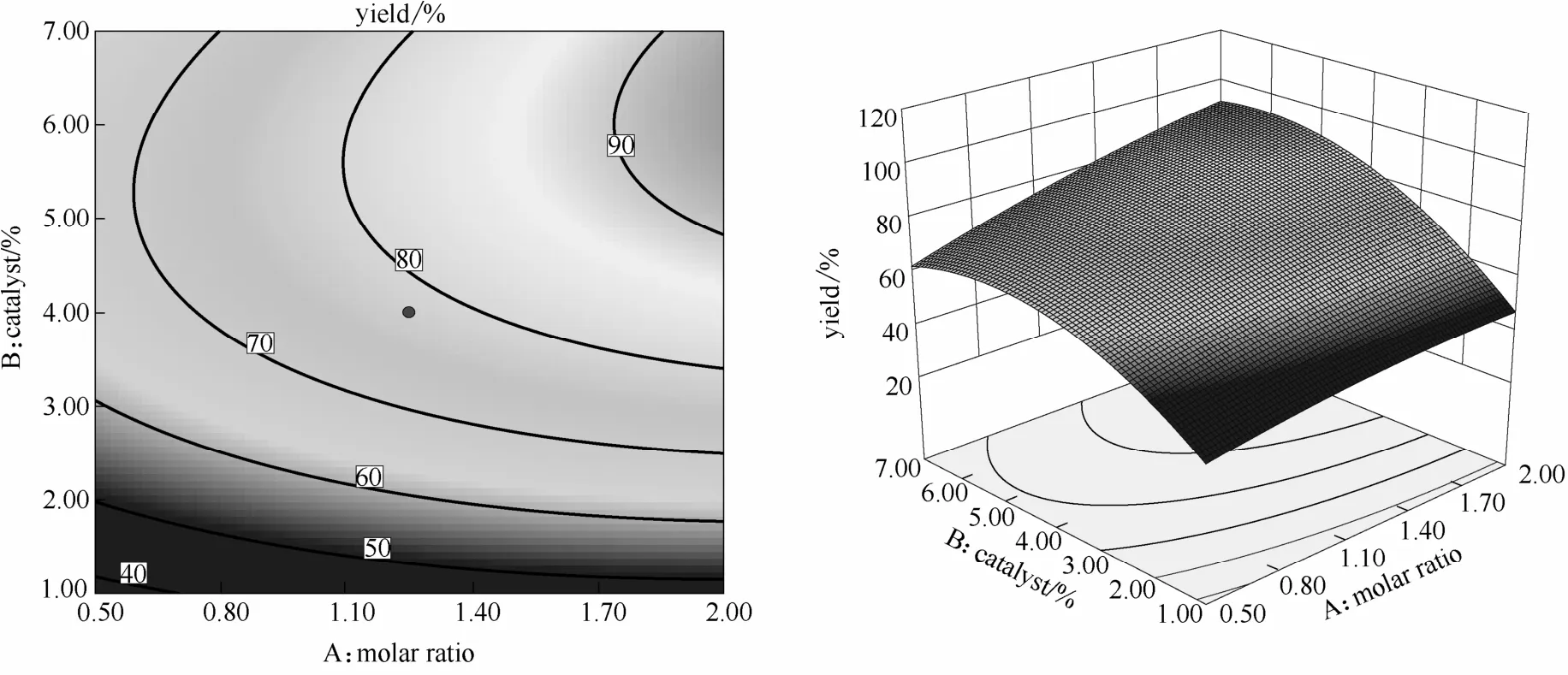
图3 醇酸摩尔比和催化剂用量对酯收率的影响Fig. 3 Response surface plots for effect of molar ratio of reactant and catalyst dosage on esterification rate

图4 酸醇摩尔比和带水剂用量对酯收率的影响Fig.4 Response surface plots for effect of molar ratio of reactant and amount of water carrying agent on esterification rate

图5 醇酸摩尔比和反应时间对酯收率的影响Fig.5 Response surface plots for effect of molar ratio of reactant and reaction time on esterification rate
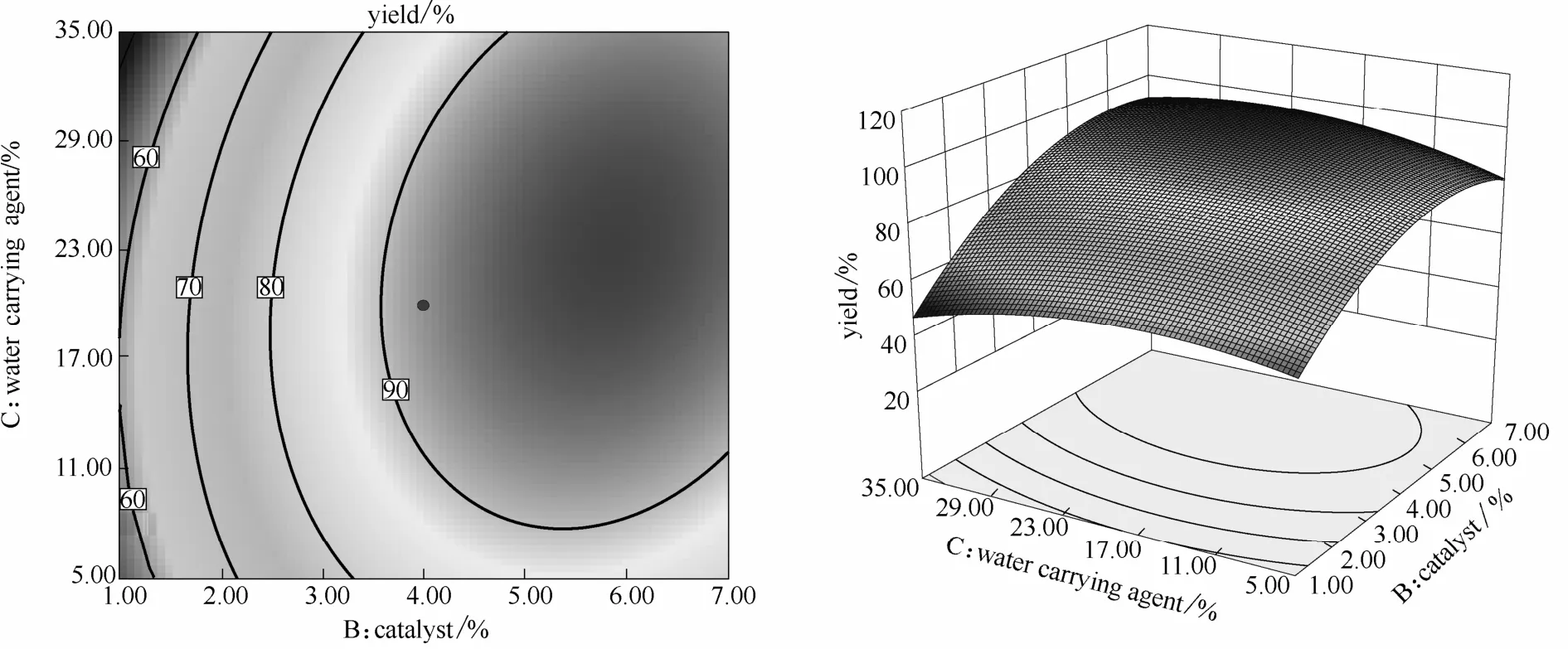
图6 催化剂用量和带水剂用量对酯收率的影响Fig. 6 Response surface plots for effect of catalyst dosage and water carrying agent on esterification rate

图7 催化剂用量和反应时间对酯收率的影响Fig.7 Response surface plots for effect of catalyst dosage and reaction time on esterification rate
由图7可以看出,在催化剂用量一定时,随着反应时间的延长,酯收率增大后趋于稳定;在催化剂用量较大的范围内,反应时间对酯收率的影响也比较小,说明两因素对酯收率的交互作用并不显著,这与方差分析结果相一致。
由图8可以看出,带水剂用量和反应时间两因素的等高线呈圆形,在带水剂用量一定时,随着反应时间的增长,酯收率的增大和减小都比较缓慢,而且变化范围很小,只改变带水剂用量酯收率的变化也很小,证明两因素对酯收率的交互作用不显著,这与方差分析结果相一致。
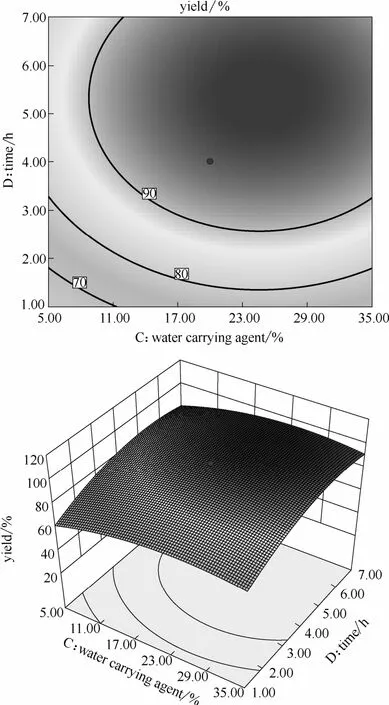
图8 带水剂用量和反应时间对酯收率的影响Fig.8 Response surface plots for effect of water carrying agent and reaction time on esterification rate
2.7.4 最佳工艺条件的确定 根据回归模型的数学分析,以离子液体[2(C3SO3H-MOR)-(OEt)400][2MeSO3]作为催化剂制备乙酸正丁酯,结合回归方程与各因素对乙酸正丁酯收率的影响,得出最优的反应条件为:酸醇摩尔比为1.2:1,催化剂用量为醇质量的4.96%,带水剂用量为醇质量的15.91%,反应时间为5.17 h。在此最优工艺下,预测乙酸正丁酯的收率可达98.67%。
2.8 离子液体的重复使用性
催化剂的使用寿命是其实际应用中的一项重要考察指标,催化剂寿命增加可以降低整个反应的成本。根据响应曲面法得到的最优工艺条件,为方便实际操作,将最佳操作条件定为:酸醇摩尔比为1.2:1,催化剂用量为醇质量的 5%,带水剂用量为醇质量的16%,反应时间为5 h。在此条件下进行3组平行实验,最终的乙酸正丁酯收率为97.8%,与预测结果基本相符。
反应结束后,离子液体与产品分层,将分离出的离子液体在60℃下真空干燥24 h后继续使用。在最优操作条件下重复使用离子液体,酯收率结果如图9所示。离子液体在使用8次后催化活性并没有明显降低。催化活性的下降主要是由于在催化剂回收过程中的质量损失造成的,在催化剂的回收过程中会有微量的离子液体溶解在水中或反应体系中,在分液时会造成离子液体的损失。
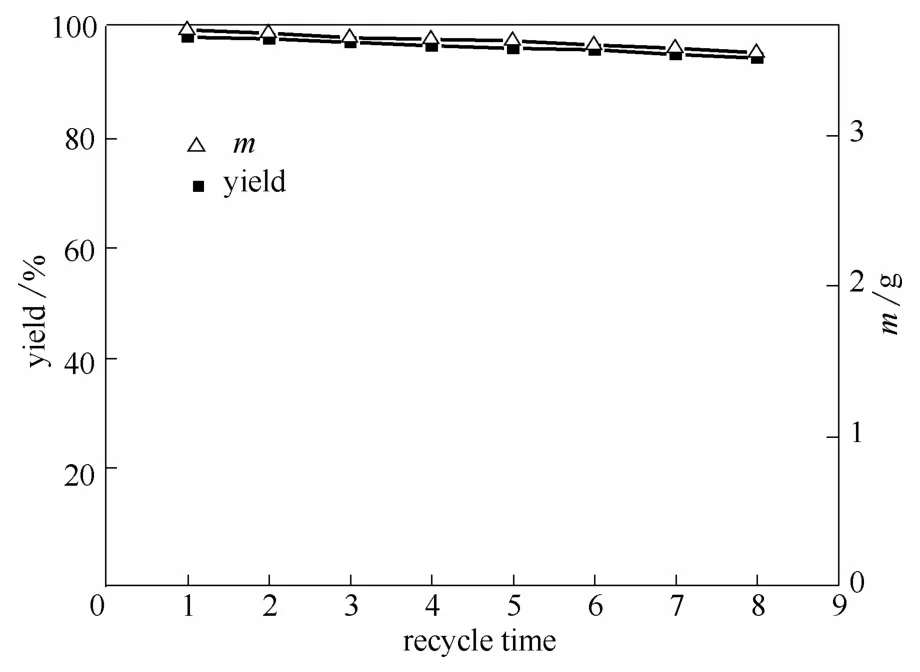
图9 [2(C3SO3H-MOR)-(OEt)400][2MeSO3]重复使用性能Fig. 9 Recycling ability tests of [2(C3SO3H-MOR)-(OEt)400][2MeSO3]
3 结 论
通过烷基化反应,将醚基侧链引入到吗啡啉环上,再引入磺酸基团,由此得到一类新型的醚基磺酸功能化双核酸性离子液体,将其用于催化合成乙酸正丁酯的反应中。此类离子液体黏度小,可以解决离子液体在运输、使用中出现的问题,而且此类离子液体仍具有较高的催化活性,可以保证酯化反应在较为温和的条件下进行,并且重复使用效果好,为酯化反应提供了一种新的催化剂,为酯化反应工艺的优化提供了新的思路。
[1]KIRK O. Encyclopedia of Chemical Technology[M]. New York: Wiley, 1994: 755-780.
[2]ARPORNWICHA A, KOOMSUP K, KIATKITTIPONG W, et al. Production of n-butyl acetate from dilute acetic acid and n-butanol using different reactive distillation systems: economic analysis[J]. J. Taiwan Inst. Chem. Eng., 2009, 40(40): 21-28.
[3]黄世丰, 陈国, 方柏山. 酯化及转酯化法制备生物柴油过程中催化剂的研究进展[J]. 化工进展, 2008, 27(4): 508-514. HUANG S F, CHEN G, FANG B S. Progress of catalysts for producing biodiesel by esterification and transesterification reaction[J]. Chem. Ind. Eng. Prog., 2008, 27(4): 508-514.
[4]李秋荣, 赵倩. 固体超强酸 S2O2-8/TiO2催化合成乙酸正丁酯[J].工业催化, 2006, 14(7): 35-37. LI Q R, ZHAO Q. Synthesis of n-butyl acetate catalyzed by solid S2O2-8/TiO2superacid [J]. Industrial Catalysts, 2006, 14(7): 35-37.
[5]CAO X H, REN J, XU C L, et al. Preparation, characterization of Dawson-type heteropoly acid cerium (Ⅲ) salt and its catalytic performance on the synthesis of n-butyl acetate[J]. Chin. J. Chem. Eng., 2013, 21(5): 500-506.
[6]KUZMINSKA M, BACKOV R, GAIGNEAUX E M. Behavior of cation-exchange resins employed as heterogeneous catalysts for esterification of oleic acid with trimethylolpropane[J]. Appl. Catal. A, 2015, 504(6): 509-518.
[7]CHEN L, YIN P, HU Y C, et al. Optimization of production conditions of n-butyl acetate over NaY supported organophosphonic acid catalyst using response surface methodology[J]. J. Taiwan Inst. Chem. Eng., 2011, 42(5): 768-774.
[8]ESCANDELL J, WURM D J, BELLEVILLE M P, et al. Enzymatic synthesis of butyl acetate in a packed bed reactor under liquid and supercritical conditions[J]. Catal. Today, 2015, 255: 3-9.
[9]WIIKES J S. A short history of ionic liquids-from molten salts to neoteric solvents[J]. Green Chem., 2002, 4(2): 73-80.
[10]SHIRINI F, SEDDIGHI M, MAZLOUMI M, et al. One-pot synthesis of 4,4ʹ-(arylmethylene)-bis-(3-methyl-1-phenyl-1H-pyrazol-5-ols) catalyzed by Brönsted acidic ionic liquid supported on nanoporous Na+-montmorillonite[J]. J. Mol. Liq., 2015, 208: 291-297.
[11]NALE D B, SAIGAONKAR S D, BHANAGE B M. An efficient synthesis of quinazoline-2,4(1H,3H)-dione from CO2and 2-aminobenzonitrile using [Hmim]OH/SiO2as a base functionalized supported ionic liquid phase catalyst[J]. J. CO2Util., 2014, 8(6): 67-73.
[12]UCHYTIL P, SCHAUER J, PETRYCHKOVYCH R, et al. Ionic liquid membranes for carbon dioxide-methane separation[J]. J. Membr. Sci., 2011, 383(1): 262-271.
[13]ALBO J, SANTOS E, NEVES L A, et al. Separation performance of CO2through Supported Magnetic Ionic Liquid Membranes (SMILMs)[J]. Sep. Purif. Technol. 2012, 97(36): 26-33.
[14]WENG W, ZHANG Z C, SCHLUETER J A, et al. Synthesis and electrochemical property of sulfone-functionalized imidazolium ionic liquid electrolytes[J]. Electrochim. Acta, 2013, 92(1): 392-396.
[15]HAYASHI A, MORISHIMA H, TADANAGA K, et al. Characterization of solid electrolytes prepared from ionic glass and ionic liquid for all-solid-state lithium batteries[J]. Solid State Ionics, 2011, 192(192): 126-129.
[16]COLE A C, JENSEN J L, NTAI I, et al. Novel Brönsted acidic ionic liquids and their use as dual solvent-catalysts[J]. J. Am. Chem. Soc., 2002, 124(21): 5962-5963.
[17]王璐璐, 郭王欢, 王吉林,等. 吗啡啉类酸性离子液体的合成及其催化酯化反应[J]. 精细石油化工, 2015, 32(5): 5-9. WANG L L, GUO W H, WANG J L, et al. Synthesis of morpholine acidic ionic liquid and application for esterification reaction[J]. Speciality Petrochemicals, 2015, 32(5): 5-9.
[18]黄宝华, 黎子进, 汪艳飞, 等. Brönsted酸性离子液体催化酯化反应研究[J]. 化学学报, 2008, 66(15): 1837-1844. HUANG B H, LI Z J, WANG Y F, et al. Esterification catalyzed by Brönsted acidic ionic liquids[J]. Acta Chim. Sinica, 2008, 66(15): 1837-1844.
[19]黄宝华, 汪艳飞, 张煜, 等. 吡咯烷酮酸性离子液体的合成及其对酯化反应的催化活性[J]. 催化学报, 2007, 28(8): 743-748. HUANG B H, WANG Y F, ZHANG Y, et al. Synthesis of pyrrolidonium acidic ionic liquids and their catalytic activity foresterification of acetic acid and butanol [J]. Chin. J. Catal., 2007, 28(8): 743-748.
[20]黄宝华, 黎子进, 史娜, 等. 吗啡啉功能化酸性离子液体的合成、表征及其催化酯化性能[J]. 有机化学, 2009, 29(5): 770-775. HUANG B H, LI Z J, SHI N, et al. Functionalized acidic ionic liquid with morpholinium cation: synthesis, characterization and catalysis performance in esterification[J]. Chin. J. Org. Chem., 2009, 29(5): 770-775.
[21]SCHREKKER H S, SILVA D O, GELESKY M A, et al. Preparation, cation-anion interactions and physicochemical properties of ether-functionalized imidazolium ionic liquids[J]. J. Braz. Chem. Soc., 2008, 19(3): 426-433.
[22]DONATO R K, LAVORGNA M, MUSTO P, et al. The role of ether-functionalized ionic liquids in the sol-gel process: effects on the initial alkoxide hydrolysis steps[J]. J. Colloid Interface Sci., 2015, 447: 77-84.
Synthesis of n-butyl acetate by ether-functionalized ionic liquid
HU Tiantian1, ZHAO Dishun1, WU Yu1, ZHANG Shuanli2, HU Shihai2, ZHAI Jianhua1
(1College of Chemical and Pharmaceutical Engineering, Hebei University of Science and Technology, Shijiazhuang 050018, Hebei, China;2Shijiazhuang XinyuSanyang Industrial Co., Ltd., Shijiazhuang 051430, Hebei, China)
Five ether-functionalized ionic liquids (ILs), containing [Me(OEt)1-MOR-C3SO3H][MeSO3], [Me(OEt)2-MOR-C3SO3H][MeSO3], [Me(OEt)3-MOR-C3SO3H][MeSO3], [2(C3SO3H-MOR)-(OEt)200][2MeSO3]and [2(C3SO3H-MOR)-(OEt)400][2MeSO3]were synthesized and characterized by the Fourier transform infrared spectrometer and nuclear magnetic resonance spectrometer . The ionic liquid viscosity, solubility and corrosion were investigated.The promotion effect of ether-functionalized ILs in esterification of acetic acid with butyl alcohol was investigated and the reaction process was optimized using response surface analysis. The yield of n-butyl acetate was up to 97.8% under the optimized conditions: response surface analysis (RSA) of n(CH3COOH):n(C4H9OH)= 1.2:1, the mass of catalyst [2(C3SO3H-MOR)-(OEt)400][2MeSO3]was 5% of the quality of butyl alcohol, the mass of water carrying agent was 30% of the quality of butyl alcohol, temperature was 90℃, and reaction time was 5 h. The catalysts could be recycled for 8 times without obviously decline of catalytic activity.
ether-functionalized; morpholine; ionic liquid; catalysis; esterification; RSA
Prof. ZHAO Dishun, zhao_dsh@hebust. edu.cn
O 643.32
:A
:0438—1157(2017)01—0136—10
10.11949/j.issn.0438-1157.20161017
2016-07-20收到初稿,2016-10-12收到修改稿。
联系人:赵地顺。
:胡甜甜(1991—),女,硕士研究生。
国家自然科学基金项目(20576026, 21106032);石家庄市科学技术研究与发展计划资助项目(161070251A)。
Received date: 2016-07-20.
Foundation item: supported by the National Natural Science Foundation of China (20576026, 21106032) and the Shijiazhuang Science Technology Research and Development Program(161070251A)。

