核-壳光催化剂Cu-CdS@C3N4的制备及其性能研究
江珍珍,郑晋生,王 晟
(浙江理工大学先进纺织材料与制备技术教育部重点实验室,杭州 310018)
核-壳光催化剂Cu-CdS@C3N4的制备及其性能研究
江珍珍,郑晋生,王 晟
(浙江理工大学先进纺织材料与制备技术教育部重点实验室,杭州 310018)
以商业CdS粉末为原料,以硝酸铜(CuNO3)为铜源,在NaOH溶液的溶剂中通过水热法合成Cu2+掺杂六方相CdS微米棒,并在其表面包覆一层C3N4以制备得到一种具有核壳结构的光催化剂Cu-CdS@C3N4。利用SEM、TEM、XRD、UV-Vis、FT-IR等测试手段对其形貌结构及相关性能进行表征,并使用亚甲基蓝(MB)溶液作为目标污染物,通过改变Cu2+的掺杂量和包覆C3N4的比率,研究Cu-CdS@C3N4光催化性能。实验结果表明:当Cu2+掺杂量为10 wt%,包覆的C3N4量为20 wt%时,可得到形貌规整且光催化性能最佳的可见光催化剂。
可见光催化;水热法;Cu2+掺杂;核-壳光催化剂
0 引 言
在高科技迅猛发展的今天,人们日益关注工业生产和生活污染物的清除,利用光催化技术降解污染物成为近年来研究的热点。由于可见的太阳光取之不尽,用之不竭且绿色无污染,因此深受人们的青睐。如何高效地利用自然光进行光催化反应,开发能够被可见光激发的光催化剂正日益引起人们的兴趣[1]。
半导体光催化剂具有强氧化性、污染物矿化完全、可直接利用太阳光等优点,近年来该类催化剂研究取得了较大进展[2-3]。CdS是一种重要的Ⅱ-Ⅵ族半导体材料,其禁带宽度在室温下为2.42 eV,表现出良好的光学性质和光电特性,被广泛应用于光、磁、电、催化等领域。近年来,CdS材料在物理学、化学、材料学和生物医学等多学科引发关注的热点[4]。目前有众多关于CdS材料的各种形貌的报道,如球[5]、纳米管[6]、纳米线[7]、纳米棒[8]和花状[9]等。此外,虽然CdS被认为是一种优秀的可见光催化剂,但是也存在光腐蚀问题[10-11]。近年来,很多方法被研发用来提高CdS的光催化活性以及光稳定性,如将CdS与高分子的杂化[12]、与其他纳米材料的杂化[3]、金属离子的掺杂[13]等等。其中利用离子掺杂可以使CdS催化剂的禁带宽度变小,同时还可以扩大材料对可见光区的利用范围,从理论上可使得CdS催化剂具备更好的可见光光催化活性,因此日益受到研究者的青睐。例如,Yang等[13]利用Zn掺杂水热合成的CdS微米球,在摩尔比Zn∶Cd=1∶10时比纯CdS的光催化性能与光稳定性更好。Li等[14]用微波合成法制备出ZnxCd1-xS纳米棒,其中Zn0.28Cd0.72S的样品在可见光光照下降解甲基橙的能力远超过纯CdS和 P25。除了锌之外,还有其他金属如铂[15]、金[16],也都被尝试掺杂到CdS光催化剂中,都能获得增强的光催化性能和稳定性。
目前,一维 CdS 微米材料已经实现了多种方法合成,如Peng等[17]通过电化学沉积的方法合成了CdS微米管;Cao等[7]用阳极Al2O3为模板通采用溶胶-凝胶法(Sol-Gel) 制得CdS 纳米线;Soumitra Kar等[18]利用硅片作为基底制备出定向生长的CdS微米线。在熟知的众多试验方法中,溶剂热法因为有着合成工艺简单、可批量化生产的潜质,更加受到关注。通常用有机胺类如乙二胺、十二烷胺等作为溶剂热法中的溶剂,钱逸泰课题组在这方面做了深入的研究[19-21]。Jun等[22]在十六胺中热分解单一分子前驱体Cd(S2CNEt2)2,制得了多壁 CdS 纳米棒;Li等[4]以乙二胺为溶剂通过溶剂热的方法合成了CdS微米棒,然而有机胺类有毒性且价格不便宜,难以实现工业化生产。所以对于研究一种成本低廉CdS 光催化剂材料制备方法意义重大。衣晓凤等[23]利用NaOH溶液水热生长合成CdS光催化剂既简单又环保。
本文基于NaOH溶液合成CdS 微米棒的方法,以商业CdS粉末为原料,在NaOH溶液的溶剂中通过水热生长法一步合成六边棱柱状的六方相CdS微米棒。探索NaOH溶液的浓度对其形貌影响,在此基础上,成功实现Cu掺杂提高其光催化性能,同时在CdS表面包覆C3N4形成核-壳结构光催化剂Cu-CdS@C3N4。Cu掺杂提高了CdS的可见光吸收范围,而C3N4的包覆,在减少CdS光腐蚀的同时,三者之间的协同效应使复合物光催化剂获得了增强的可见光活性以及循环稳定性。为开发高效、环保CdS基可见光催化剂提供了有效的制备方案。
1 实验部分
1.1 实验试剂
硫化镉(CdS,95%,上海金山亭新化工试剂厂),氢氧化钠(NaOH,98%~100.5%,阿拉丁),硝酸铜(CuNO3,AR,天津市永大化学试剂有限公司),单氰胺(CH2N2,99%,阿拉丁),P25(TiO2,AR,德国Degussa公司),无水乙醇(C2H5OH,99.7%,国药集团化学试剂有限公司),亚甲基蓝(MB,上海三爱思试剂有限公司);实验用水为二次蒸馏水。
1.2 实验仪器
XPA-2光化学反应仪(南京胥江机电厂,500 W氙灯,插入滤光片,滤掉波长在420 nm以下的光源),SXL-1008马弗炉(上海精宏实验设备有限公司),S-4800发射扫描电子显微镜(FESEM,HITACHI),TEM -2010(HR)透射电子显微镜(日本电子公司),Bruker D8X X射线粉末衍射仪(XRD,美国热电ARL公司),INGA-Energy 200电子能谱(EDS,英国 Oxford 公司),LAMBDA 900紫外分光光度计(美国PERKIN ELMER公司),NICOLET 5700 傅立叶红外光谱仪(美国热电公司)。
1.3 表征与测试
使用S-4800发射扫描电子显微镜观察光催化剂的微观形貌;采用TEM-2010(HR)透射电子显微镜进一步观察光催化剂的微观形貌;采用Bruker D8X X射线粉末衍射仪测定不同光催化剂晶型;使用INGA-Energy 200电子能谱分析光催化剂中的元素;采用LAMBDA 900紫外分光光度计测试光催化剂的光催化性能,并以KBr为背景测得样品的紫外-可见漫反射光谱;采用NICOLET 5700 傅立叶红外光谱仪以KBr为背景测得样品的红外光谱图。
1.4 Cu-CdS微米复合材料的制备
首先根据已有文献[23]中的实验方案将0.2 g CdS 粉末投入15 mL 一定浓度的NaOH溶液中(浓度依次取10、12、16、20 M),充分搅拌。待CdS粉末与NaOH溶液混合均匀后,将其倒入带有对位聚苯(PPL)内衬的不锈钢反应釜中,置于 240 ℃下分别反应48 h。反应釜自然冷却后将产物用蒸馏水和无水乙醇多次洗涤、过滤。将洗涤过滤后的产物置于80 ℃的烘箱中干燥5 h。
称量0.2 g CdS、适量的CuNO3(含量依次取0、5、10、15 wt%)及DTA-Na (EDTA-Na作为络合剂CuNO3∶EDTA=1∶1)投入盛有15 mL 20 M NaOH溶液的PPL反应釜内衬中,接下来的操作和上面相同。称量0.2 g CdS、10 wt% CuNO3、10 wt% EDTA-Na (EDTA-Na作为络合剂CuNO3∶EDTA=1∶1)投入盛有15 mL 20 M NaOH溶液的PPL反应釜内衬中,接下来的操作和前面相同。
1.5 Cu-CdS@C3N4复合光催化剂的制备
称取一定量的CH2N2放入方形刚玉坩埚中,在500℃的马弗炉中煅烧4 h 得到C3N4,称取适量C3N4投入20 mL甲醇溶液中超声2 h,再加入制备好的0.2 g Cu-CdS超声3 h,搅拌20 h。 C3N4的含量依次取10、20、30、50 wt%分别记为Cu0.1Cd0.9S@C3N4-10、Cu0.1Cd0.9S@C3N4-20、Cu0.1Cd0.9S@C3N4-30、Cu0.1Cd0.9S@C3N4-50。
1.6 Cu-CdS@C3N4复合光催化剂降解亚甲基蓝
采用可见光光催化降解目标污染物亚甲基蓝溶液,可见光光催化降解使用的亚甲基蓝溶液的浓度为5 mg/L,使用500 W氙灯作为反应光源(插入滤光片,滤掉波长在420 nm以下的光源)。测试亚甲基蓝溶液降解的吸光度来评价Cu-CdS@C3N4光催化剂的可见光光催化活性。将15 mg P25、纯CdS、Cu-CdS、及Cu0.1Cd0.9S@C3N4复合物分别加入20 mL的亚甲基蓝溶液中,遮光搅拌30 min,超声分散15 min,使均匀分散。用500 W氙灯进行催化降解,反应时每隔一段时间取样,离心后取上清液在紫外-可见分光光度计下测其吸光度。
2 结果与讨论
2.1 产物形貌表征
不同浓度NaOH溶液中生长得到的CdS形貌如图1所示,从图中可以看出生成的CdS均为棒状形貌,且随着NaOH溶液浓度的增大,CdS微米棒的形貌逐渐规整。如图1(a-b)所示,在浓度为10 M和12 M的 NaOH溶液中所制备的CdS微米棒直径大小不一(50~400 nm),而当NaOH溶液的浓度为16 M 时可得到形貌规整,大小均一的棒状结构,其直径规整至400 nm 左右,如图1(c)。当NaOH溶液的浓度进一步提高到20 M时,如图1(d),微米棒的尺寸再次变得不均一,尺寸分布在400~800 nm。因此,后续实验选取16 M为Cu掺杂CdS的最佳制备浓度。

图1 不同NaOH浓度中制备的CdS微米棒的扫描电镜图
图2为Cu2+掺杂及包覆C3N4后CdS微米棒的扫描电镜图和透射电镜图。实验中,以不同比重的Cu2+掺杂,以提高CdS微米棒光催化性能。掺杂过程中,当CdS微米棒形貌受到破坏时,其光催化稳定性将受到影响。如图2(a)、图2(b),当铜掺杂量为5 wt%和10 wt%时,CdS微米棒基本没有破损,而当Cu2+的掺杂量达15 wt%时,CdS微米棒的形貌已被破坏。图2(d)是Cu2+的掺杂量10 wt%时,包覆C3N4的CdS 微米棒SEM图,图中因C3N4包覆量小,因此很难看出。但在图2(e)的透射电镜照片中,可以明显看出C3N4包覆层,其厚度约10 nm。经C3N4包覆,不仅可以提高CdS微米棒的光催化性能,增强其光催化稳定性,减少光腐蚀,而且还可减小剧毒CdS引起的潜在伤害。图2(f)为高倍镜的TEM图,图中CdS微米棒的晶格条纹清晰可见,其晶面间距约0.67 nm左右。

图2 16 M NaOH溶液反应液所获得的不同掺杂比率的Cu-CdS的扫描电镜图和透射图
2.2 EDS分析
不同光催化剂的X射线能谱(EDS)图如图3所示。图3(a)中,除去硅片产生的Si原子外,所制CdS微米棒仅含有Cd和S原子。而图3(b)和3(c)中分别出现了Cu原子、C原子和N原子,表明实验成功实现了Cu2+掺杂和C3N4包覆。

图3 不同光催化剂的X射线能谱图
2.3 XRD分析
不同催化剂样品的X射线衍射谱见图4。从图4中可以看出,用水热法合成的CdS光催化剂的特征峰值2θ分别为24.80°、26.50°、28.18°、36.62°、43.18°、47.83°、50.88°、51.82°、52.79°、54.58°、58.27°、60.83°、66.77°和69. 26°,与之对应的晶面值为(100)、(002)、(101)、(102)、(110)、(103)、(200)、 (112)、(201)、(004)、(202)、(104)、(203)和(210),各个衍射峰与CdS标准卡片一致。图中的衍射峰高且尖锐,说明CdS的结晶度很高,其中(002)晶面相对峰值远低于(100)和(101)晶面,这是因为 CdS 微米棒择优在[001]方向沿c轴生长。当掺杂Cu2+之后,结晶完好性略有越低,表现为XRD谱线相对峰值稍稍降低,(002)面的相对峰值升高。
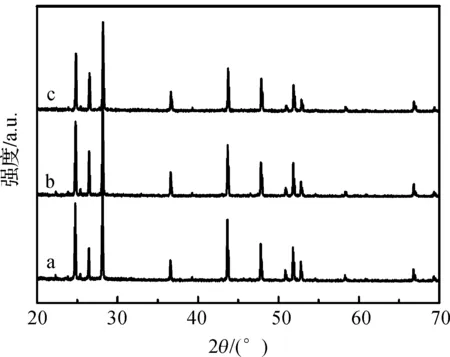
图4 不同催化剂样品的X射线衍射谱图:(a. CdS微米棒, b. Cu0.05Cd0.95S复合物微米棒, c. Cu0.1Cd0.9S@C3N4-20复合物微米棒)
2.4 红外光谱及紫外可见漫反射光谱分析
Cu-CdS@C3N4复合物微米棒的红外光谱图如图5所示,纯C3N4有三个特征吸收峰,其中小于1000 cm-1的吸收峰源于N-H键的拉伸振动,1200~1700 cm-1吸收峰是由于碳氮杂环化合物的拉伸振动,而三嗪的收缩振动在800 cm-1左右出现了吸收峰。上述三个峰表明在以C3N4包覆的过程中,C3N4并没有发生结构变化。
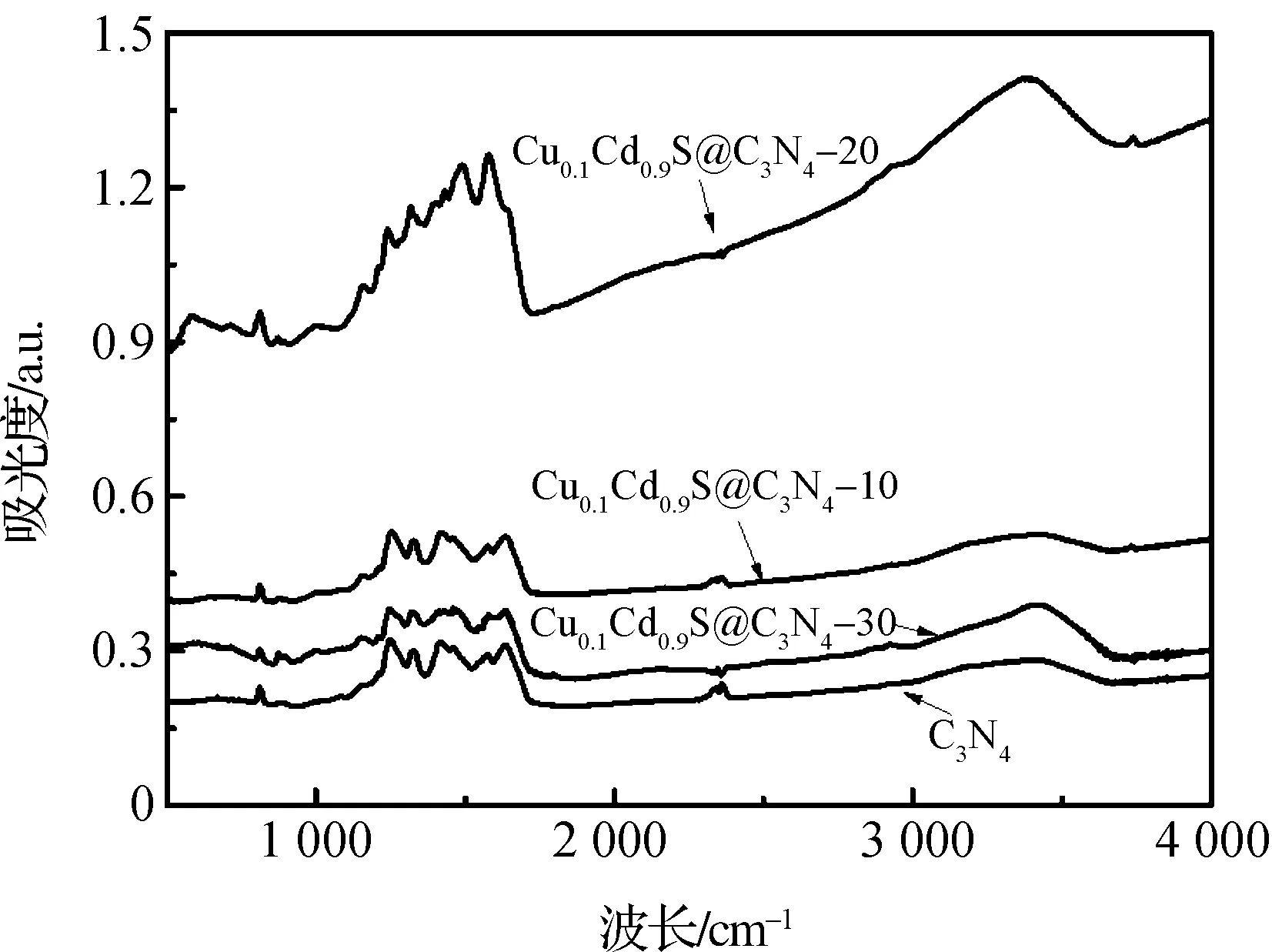
图5 纯C3N4以及Cu-CdS@C3N4复合物微米棒的红外光谱图
图6分别为纯C3N4,Cu0.1Cd0.9S,和包覆不同C3N4量的样品的紫外可见漫反射光谱图。纯C3N4样品的基本吸收边缘在460 nm左右。在掺杂Cu2+后,Cu-CdS复合物吸收边缘发生红移,对可见光区的吸收有所增强。这是因为铜离子掺杂使硫化镉催化剂的禁带宽度变小,增大了对应的最大激发波长,即掺杂扩大了光催化剂对可见光区的利用范围。在包覆C3N4时,随着包覆C3N4量的增加,其吸收强度呈现先增大后减小的趋势,研究表明复合材料Cu0.1Cd0.9S@C3N4-20吸收峰值达到最高。
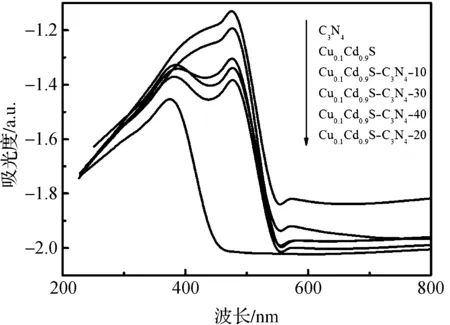
图6 纯C3N4和不同包覆量的Cu-CdS@C3N4复合材料的紫外可见漫反射图谱
3 光催化活性分析
不同催化剂在可见光下对MB溶液的降解效果列于图7中。经可见光照射120 min后,加入P25催化剂MB浓度降低约为70%。相比P25,纯CdS,Cu0.1Cd0.9S,Cu0.1Cd0.9S&C3N4,Cu0.1Cd0.9S@C3N4催化剂的可见光光催化效果很明显。2 h光照后,CdS、Cu0.1Cd0.9S&C3N4、Cu0.1Cd0.9S、Cu0.1Cd0.9S@C3N4-20对MB的降解率分别达到75%、80%、90%、100%。其中,Cu0.1Cd0.9S@C3N4-20样品可见光催化性能最好。

图7 同光催化剂降解亚甲基蓝(MB)的紫外可见吸收光谱图(可见光照射λ>450 nm),催化剂用量:15 mg, MB溶液:5 mg/L, 20 mL)。
上述结果证明Cu0.1Cd0.9S@C3N4-20复合材料是一种有效的可见光催化剂。鉴于实际应用对光催化剂催化稳定性的需求,图8进行了纯CdS和Cu0.1Cd0.9S@C3N4-20复合材料光降解循环测试。很明显,由于CdS的光腐蚀性,纯CdS光催化性能是非常不稳定的,其光催化活性在循环周期中呈现逐步衰减的现象。经过4次循环后,纯CdS光催化能力下降到40%左右。然而,Cu0.1Cd0.9S@C3N4-20复合材料在经过4个周期后,其光催化活性没有明显降低,表明包覆C3N4后,复合材料光催化稳定性明显提高。
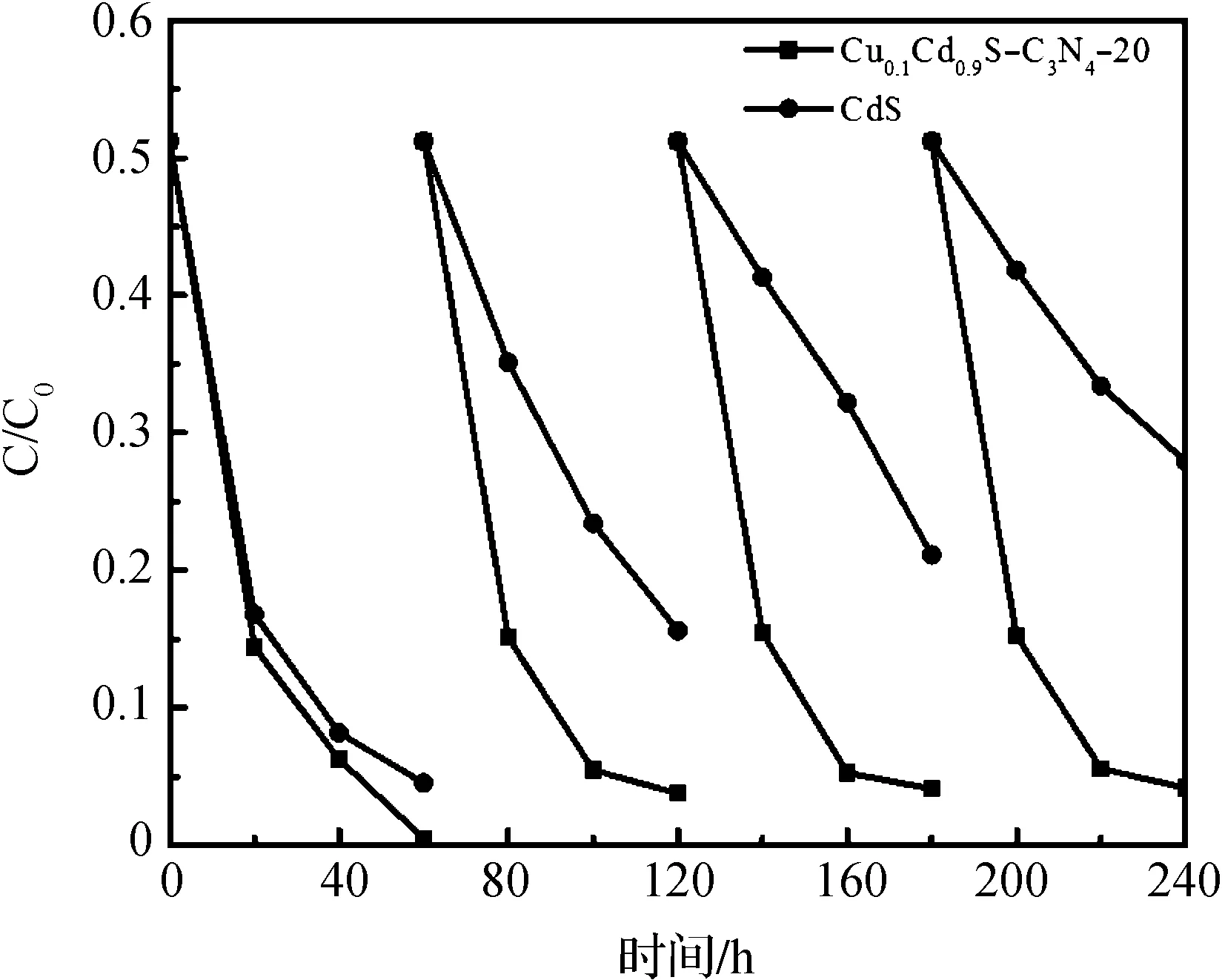
图8 纯CdS和Cu0.1Cd0.9S@C3N4-20光催化降解MB的速率曲线。
4 结 论
本文在NaOH溶液中,以水热法合成核-壳结构光催化剂CdS@C3N4。研究表明,NaOH溶液浓度为16 M时,所得CdS微米棒形貌规整、结晶度高。在此基础上,成功实现了Cu2+掺杂及C3N4对CdS微米棒的包覆,且发现当掺铜量为10 wt%,C3N4包覆量为20 wt%时,可得到形貌规整,光催化性能良好的光催化微米棒复合物。光催化降解MB的实验证明,Cu2+掺杂提高了CdS的可见光波长吸收范围,而C3N4的包覆,在减少CdS光腐蚀的同时,三者之间的协同效应使复合物光催化剂获得了增强的可见光活性以及循环稳定性。上述研究结果为开发高效、环保CdS基可见光催化剂提供了有效的技术支撑。
[1] 陈崧哲,张彭义,祝万鹏,等.可见光响应光催化剂研究进展[J].化学进展,2004,16(4):613-619.
[2] KLIMOV V I, IVANOV S A, NANDA J, et al. Single-exciton optical gain in semiconductor nanocrystals[J]. Nature,2007,447(7143):441-446.
[3] BAEK S W, SHIM J H, SEUNG H M, et al. Effect of core quantum-dot size on power-conversion-efficiency for silicon solar-cells implementing energy-down-shift using CdSe/ZnS core/shell quantum dots[J]. Nanoscale,2014,6(21):12524-12531.
[4] LI Y, HU Y, PENG S, et al. Synthesis of CdS nanorods by an ethylenediamine assisted hydrothermal method for photocatalytic hydrogen evolution[J]. The Journal of Physical Chemistry C,2009,113(21):9352-9358.
[5] BAO N, SHEN L, TAKATA T, et al. Self-templated synthesis of nanoporous CdS nanostructures for highly efficient photocatalytic hydrogen production under visible light[J]. Chemistry of Materials,2007,20(1):110-117.
[6] JIMMY C. Photochemical growth of cadmium-rich CdS nanotubes at the air-water interface and their use in photocatalysis[J]. Journal of Materials Chemistry,2009,19(37):6901-6906.
[7] CAO S, LOW J, YU J, et al. Polymeric photocatalysts based on graphitic carbon nitride[J]. Advanced Materials,2015,27(13):2150-2176.
[8] AN X, YU X, JIMMY C Y, et al. CdS nanorods/reduced graphene oxide nanocomposites for photocatalysis and electrochemical sensing[J]. Journal of Materials Chemistry A,2013,1(16):5158-5164.
[9] HU Y, GAO X, YU L, et al. Carbon‐Coated CdS Petalous Nanostructures with Enhanced Photostability and Photocatalytic Activity[J]. Angewandte Chemie,2013,125(21):5746-5749.
[10] ZHANG J, WANG Y, JIN J, et al. Efficient visible-light photocatalytic hydrogen evolution and enhanced photostability of core/shell CdS/g-C3N4nanowires[J]. ACS Applied Materials & Interfaces,2013,5(20):10317-10324.
[11] FU J, chANG B, TIAN Y, et al. Novel C3N4-CdS composite photocatalysts with organic-inorganic heterojunctions:in situ synthesis, exceptional activity, high stability and photocatalytic mechanism[J]. Journal of Materials Chemistry A,2013,1(9):3083-3090.
[12] ZHANG H, ZHU Y. Significant visible photoactivity and antiphotocorrosion performance of CdS photocatalysts after monolayer polyaniline hybridization[J]. The Journal of Physical Chemistry C,2010,114(13):5822-5826.
[13] YANG F, YAN N N, HUANG S, et al. Zn-doped CdS nanoarchitectures prepared by hydrothermal synthesis:mechanism for enhanced photocatalytic activity and stability under visible light[J]. The Journal of Physical Chemistry C,2012,116(16):9078-9084.
[14] LI W, LI D, ZHANG W, et al. Microwave synthesis of ZnxCd1-xS nanorods and their photocatalytic activity under visible light[J]. The Journal of Physical Chemistry C,2010,114(5):2154-2159.
[15] CONCA E, ARESTI M, SABA M, et al. Charge separation in Pt-decorated CdSe@CdS octapod nanocrystals[J]. Nanoscale,2014,6(4):2238-2243.
[16] LIU S, XU Y J. Efficient electrostatic self-assembly of one-dimensional CdS-Au nanocomposites with enhanced photoactivity, not the surface plasmon resonance effect[J]. Nanoscale,2013,5(19):9330-9339.
[17] PENG T, YANG H, DAI K, et al. Fabrication and characterization of CdS nanotube arrays in porous anodic aluminum oxide templates[J]. Chemical Physics Letters,2003,379(5):432-436.
[18] KAR S, CHAUDHURI S. Shape selective growth of CdS one-dimensional nanostructures by a thermal evaporation process[J]. The Journal of Physical Chemistry B,2006,110(10):4542-4547.
[19] LI B, XIE Y, HUANG J, et al. Solvothermal synthesis to NiE2 (E= Se, Te) nanorods at low temperature[J]. Nanostructured Materials,1999,11(8):1067-1071.
[20] YANG J, ZENG J H, YU S H, et al. Formation process of CdS nanorods via solvothermal route[J]. Chemistry of Materials,2000,12(11):3259-3263.
[21] LI Y, LIAO H, DING Y, et al. Solvothermal elemental direct reaction to CdE (E= S, Se, Te) semiconductor nanorod[J]. Inorganic Chemistry,1999,38(7):1382-1387.
[22] JUN Y, LEE S M, KANG N J, et al. Controlled synthesis of multi-armed CdS nanorod architectures using monosurfactant system[J]. Journal of the American Chemical Society,2001,123(21):5150-5151.
[23] 衣晓凤,郑晋生,赵一兵.NaOH溶液中CdS微米棒的水热合成[J].高等学校化学报,2012,(12):2597-2603.
(责任编辑: 唐志荣)
Preparation of Core-Shell Photocatalyst Cu-CdS@C3N4and Study on Its Performance
JIANGZhenzhen,ZHENGJinsheng,WANGSheng
(Key Laboratory of Advanced Textile Materials and Manufacturing Technology, Ministry of Education, Zhejiang Sci-Tech University, Hangzhou 310018, China)
Cu2+-doped CdS microrods (Cu-CdS) were prepared via hydrothermal method by using CdS and Cu(NO3)2as raw material and copper source respectively in NaOH solution. Then, Cu-CdS was coated with a layer of C3N4to produce a visible-light photocatalyst with core-shell structure Cu-CdS@C3N4. The morphology, structure and relevant performance of Cu-CdS@C3N4composites were characterized by SEM, TEM, XRD, UV-Vis and FT-IR. Besides, methylene blue (MB) solution was used as the target pollutant to study photocatalytic performance of Cu-CdS@C3N4by changing doping content of Cu2+and the ratio of coated C3N4. The experimental results reveal that the visible-light photocatalysis with regular morphology and optimal photocatalytic performance could be gained under the following conditions: doping content of Cu2+10 wt% and amount of coated C3N420 wt%.
visible-light photocatalysis; hydrothermal method; Cu2+doping; core-shell photocatalyst
10.3969/j.issn.1673-3851.2017.01.05
2016-04-22
日期: 2017-01-03
国家自然科学基金项目(51372227)
江珍珍(1991-),女,安徽桐城人,硕士研究生,主要从事纳米催化剂方面的研究。
王 晟,E-mail:wangsheng571@hotmail.com
O611.2
A
1673- 3851 (2017) 01- 0024- 07

