水提取法对游离烟碱测定的研究*
魏建科,赖东辉,毛寒冰,罗 熹,王加忠,刘 剑,马云飞,杨 承
(1贵州中烟工业有限责任公司技术中心,贵州 贵阳 550009;2 贵州铜仁烟草公司德江分公司,
贵州 铜仁 565200)
水提取法对游离烟碱测定的研究*
魏建科1,赖东辉1,毛寒冰1,罗 熹1,王加忠1,刘 剑1,马云飞2,杨 承2
(1贵州中烟工业有限责任公司技术中心,贵州 贵阳 550009;2 贵州铜仁烟草公司德江分公司,
贵州 铜仁 565200)
主要研究水提取-气相色谱法对烟草中游离烟碱的测定。首先对游离烟碱测定的内标、提取时间与萃取溶剂等进行优化,确定内标、提取时间与萃取溶剂分别为正十六烷、30 min和三氯甲烷。通过基质加标、缓冲液模拟等实验,找到了观测回收率偏低的原因。最后比较了水提取法与pH计算法测定游离生物碱的差异,结果表明:绝对含量差异较大,但二者线性相关系数达到0.950(极显著水平),说明方法之间有较好的一致性。
水提取法;游离烟碱;气相色谱;pH计算法
烟碱是烟草中特有的物质之一,是通过氮代谢途径由吡咯烷环与烟酸结合形成的生物碱类物质。在烟草中一般以游离态、单质子态和双质子态三种形式存在[1],如图1所示。
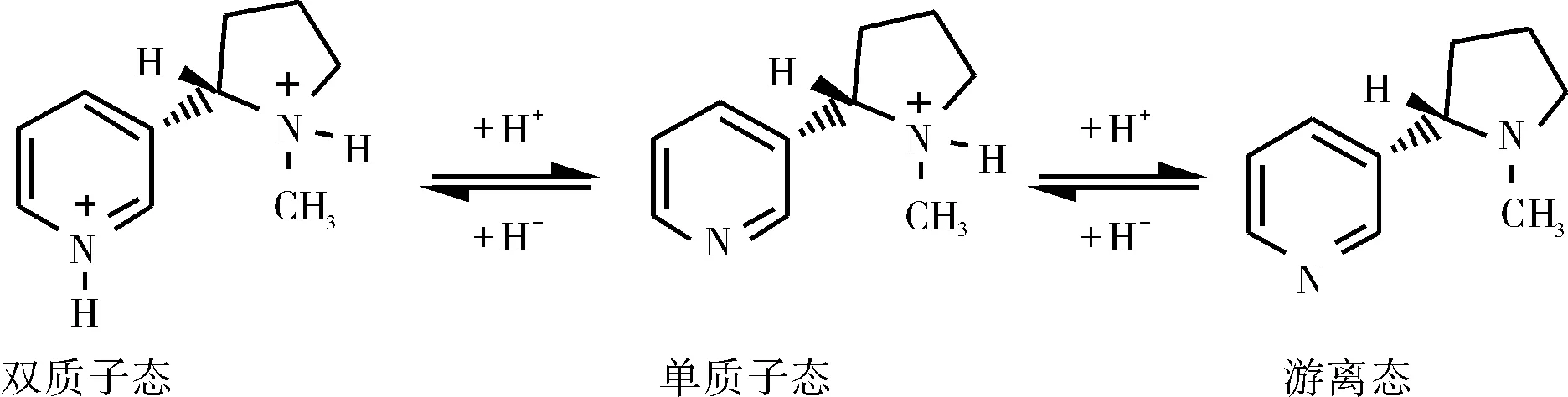
图1 烟碱各形态之间的转换关系及结构
吸烟者的依赖性与烟草及主流烟气中的烟碱含量有关,且与其中的游离态烟碱关系更为密切。这是因为非质子化的游离烟碱挥发性特别强,主要存在于烟气的气相中,且由于其亲脂特性,游离烟碱能被人体快速的吸收,从而刺激中枢神经。因此,已有研究表明游离烟碱是导致吸烟者产生依赖性的主要原因之一[2-3]。因此,对烟草中的游离烟碱进行定量分析显得尤为重要。
由于烟草中的烟碱与阴离子形成的盐均为极易分解的弱酸弱碱盐,组成比例与pH值密切相关,且烟草本身足一个复杂的非均相体系,所以提取技术成为烟草游离烟碱测定的关键点,且萃取方法不同,测定结果也各异,因此,非常有必要对测定方法进行深入的研究。现有测定烟草中游离烟碱的方法主要是水溶液提取-色谱法[4],有机溶剂提取-紫外分光光度计法[5],固相微萃取-色谱法[6]与pH值计算法[7]。有机溶剂提取-紫外分光光度计法需要分别测定总烟碱与结合态烟碱,二者之差得到游离烟碱的含量。该方法需要对样品测定2次,操作步骤较多,耗时较长。固相微萃取方法由于易受烟末或烟丝的大小、烤烟水分含量等条件的影响,导致不同实验室之间的数据差异较大,稳定性较差。因此,本研究主要对水溶液提取-色谱法进行研究,深入分析观测回收率的变化,同时比较pH计算法与该方法之间的差异。
1 实 验
1.1 仪器与试剂
Trace GC Ultra气相色谱仪配火焰离子化检测器,美国THERMO公司; pH测定仪,瑞士METTLER TOLEDO公司;超纯水仪,德国MERCK MILLIPORE公司;振荡提取仪,韩国N-BIOTEK公司;不同体积的移液器及低速离心机等。
99.99%氢氧化钠、正十六烷、正十七烷,均购于美国SIGMA公司;pH计校正缓冲溶液(3点校正,pH=4.00、6.86与9.18);水为超纯水;其它有机溶剂均为分析纯试剂。
1.2 试液及标准溶液配制
pH=7水溶液配制:称取40 mg的氢氧化钠,用超纯水定容为100 mL,得到0.01 mol/mL的氢氧化钠溶液。利用0.01 mol/mL 的氢氧化钠调节去二氧化碳的蒸馏水至pH=7±0.1。内标溶液配制:称取99.7 mg的正十六烷于1000 mL容量瓶中,用三氯甲烷定容至刻度得99.7 μg/mL的内标溶液。烟碱标准溶液配制:称取50 mg的烟碱于50 mL容量瓶中,用三氯甲烷定容至刻度得1 mg/mL的烟碱标准溶液。
1.3 样品处理方法
1.3.1 游离烟碱提取方法
水溶液提取法:称取0.25 g烟草粉末于50 mL离心管中,加入10 mL pH=7±0.1提取溶液,涡旋混匀1 min后室温下260 rpm 振荡提取30 min,3500 rpm离心5 min,取上层水溶液清液过0.45 um滤膜。准确移取5 mL滤液于50 mL离心管中,分别加入5 mL的内标溶液提取游离烟碱2次,涡旋3 min后,3500 rpm离心5 min分层,合并有机层静置,取1~2 mL溶液进行分析。
pH计算法:参照文献[8]进行提取,按照如下公式进行计算[9]:
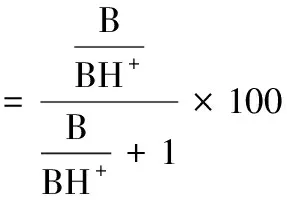
1.3.2 游离烟碱色谱条件
色谱柱为TR-1701(60 m×0.32 mm×0.25 μm),柱温为:110 ℃保持1 min,4 ℃/min升至180 ℃保持1 min,再20 ℃/min升至250 ℃保持15 min。进样口温度为250 ℃,不分流进样,0.8 min后30 mL/min吹扫进样口,载气为氦气,1.5 mL/min,恒流模式,进样量为 1 μL。火焰离子化检测器温度为260 ℃,空气、氢气及尾吹气流量分别为350、35和30 mL/min。在上述色谱条件下,烟碱与正十六烷的出峰时间分别为:15.58和18.94 min。
2 结果与讨论
2.1 内标的选择
文献中常利用正十七烷为内标进行校正[10],但通过空白比对可知,正十七烷出峰时间21.22 min有杂质峰干扰,而正十六烷18.94 min未有干扰,且正十六烷出峰时间更接近烟碱,因此,选择正十六烷为内标更佳。
2.2 提取时间与萃取溶剂的选择
为了考察pH=7±0.1水溶液在不同提取时间(10、20、30、40 min)的提取回收率,利用10 mL水溶液振荡提取0.25 g烟草中的游离烟碱,分别向烟草样品和同一烟草样品的提取液中添加2.15 mg/g的烟碱,经过三氯甲烷萃取后进样,测定提取回收率。结果在表1中可看出:30 min振荡提取获得最大的提取效率,回收率达到97.8%。

表1 提取时间对提取回收率的影响
为了考察不同有机溶剂的萃取效率,分别选择三氯甲烷、二氯甲烷、正己烷、甲基叔丁基醚、乙酸乙酯和乙醚进行萃取,结果表明:除三氯甲烷外,其它溶剂的萃取效率都非常低,因此选择三氯甲烷为萃取溶剂。此外,从表1可以看出,游离烟碱在三氯甲烷萃取阶段的回收率仍然较低,只有40%左右,不满足添加回收率的要求,因此,进一步分析三氯甲烷萃取效率较低的原因。

表2 不同溶剂对游离烟碱的萃取效率
2.3 萃取回收率的研究
为了探索游离烟碱萃取阶段回收率较低的原因,设计以下实验进行研究:
(1)没有烟草本底的回收率:在pH=7的10 mL水溶液中添加1.15 mg烟碱,振荡、过滤、移液、萃取后测定回收率;
(2)烟草本底的回收率:将1.15 mg烟碱加入到烟草粉末中进行振荡、过滤、移液、萃取后测定回收率;
(3)烟草本底的回收率:将1.15 mg烟碱加入到10 mL烟草提取液中进行振荡、过滤、移液、萃取后测定回收率;
(4)烟草本底的回收率:将1.15 mg烟碱加入到萃取后的10 mL三氯甲烷中,振荡混匀后测定回收率。
表3 游离烟碱萃取阶段回收率测试
从表3可得,将烟碱添加到烟草基质中,对游离烟碱回收率的影响较大,减少了大约60%。推测可能是因为外加烟碱受到烟草基质的影响。考虑到烟碱存在方式受到pH的影响,从而降低其萃取效率。测定了1、2与3中在添加烟碱前后的pH值变化,1中添加前后分别为7.04与8.98,2中的提取液pH为5.55,3中添加前后分别为5.55与5.58,可以看出,可能由于烟草基质呈酸性,将添加的部分游离烟碱转变为结合态(与氢离子结合),导致回收率较低。此外,pH=7的水添加前后pH值变化较大,而烟草提取液基本未变化,可能原因为烟草提取液为一种混合复杂的缓冲溶液,微量的烟碱加入对pH影响不大。为了进一步验证上述猜想,设计表4中的实验,结果表明:利用氢氧化钠溶液调节烟草提取液的pH值到7.00后进行添加,回收率达到100.5%,此外,利用缓冲液模拟烟草提取液,获得了类似的结果,进一步验证观测回收率较低是烟草基质为弱酸性的缓冲溶液导致,也从侧面证明了三氯甲烷能较好的萃取游离态烟碱。

表4 游离烟碱萃取阶段回收率验证
2.4 方法验证
以正十六烷为内标,将烟碱质量/正十六烷质量的比值为横坐标(X),烟碱峰面积/正十六烷峰面积的比值为纵坐标(Y),内标法求线性回归方程,在5~500 μg/mL范围下,Y=0.6647X-0.0406,R2=0.9997。将方法应用于测定同一样品,在相同天测定5次及5天内测定5次检验其精密度,结果表明,日内(4.04、4.18、4.25、4.10、4.15 RSD=1.92%)与日间精密度(4.18、4.28、4.02、4.15、4.29 RSD=2.63%)较好。以低浓度(5 ug/mL)进样分析,以信噪比(S/N)为3和10计算其最低检出限和最低定量限。结果表明:方法的最低检测限为0.53 ug/mL和1.76 ug/mL。从上述结果表明,方法达到了较好的定量分析要求。图2为标样与样品分析的色谱图。
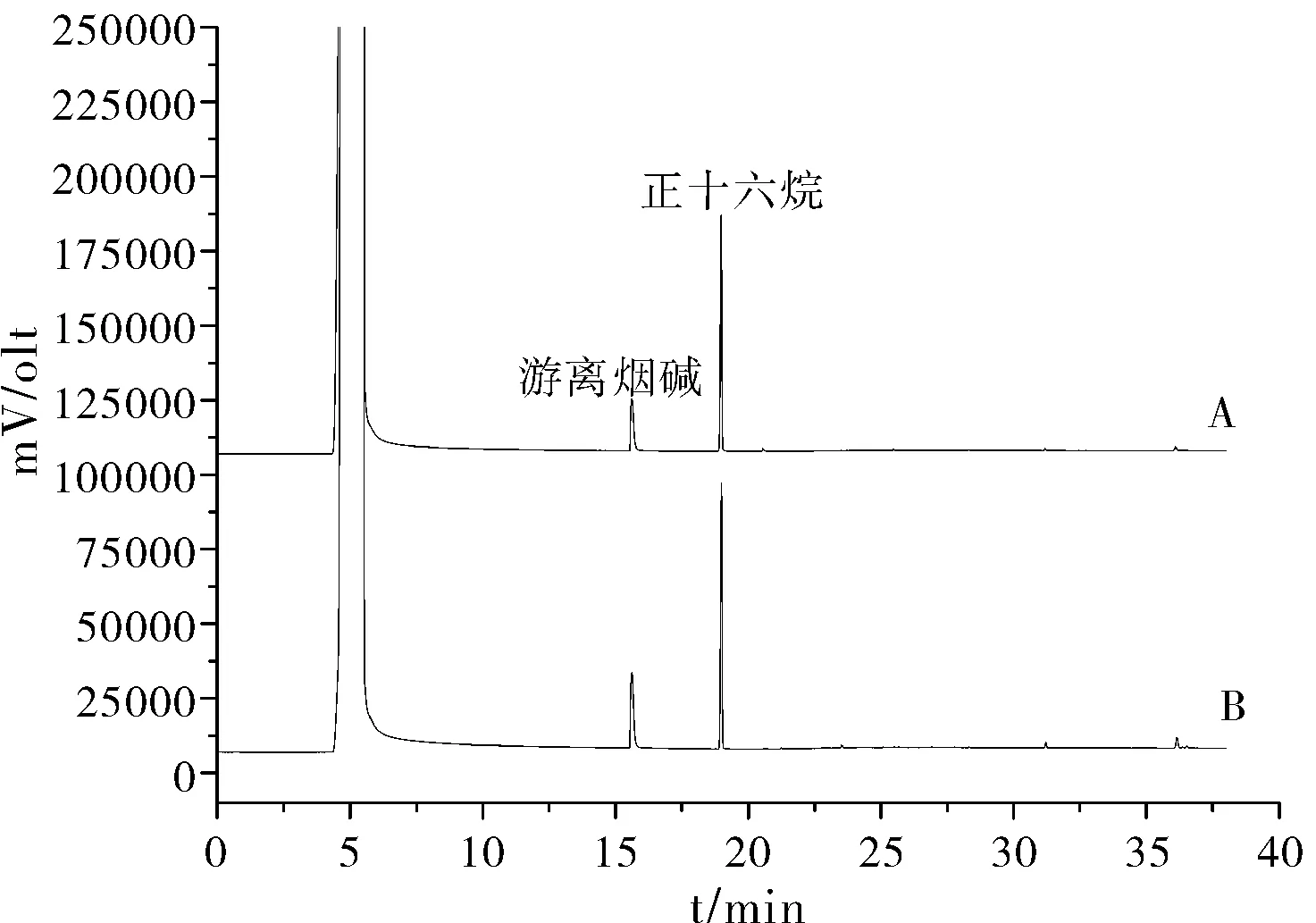
图2 标样色谱图(A)和样品色谱图(B)
2.5 水提取法与pH计算法的比较
对25个K326烤烟样品(等级C3F)的游离烟碱分别利用pH水提取法与pH值计算法进行分析,结果表明:二种方法得到的游离烟碱绝对含量差异较大,水提取法含量普遍高于pH值法,二者比值大约为50倍,线性相关系数达到0.950,达到极显著水平(P<0.01),说明方法之间有较好的一致性。水提取法通过了游离烟碱回收率、精密度等的验证,因此,利用水提取法测定游离烟碱的含量与变化具有很好的可靠性。

表5 水提取法与pH计算法对样品的测定分析
3 结 论
本文研究了水提取-气相色谱法测定烟草中的游离烟碱。本方法通过优化提取与萃取条件,并与pH计算法进行比较。结果表明:该方法准确且可靠,游离烟碱回收率、精密度等都达到了严格定量的要求。与其它方法相比,该方法操作相对简单,耗时较短,且对分析结果产生影响的因素相对较少,提高了对游离烟碱测定的准确度。
[1] 苏明亮,吴鸣,谢剑平.烟草及烟气中烟碱形态研究进展[J].烟草科学,2004(6): 20-26.
[2] 王裔耿,秦云华,陆舍铭,等.主流烟气总粒相物中游离烟碱测定方法综述[J].云南化工,2007, 34(4): 59-62.
[3] Richter P, Spierto F W. Surveillance of smokeless tobacco nicotine, pH, moisture, and unprotonated nicotine content [J]. Nicotine & Tobacco Research, 2003, 5 (6): 885-889.
[4] 卢斌斌,谢剑平,刘惠民.烟草中游离烟碱与其pH值之间的关系[J].烟草科技,2003(6): 6-10.
[5] 殷全玉,杨铁钊,郭宝银,等.紫外分光光度法测定烟草中的游离烟碱[J].中国烟草科学,2008,29(6): 20-22.
[6] Bao M L, Joza P, Rickert W S, et al. An improved headspace solid-phase microextraction method for the analysis of free-base nicotine in particulate phase of mainstream cigarette smoke [J]. Analytica Chimica Acta,2010, 663: 49-54.
[7] Stepanov I, Jensen J, Hatsukami D, et al. New and traditional smokeless tobacco: Comparison of toxicant and carcinogen levels [J]. Nicotine & Tobacco Research,2008, 10 (12): 1773-1782.
[8] 卢丽娟.烟碱形态与烟草品质的相关性研究[D].郑州:郑州轻工业学院食品与生物工程学院, 2010.
[9] Vickery H B, Pucher G W. The determination of "free nicotine" in tobacco: the apparent dissociation constants of nicotine [J]. Journal of Biological Chemistry,1929,84:233-241.
[10]卢丽娟,张弘韬,周浩,等.烟草中游离态烟碱的测定[J].安徽农业科学,2009,37(36): 17946-17947, 17956.
Study on Determination of Free-base Nicotine in Flue-cured Tobacco with Water Extraction*
WEIJian-ke1,LAIDong-hui1,MAOHan-bing1,LUOXi1,WANGJia-zhong1,LIUJian1,MAYun-fei2,YANGCheng2
(1 Technology Center of China Tobacco Guizhou Industrial Co., Ltd., Guizhou Guiyang 550009; 2 Dejiang County Branch, Tongren Tobacco Company, Guizhou Tongren 565200, China)
Water extraction combined with gas chromatography was used to determination of free-base nicotine in flue-cured tobacco.The internal standard, extraction time and extracting solvent were optimized. The result showed that hexadecane, 30 min extraction time and chloroform were the best choice. The lower observed recovery was explored by matrix addition and simulation of buffer experiment. The reason was that the tobacco aqueous solution was a kind of acidic buffering system. Water extraction and pH calculation methods were compared. The result indicated that the correlation coefficient of two methods was 0.950 (extremely significant level). There is good consistency between two methods.
water extraction; free based nicotine; gas chromatography; pH calculation method
国家烟草专卖局科技重大专项(TS-02-20110014)。
魏建科(1984-),女,助理工程师,硕士,从事烟草及烟气化学分析检测工作。
刘剑,博士,高级工程师,从事烟草及烟气化学分析研究。
TS4
A
1001-9677(2016)023-0092-04

