新型分子印迹敏感膜传感器直接快速检测饮料中的柠檬黄
刘英姿,张娟琨,万 雪,陶 强,左娟娟,鞠晓翠
(工业发酵微生物教育部重点实验室,天津市工业微生物重点实验室,天津科技大学生物工程学院,天津 300457)
新型分子印迹敏感膜传感器直接快速检测饮料中的柠檬黄
刘英姿,张娟琨,万 雪,陶 强,左娟娟,鞠晓翠
(工业发酵微生物教育部重点实验室,天津市工业微生物重点实验室,天津科技大学生物工程学院,天津 300457)
构建了一种能够直接在样品中快速检测柠檬黄(tartrazine,TZ)的分子印迹电化学传感器(MIP-PmDB/PoPDGCE).以间苯二酚(m-DB)和邻苯二胺(o-PD)为功能单体,柠檬黄为印迹分子,通过电聚合的方法在玻碳电极表面修饰了一层柠檬黄分子印迹敏感膜,通过循环伏安法(CV)和交流阻抗技术(EIS)对分子印迹敏感膜的分子印迹效应进行了表征.应用差分脉冲伏安法(DPV)研究了传感器对柠檬黄的响应性能,结果表明:响应电流与柠檬黄浓度在5.0× 10-9~1.1×10-6mol/L范围内呈良好的线性关系,检出限为3.5×10-9mol/L(S/N=3),检测时间为5,min.将该传感器应用于实际样品中柠檬黄的分析,加标回收率为96.35%,~101.32%,.
柠檬黄;电聚合;分子印迹;电化学传感器;直接快速检测
柠檬黄(tartrazine,TZ)又称酒石黄,是目前世界上使用最广泛的一种水溶性人工合成色素,被广泛应用于食品、药品、化妆品等领域.由于柠檬黄分子结构中含有偶氮基团和苯环结构,使用过量会对人体健康造成威胁,近年来因违法或过量添加人工色素引起的食品安全事件时有报道.据了解,柠檬黄可引起儿童哮喘、荨麻疹,并且可造成儿童多动症的发生[1];其能干扰染色体合成[2]、造成DNA损伤[3].对小鼠的研究发现,高浓度的柠檬黄可影响小鼠精子发育,造成精子畸形率的升高[4].我国GB 2760—2014《食品安全国家标准·食品添加剂使用标准》[5]对食品中柠檬黄的用量作出了严格限定.
目前柠檬黄的检测方法主要有高效液相色谱法(HPLC)[6]、紫外分光光度法[7]、免疫分析法[8]等.其中,液相色谱法应用最为广泛,这种检测方法灵敏可靠,但需对样品进行前处理,且难以实现现场快速检测的需求;紫外分光光度法灵敏度相对不高;免疫分析法灵敏性高且使用方便,但受环境影响较大,易出现假阳性现象.因此,探索一种方便、省时、选择性好、稳定性高、能用于直接快速检测的方法成为近年来研究的热点.
分子印迹传感器具有高度的特异性和选择性,能够识别复杂成分中的目标物质,清除本底干扰,无需复杂的样品前处理过程,设备易得,操作简便,容易实现直接快速检测,由此得到了广泛的应用研究[9-12].本文以间苯二酚和邻苯二胺为聚合单体,在玻碳电极表面通过电聚合构建了对柠檬黄敏感的分子印迹传感器.洗脱模板分子后,印迹膜上形成能对柠檬黄进行特异识别的孔穴,孔穴中形成的—OH和—NH2等极性基团能够通过氢键等弱的非共价作用力与二次吸附的柠檬黄键和,将目标分子固定,增加印迹膜的灵敏度和特异性.该方法与文献报道的检测方法[13-15]相比,检出限低,响应快,方法更简便,获得了满意的结果,有望在食品检测中获得更好的应用.
1 材料与方法
1.1 试剂与仪器
柠檬黄、间苯二酚(m-dihydroxybenzene,m-DB),上海生工生物工程有限公司;邻苯二胺(ophenylenediamine,o-PD),北京鼎国生物科技有限公司;K3[Fe(CN)6],天津永大化学试剂开发中心;所用试剂均为分析纯,实验用水为双蒸水.
Ivium compact stat电化学工作站,荷兰Ivium科技公司.三电极系统:玻碳电极(GCE,Φ=4,mm)为工作电极,武汉高仕睿联科技有限公司;Ag/AgCl电极为参比电极,天津市兰立科化学电子高技术有限公司;铂片电极为对电极,天津市艾达恒晟科技发展有限公司.超声波清洗机,宁波新芝生物科技有限公司.
1.2 实验方法
1.2.1 玻碳电极的预处理
玻碳电极依次经0.3,µm和0.05,µm的Al2O3悬浊液打磨成镜面后,分别用1∶1的HNO3、无水乙醇、蒸馏水各超声清洗5,min,再将电极放入0.5,mol/L H2SO4溶液中通过循环伏安扫描对电极进行电化学活化,扫描范围-0.2~1.0,V,扫描速率50,mV/s,反复扫描直到得到稳定可逆的循环伏安曲线.
1.2.2 修饰电极的制备
将处理好的玻碳电极放置于含有1,mmol/L邻苯二胺(o-DP)、1,mmol/L间苯二酚(m-DB)、0.5,mmol/L 柠檬黄的0.2,mol/L PBS缓冲液(pH 5.0)的聚合底液中,通氮除氧15,min,然后在0~1.0,V电位范围内采用循环伏安法,以50,mV/s的速率,聚合10圈得到分子印迹聚合膜修饰的玻碳电极.将聚合好的分子印迹膜电极置于含0.5,mol/L H2SO4的50%,乙醇溶液中磁力搅拌15,min,以去除嵌合在分子印迹膜中的柠檬黄分子,即得到带有与柠檬黄分子相匹配的印迹位点的分子印迹膜电极(MIP-PmDB/PoPDGCE).非印迹膜电极(NIP-PmDB/PoPD-GCE)的制备除不加模板分子外,其余步骤与印迹膜电极相同.
1.2.3 电化学检测
将制备好的分子印迹膜电极置于一定浓度的柠檬黄溶液中吸附5,min,取出电极用二次蒸馏水淋洗除去非特异性吸附在膜电极表面的柠檬黄分子.采用三电极系统,以分子印迹膜修饰的玻碳电极为工作电极,铂片电极为对电极,Ag/AgCl电极为参比电极,在室温条件下,以10,mL 含5,mmol/L K3[Fe(CN)6]、0.1,mol/L KCl的PBS(pH 6.4)溶液作为检测底液进行差分脉冲伏安扫描.每次使用后浸于50%,乙醇中并磁力搅拌15,min,以除去二次吸附的印迹分子.
2 结果与讨论
2.1 电聚合过程分析
分子印迹聚合膜电聚合过程的循环伏安曲线(扫描速度50,mV/s,扫描圈数10圈)如图1所示.由图1可知:第1圈扫描时出现明显的氧化峰而反向扫描时没有还原峰出现,这说明聚合单体o-PD和m-DB在电极表面发生了氧化反应,产生的阳离子自由基进行缩合反应生成聚合膜直接沉积在电极表面.同时单体与柠檬黄之间通过氢键或离子键等相互作用,使模板分子在单体电聚合过程中嵌合到聚合膜中.随着扫描圈数的增加氧化峰电流逐渐减小,直到最后电流值不再发生变化.这是因为在聚合过程中电极表面形成的聚合膜为非导电性膜,使得[Fe(CN)6]3-/ [Fe(CN)6]4-不能到达电极表面进行电子传递.对比图1中分子印迹膜电极和非分子印迹膜电极制备过程的循环伏安图可知,两图基本没有差异.因此,在0~1.0,V范围内,聚合过程中柠檬黄没有参与电化学氧化还原反应,且未对单体的电聚合过程造成影响.

图1 分子印迹膜和非分子印迹膜电聚合过程的循环伏安曲线Fig. 1 Cyclic voltammograms curves of MIP-PmDB/ PoPD-GCE and NIP-PmDB/PoPD-GCE membranes for electropolymerization
2.2 分子印迹效应的验证
2.2.1 循环伏安表征
采用循环伏安法对分子印迹膜进行了表征,印迹膜洗脱掉模板分子以后所留下的印迹孔穴可作为电子传质通道,其能够允许[Fe(CN)6]3-/[Fe(CN)6]4-与电极之间发生电子传递,从而使K3[Fe(CN)6]氧化还原电流发生变化,因此可以通过K3[Fe(CN)6]氧化还原电流变化,分析分子印迹膜的形态并验证分子印迹膜的印迹效应.图2为5,mmol/L K3[Fe(CN)6]在不同修饰电极上的循环伏安曲线.分子印迹电极洗脱模板分子前(曲线 b)没有氧化还原峰电流,是因为经过电聚合,o-PD、m-DB与柠檬黄在电极表面聚合形成一层致密的不导电聚合膜,阻止了电子传递.经过洗脱模板分子后的分子印迹膜电极(曲线c)由于模板分子从聚合膜中逸出,从而在印迹膜上留下孔穴,这些孔穴使K3[Fe(CN)6]能够重新到达电极表面发生氧化还原反应,产生电流信号,但峰电流强度明显小于裸电极(曲线a).将洗脱模板分子后的膜电极置于0.5,µmol/L 柠檬黄溶液中孵化3,min后的氧化还原峰电流与洗脱模板分子后(曲线c)相比出现明显下降,这是由于印迹分子重新占据部分印迹位点,导致电子传递速率减慢.

图2 不同修饰电极在5,mmol/L K3[Fe(CN)6]溶液中的循环伏安曲线Fig. 2Cyclic voltammograms for different electrodes in 5,mmol/L K3[Fe(CN)6] solution
2.2.2 交流阻抗表征
交流阻抗法是表征修饰电极表面特征的一种有效方法.在交流阻抗法中,Nyquist曲线的高频半圆部分直径代表电子转移阻抗,与电极表面的绝缘特性相关.低频线性部分与溶液扩散相关.在室温条件下,频率范围0.1,Hz~100,KHz条件下测试了分子印迹聚合膜电极的交流阻抗行为,图3为传感器制备各阶段在5,mmol/L K3[Fe(CN)6]溶液中的Nyquist曲线.
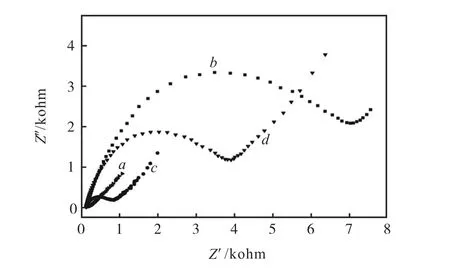
图3 不同修饰电极的交流阻抗图谱Fig. 3The electrochemical impedance spectroscopy of different electrodes
由图3可见:裸电极的Nyquist曲线(曲线a)半圆部分直径很小,近似于一条直线,说明裸玻碳电极表面具有较快的电子转移速率.通过电聚合将分子印迹聚合膜修饰到玻碳电极上以后(曲线b),电极表面的电子转移阻抗急剧增大,说明分子印迹聚合膜的形成阻碍了电子传递,导致[Fe(CN)6]3-/[Fe(CN)6]4-无法到达电极表面发生氧化还原反应,证明所制备的分子印迹聚合膜具有良好的绝缘性能.经洗脱去除模板分子后(曲线c),分子印迹膜上形成印迹孔穴,使电化学探针K3[Fe(CN)6]更容易穿过印迹膜发生电子传递,电子转移阻抗减小.将去除模板分子的分子印迹膜电极置于柠檬黄溶液中重新吸附后(曲线d),印迹位点被重新占据,电子传递速率减慢,阻抗增大,进一步印证了分子印迹效应的存在.
2.3 聚合圈数对分子印迹膜厚度的影响
分子印迹膜修饰电极的吸附性能与电极上分子印迹聚合物的覆盖量有关,覆盖量过少,聚合膜太薄,有效识别位点较少,达不到吸附效果;分子印迹聚和物覆盖量过多,聚合膜太厚,降低电子传递速率和修饰电极自身的吸附性能,一般修饰电极上聚合物的厚度可以由聚合圈数表征.将不同圈数下聚合的分子印迹膜传感器分别置于5,mmol/L K3[Fe(CN)6]溶液中进行循环伏安扫描,结果如图4所示.

图4 不同聚合圈数制备的分子印迹膜电极在5,mmol/L K3[Fe(CN)6]溶液中的循环伏安曲线Fig. 4 Cyclic voltammograms of MIPS electrodes with different cyclic circles in 5,mmol/L K3[Fe(CN)6] solution
随着扫描圈数的增多,分子印迹膜传感器在K3[Fe(CN)6]溶液中的导电能力越来越小.这是由于随着聚合圈数的增加,功能单体聚合形成的分子印迹膜逐渐在电极表面沉积,阻止了K3[Fe(CN)6]到达电极表面发生氧化还原反应.扫描圈数达到7圈时,已经没有氧化还原峰出现,说明此时电极表面已经形成一层非常致密的聚合膜;当继续增加扫描圈数,循环伏安曲线基本已经不再变化.洗脱模板过程中发现,聚合7圈所制备的分子印迹膜容易脱落,这可能是聚合膜与玻碳电极之间的结合还不牢固.分子印迹膜聚合15圈所制备的分子印迹膜传感器模板分子不易洗脱,而聚合10圈所制备的分子印迹膜传感器在洗脱过程中可以既保持膜的完整性,又能快速将模板分子去除,因此聚合10圈时分子印迹膜厚度最佳.
2.4 洗脱体系及洗脱时间的选择
分别考察了印迹膜电极和非印迹膜电极在0.5,mol/L NaOH、0.5,mol/L H2SO4、50%,乙醇溶液、含0.5,mol/L H2SO4的50%,乙醇溶液以及含0.5,mol/L NaOH的50%,乙醇溶液的洗脱效果,结果发现:0.5,mol/L NaOH溶液和含0.5,mol/L NaOH的50%,乙醇溶液易破坏分子印迹膜的完整性,50%,乙醇溶液对模板分子的洗脱不完全,洗脱后在电极表面不能形成可逆氧化还原反应.含0.5,mol/L H2SO4的50%,乙醇溶液在保持印迹膜完整性的情况下能够快速去除模板分子.因此选择含0.5,mol/L H2SO4的50%,乙醇溶液作为洗脱溶液.
将印迹膜电极在含0.5,mol/L H2SO4的50%,乙醇溶液中分别浸泡2、5、10、15、20、25,min后,取出用蒸馏水冲洗干净,置于5,mmol/L K3[Fe(CN)6]溶液中差分脉冲伏安扫描.洗脱时间与响应电流之间的关系如图5所示.结果显示15,min以后响应电流基本不再发生变化,因此选择洗脱时间为15,min.

图5洗脱时间对分子印迹膜电极和非分子印迹膜电极在5,mmol/L K3[Fe(CN)6]溶液中响应电流的影响Fig. 5Influence of elution time on the response of MIPPmDB/PoPD-GCE and NIP-PmDB/PoPD-GCE sensor in 5,mmol/L K3[Fe(CN)6] solution.
2.5 孵化时间的选择
孵化时间可以反映分子印迹传感器的响应时间,将洗脱完全的印迹膜电极置于浓度为1,µmol/L的柠檬黄溶液中分别孵化1、3、5、10,min.取出后用双蒸水淋洗以去除电极表面非特异性吸附的柠檬黄分子,然后置于5,mmol/L K3[Fe(CN)6]溶液中进行差分脉冲伏安扫描,结果如图6所示.随着孵化时间的延长,峰电流逐渐降低,这是因为目标分子不断被分子印迹膜吸附,导致分子印迹膜上可供K3[Fe(CN)6]通过的传质通道逐渐减少,直到5,min后峰电流基本已经不再变化,表明此时分子印迹膜对柠檬黄的结合已经达到吸附-解吸平衡.因此选择孵化时间5,min.

图6 孵化时间对印迹膜电极在5,mmol/L K3[Fe(CN)6]溶液中DPV峰电流的影响Fig. 6 Effect of different incubation time on the differenttial pulse voltammograms responses of MIP-PmDB/ PoPD-GCE in 5,mmol/L K3[Fe(CN)6] solution
2.6 线性关系和检出限
优化实验条件下,将制备好的分子印迹膜电极置于系列浓度(0.005、0.05、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1.0、1.1,µmol/L)的柠檬黄溶液中孵化5,min后,双蒸水淋洗电极表面以去除非特异性吸附的柠檬黄分子,然后置于5,mmol/L浓度的K3[Fe(CN)6]溶液中,利用差分脉冲伏安法测定不同浓度柠檬黄溶液相应的差分脉冲伏安峰电流值,结果如图7所示.随着柠檬黄浓度的不断增大,越来越多的印迹位点被占据,峰电流值逐渐降低,其与柠檬黄的浓度在5×10-9~1.1×10-6,mol/L范围成良好的线性关系,线性方程为i=-63.294C+77.120,R2=0.991,8,检出限为3.5×10-9,mol/L(S/N=3).


图7 印迹传感器在不同柠檬黄浓度下的差分脉冲伏安曲线和校正曲线Fig. 7Differential pulse voltammograms and the calibration curves of MIP-PmDB/PoPD-GCE after incubated in different concentration of tartrazine
2.7 选择性与重复性
选择与柠檬黄分子结构类似的苋菜红、日落黄、胭脂红,易对K3[Fe(CN)6]电信号产生干扰的抗坏血酸和多巴胺以及易与柠檬黄共存的阿斯巴甜作为干扰物.将印迹膜电极分别置于浓度为5×10-7,mol/L柠檬黄溶液以及相同浓度柠檬黄与10倍浓度干扰物的混合溶液中孵化5,min,于K3[Fe(CN)6]溶液中进行差分脉冲伏安扫描,结果如图8所示.
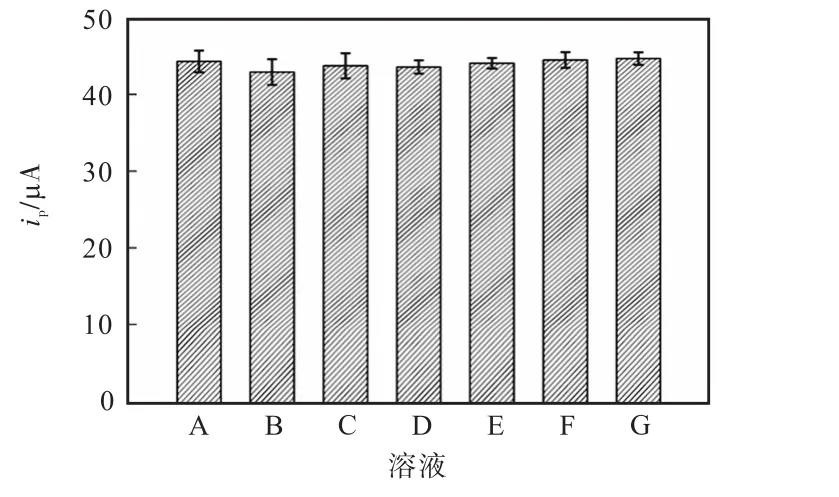
图8 干扰物对柠檬黄响应电流的影响Fig. 8Influence of interferents on the current response of tartrazine
结果表明(图8),抗坏血酸、多巴胺以及阿斯巴甜对柠檬黄几乎不造成干扰,引起的电流变化在-0.54%,~0.83%,.结构类似物对柠檬黄检测产生微弱影响,引起的电流变化在-3.15%,~-1.30%,.这是由于三者与柠檬黄结构类似,使得少量结构类似物能够吸附到分子印迹孔穴中,从而引起微弱的电化学响应,但对柠檬黄的检测没有造成显著干扰.由此可见该传感器具有良好的选择性.
在最佳实验条件下,用同一支分子印迹膜电极多次测定5×10-7,mol/L 柠檬黄溶液,计算其相对标准偏差(RSD,n=10)为1.6%,,表明分子印迹膜电极具有良好的重复性,柠檬黄与印迹位点之间的结合是可逆的过程.
2.8 实际样品分析
为研究传感器在实际样品检测中的可行性,取不同品牌市售橙色饮料0.1,mL,其中橙味汽水加热去除其中的CO2,用NaOH调pH至6.4,用PBS(pH 6.4)溶液稀释至10,mL,检测样品溶液中柠檬黄的初始含量;然后按照标准加入法加入不同含量柠檬黄,每个样品平行测定3次,经分子印迹传感器吸附后,置于含5,mmol/L K3[Fe(CN)6]、0.1,mol/L KCl的PBS溶液中检测.为了与现行成熟方法对比,每个样品同时用HPLC检测,检测结果见表1.该传感器回收率为96.35%,~101.32%,,RSD为1.24%,~3.19%,.该传感器与HPLC法相比,相对误差介于-3.5%,~1.7%,之间,可满足实际样品检测的需求.

表1 实际样品中柠檬黄检测Tab. 1 Tartrazine in real sample
3 结 语
采用分子印迹技术,以间苯二酚和邻苯二胺为聚合单体构建了一种能够特异性识别柠檬黄的分子印迹敏感膜传感器.分子印迹聚合膜的制备采用循环伏安电聚合法,该方法可以通过改变聚合圈数等方式控制聚合膜的厚度,相对于其他聚合方法成膜快、重复性好.利用循环伏安法和交流阻抗技术验证了电极表面聚合膜的分子印迹效应.通过对分子印迹膜洗脱时间和吸附时间的考察确定了传感器的最佳洗脱时间为15,min,最佳吸附平衡时间为5,min.传感器对柠檬黄具有良好的响应性能,差分脉冲伏安响应电流峰值与柠檬黄浓度在5.0×10-9~1.1×10-6,mol/L范围内呈现良好的线性关系,检出限3.5×10-9,mol/L (S/N=3).该方法无需复杂的样品前处理过程,检测时间短,选择性好,灵敏性高,有望在食品中人工色素的检测方面获得更好的应用.
[1] Bateman B,Warner J O,Hutchinson E,et al. The effects of a double blind,placebo controlled,artificial food colourings and benzoate preservative challenge on hyperactivity in a general population sample of preschool children[J]. Archives of Disease in Childhood,2004,89(6):506-511.
[2] Giri A K,Das S K,Talukder G,et al. Sister chromatid exchange and chromosome aberrations induced by curcumin and tartrazine on mammalian cells in vivo[J]. Cytobios,1990,62(249):111-117.
[3] Sasaki Y F,Kawaguchi S,Kamaya A,et al. The comet assay with 8,mouse organs:Results with 39,currently used food additives[J]. Mutation Research/Genetic Toxicology and Environmental Mutagenesis,2002,519 (1/2):103-119.
[4] 蒋利刚,程东,韩晓英,等. 柠檬黄对雄性小鼠生殖细胞的影响[J]. 生物医学工程研究,2011,30(3):174-176.
[5] 中华人民共和国国家卫生和计划生育委员会. GB 2760—2014食品安全国家标准·食品添加剂使用标准[S]. 北京:中国标准出版社,2014.
[6] Pual M,Jarry G,Elhkim M O,et al. Lack of genotoxic effect of food dyes amaranth,sunset yellow and tartrazine and their metabolites in the gut micronucleus assay in mice[J]. Food and Chemical Toxicology,2009,47(2):443-448.
[7] Alves S P,Brum D M,Andrade E C B,et al. Determination of synthetic dyes in selected foodstuffs by high performance liquid chromatography with UV-DAD detection[J]. Food Chemistry,2008,107(1):489-496.
[8] Lei Y J,Zhang S J,Fang L Z,et al. A sensitive and specific enzyme immunoassay for detecting tartrazine in human urinary samples[J]. Analytical Methods,2013,5(4):925-930.
[9] Mazzotta E,Malitesta C,Díaz-Álvarez M,et al. Electrosynthesis of molecularly imprinted polypyrrole for the antibiotic levofloxacin[J]. Thin Solid Films,2012,520(6):1938-1943.
[10] Tonelli D,Ballarin B,Guadagnini L,et al. A novel potentiometric sensor for L-ascorbic acid based on molecularly imprinted polypyrrole[J]. Electrochimica Acta,2011,56(20):7149-7154.
[11] 齐玉冰,刘瑛,宋启军. 碳纳米管修饰电极分子印迹传感器快速测定沙丁胺醇[J]. 分析化学,2011,39(7):1053-1057.
[12] 余会成,黄学艺,谭学才,等. 基于电聚合的苯巴比妥分子印迹电化学传感器的制备及其应用研究[J]. 分析测试学报,2014,33(7):752-757.
[13] 王曼丽,明华蜜,尹洪宗,等. 表面等离子体共振生物传感器的构建及对柠檬黄的检测[J]. 分析化学,2014,42(1):53-58.
[14] Abu-Shawish H M,Ghalwa N A,Saadeh S M,et al. Development of novel potentiometric sensors for determination of tartrazine dye concentration in foodstuff products[J]. Food Chemistry,2013,138(1):126-132.
[15] Ye X L,Du Y L,Lu D B,et al. Fabrication of β-cyclodextrin-coated poly(diallyldimethylammonium chloride)-functionalized graphene composite film modified glassy carbon-rotating disk electrode and its application for simultaneous electrochemical determination colorants of sunset yellow and tartrazine[J]. Analytica Chimmica Acta,2013,779:22-34.
责任编辑:郎婧
A Novel Sensor for Fast and Direct Determination of Tartrazine in Soft Drinks Based on Molecularly Imprinted Film
LIU Yingzi,ZHANG Juankun,WAN Xue,TAO Qiang,ZUO Juanjuan,JU Xiaocui
(Key Laboratory of Industrial Fermentation Microbiology,Ministry of Education,Tianjin Key Laboratory of Industrial Microbiology,College of Biotechnology,Tianjin University of Science & Technology,Tianjin 300457,China)
A novel molecularly imprinted polymer sensor(MIP-PmDB/PoPD-GCE)for fast and direct tartrazine(TZ) determination was developed.The polymer was coated on the surface of the glassy carbon electrode(GCE)directly via electropolymerization,with m-dihydroxybenzene(m-DB)and o-Phenylenediamine(o-PD)as monomers.The new sensor can be bound to tartrazine in real samples without sample pretreatment.The molecularly imprinting effect was characterized with cyclic voltammetry(CV)and electrochemical impedance spectroscopy(EIS).The response performance was studied with differential pulse voltammetry(DPV).The linear relationship between the current and the tartrazine concentration was observed from 5.0×10-9mol/L to 1.1×10-6mol/L,with the detection limit of 3.5×10-9mol/L and detection time of 5,min.The new sensor was successfully applied to the analysis of tartrazine in soft drink samples and the recovery rate was between 96.35%, and 101.32%,
tartrazine;electropolymerization;molecular imprinting;electrochemical sensor;fast and direct determination
O656
A
1672-6510(2016)06-0021-06
10.13364/j.issn.1672-6510.20160001
2016-01-03;
2016-03-14
天津市科委国际合作项目(14RCCFSF00140)
刘英姿(1990—),女,河北人,硕士研究生;
张娟琨,教授,zhangjk@tust.edu.cn.

