复合酵母在赤霞珠发酵过程中酵母菌相互作用研究
李梅花
(云南省宜良县北古城镇人民政府,云南宜良652112)
复合酵母在赤霞珠发酵过程中酵母菌相互作用研究
李梅花
(云南省宜良县北古城镇人民政府,云南宜良652112)
利用WL营养琼脂培养基对发酵过程不同阶段分离的菌株进行初步分类,结果表明,这些菌株分为5属8种:酿酒酵母(Saccharomyces serevisiae)、有孢汉逊酵母(Hanseniaspora uvarum)、克鲁维毕赤氏酵母(Pichia kluyveri)、东方伊萨酵母(Issatchenkia orientalis),假丝酵母(Candida)。对初步分类菌株进行26S rDNAD1/D2区扩增和测序,测序结果经Blast比对后证实,研究了这几种酵母在不同阶段的构成比,揭示了整个过程中酵母菌的生物多样性和不同菌种的动态变化。在此基础上选用interdelta分析对161株酿酒酵母进行菌株区分,结果显示,这些酿酒酵母可归为9个基因型。研究了这9个基因型在复合发酵过程中的菌株组成及变化,为利用降酸酵母降酸研究提供依据。
复合发酵; 分类鉴定; 相互作用; interdelta分析; 葡萄酒
葡萄酒发酵过程是一个复杂的生态和生化过程,包含不同酵母属种此消彼长的变化。多种酵母在发酵过程中的相互协作,可以有效地增加葡萄酒风味的多样性,但也可能影响葡萄酒质量的稳定性。研究发酵过程中酵母菌的动态变化,揭示在发酵不同阶段中酵母菌的消长规律,有利于葡萄酒发酵过程中对微生物的控制,也可以为研究酵母菌对葡萄酒风味的影响提供依据。
本实验通过WL营养琼脂聚类分析、26S rDNAD1/ D2和interdelta等方法和手段,对所采集的菌株进行较系统的分类鉴定,探究葡萄酒复合酵母发酵过程中酵母菌的种类、分布及特性,旨在揭示赤霞珠葡萄复合发酵过程中酵母菌的消长规律,为葡萄酒微生物降酸研究提供依据。
1 材料与方法
1.1材料、试剂及仪器
葡萄原料:赤霞珠(CabernetSauvignon)。
试剂:葡萄糖、蛋白胨、酵母浸粉、琼脂等培养基成分试剂均为国产分析纯试剂,引物、dNTPs、Taq酶、PCR buffer、MgCl2等分子生物学试剂。
仪器设备:霉菌培养箱、电热鼓风干燥箱、洁净工作台、冰箱、pH计、凝胶成像系统、电泳仪、PCR扩增仪、研磨式匀浆机、台式冷冻离心机、M ilipore超纯水制备系统、高压蒸汽灭菌锅。
1.2培养基
YEPD液体培养基:酵母浸粉10g/L(1%),蛋白胨20g/L(2%),葡萄糖20g/L(2%),氯霉素100 mg/L(0.01%),蒸馏水。121℃高压灭菌20m in。
YEPD固体培养基:酵母浸粉10g/L(1%),蛋白胨20g/L(2%),葡萄糖20g/L(2%),氯霉素100 mg/L(0.01%),琼脂20g/L(2%),蒸馏水。121℃高压灭菌20m in。
WL琼脂培养基配方:酵母浸粉4g/L,蛋白胨5g/L,葡萄糖5g/L,磷酸二氢钾0.55g/L,氯化钾0.425g/L,氯化钙0.125g/L,硫酸镁0.125g/L,氯化铁0.0025g/L,硫酸锰0.0025g/L,溴甲酚绿22 mg/L,琼脂20g/L,调pH5.5~6.5。
配制方法:先将盐类和溴甲酚绿配制成储备液,置于4℃冰箱。
储备液A:磷酸二氢钾5.5g,氯化钾4.25g,氯化钙1.25g,硫酸镁1.25g,使用蒸馏水定容至400m L,高压灭菌后4℃保存,使用时按40m L/1000m L加入。
储备液B:氯化铁0.25g,硫酸锰4.25g,蒸馏水定容至100m L,高压灭菌后4℃保存,使用时按1m L/1000m L加入。
储备液C:溴甲酚绿0.44g,溶解于100m L 50%乙醇溶液中(配制50%乙醇溶液时所有使用的器皿和蒸馏水都需经高压灭菌),使用时按1m L/1000m L加入。
配制培养基时按比例加入储备液A和储备液B以及剩余培养基组分,加入蒸馏水至目标体积,调节pH5.5~6.5。高压灭菌后冷却至65℃加入储备液C,混匀制备平板。
1.3实验方法
1.3.1菌株的分离保藏
将葡萄破碎,用20 L已预先灭菌的玻璃发酵瓶,每瓶加入15 L带葡萄皮的葡萄汁,取其中2瓶作为对照,在另3个瓶中按接种表中组合加入酵母,置于25℃恒温下进行发酵。
其中1号、2号罐在破碎入罐后分别加入活性干酵母(RC212)和降酸酵母(R312);3号罐破碎入罐后同时加入两种酵母;4号罐破碎时加入R312,2 d后加入RC212;5号罐破碎时加入RC212,2 d后加入R312。
酵母菌的分离分别在葡萄酒发酵过程的前期、中期、后期3个时期取样。前期从葡萄破碎进罐至发酵启动(此时罐底部有少量气泡向顶部上升);中期即发酵旺盛期(此时葡萄皮渣上升形成“冒”,罐内大量气泡上升);后期为发酵消退期(此时液面又降至初期,发酵醪中无明显气泡上升)。于发酵的前、中、后期,每次取1m L发酵液,稀释至适当梯度,取0.2 m L样品稀释液涂布YEPD和WL平板,28℃下分别培养3 d和5 d,选取合适稀释浓度的平板进行总酵母菌和不同类别酵母菌的计数。在YPD平板上,每个时期随机挑取15~20个酵母单菌落,于20%甘油中保藏备用。
1.3.2菌株的初步形态分类
将保藏的酵母菌种在25℃下于5m LYEPD液体培养基中活化24 h,用接种环划线接种于WL营养培养基,于培养箱中28℃下倒置5 d后观察,记录菌落颜色和形态,对照WL菌落特征表进行初步分类。
1.3.326S rDNAD1/D2区序列分析
1.3.3.1总DNA的提取
①用接种环取平板上菌落2~4环于200μL裂解液中,加入3/10总体积石英砂在匀浆机振荡8min,每隔2m in将离心管取出用力甩几下(如果菌龄过大可将破壁时间延长),然后65℃水浴10m in。
②加入200μL 5mol/LKAc,冰浴8m in。
③14000 r/m in×5m in转移上清液至新的离心管中。
④加入3mol/LNaAc 35μL,加入异丙醇200μL混匀后,冰浴8m in,14000 r/m in×5m in收集沉淀。
⑤200μL TE溶解,加入RNase 3μL,65℃水浴10m in。
⑥加入200μL氯仿-异戊醇(24∶1),抽提。
⑦转移上清液至另一离心管中,加入35μL 3mol/L NaAc及390μL无水乙醇,混匀后以14000 r/m in×8m in收集DNA。
⑧用150μL 70%乙醇洗涤沉淀,吹干后TE溶解,-20℃保藏。
1.3.3.226S rDNAD1/D2区扩增
①PCR引物。使用引物NL1(5′-GCATATCAATAAGCGGAGGAAAAG-3′)和 NL4(5′-GGTCCGTGTTTCAAGACGG-3′)。
②PCR体系(50μL)。每管中含PCR缓冲液(10×)5.0μL;25mM MgCl23.0μL;10mM dNTP 1.0μL;10μM NL1和NL4各1μL;0.5U/μLDNA聚合酶3μL;10μg/μL模板DNA 1.0μL;最后添加ddH2O定容到50μL。
③PCR反应程序
95℃预变性5m in,94℃变性1m in,52℃退火1min,72℃延伸80 s;循环36次;再72℃延伸8m in。
1.3.3.326S rDNAD1/D2区序列测定
所得产物委托生物技术公司测序。
1.3.3.4测序结果分析
根据测序结果,利用BLAST软件从GenBank核酸序列数据库中进行同源序列搜索(BLAST search),比较供试菌株与已知酵母菌相应序列的相似程度。序列的搜索,可以得到该酵母菌株在这段序列上与其他亲缘关系相近的已知酵母菌的相关信息,因为绝大多数已发表的种的26S rDNA的Dl/D2区、ITS序列已经在EMBL/DDBJ/GenBank中。因此,可以根据同源搜索的结果初步确定所做菌株的分类地位。
1.3.4酒酵母的interdelta分析
1.3.4.1总DNA的提取
具体操作同上1.3.3.1。
1.3.4.2interdelta区扩增
①PCR引物
采用引物为delta12(5′-TCAACAATGGAATCCCAAC-3′)和delta21(5′-CATCTTAACACCGTATATGA-3′)。
②PCR体系(25μL)
5×PCR buffer(Taq buffer w ith KCL)5μL;25 mMMgCl25μL;1mM dNTPs 5μL;10μM引物各1.25μL;5 U/μL Taq酶0.4μL,模版DNA 1μL;加ddH2O(双蒸水)至25μL。
③PCR反应程序
95℃4m in;95℃30 s,46℃30 s,72℃90 s,循环35次;72℃10m in。
1.3.4.3PCR产物的琼脂糖凝胶电泳
①称取1.5%琼脂糖,加入40m L 1×TAE加热至胶完全融化,待胶冷却至60℃左右时,加入4μLEB,摇匀。
②放好梳子,将液体倒在制胶槽内,3~5mm厚,除气泡。
③室温下放置待胶完全凝固后,去掉两端封条,将凝胶槽移至电泳槽,然后小心地拔掉梳子,保持点样孔完整。
④将7~8μL PCR产物与2μL上样缓冲液一次点到加样孔内,其中1个为对照样品。
⑤60~100 V恒温电泳,当溴酚蓝染料移至距凝胶前沿1~2 cm处,停止电泳。
⑥取出凝胶,用紫外分析仪(300 nm)观察,并照相记录。
1.3.4.4图谱统计及聚类分析
对照100 bp DNA Marker的电泳谱带,将特定位置上的PCR产物电泳谱带按“1”(有)和“0”(无)进行人工读带并统计,应用DPS软件进行聚类分析。聚类距离为欧式距离,聚类方法为类平均法(UPGMA)。
2 结果与分析
2.1菌株的初步培养分类结果
本实验直接取样稀释,取不同的梯度样划线于WL培养基。最后选取合适梯度计数,共分离857株酵母,并初步可以分为:酿酒酵母(Saccharomyces serevisiae),有孢汉逊酵母(Hanseniaspora),克鲁维毕赤氏酵母(Pichia kluyveri),东方伊萨酵母(Issatchenka orientalis),假丝酵母(Candida species)。其代表性菌株的菌落形态见图1。
2.2菌株26S rDNAD1/D2区序列分析
使用引物对NLI/NL4对所挑选出的20个菌株的26S rRNA基因序列进行扩增,测定其片断大小在550~620 bp之间。经BLAST分析,与菌株26S rRNA基因序列相似性最大的酵母菌见表1。
2.3酵母菌群的种类组成和变化
5组对照实验发酵过程中菌种组成和变化见表2、表3、表4、表5、表6。
观察以上结果,破碎时期一般以葡萄汁有孢汉逊酵母和克鲁维毕赤氏酵母为主,还有少量东方伊萨酵母等。在培养过程中,酿酒酵母慢慢增多,葡萄汁有孢汉逊酵母、克鲁维毕赤氏酵母等其他酵母逐渐减少,最后酿酒酵母占主导地位,其他酵母基本消失。
表2中主要以酿酒酵母和葡萄汁有孢汉逊酵母为主,少数其他酵母。前期酿酒酵母少,葡萄汁有孢汉逊酵母为主,中期则相反,后期大多酿酒酵母,少数葡萄汁有孢汉逊酵母。
表3中破碎期到前期,葡萄汁有孢汉逊酵母减少,酿酒酵母突然增多。前期到中期,酿酒酵母减少,葡萄汁有孢汉逊酵母增多,后期,酿酒酵母又增多,葡萄汁有孢汉逊酵母消失。
表4中还是以酿酒酵母和葡萄汁有孢汉逊酵母为主,酿酒酵母前期到中期略有降低,葡萄汁有孢汉逊酵母略有升高,后期只剩酿酒酵母。
表5中前期到中期酿酒酵母降低,葡萄汁有孢汉逊酵母升高,最后只剩酿酒酵母。和表3变化情况相似,只是比例变化高低不同。
表6中前期2种酵母比例和表2相近,中期酿酒酵母比例明显低于表2,葡萄汁有孢汉逊酵母比例明显高于表2。
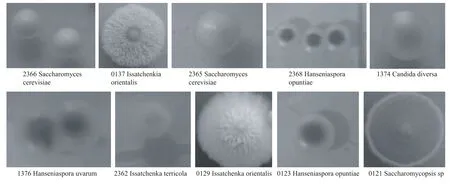
图1 8种酵母菌在WL培养基上的菌落形态
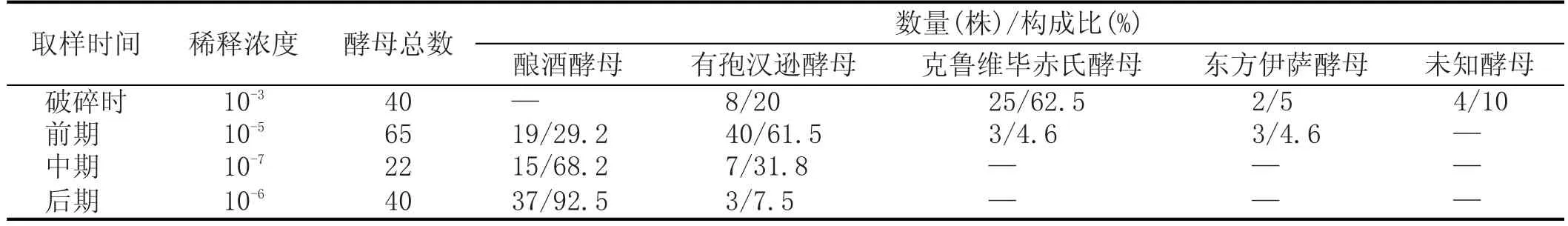
表2 1号酒样菌株WL营养培养基聚类结果(酿酒酵母)

表3 2号酒样菌株WL营养培养基聚类结果(降酸酵母)

表4 3号酒样菌株WL营养培养基聚类结果(酿酒酵母+降酸酵母)

表5 4号酒样菌株WL营养培养基聚类结果(降酸酵母,2 d后加入酿酒酵母)
由以上实验分析可以说明:此降酸酵母也是酿酒酵母的一种;酿酒酵母是酒精发酵的主要酵母;此降酸酵母在前期中期有助于葡萄汁有孢汉逊酵母增长,抑制其他酿酒酵母和自身的繁殖。即此降酸酵母在和酿酒酵母的前期中期竞争中取胜,后期失败;有1种未知酵母受此降酸酵母影响较大。
2.4酿酒酵母interdicts分析
2.4.1酿酒酵母interdelta分类情况
将以上实验分离到的161株酿酒酵母进行interdelta PCR,扩增产物经琼脂糖凝胶电泳得到相应的图谱,根据电泳图谱的差异将全部酿酒酵母分为9种基因型,分类情况见表7。
2.4.2酿酒酵母基因型组成及变化
本实验应用interdelta分析区分酿酒酵母种内不同的基因型,达到了展示复合发酵过程中酿酒酵母不同基因型的组成及变化的效果,见表8。
实验中,酿酒酵母基因型在各时段变化如下:

表6 5号酒样菌株WL营养培养基聚类结果(酿酒酵母,2 d后+降酸酵母)
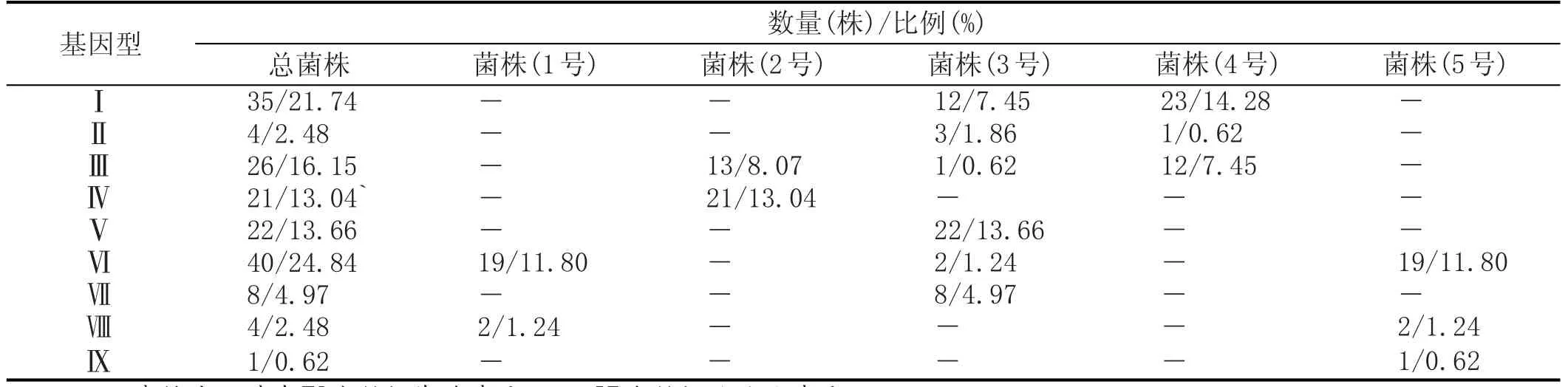
表7 161株酿酒酵母的interdel ta分析结果
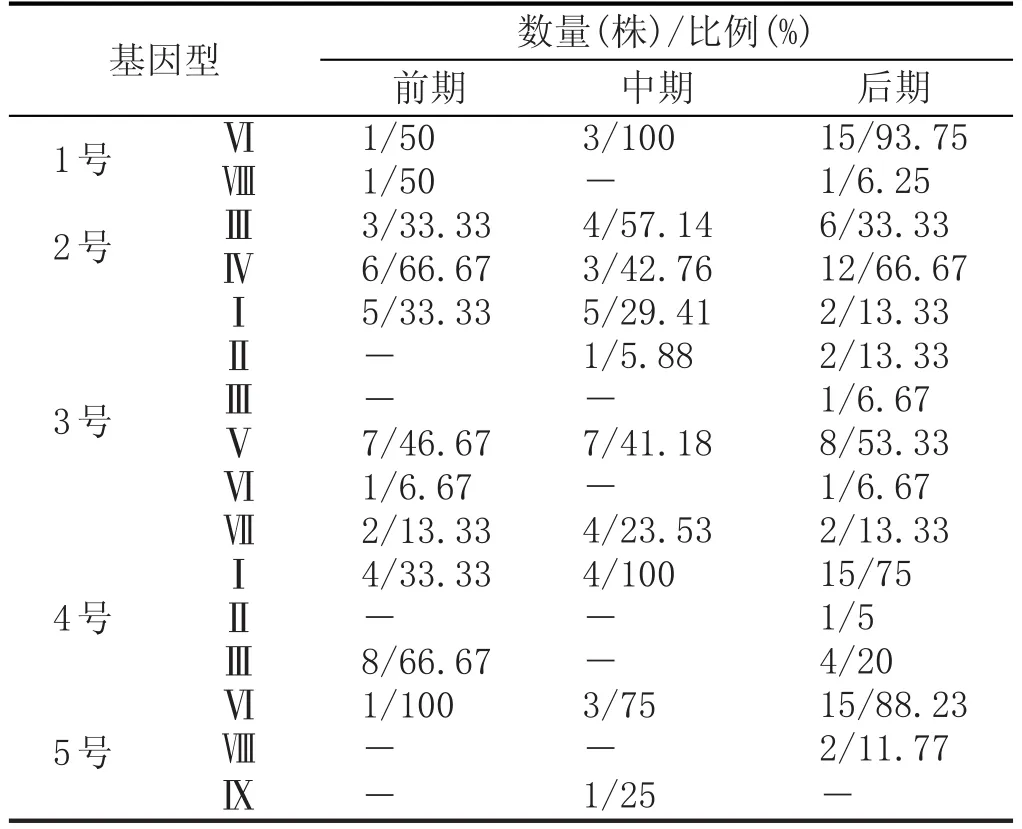
表8 赤霞珠复合发酵过程中酿酒酵母的基因型种类、数量、比例
(1)在开始添加活性干酵母的发酵过程中分出2种基因型:Ⅵ和Ⅷ。其中Ⅵ是添加酵母,从开始到最后一直存在,并渐渐占主导地位,Ⅷ少量出现,变化不大。
(2)在开始添加降酸酵母的发酵过程中分离出2种基因型:Ⅲ和Ⅳ。其中Ⅳ是添加降酸酵母,前期较多,中期减少,最后很多,主导发酵。Ⅲ发酵过程中一直增长,但增幅较小。
(3)在开始同时添加降酸酵母和活性干酵母的发酵过程中分离出6种基因型:Ⅰ、Ⅱ、Ⅲ、Ⅴ、Ⅵ和Ⅶ。前中期主要以Ⅰ和Ⅴ为主,Ⅱ、Ⅵ和Ⅶ少量出现。后期Ⅴ较多,其他几种都在减少,出现Ⅲ。
(4)在开始加入降酸酵母,2 d后加入干酵母的发酵过程中分离出3种基因型:Ⅰ、Ⅱ和Ⅲ。前期Ⅰ和Ⅲ为主,渐渐Ⅲ减少,Ⅰ增多,最后Ⅰ占主导地位,后期出现少量Ⅱ。
(5)在开始加入干酵母,2 d后加入降酸酵母的发酵过程中分离出3种基因型:Ⅵ、Ⅷ和Ⅸ。Ⅵ在此过程中渐渐变多主导发酵,Ⅷ、Ⅸ开始不存在,中后期突然出现。
3 结论
破碎时期一般以葡萄汁有孢汉逊酵母和克鲁维毕赤氏酵母为主,还有少量东方伊萨酵母等。酿酒酵母数量缓慢增多,葡萄汁有孢汉逊酵母、克鲁维毕赤氏酵母等其他酵母逐渐减少,最后酿酒酵母占主导地位,其他酵母基本消失。
[1]刘爱国,刘延琳.宁夏葡萄自然发酵过程中酵母菌的分子生物学鉴定[J].西北农林科技大学学报,2008(11):203-207.
[2]王恭堂.葡萄酒与微生物[J].中外葡萄与葡萄酒,1999(3):52-73.
[3]宋尔康.葡萄酒微生物学[M].北京:轻工业出版社,1989.
[4]李华,王华,袁春龙,等.葡萄酒化学[M].北京:科学出版社,2005.
[5]李华,王华,袁春龙,等.葡萄酒工艺学[M].北京:科学出版社, 2007.
[6]张春晖,李华.葡萄酒微生物学[M].西安:陕西人民出版社, 2003.
[7]罗惠波,李光辉.耐酸酵母菌的筛选研究[J].四川理工学院学报(自然科学版),2004,17(3):151-154.
[8] 薛军侠,徐艳文,刘延琳,等.WL培养基在酿酒酵母筛选中的应用[J].中国酿造,2007(9):36-39.
[9]王泽举,刘延琳.新疆葡萄酒自然发酵过程酵母菌的种类和动态变化[J].华中农业大学学报,2008(10):271-280.
[10]申彤.果酒酵母的选育研究进展[J].酿酒,2005,32(1):43-44.
[11]黄亚东.优良葡萄酒酵母分离选育的研究[J].酿酒,1998(5):38-39.
[12]张红梅,郭俊艳,于莲波.葡萄酒的生产及对微生物的控制[J].食品工业,2003(4):27-28.
Interactionsof Yeast Strains in the Fermentation Processof Cabernet Sauvignon
LIMeihua
(People'sGovernmentof Beigu,Yiliang,Yunnan 652112,China)
WL nutrientagar culturemedium was used for preliminary classification of strains isolated from different fermentation process.The results suggested that those strainsbelonged to 5genera including S.cerevisiae,Hanseniaspora uvarum,Pichia kluyveri,Issatchenkia orientalis and Candida.Then 26S rDNA D1/D2 amplification and sequencing of the isolated strains were performed.The sequencing results through Blast comparison indicated the constituent ratio of these strains in different fermenting stage and further revealed the bio-diversity of yeast strainsand the dynamic changeof differentbacteria species.On thisbasis,161 yeaststrainswere classified into 9gene typesby using interdelta analysis.Furthermore,the composition and the change of yeaststrainsof these 9gene types in compound fermentationwere investigated to provideevidence for theutilization of acid-reducing yeaststrains.(Trans.by YUEYang)
compound fermentation;classification and identification;interaction;interdeltaanalysis
TS261.1;TS262.6;TS261.4
A
1001-9286(2016)11-0060-05
10.13746/j.njkj.2016254
2016-08-15
李梅花(1975-),女,云南宜良人,工程师,研究方向为葡萄栽培与酿酒。

