婴儿食品中牛磺酸含量测定及其不确定度分析
娄婷婷,赵婷,温华蔚,郑文杰
(天津出入境检验检疫局,天津300461)
婴儿食品中牛磺酸含量测定及其不确定度分析
娄婷婷,赵婷,温华蔚,郑文杰
(天津出入境检验检疫局,天津300461)
利用高效液相色谱法测定婴幼儿食品中牛磺酸的含量并根据《化学分析测量不确定度评定》和《测量不确定度评定与表示》中的有关规定对其进行测量不确定度的分析评估,最后进行标准不确定度的合成以及计算其扩展不确定度;婴幼儿食品中牛磺酸检测结果为(33.85±0.94)mg/100g,k=2,p=95%,最低检出限为0.016 5mg/100 g。
牛磺酸;不确定度;婴幼儿食品
牛磺酸(Taurine)即β-氨基乙磺酸,又称牛胆碱、牛胆素,在动物组织中主要以游离形式存在,是一种非蛋白质形式的氨基酸,为婴幼儿生长发育过程中至关重要的营养素[1-2]。对婴幼儿早期大脑发育、神经系统发育、视力发育以及钙质的吸收等具有非常重要的作用[3]。婴幼儿体内合成牛磺酸的酶系尚未成熟,因此奶粉中添加接进母乳水平的牛磺酸能有效保障婴幼儿的身体发育[4]。此外,牛磺酸具有特殊的生理功能,提高免疫力、缓解疲劳、调节神经传导以及抗病毒等生物活性[5]。但是补充过量的牛磺酸对身体健康则可能抑制体内其它营养元素的吸收,因此我国及欧盟等均规定婴幼儿食品中牛磺酸的含不高于3mg/100 kJ[6-7]。因此,分析测定婴幼儿食品中牛磺酸的含量对于评价婴幼儿食品的营养品质是非常有必要的。
目前,国内外测定牛磺酸主要方法有滴定法[8]、比色法[9]、氨基酸自动分析法及高效液相色谱法[10]等。滴定法和比色法容易受到其他氨基酸的干扰,误差相对较大;氨基酸自动分析法因价格昂贵限制使用范围;高效液相色谱法因精确度、灵敏度较高,样品处理比较简单,能够快速进行样品分析而被广泛地应用。高效液相色谱法有柱前衍生和柱后衍生法,后者需要柱后衍生器等专用设备。鉴于以上测定方法优缺点,本试验采用柱前衍生法,以丹磺酰氯作为衍生试剂,来测定婴幼儿蔬果辅食泥中牛磺酸含量,并针对高效液相色谱法(HPLC)测定乳制品中牛磺酸含量的方法[11]GB 5413.26-2010《食品安全国家标准婴幼儿食品和乳品中牛磺酸的测定》,根据JJF 1135-2005《化学分析测量不确定度评定》和JJF 1059.1-2012《测量不确定度评定与表示》[12]中的有关规定对婴幼儿辅食中牛磺酸含量测定的不确定度进行分析,为保证测定测量结果的可靠性和科学性提供依据。
1 材料与方法
1.1 材料与仪器设备
牛磺酸标准品:德国Dr.Ehrenstorfer GmbH;乙腈(色谱纯):迪马科技公司;无水乙醇;丹磺酰氯(分析纯):Sigmaaldrich公司。
Waters高效液相色谱仪配2998紫外检测器:美国Waters公司;C18色谱柱(4.6mm×250mm×5m):迪马科技;纯水仪;分析天平:梅特勒-托利多仪器上海有限公司;超声波清洗器:昆山市超声仪器有限公司;台式高速离心机:德国Eppendorf公司。
1.2 样品预处理
1.2.1 样品制备
参考GB 5413.26-2010《食品安全国家标准婴幼儿食品和乳品中牛磺酸的测定》中前处理的方法,称取待测样品约2.0 g(精确到0.01 g)于50mL容量瓶中,加入40mL温水溶解,充分混匀,置超声波振荡器上振荡10min,冷却到室温。加1.0mL乙酸锌溶液沉淀剂,涡旋混合后,加入1.0mL,涡旋混合,用水定容至50mL,充分混匀,试液于5 000 r/min下离心5min,取上清液备用。
1.2.2 柱前衍生
将上述上清液1mL加入到试管中,加1mL碳酸钠缓冲液和1mL丹磺酰氯溶液,充分涡旋混合,在室温下避光反应2 h进行衍生(反应过程中要摇晃几次),然后加入0.1mL盐酸甲胺溶液涡旋混合用来终止反应,混合液静置避光,沉淀完全后,取上清液经0.45μm微孔滤膜过滤,取滤液备用。衍生物在4℃可避光保存48 h。另取一系列标准工作液各1mL,与待测试液同步进行衍生。
1.3 色谱条件
色谱柱:C18色谱柱(4.6mm×250mm×5m)。
流动相:乙酸钠缓冲液(pH4.2)(10mmol/L)。称取1.36 g乙酸钠,加800mL水溶解,用冰乙酸调节pH值至4.2,用水定容到1000 mL,经0.45μm微孔滤膜过滤。
流量:1.0mL/min;检测波长:245nm;进样量:10μL;柱温:35℃。
2 结果与分析
2.1 波长选择
牛磺酸与单磺酰氯反应生成的衍生物在254 nm处有最大吸收峰,采用254 nm为测定波长。
2.2 流动相配比选择
选用乙腈与10mmol/L的乙酸钠作为流动相,试验证明在流速为1mL/min,随着流动相中乙腈比例的增加,牛磺酸的出峰时间明显提前,乙腈-0.01mol/L乙酸钠70∶30(体积比)的流动相出峰时间为6min左右,分离效果最佳,选择体积比为70∶30(体积比)的乙酸钠-乙腈缓冲液作为流动相。
2.3 工作曲线
分别配置浓度为为 0、0.2、1.0、5.0、10.0、15.0、20.0μg/mL牛磺酸标准溶液,进行HPLC分析,每种浓度测定2次,取平均峰面积,以牛磺酸的浓度与色谱峰面积来绘制标准工作曲线,所得线性回归方程为y= 19 143x+1227,R2=0.999 7,标准工作曲线及各浓度叠加色谱图见图1。

图1 标准曲线及牛磺酸标准溶液色谱图Fig.1 Calibration curvesand thespectra of standard solutionsof taurine
所有标准溶液以及待测样品的衍生化反应时间应保持一致。
2.4 含量计算公式
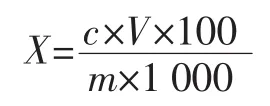
式中:X为待测样品中牛磺酸的含量,mg/100g;c为由标准曲线得出的样品浓度,mg/L;m为称取样品的质量,g;V为待测样品溶液体积,mL。
3 不确度评定
3.1 不确定度的来源
测定的不确定度主要标准物质、样品峰面积的积分、标准工作曲线的拟合、样品称量、定容体积、样品前处理操作过程等几个方面引入的。使用方法回收率表征方法偏倚和反复性,将其他分量归并成实验室偏倚分量,它们都会对测定结果的不确定度产生影响。
3.2 不确定度分量的计算
3.2.1 由标准物质引入的相对不确定度
3.2.1.1 标准物质的相对不确定度
根据牛磺酸标准物质证书提供的信息,其不确定度为0.5%,包含因子k=2,属B类评定,其相对标准不确定度为:
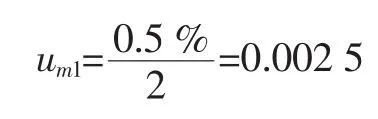
3.2.1.2 标准储备液配制过程引起的不确定度
1)称量过程中引入的不确定度
用最小刻度值为0.01mg的电子天平称取待测样品,其重复性已包含于回收试验中,校准天平过程中引入了独立的不确定度分量。根据电子天平计量检定证书提供的信息,其允许误差极限为±0.01mg,该不确定度按均匀分布考虑,包含因子,则标准不确定度可用下式计算
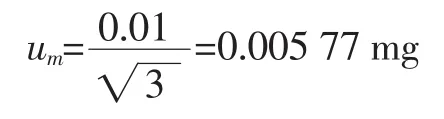
标准储备液配制的过程是精确称取100.00mg牛磺酸标准物质,称标样量为0.100 00 g,则其相对标准不确定度为:

2)配制校准溶液过程中由玻璃器皿体积校准产生的不确定度
按照JJG 196-2006《常用玻璃量器检定规程》[13]的要求,该过程使用的玻璃容器,均有相应的最大容量允差,按矩形分布考虑,k=。试验中采用的100mL容量瓶(A级),按检定证书给定其最大允许误差为±0.10mL,按照矩形分布换算成标准偏差为:
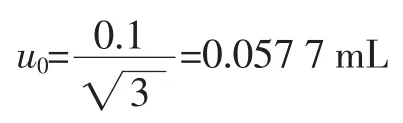
其标准标准不确定度为:

3)稳定引起的玻璃器皿的不确定度
实验室的温度在(20±4)℃变化,20℃玻璃膨胀系数为2.5×10-5/℃,水体积膨胀系数为2.1×10-4/℃,容量瓶校准温度与使用温度不同引起的的标准不确定度为:

由以上合成得出
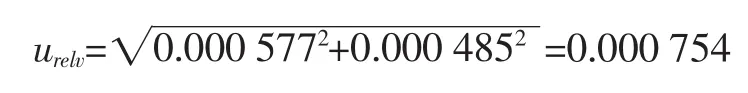
因此,标准储备液配制过程的相对不确定度:
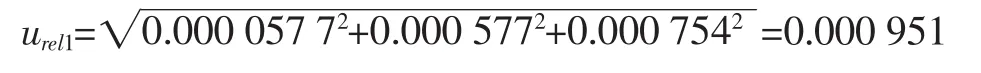
3.2.1.3 配制标准工作溶液过程中产生的不确定度评定
由牛磺酸标准储备液逐级稀释得到一系列标准工作溶液。在配制标准工作液过程中使用的一系列玻璃量具,均有相应的最大允差,按照JJG 196-2006《常用玻璃量器检定规程》的要求,按照矩形分布考虑,取,相对不确定度分量见表1。
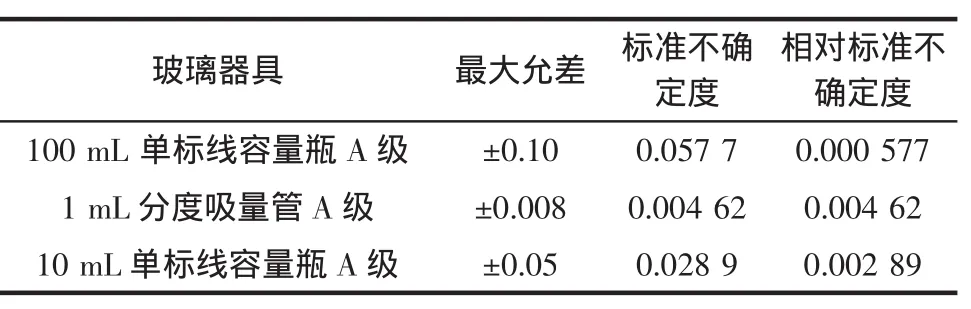
表1 玻璃容器的不确定度分量Table1 Uncertainty of glassapparatus
合成不确定度为
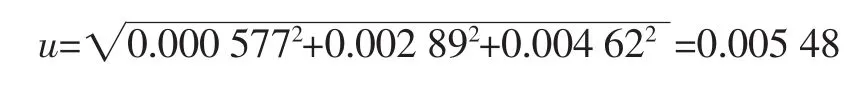

表2 溶液配制过程中由温度变化引起的不确定度Table2 Uncertainty of tem perature change during the p reparation of thesolution
合成的相对标准不确定度为:
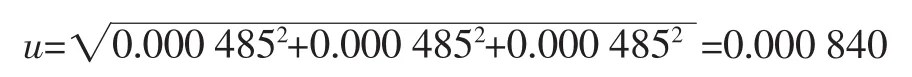
标准工作液配制过程产生的不确定度评定合成为

3.2.2 标准工作曲线拟合引入的相对不确定度
分别配置浓度为为0.2、1.0、5.0、10.0、15.0、20.0μg/mL牛磺酸标准溶液,进行HPLC分析,每种分析测定2次,则自由度n=12,拟合标准溶液浓度和峰面积曲线,标准曲线数据见表3。
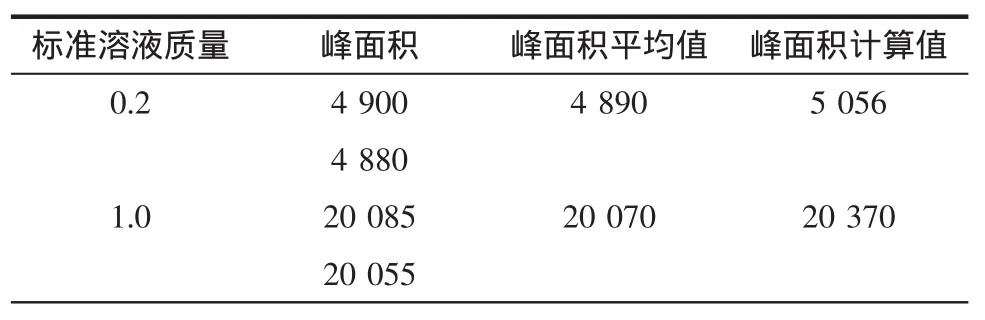
表3 标准曲线数据表Table3 Data of calibration curves

续表3 标准曲线数据表Continue table3 Data of calibration curves
牛磺酸的浓度与色谱峰面积之间回归方程为y= 19 143x+1 227,R2=0.999 7,其中b=19 143,a=1 227,
其中标准曲线的残余偏差SR为:
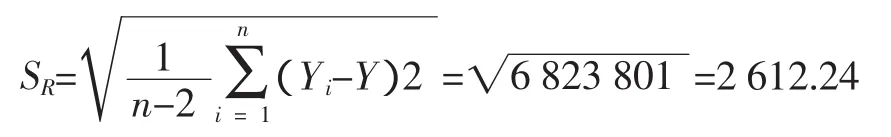
则由拟合曲线产生的标准不确定度利用以下公式计算:
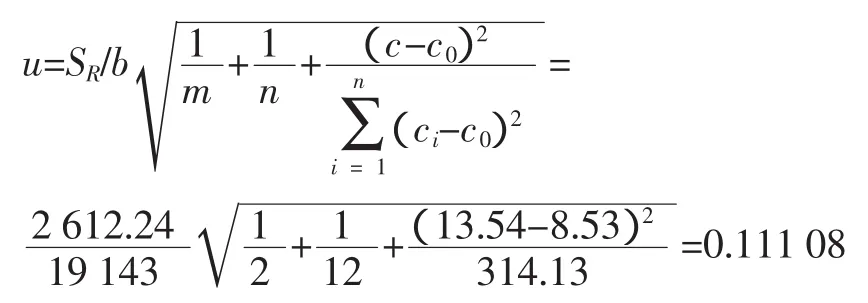
3.2.3 重复测定引入的不确定度
样品经测定6次后,峰面积分别为254404、251739、245 189、256 907、286 589、268 179。计算得到样品溶液中牛磺酸的平均质量浓度为13.54μg/mL。
样品溶液峰面积的标准不确定度按贝塞尔公式计算:

3.2.4 标准工作液与样品液峰面积比的不确定度
标准工作液与样品液峰面积的重复性已包含于回收率的不确定度中,峰面积的偏倚主要由HPLC的校准过程引入。根据HPLC的校准证书,其衰减期的相对误差为0.8%,按照均匀分布处理,峰面积的相对标准不确定度为:

则峰面积比的不确定度为:
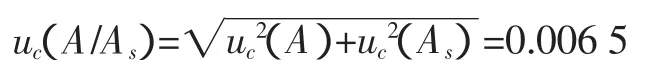
3.2.5 前处理回收率
由于样品前处理不完全或处理过程中导致损失或污染等,将使牛磺酸不能100%进入到测定液中,通过对待测样品添加标准溶液来计算回收率,单独6次样品添加回收率的结果分别为104.0%、95.7%、108.1%、103.2%、98.3%、106.2%。平均回收率为r= 102.6%,标准偏差s为0.046 060 2,根据A类评定,采用平均值的标准偏差来计算标准不确定度,则标准不确定度如下式表示:

相对不确定度为:
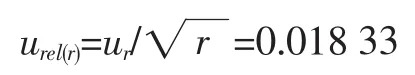
3.3 样品进样引入的不确定度
3.3.1 称样量的不确定度评定
称量使用的电子天平经计量合格,根据检定证书,其最大允许误差±0.01mg,其置信水平99%,按正态分布考虑,包含因子k=3,则标准不确定度为:
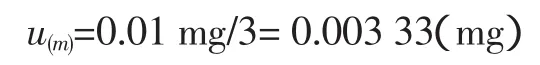
样品称样量为2.00 g,则其相对标准不确定度为:
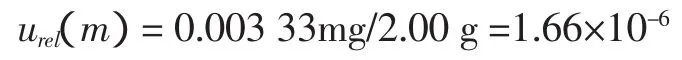
3.3.2 进样引入的不确定度
HPLC进样采用的是微量进样器(根据证书,其为不确定度1%),按均匀分布考虑,B类评定,进样引入的相对不确定度分量为:
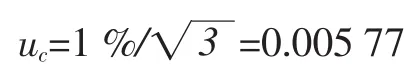
3.3.3 进样量的不确定度
采用同一进样器进行等体积进样,而这两个体积量并没有体现在被测量的计算公式中,但实际上是使用了两个体积量的比值,而且两者之间存在正相关关系,当实验室的温度变化不大时,可以认为其不确定度近似相等,因此可以认为对不确定度没有贡献。
3.4 由分析仪器引入的相对标准不确定度
根据计量检定证书,采用的HPLC仪器的相对标准不确定度为3%。由进样引起的合成相对标准不确定度为:

3.5 相对合成标准不确定度
根据以上计算结果,利用此方法测定的合成标准不确定度可用下式进行计算:

3.6 扩展不确定度
依据JJF 1135-2005《化学分析测量不确定度评定》[14],本试验可采用置信概率p=95%、包含因子k=2进行计算,则扩展不确定度为:
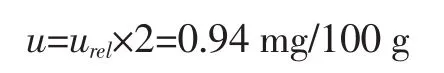
3.7 样品的测定
对样品进行相应的前处理,得到的待测样品溶液按照上述的分析方法进行HPLC检测,记录待测样品中相应的峰面积,根据标准工作曲线,外标法定量,经测定,婴儿辅食泥中牛磺酸的含量为(33.85±0.94)mg/ 100 g,k=2,p=95%。
4 结论
本试验通过分析利用HPLC法测定样品中牛磺酸含量的试验过程,对影响牛磺酸测定不确定度各分量进行评价,得出标准曲线的拟合过程、样品前处理过程等对不确定度贡献相对较大,因此在试验过程中应在这几方面注意控制,以进一步提高检测结果的准确性。经测定,本试验样品中牛磺酸的含量为(33.85± 0.94)mg/100 g,k=2,p=95%。最低检出限为0.016 5mg/ 100 g,线性相关系数为0.999 7。本方法测定婴幼儿食品中牛磺酸的浓度,具有前处理操作简便,检测灵敏度高,结果准确等优点,适合一般实验室进行含量分析。
[1] 赵振宇,张韻慧.牛磺酸药理作用的研究新进展[J].中国医院药学杂志,2009,29(16):1390-1393
[2] 王芬,张婷,顾振新,等.高效液相色谱法测定紫菜中牛磺酸含量[J].食品科学,2012,33(18):162-164
[3] 刘亚风,祝伟霞,袁萍,等.婴幼儿配方奶粉中牛磺酸质量分数的检测方法[J].中国乳品工业,2010,38(2):52-54
[4] 黄喆雯,唐钦强.2,4-二硝基氟苯柱前衍生高效液相色谱法测定婴幼儿配方乳粉中牛磺酸含量[J].食品科学,2008,29(3):415-417
[5]白小琼,孔德义.牛磺酸研究进展[J].中国食物与营养,2011,17(5): 78-80
[6]中华人民共和国卫生部.GB 10765-2010食品安全国家标准婴儿配方食品[S].北京:中国标准出版社,2010:1-7
[7]中华人民共和国卫生部.GB 10767-2010食品安全国家标准较大婴儿和幼儿配方食品[S].北京:中国标准出版社,2010:1-6
[8]卢忠,罗一帆.中和滴定法测定牛磺酸含量[J].数理医药学杂志, 2000,13(4):350
[9] 李咏梅,李人宇.高灵敏度分光光度法测定饲料中牛磺酸含量[J].中国粮油学报,2013,28(12):110-114
[10]孙洁.氨基酸分析仪和HPLC测定食品中牛磺酸的研究比较[J].食品工业,2012(8):123-125
[11]中华人民共和国卫生部.GB 5413.26-2010食品安全国家标准婴幼儿食品和乳品中牛磺酸的测定[S].北京:中国标准出版社, 2010
[12]国家质量监督检验检疫总局.JJF 1059.1-2012测量不确定度评定与表示[S].北京:中国质检出版社,2012:1-27
[13]国家质量监督检验检疫总局.JJG 196-2006常用玻璃量器检定规程[S].北京:中国计量出版社,2006:6-9
[14]国家质量技术监督局.JJF 1135-2005化学测量分析中的不确定度评定[S].北京:中国计量出版社,2005:1-8
Determ ination and Uncertainty Evaluation for Taurine in Infant Formula
LOU Ting-ting,ZHAOTing,WENHua-wei,ZHENGWen-jie
(Tianjin Entry-Exit Inspection and Quarantine Bureau,Tianjin 300461,China)
Amethod of high performance liquid chromatography was developed to detect taurine in infant food and uncertainty for determining taurine in infant formula food wasestablished to evaluate the uncertainty of determining taurineaccording to the relevant regulationsgiven in
taurine;uncertainty;infant formula food
10.3969/j.issn.1005-6521.2016.24.028
2015-12-23
天津检验检疫局科技项目(TK079-2013,TK044-2013)
娄婷婷(1985—),女(汉),高级工程师,博士,研究方向:食品分析与检测。

