遍山红总黄酮的含量测定
潘立卫 罗泽萍 韦志巧 何燕
(1.河池学院 化学与生物工程学院, 广西 宜州 546300; 2.广西大学 农学院, 广西 南宁 530000)
遍山红总黄酮的含量测定
潘立卫1罗泽萍1韦志巧2何燕1
(1.河池学院 化学与生物工程学院, 广西 宜州 546300; 2.广西大学 农学院, 广西 南宁 530000)
目的:建立遍山红中总黄酮含量的测定方法,为其研究开发提供科学依据。方法:总黄酮的含量采用紫外分光光度法进行测定,以杨梅苷为对照品,在最大吸收波长500 nm处测定吸光度。结果:遍山红总黄酮的线性范围为20~120 μg (r=0.999 7),加样回收率为100.96%,RSD为2.29%;叶子的总黄酮含量略高于茎的总黄酮含量。结论:该方法简便、准确、灵敏度高,可用于遍山红药材的质量控制参考。
遍山红;总黄酮;杨梅苷;紫外分光光度法
遍山红(Oxysporapaniculata(Don) DC.)为野牡丹科植物尖子木的根或全株,又名大叶朝天罐,分布于广西、贵州、云南、西藏等地[1]。民间常用于治疗湿热泻痢,风湿痛,吐血,尿血,月经过多,产后血崩,带下,外伤出血,跌打肿痛,疮肿,腹泻和痢疾等症[2-4],现代药理研究报道遍山红具有可抑制结核杆菌的作用[5]。此外,遍山红可做为一种蔬菜食用[6],其主要化学成分含有β-谷甾醇、胡萝卜苷、齐墩果酸、熊果酸、没食子酸、杨梅苷、山奈酚、槲皮素等[5]。目前,国内外对遍山红的研究主要集中在植物分类学、园林景观学和资源学等领域[7-9],但对其化学成分和药理作用的研究甚少,质量标准控制方面也未见报道。本文首次建立了紫外分光光度法测定遍山红中总黄酮含量的测定方法,该方法简单、快捷,为进一步研究遍山红的质量标准控制和药用植物资源深度开发利用提供科学依据。
1 仪器与材料
1.1 仪器
Agilent 8453型紫外可见分光光度计;AR224CN电子分析天平;Millipore D-Q3超纯水器;KQ250DE型超声波清洗器。
1.2 材料
杨梅苷对照品由河池学院化学与生物工程学院制药工程实验室提供,经HPLC检测,杨梅苷含量>98%;超纯水;其他试剂均为分析纯。遍山红药材于2015年7-8月份在广西河池市5个县市采集,经河池学院化学与生物工程学院植物学邓晰朝副教授鉴定为野牡丹科尖子木Oxysporapaniculata(Don) DC.的干燥茎叶。
2 总黄酮含量测定
2.1 对照品溶液的制备
精密称取干燥至恒重的杨梅苷对照品10.0 mg,置于50 mL量瓶中;加入70%乙醇使其溶解,定容,得对照品溶液(每1 mL含杨梅苷0.20 mg)。
2.2 供试品溶液的制备
遍山红药材地上茎,用铡刀切成3-5 mm薄片后,自然干燥,对角线法取样,粉碎,过2号筛。精密称取药材粉末1 g,置具塞锥形瓶中,精密加入70%乙醇25 mL,密塞,称定质量,设定温度30 ℃,超声提取(功率: 250 W,频率: 40 kHz) 40 min,冷却至室温称质量,补足损失的溶剂质量,摇匀,滤过,取续滤液10 mL,定容至100 mL,即得。
2.3 标准曲线的绘制
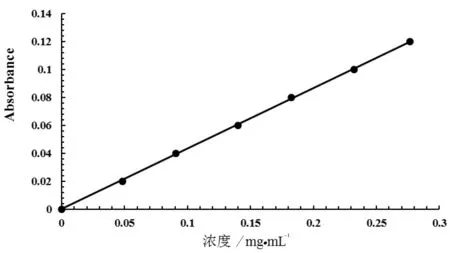
图1 杨梅苷线性关系图
精密吸取对照品溶液1.0, 2.0, 3.0, 4.0, 5.0, 6.0和0 mL(空白),分别置于10 mL容量瓶中,加入70%乙醇至7 mL,加5%亚硝酸钠溶液0.3 mL,混匀,放置10 min,加10%三氯化铝溶液0.3 mL,混匀,放置10 min,加1 mol/L氢氧化钠溶液2 mL,加70%乙醇至刻度,摇匀,静置10 min,在最大吸收波长500 nm处测定吸收度。以吸收度(A)为纵坐标,浓度(C)为横坐标做标准曲线,得回归方程为A=0.434 2C-0.000 2(r=0.999 7,n=6)。结果表明,杨梅苷在20~120 μg范围内与吸收度呈良好的线性关系(见图1)。
2.4 精密度试验
精密移取对照品溶液1 mL,按“2.3”项的方法,自“加入70%乙醇至7 mL”起,依次显色,测定6次,结果对照品平均吸光度值为0.047 6,RSD为1.44%,表明仪器精密度良好。
2.5 稳定性试验
精密移取供试品溶液1 mL,按“2.3”项的方法,自“加入70%乙醇至7 mL”起,依次显色,每隔20 min测其吸收度,连测12次,每次平行测定3次取平均值,结果供试品平均吸光度值为0.154 6,RSD为2.61%,表明样品在3 h内稳定,满足测定要求。
2.6 重复性试验
精密称取同一批(BHS-1)遍山红药材粉末共6份,每份1 g,按“2.2”项的方法制备样品溶液,按“2.3”项的方法测定,自“加入70%乙醇至7 mL”起,依次显色,测定吸光值,结果平均吸光度值为0.155 8,RSD为1.06%,表明方法重复性良好。
2.7 加样回收率试验
取已知遍山红药材粉末共6份,每份0.5 g,精密称定,再分别精密加入5.3 mg/mL杨梅苷对照液1 mL,按“2.2”项的方法操作,得到供试品溶液后,照“2.3”项的方法,自“加入70 %乙醇至7 mL”起,依次显色,测定吸光度,结果见表1。
表1 加样回收率实验(n=6)
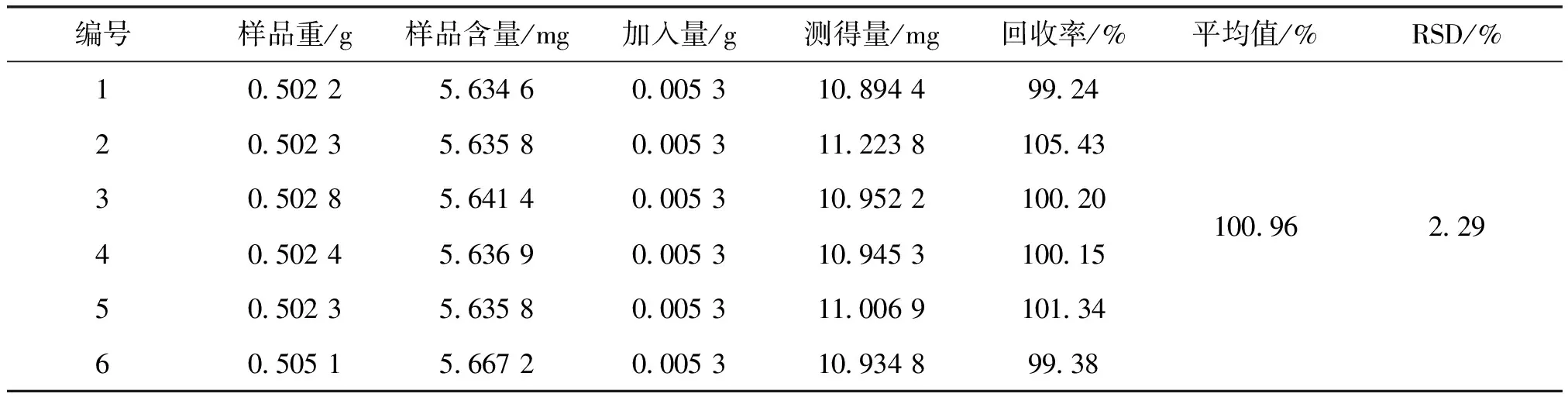
编号样品重/g样品含量/mg加入量/g测得量/mg回收率/%平均值/%RSD/%105022563460005310894499242050235635800053112238105433050285641400053109522100204050245636900053109453100155050235635800053110069101346050515667200053109348993810096229
2.8 样品测定
精密称取5批遍山红茎和叶的药材粉末各5份,每份1 g,按“2.2”项的方法制备样品溶液,按“2.3”项的方法测定,自“加入70 %乙醇至7 mL”起,依次显色,测定吸光值,同一批次药材平行测定3份,取平均值计算总黄酮含量,结果5批不同产地遍山红药材的测定结果见表2。
表2 5批不同产地遍山红药材及其杨梅苷含量测定结果

编号产地批号叶含量/mg·g-1茎含量/mg·g-11保 安BSH-1108710722大 兴BSH-210499973地 苏BSH-39809374大 化BSH-48618185七百弄BSH-510801056
3 讨论
杨梅苷是具有多酚羟基的黄酮苷类物质,多存在于杨梅、藤茶、龙眼叶和蛇葡萄属等植物中[9-11],具有多种药理活性,表现出抗氧化、抗扩张血管、抗炎镇痛的作用[12],还具有降压、降血糖、抑菌作用[13-15]。本实验研究表明杨梅苷做为主要的黄酮类成分存在于遍山红中,含量达到1%左右。目前,2015版药典尚未收录有关遍山红的质量控制标准,本研究首次采用紫外分光光度法对遍山红中的茎叶总黄酮含量进行测定,发现其叶子含量略高于茎的含量,为合理选择药用部位、深度开发利用药材提供实验基础。
目前,总黄酮的含量测定方法有:紫外区直接测定法、可见区络合法、液相色谱法等,其中前两种方法较为常见,且方法成熟快速,而液相色谱主要应用于单一黄酮化合物的测定;另外,紫外区直接测定总黄酮的方法易受测液的基底(苯类,共轭烯烃等)影响产生误差。络合法与直接测定法不同,其原理为:金属离子与酮羰基、邻位羟基形成配位化合物,使吸收带发生位移,从而克服了被测液基底的影响,故本文选择使用紫外可见区络合法测定药材总黄酮含量。
4 结论
本文建立了紫外分光光度法检测遍山红中总黄酮的方法,该法快速,简单,准确,可为该药材的质量控制和定量分析提供一定科学依据。
[1] 国家中医药管理局《中华本草》编委会.中华本草[M].上海科技出版社, 1999: 689.
[2] 贵州中医药研究所. 贵州中草药名录[M]. 贵阳: 贵州人民出版社, 1988: 375.
[3] 四川省中药研究所. 四川常用中草药[M]. 成都: 四川人民出版社, 1971: 603.
[4] 云南省卫生局革命委员会. 云南中草药(续集) [M]. 昆明: 云南人民出版社, 1975: 78, 440, 316.
[5] 王皓,陈燕方,温远影.尖子木化学成分研究∥中国植物学会七十周年年会论文摘要汇编[C].北京:高等教育出版社,2003.
[6] Kayang H.Tribal knowledge on wild edible plants of Meghalaya, Northeast India [J]. Indian Journal of Traditional Knowledge, 2007, 6 (1): 177-181.
[7] CHEN Wen-Hong, SHUI Yu-Min, ZHOU Lu-Men. Additional notes on Melastomataceae of China[J]. Acta Phytotaxonomica Sinica, 2007, 45(4): 587-592.
[8] 赵健, 仇硕, 李秀娟,等. 广西野牡丹科观赏植物种质资源及开发前景[J]. 河北农业科学, 2008, 12(7): 80-82.
[9] Liao HW, Liu EG, Wang DY. Chemical constituents of the bark of Myrica ruba[J]. Cent South Pharm, 2006,4(3):196-199.
[10] A Suga,Y Takaishi,H Nakagawa,et al. Chemical Constituents from Fruits and Seeds of Myrica rubra (Myricaceae)[J]. Natural Medicines,2005,59(2):70-75.
[11] Liu ZG, Zhang YC, Ji S, et al. Isolation and identification of constituents from bark of Myrica ruba (Lour.) Sieb. et Zucc [J]. J Shenyang Pharm Univ, 2010, 27(1): 34-36.
[12] Meotti FC, Posser T, Missau FC, et al. Involvement of p38MAPK on the antinociceptive action of myricitrin in mice [J]. Biochem Pharmacol, 2007, 74(6): 924-931.
[13] 张立. 杨梅苷对四氧嘧啶模型小鼠降血糖作用的初步研究[J]. 中国现代药物应用, 2009, 3(15): 29-30.
[14] 张秀桥, 沈伟, 陈树和, 等. 大叶蛇葡萄提取物对肾性高血压大鼠降压作用的实验研究[J]. 中国医院药学杂志,2008,28(24): 2095-2096.
[15] 张绍勇,李桥,陈安良.杨梅叶抑菌活性成分初步分离与鉴定[J].农药学学报,2011, 13(2) :149-154.
[责任编辑 刘景平]
Determination of Total Flavones ofOxysporaPaniculata(Don) DC.
PAN Liwei1, LUO Zeping1, WEI Zhiqiao2, HE Yan1
(1.School of Chemistry and Biological Engineering, Hechi University, Yizhou, Guangxi 546300; 2.Agriculture College, Guangxi Unicersity, Nangning, Guangxi 530000, China)
Objective: To establish the method for determining the content of total flavonoids ofOxysporapaniculataand provide scientific basis for the development and utilization of this plant. Method: The total flavonoids are analyzed by spectrophotometry at the maximum absorption wavelength 500 nm with myricitrin as reference substance. Result: The linear range of total flavonoids is 20~120 μg (r=0.999 7), and its average recovery is 100.96%, RSD = 2.29%. The content of total flavonoids in the extract from the lea-ves is higher than that of the aerial parts. Conclusion: The method is simple, sensitive and accurate, and can be used for the quality control of Oxyspora paniculata.
Oxysporapaniculata(Don) DC.; total flavonoids; myricitrin; UV
R284.1
A
1672-9021(2016)05-0019-04
潘立卫(1987-),男,广西都安人,河池学院化学与生物工程学院实验师,主要研究方向:中草药有效成分。
广西教育厅高校科学技术研究基金资助项目(KY2015LX367);河池学院青年科研基金资助课题(XJ2015QN010);“广西高等教育创优计划”本科教学项目(桂教高教〔2015〕93号)。
2016-06-21

