拉科酰胺中脲类化合物杂质的合成及结构鉴定*
彭海燕,蔡润发,廖祝元,曾繁荣,范卫永
(江西青峰药业有限公司技术中心,江西 赣州 341000)
·有机药物化学·
拉科酰胺中脲类化合物杂质的合成及结构鉴定*
彭海燕,蔡润发,廖祝元,曾繁荣,范卫永†
(江西青峰药业有限公司技术中心,江西 赣州 341000)
以N-Boc-D-丝氨酸为起始原料,合成了拉科酰胺原料药生产中可能产生的两种脲类化合物杂质,其结构经1H NMR和13C NMR谱及MS确证;讨论了两种杂质可能的产生途径,并提出了减少和避免杂质产生的方法.
拉科酰胺;杂质;化学合成;脲类化合物
拉科酰胺[1-4](1acosamide)化学名为(R)-2-乙酰氨基-N-苄基-3-甲氧基丙酰胺,是由比利时优时比公司(UCB Pharma)的子公司施瓦茨法姆制药公司(Schwarz Pharma)开发的一种新型N-甲基-D-天门冬氨酸(NMDA)受体甘氨酸位点结合拮抗剂,分别于2008年8月、9月和10月由欧盟、德国与英国和美国FDA批准上市,商品名为Vimpat.临床上主要用于有一定攻击性的癫痫患者治疗的辅助疗法.

图1 杂质G 图2 杂质H
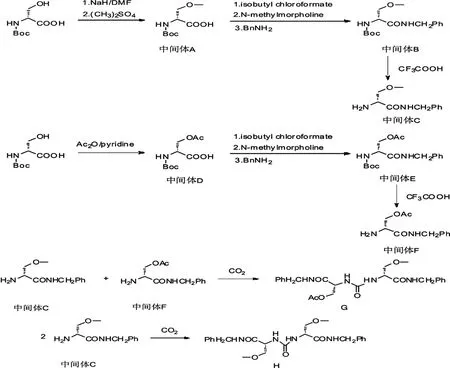
图3 拉科酰胺杂质G、杂质H的合成路线
在对原料药拉科酰胺进行HPLC分析中,采用面积归一化法,检测波长为258 nm,发现两种杂质G(图1)和H(图2),其保留时间分别为25 min和26 min.经过1H NMR和13C NMR谱及质谱分析确定了其结构.为制定拉科酰胺质量标准,有效控制产品质量,同时验证杂质可能形成的原因,本实验设计杂质G和H的合成路线(图3),以N-Boc-D-丝氨酸为起始原料,经羟基保护[5-6]、酰胺化[7]、脱Boc[8]、脲[9-10]形成反应分别得到杂质G和H.并讨论了两种杂质的产生原因,以便今后生产中能有效控制.
1 实验部分
1.1 仪器与试剂
HP1100 高效液相色谱仪(美国安捷伦公司);Agilent 6210质谱仪;1H NMR和13C NMR用Bruker-400M型超导核磁共振仪测定(TMS为内标);试剂均为市售分析纯.
1.2 杂质G的合成
1.2.1 中间体C的合成:
将30.0 g N-Boc-D-丝氨酸溶解在250 m的LDMF中,将内温控制在-15 ℃,分批加入3.6 g NaH.加完后在-15 ℃搅拌反应1.0 h;控制内温在-15 ℃滴加30.0 g硫酸二甲酯,滴加完毕,在-15 ℃先保温反应1 h后,再升温到5 ℃反应3 h;将反应混合液慢慢加入到300 g冰水,加完后用150 mL甲苯萃取,水相中分批加入210.0 g 柠檬酸固体,用3×150 mL二氯甲烷萃取,合并有机相.依次用150 mL水、150 mL饱和食盐水洗涤,有机相用无水硫酸钠干燥,过滤,滤液浓缩至干,得29.1 g中间体A.
将上述29.1 g中间体A、150 mL二氯甲烷加入反应瓶中,将内温控制在-15 ℃,滴加18.0 g氯甲酸异丁酯,滴毕,在-15 ℃保温反应10 min,控制内温在-15 ℃滴加17.4 g N-甲基吗啉,滴毕,在-15 ℃保温反应1 h,控制内温在-15 ℃,分次加入16.5 g苄胺,加毕,升温到10 ℃反应3 h;TLC监测反应完全.反应液依次用100 mL水、60 mL 1M HCl、60 mL饱和NaHCO3溶液洗涤、60 mL水洗涤,无水硫酸钠干燥14 h.过滤,浓缩得油状物27.3 g中间体B.
将27.3 g中间体B和100 mL二氯甲烷加入反应瓶中,室温下加入33 mL三氟乙酸,搅拌反应2 h,TLC监测反应完全.反应液减压浓缩至干,加入150 mL乙酸乙酯后,用饱和NaHCO3洗涤至PH=7~8,无水硫酸钠干燥.过滤,浓缩得油状物9.6 g中间体C.
1.2.2 中间体F的合成:
将10.0 g N-Boc-D-丝氨酸溶解在50 mL吡啶中,加入10.0 g乙酸酐.加完后115 ℃搅拌反应8 h;减压浓缩除去吡啶,浓缩物加入100 mL二氯甲烷,依次用50 mL柠檬酸饱和溶液、用50 mL水、50 mL饱和食盐水洗涤,有机相用无水硫酸钠干燥,过滤,滤液浓缩至干,得11.8 g中间体D.
将上述11.8 g中间体D和50 mL二氯甲烷加入反应瓶中,将内温控制在-15 ℃,滴加6.0 g氯甲酸异丁酯,滴毕,在-15 ℃保温反应10 min,控制内温在-15 ℃滴加5.8 g N-甲基吗啉,滴毕,在-15 ℃保温反应1 h,控制内温在-15 ℃,分次加入5.5 g苄胺,加毕,升温到10 ℃反应3 h;TLC监测反应完全.反应液依次用30 mL水、20 mL 1M HCl、20 mL饱和NaHCO3溶液洗涤、30 mL水洗涤,无水硫酸钠干燥14 h.过滤,浓缩得油状物9.5 g中间体E.
将9.5 g中间体E、30 mL二氯甲烷加入反应瓶中,室温下加入11 mL三氟乙酸,搅拌反应2 h,TLC监测反应完全.反应液减压浓缩至干,加入50 mL乙酸乙酯后,用饱和NaHCO3洗涤至PH=7~8,无水硫酸钠干燥.过滤,浓缩得油状物3.4 g中间体F.
1.2.3 目标化合物杂质G的合成:
100 mL高压反应釜中,依次加入2.5 g中间体C、2.5 g中间体F、8 mL 1-丁基-3-甲基咪唑四氟硼酸盐和0.25 g氢氧化铯,密封后,导入50 atm的二氧化碳,搅拌,加热至160 ℃反应5 h,停止反应,体系降至室温后,加入30 mL饱和氯化铵溶液和50 mL乙酸乙酯,萃取分层,有机层用30 mL水洗涤,无水硫酸钠干燥.过滤,浓缩得油状物1.7 g.过柱分离得160 mg白色固体杂质G(展开剂:二氯甲烷/甲醇=10/1,Rf为0.7),经HPLC分析杂质G的纯度为99.7%.ESI-MS(m/z):493[M+Na]+.1H-NMR(CDCl3)δ:8.43(S,1H,NH1COCHCH2OAC),8.05(S,1H,NH1COCHCH2OCH3),7.09(S,2H,2NH1CH2Ph),7.20-7.32(m,10H,ArH),4.57(t,1H,CHCH2OAC),4.34(m,2H,CH2OAC),4.25(t,1H,CHCH2OCH3),4.12(m,2H,CH2OCH3),3.52(m,4H,2CH2Ph),3.25(m,3H,OCH3),1.87(S,3H,COCH3);13C-NMR (CDCl3, 400MHz) δ:174.02,174.62,175.19,143.70,143.67,133.16,133.15,131.83,131.81,131.69,76.69,68.90,63.11,59.39,57.07,47.00,27.25.
1.3 杂质H的合成
高压反应釜中,依次加入5.0 g中间体C、8 mL 1-丁基-3-甲基咪唑四氟硼酸盐和0.25 g氢氧化铯,密封后,导入50 atm的二氧化碳,搅拌,加热至160 ℃反应5 h,停止反应,体系降至室温后,加入30 mL饱和氯化铵溶液和50 mL乙酸乙酯,萃取分层,有机层用30 mL水洗涤,无水硫酸钠干燥.过滤,浓缩得油状物1.7 g.过柱分离得160 mg杂质H(展开剂:二氯甲烷/甲醇=3/1,Rf为0.3),经HPLC分析杂质G的纯度为99.7%.(展开剂:展开剂:二氯甲烷/甲醇=5/1,Rf为0.3)ESI-MS(m/z):443[M+H]+.1H-NMR(CDCl3)δ:8.31(t,2H,2NHCH2Ph),7.20-7.32(m,10H,2ArH),6.54(d,2H,NHCONH),4.55(m,4H,2PhCH2),3.41-4.36(m,4H,CH2OCH3),3.24(m,6H,2OCH3);13C-NMR (CDCl3, 400MHz) δ:170.61,157.04,139.39,128.23,127.04,126.71,73.02,58.36,53.36,42.14.
2 结果与讨论
杂质G和H属脲类化合物,分析拉科酰胺合成工艺,杂质G产生的可能原因:中间体(R)-N-苄基-2-((叔丁氧基)羰基氨基)-3-甲氧基丙酰胺在脱Boc时,同时有一部分羟基的甲基保护在氯化氢气体作用下也失去甲基保护,进而在后步反应中羟基也发生了乙酰化反应,在用碳酸氢钠后处理时产生的二氧化碳作用下与未失去甲基保护的中间体反应导致.杂质H可能原因:中间体(R)-N-苄基-2-((叔丁氧基)羰基氨基)-3-甲氧基丙酰胺在脱Boc保护后,在用碳酸氢钠后处理时产生的二氧化碳作用下反应导致.故脱Boc后处理时,用碳酸氢钠饱和溶液洗涤时减少洗涤时间或使用氢氧化钠替代碳酸氢钠,可减少和避免杂质G的产生;故乙酰化反应后处理时,用碳酸氢钠饱和溶液洗涤时减少洗涤时间或使用氢氧化钠替代碳酸氢钠,可减少和避免杂质H的产生.
以N-Boc-D-丝氨酸为起始原料,经羟基保护、酰胺化、脱Boc、脲形成反应分别得到杂质G和H.并用1H NMR和13C NMR谱及MS进行了结构确证.同时验证了杂质G和H在原料药拉科酰胺生产中可能产生的原因, 以便今后生产中能有效控制产生,提高药品质量.
[1] 庞素凤,刘海净,吴叶红,等.抗癫痫新药拉考沙胺概述[J].药物流行病学杂志,2010,(8):476-478.
[2] J.里德纳,G.邓恩.改进的拉科酰胺的合成方法[P].CN101928230A.
[3] Harold Kohn, ShridharV.Andurkar. Anticonvulsant enantiomeric amino acid derivatives[P].US006048899A.
[4] 靳淑云.拉科酰胺的合成研究[D].杭州:浙江大学化学系,2013.
[5] Panayiotis A. Procopiou, Simon P. D. Baugh, Stephen S. Flack, Graham G. A. Inglis. An Extremely Powerful Acylation Reaction of Alcohols with Acid Anhydrides Catalyzed by Trimethylsilyl Trifluoromethanesulfonate[J].J. Org. Chem., 1998,63(7):2342-2347.
[6] Kazuaki Ishihara, Hideki Kurihara, Hisashi Yamamoto. An Extremely Simple, Convenient, and Selective Method for Acetylating Primary Alcohols in the Presence of Secondary Alcohols[J].J. Org. Chem.1993,58:3791-3793.
[7] JR Vaughan, RL Osato. Preparation of Peptides Using Mixed Carboxylic Acid Anhydrides[J].Journal of the American Chemical Society.1951,73(12):676-678.
[8] Deborah J. Hamilton and Andrew Sutherland. A flexible approach for the synthesis of selectively labelled L-arginine[J].Tetrahedron Letters. 2004,45:5739-5741.
[9] Chih-Cheng Tai, Melissa J. Huck, Erin P. McKoon, et al. Jessop Low-Temperature Synthesis of Tetraalkylureas from Secondary Amines and Carbon Dioxide[J].J.Org. Chem., 2002,67(25):9070-907.
[10] Feng Shi, Youquan Deng, Tianlong SiMa, et al. Alternatives to Phosgene and Carbon Monoxide:Synthesis of Symmetric Urea Derivatives withCarbon Dioxide in Ionic Liquids[J].Angew. Chem. Int. Ed. 2003,42:3257-3260.
Synthesis and Structure Identification of Impurities in Urea Compounds of Lacosamide
PENG Haiyan, CAI Runfa, LIAO Zhuyuan, ZENG Fanyong, FAN Weiyong
(TechnicalCenter,JiangxiQingfengPharmaceuticalCo.Ltd,Ganzhou341000,China)
Two impurities of urea compounds formation probably in lacosamide API production were synthesized, using N-Boc-D-serine as starting material,its structure was confirmed by1H NMR,13C NMR and MS. The possible ways of generatingtwo kinds of impurities are discussed. Methods to reduce and avoid the generation of impurities are proposed.
lacosamide; impurity; chemical synthesis; urea compounds
2016-08-24
10.13698/j.cnki.cn36-1346/c.2016.06.016
彭海燕(1982-),女,江西赣州人,江西青峰药业有限公司工程师,研究方向:有机药物合成.
† 通讯作者:范卫永(1980-),男,河北邢台人,江西青峰药业有限公司工程师,有机化学硕士,研究方向:有机药物合成.
http://www.cnki.net/kcms/detail/36.1037.C.20161209.1521.044.html
R914
A
1004-8332(2016)06-0069-03

