Box-Behnken设计-响应面法优化乙醇提取黄芪甲苷工艺研究
王玉,李远辉,王佳,王欢,吴莹,李 希,2
·炮制制剂·
Box-Behnken设计-响应面法优化乙醇提取黄芪甲苷工艺研究
王玉1,李远辉1,王佳1,王欢1,吴莹1,李 希1,2
目的:运用Box-Behnken设计-响应面法优化乙醇提取黄芪甲苷最佳工艺条件。方法:以黄芪甲苷的提取量为考察指标,HPLC-ELSD色谱法为含量测定法,对乙醇浓度、乙醇用量、提取时间、提取次数进行考察,采用Box-Behnken设计-响应面法优化提取工艺。结果:乙醇提取黄芪甲苷最佳工艺条件是乙醇的体积分数为65%,乙醇用量10 倍量,提取时间2 h,提取次数3 次。结论:采用Box-Behnken设计-响应面法优化乙醇提取黄芪甲苷工艺,稳定可行、重现性好。
黄芪甲苷;Box-Behnken响应面法;提取工艺
黄芪(Radix Astragali)为豆科植物蒙古黄芪(Astragalus membranaceus (Fisch.)Beg. Var.mongholicus(Beg.)Hsiao)或膜荚黄芪(A.membranceus(Fish)Beg.)的干燥根。味甘,性微温,具有补气固表、利尿排毒、敛疮生肌、补中益气等功效[1],是一味常见的扶正中药[2]。据目前研究报道,黄芪主要成分为皂苷、黄酮、多糖等,其中黄芪甲苷是黄芪增强机体免疫功能的主要活性成分之一,也是多种黄芪制剂含量检测指标成分之一[3-6]。
Box-Behnken设计-响应面法是一种优化工艺条件的有效方法,已广泛用于优化中药有效成分提取工艺[7-8],此方法与正交设计不同,主要通过多元二次回归方程来拟合因素与响应值之间的函数关系,能够准确表示试验设计与优化结果,准确度高、可预测性强。本实验以黄芪甲苷的提取量为考察指标,HPLC-ELSD为含量测定法,采用Box-Behnken设计-响应面法优化提取工艺,对乙醇浓度、乙醇用量、提取时间、提取次数进行考察,目前没有类似的研究报道。
1 仪器与材料
Agilent1260型高效液相色谱仪(美国Agilent公司);Alltech2000型蒸发光散射检测器(Agilent公司);BT125D型分析天平(Sartorius公司);黄芪甲苷(中国药品生物制品检定所,批号:110781-200613);黄芪药材(四川禾一天然药业有限公司),按《中国药典》2015年版一部黄芪项下规定检测,均符合要求。甲醇、乙腈为色谱纯,所用水为纯净水,本文中所涉及的其他试剂均为分析纯(成都市科龙化工试剂厂)。
2 方法与结果
2.1 对照品溶液的配制
取黄芪甲苷对照品适量,精密称定,加甲醇制成每1 mL含0.5 mg的溶液,即得。
2.2 供试品溶液的配制
精密移取提取液适量,水浴挥干,残渣加水10 ml,微热使溶解,用水饱和的正丁醇振摇提取4次,每次40 ml,合并正丁醇液,用氨试液充分洗涤2次,每次40 ml,弃去氨液,正丁醇液蒸干,残渣加水5 ml使溶解,放冷,通过D101型大孔吸附树脂柱(内径为1.5 cm,柱高为12 cm),以水50 ml洗脱,弃去水液,再用体积分数为40%的乙醇30 ml洗脱,弃去洗脱液,继用体积分数为70%的乙醇80 ml洗脱,收集洗脱液,蒸干残渣加甲醇溶解,转移至5 ml量瓶中,加甲醇至刻度,摇匀,即得。
2.3 色谱条件及专属性考察
安捷伦C18色谱柱(4.6×250 mm,5 µm);流动相为乙腈-水(32∶68,v/v),漂移管温度100 ℃,气体流速为2.6 L.min-1,柱温30 ℃,流速为1 mL.min-1,进样量10 µL,理论板数按黄芪甲苷峰计算应不低于4000。分别取对照品溶液、空白溶剂、供试品溶液,按上述色谱条件进行试验,HPLC图如下图1。峰型良好,阴性无干扰,表明该方法专属性良好。
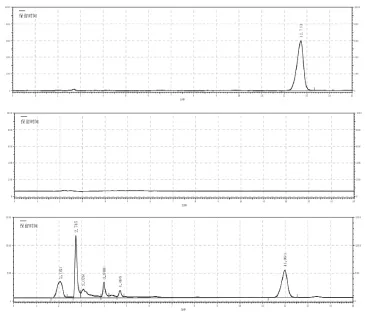
图1
2.4 标准曲线制备
分别精密移取不同浓度对照品溶液(0.998,2.001 ,2.999,4.002,4.998,7.005,10.006 mg/mL)各10 µL,以对照品峰面积积分值自然对数为纵坐标,以进样量自然对数为横坐标,进行线性拟合,得回归方程:Y=1.199 0X+6.253 8,(r=0.999 3,n=7),表明黄芪甲苷浓度在0.998~10.006 mg/mL范围内呈良好的线性关系。
2.5 精密度试验
精密吸取以上对照品溶液,按上述色谱条件重复进样5 次,RSD=1.37%(n=5),表明仪器精密度良好。
2.6 重复性试验
精密移取黄芪提取液5 份,每份20 mL,按“供试品溶液的制备”项下操作,并按上述色谱条件测定,RSD=0.91%(n=5),表明该方法重复性良好。
2.7 加样回收率试验
精密移取上述已知含量的黄芪提取液9 份,每份20 mL,分别按高、中、低浓度精密加入对照品溶液,按“供试品溶液的制备”项下处理,并按上述色谱条件测定,平均回收率=100.1%,RSD=1.21%。表明该方法准确度良好。
2.8 响应面优化实验
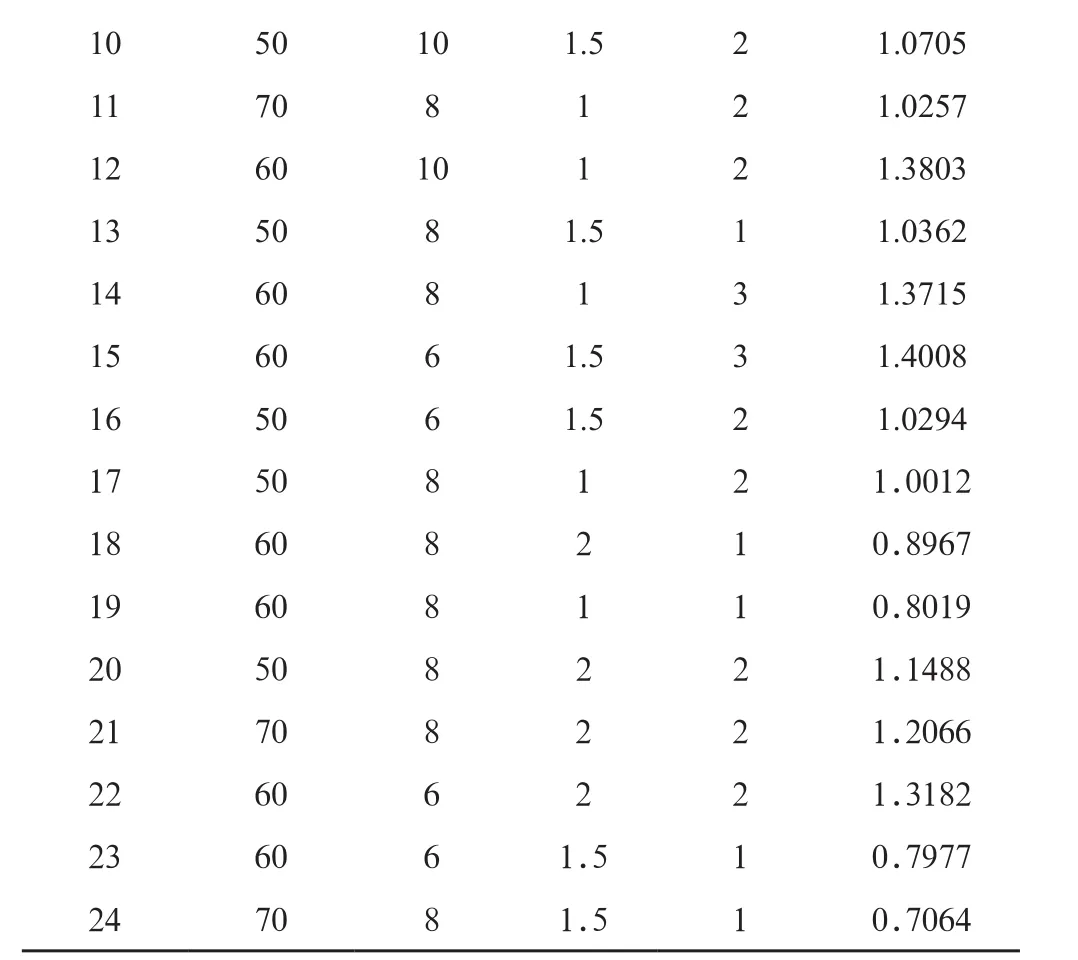
2.8.1 响应面实验设计 在查阅文献[9-11]的基础上,以乙醇浓度(X1)、乙醇用量(X2)、提取时间(X3)、提取次数(X4)为考察因素,因素水平表见表1,以黄芪甲苷提取量(Y)为指标,采用Box-Behnken设计方法设计试验,试验设计见表2,使用统计软件Design-Exoert8.0.6,对表2中数据进行多元回归拟合,得到二次多项回归方程模型:Y=11.408-5X1+0.069X2+0.064X3+0.27 X4+0.014X1X2-3X1X3+0.085X1X4+0.024X2X3-0.012X2X4+0.029X3X4-0.19X12+0.02X22-3X32 -0.11X42(r=0.9921,P<0.01)。统计学分析见表3。
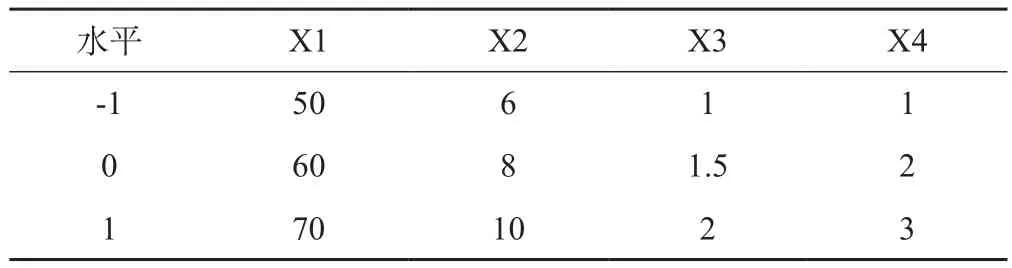
表1 因素与水平
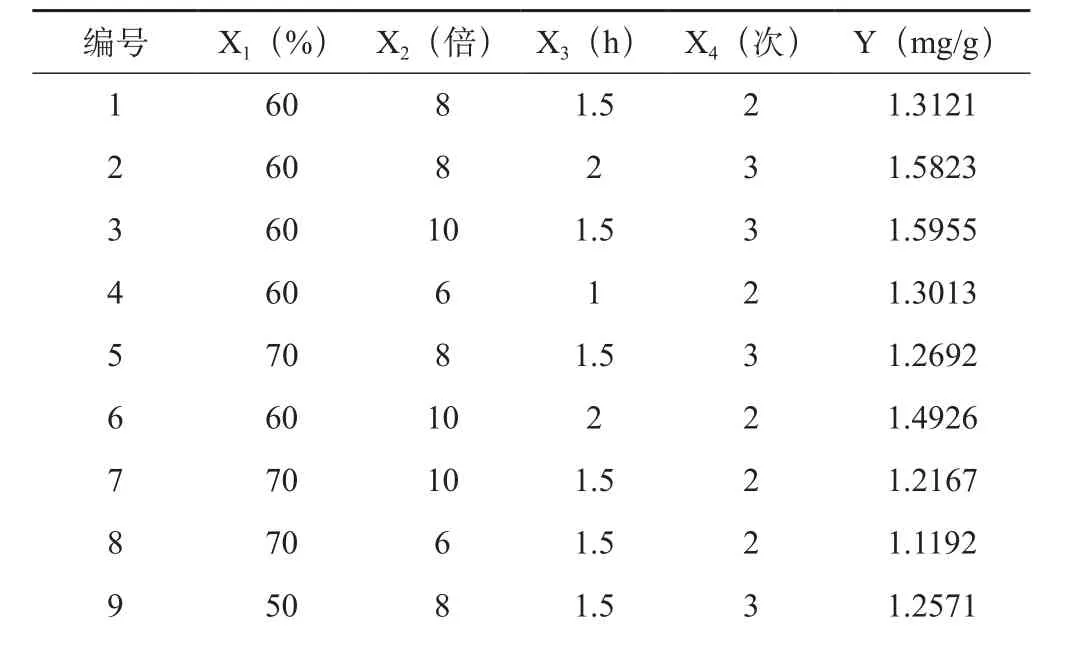
表2 黄芪甲苷提取工艺Box-Behnken试验设计
?
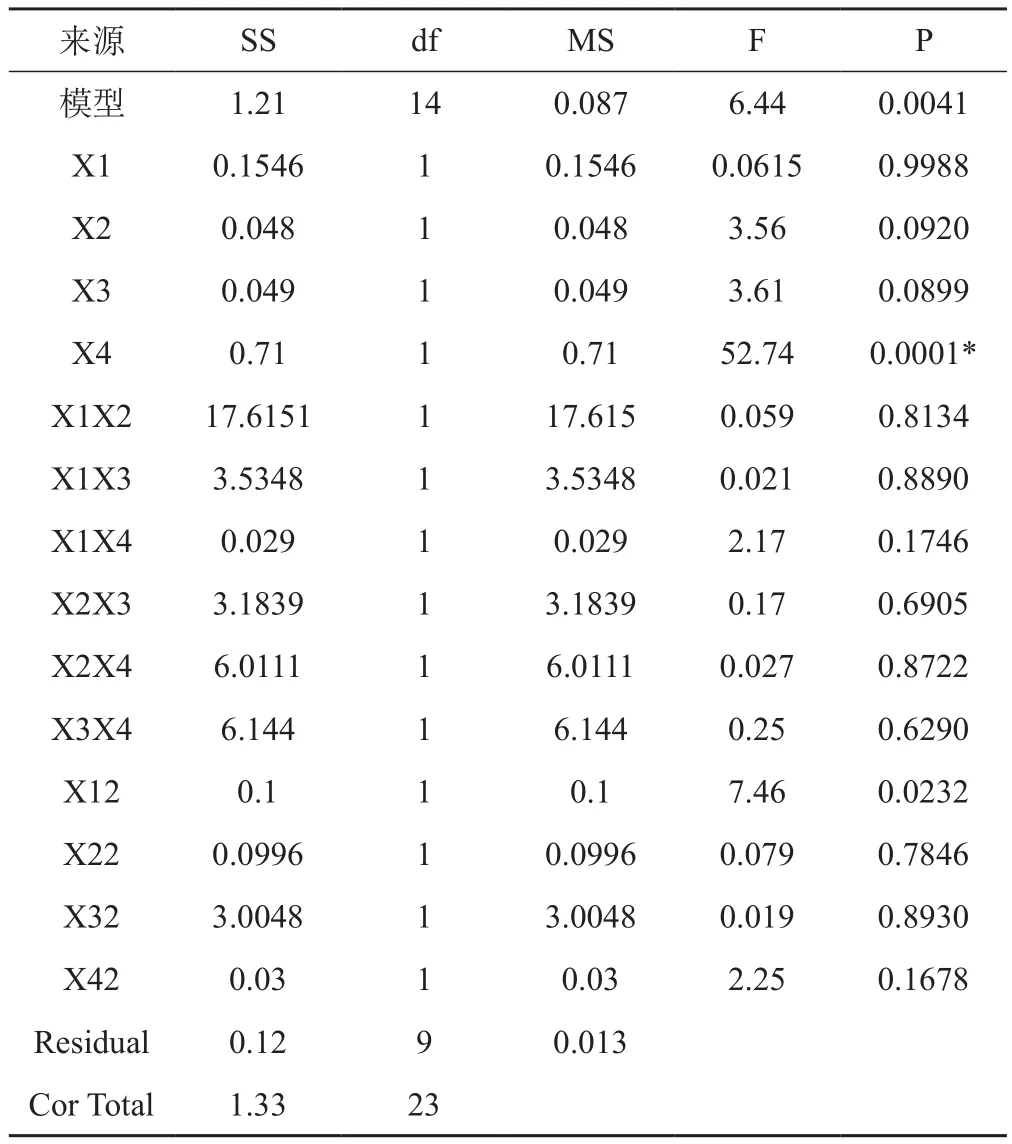
表3 回归方程方差分析
由表3可知,F=6.44,此模型P<0.000 1,表明响应面回归模型具有极显著性;多元相关系数r=0.992 1,表明二次多元方程拟合度良好。可用于优化乙醇提取黄芪甲苷工艺。
2.8.2 响应面分析 应用Design-Expert8.0.6软件绘制乙醇浓度、乙醇用量,提取时间、提取次数的响应面图,如下图2,图3所示。乙醇体积分数为约65%,乙醇用量约为原药材10 倍量时,黄芪甲苷提取量有最大值;提取时间约为2 h,提取次数为3 次时黄芪甲苷提取量有极大值。
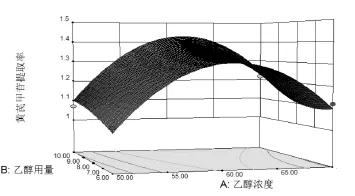
图2
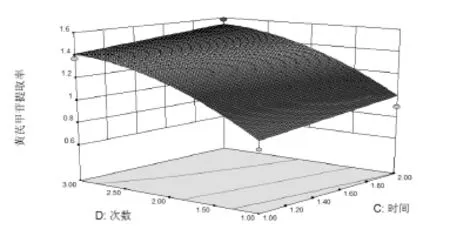
图3
2.8.3 工艺优化与验证试验 应用Design-Expert8.0.6软件优化提取工艺,得最佳提取工艺条件为乙醇体积分数65.57%,乙醇用量9.88 倍,提取时间2 h,提取次数3 次,黄芪甲苷提取量可达到1.590 4 mg/g,结合实际生产,优化工艺参数乙醇体积分数65%,乙醇用量10 倍量,提取时间2 h,提取次数3 次。按以上优化结果进行3 次验证试验,结果黄芪甲苷提取量分别为1.580 5,1.590 0,1.588 4 mg/g,平均值为1.586 3 mg/g。与理论预测值相比,其相对误差小于5%,验证值与回归方程预测值吻合较好,说明该模型有良好的预测性。
3 讨论
现代研究表明,黄芪甲苷是黄芪的主要活性成分之一,具有调节机体免疫力,降低血糖、保护组织器官、抗炎抗病毒、抗细胞凋亡等多方面药理作用。目前,工艺优化应用最普遍的是正交设计和均匀设计,但精度不够,建立的数学模型预测性差,因此,本研究采用Box-Behnken设计-响应面法,在因素与响应值之间建立非线性模型,从众多影响因素中筛选出显著影响因素,通过对试验结果的统计分析比较,优化得到最佳工艺条件为:乙醇体积分数65%,乙醇用量10 倍量,提取时间2 h,提取次数3 次,在此条件下黄芪甲苷的提取量为1.590 4 mg/ g,精确度高,可预测性强,重现性好。本研究采用Box-Behnken设计-响应面法优化提取工艺,为工业化大生产提供了科学依据。
[1]中国药典.一部[S].2015:283.
[2] 沈小钟,杨 帆,于荣敏.黄芪甲苷的研究进展[J].沈阳药科大学学报.2011.28(5):410-414.
[3] 昝丽霞.黄芪的乙醇提取工艺优化研究[J].安徽农业科学,2009,37(9);41101.
[4] 王鑫,张振秋,吕佳,等.黄芪提取工艺研究[J].中国实验方剂学杂志,2010,16(9):17.
[5] 陈涛,李进,褚治德,等.黄芪药材的微波提取工艺研究[J].时珍国医国药,2009,20(2):349.
[6] 昝日增,胡万杨,余跃,等.黄芪中主要活性成分提取工艺的研究[J].中华中医药学刊,2010,28,(12):2570.
[7] 叶良红,朱红云,李芸霞.响应面法优化大黄附子药对中蒽醌类成分的提取工艺[J].中药与临床,2011,2(4):16.
[8] 董自亮,徐瑞超.基于Box-Behnken设计响应面法优化白芷香豆素闪式提取工艺[J].中药与临床,2013,4(1):13.
[9] 杨晓雷,曹云.从黄芪生药中提取黄芪甲苷的工艺研究[J].现代化工,2008,28增刊(2):373.
[10] 郑晓峰.正交试验优选黄芪甲苷的分离纯化工艺[J].中国药房,2008,19(21):1630.
[11] 赵强强,韩丽,谢兴亮,等.田口试验设计法优选黄芪皂苷的提取工艺[J].中成药,2010,32(11):1988.
(责任编辑:傅舒)
Study on extraction technology of Astragaloside A with ethanol using Box-Behnken design-response surface methodology
WANG Yu1, LI Yuan-hui1, WANG Jia1, WANG Huan1, WU Ying1, LI Xi1,2//(1.School of Pharmacy, Chengdu University of Traditional Chinese Medicine, Chengdu 610075, Sichuan; 2.Institute of TCM, Sichuan Academy of Traditional Chinese Medicine sciences, Chengdu 611137 Sichuan )
Objective: To optimize the extraction conditions of Astragaloside A with ethanol using Box-Behnken designresponse surface methodology. Method: Astragaloside A content was detected by HPLC-ELSD method. With Astragaloside A extraction amount as index, ethanol concentration, ethanol volume, extraction time, and extraction times were investigated using Box-Behnken design-response surface method to optimize the extraction process. Result: The optimum conditions for ethanol extract of Astragaloside A was 65% ethanol, 10 volume ethanol, extraction time 2h, extracted 3 times. Conclusion: The extraction technology of Astragaloside A with ethanol optimized using Box-Behnken design-response surface methodology is stable, feasible and reproducible.
Astragaloside A; Box-Behnken response surface methodology; extraction technology
R283.3
A
1674-926X(2016)04-003-03
1. 成都中医药大学,四川 成都 611137
2. 四川省中医药科学院中医研究所,四川 成都 610031
王玉,在读研究生,从事中药新药、新技术、新工艺、新剂型的研究工作
Tel:18382284431 Email:272429134@qq.com
李希,硕士,教授,从事中药新药、新技术、新工艺、新剂型的研究工作
Tel:18030897734 Email:1836820767@qq.com.
2015-09-18

